用于NOx低温下吸附还原的CoOx/CeO2二元氧化物的制备
刘海弟 魏连启 岳仁亮 陈运法
(中国科学院过程工程研究所多相复杂系统国家重点实验室,北京 100190)
用于NOx低温下吸附还原的CoOx/CeO2二元氧化物的制备
刘海弟*魏连启 岳仁亮 陈运法
(中国科学院过程工程研究所多相复杂系统国家重点实验室,北京 100190)
研究了以多孔二氧化硅微球和活性炭为载体制备NOx吸附/还原催化剂的方法,摸索了最佳Ce/Co物质的量的比例。采用低温氮吸附方法测定了样品的BET比表面和孔容,利用XRD方法表征了样品中所掺杂的金属元素的晶型。研究发现:当nCe/nCo=75/25时,材料获得最佳NOx吸附能力,当以多孔二氧化硅微球作载体时,材料对于NOx的吸附主要来自CoOx和CeO2的二元氧化物;当以活性炭作为载体时,活性炭参与了NOx的吸附,因此其吸附容量大大提高。对NOx的吸附机理进行了探讨,并研究了样品的NH3还原性质。
氮氧化物;氧化铈;氧化钴;吸附;还原
燃煤电厂锅炉、钢铁企业烧结机等固定源造成的氮氧化物(NOx)排放已成为我国最主要的大气污染源之一[1]。我国是世界最大钢铁生产国,钢铁烧结烟气NOx排放约占NOx总排量10%,尚未采用脱硝处理,已严重威胁我国生态环境。
燃煤锅炉烟气的NOx污染控制一直是人们关注的热点,目前已发展了选择性非催化还原(SNCR)[2]和选择性催化还原(SCR)[3]等脱硝技术用于控制NOx排放,并已有相对成熟的技术投入使用。然而不同燃煤锅炉烟气,钢铁行业的烧结烟气很难直接采用SNCR或SCR技术加以处理,因为首先:烧结烟气温度较低(<200℃)难以达到SNCR方法的窗口温度(>800℃),也明显低于 SCR方法的窗口温度(>300 ℃);其次烧结烟气流量大、NOx浓度低,当采用SNCR方法处理时,加入烟气中的还原剂不能有效发挥作用。
NOx储存还原技术(NSR)是通过 “NOx催化储存-催化还原”循环操作净化富氧尾气的NOx[4-7]。该方法是先通过催化剂将烟气中的低浓NOx吸收,然后在更高温度下通过还原剂使催化剂再生,其理论上比较适合烧结烟气脱硝。目前已有将M-Ba-Al等三元物系用于NSR操作的报道(M代表贵金属)[8-10],然而由于采用昂贵的贵金属,其应用受到限制。众所周知,稀土具有特殊的4f电子层、大离子半径、适度碱性和氧化还原性,因此稀土元素在制备NSR催化剂方面很有前途。Machida[11]报道了采用CeO2和MnOx二元氧化物吸收并还原NOx的方法,然而其NOx吸附容量低于 0.2[mmolNOx·g-1催化剂],工业应用前景不佳。目前研究较多的M-Ba-Al三元物系催化剂的NOx吸附容量一般低于60[μmolNOx·g-1催化剂][12];康守方[13]采用 Pt和Cu-Mg-Al水滑石制备了NOx吸附-还原阱催化剂,但其NOx吸附容量<0.175[mmolNOx·g-1催化剂],如此低的吸附容量虽然在贫燃发动机上具有一定应用价值,但对于烧结机烟气处理意义不大。倪哲明[14]和曹根庭[15]等利用水滑石类材料进行了NOx的吸附研究,并获得了很高的NOx吸附容量(≈1500[mgNOx·g-1催化剂]),然而其NOx主要成分为NO2,其吸收过程和工业实际相去甚远。本研究旨在充分利用稀土元素(Ce)的氧化还原能力和络合能力,在避免采用昂贵的贵金属的基础上制备出相对廉价且吸附容量较高的NOx吸附/还原催化剂。
1 实验部分
1.1 主要原料和试剂
丙酮(CH3COCH3)、硝酸铈[Ce(NO3)3·6H2O]、硝酸钴[Co(NO3)2,50%,ω]均为分析纯,北京益利化学试剂公司。多孔二氧化硅微球,青岛海浪硅胶干燥剂厂,其扫描电子显微镜照片和比表面信息见下文。活性炭,北京活性炭厂,297~840 μm,其比表面信息见下文,NO 标准气体(1 MPa,含 NO 5 mL·L-1,其余为平衡N2),北京华元气体化工有限公司。下文中的NOx代表NO和NO2的混合物,组成决定于温度以及其中的O2浓度。
1.2 实验方法
1.2.1 活性炭载体的前处理
将15 g活性炭颗粒浸渍于100 mL 20wt%的硝酸中,在回流下加热至沸腾,再缓慢加入100 mL 20wt%硝酸,加热回流下氧化3 h,滤出后充分洗涤,空气中100℃下烘干。
1.2.2 吸收材料的制备
将一定量的Ce(NO3)3·6H2O和Co(NO3)2溶于丙酮中,并加入称量好的多孔二氧化硅微球或活性炭颗粒,在旋转蒸发仪上于30℃下蒸发至干,烘箱内100℃干燥5 h,以二氧化硅微球为载体的样品在马弗炉中450℃空气气氛下灼烧4 h,样品命名为Si-CeCoy-z,其中y为Co的物质的量的百分比(nCo/(nCe+nCo)×100%),z 代表样品中金属元素的掺杂量(mol·g-1多孔二氧化硅微球);以活性炭颗粒为载体的样品则在氮气气氛下灼烧4 h,以经过前处理的活性炭为载体的样品命名为oxAC-Coy-z,以未经前处理的活性炭为载体的样品命名为AC-Coy-z,其中y的意义同上,而z代表样品中金属元素的掺杂量(mol·g-1活性炭载体)
1.2.3 样品的表征
将样品研磨粉碎后,采用Philip X′Pert Pro型X射线衍射分析仪分析其中金属氧化物的晶型(测试条件:Cu靶,Kα射线,Ni滤波,管电压40 kV,电流30 mA,λ =0.154 18 nm;2θ范 围 10°~90°; 步 长0.017°)。用JSM-6700F型场发射扫描电子显微镜分析样品的外形和断面形貌(加速电压30 kV),采用Beckman Coulter SA3100型氮吸附比表面仪测定其比表面和孔容(250℃、抽真空状态下预处理5 h)。
1.2.4 吸附性能和还原性能的表征
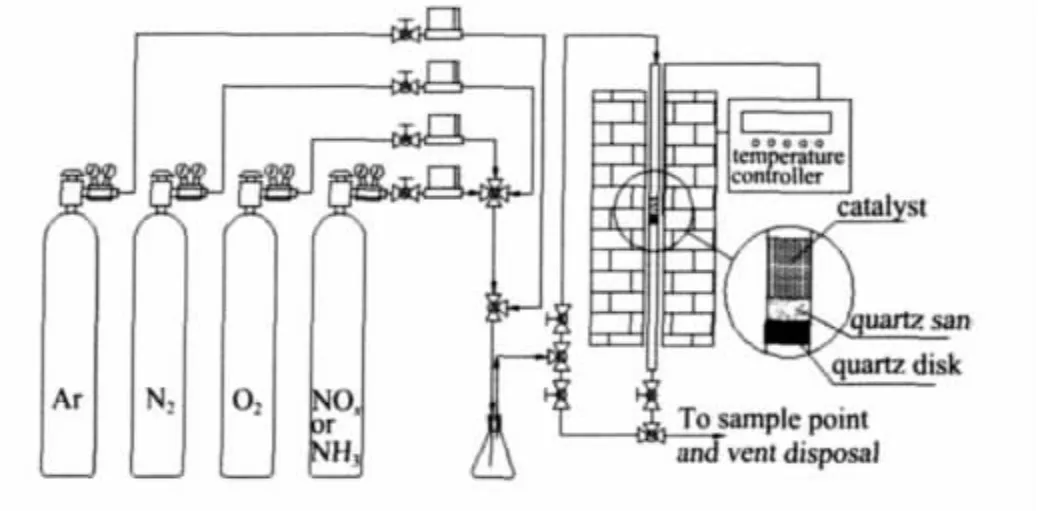
图1 NOx吸附装置图Fig.1 Graphic representation of the setup for NOxadsorption
在图1所示的装置上进行样品的NOx吸附和NH3还原性能表征,为了气体分布均匀,每次实验中预先在石英烧结板上铺垫1 g石英砂,以二氧化硅微球为载体的催化剂每次加入0.5 g;以活性炭为载体的催化剂每次加入0.25 g,反应气流量为7.2 L·h-1,在NOx吸收过程中,实验气体组成为:NOx:0.2 mL·L-1(266 mg·m-3以 NO 计),O218%,其余为平衡氮气,反应温度150℃。采用氮氧化物检测管(检测范围 0~300 mg·m-3)测定尾气中的 NOx浓度。在催化剂床层吸附饱和后,用氩气吹扫床层并升温至200℃,然后通入氮气和氨气的混合气对所吸附的NOx进行还原,气量仍为 7.2 L·h-1,氨气浓度 0.5 mL·L-1,检测出口中NOx的含量和NH3含量,还原反应结束后再以氩气吹扫床层至室温,进而以氮气为载气进行程序升温脱附(室温~500℃,5℃·min-1)
2 结果与讨论
2.1 样品的NOx吸附效果
在图1所示的装置中进行样品的NOx吸附性能表征,反应温度为150℃时的气体流出曲线如图2所示。由图可知,Ce和Co的掺杂对NOx的吸收有明显的协同作用,当单独掺杂CoO2和CeO2的情况下,样品对NOx的吸收性能很差,样品Ce100-Co0-0.0017在通气后20 min以内完全穿透;而样品Ce0-Co100-0.0017则在通气以后10 min左右完全穿透。当Ce和Co以适当比例配合的时候,样品可以获得较好的NOx吸收效果。实验中尝试了nCe/nCo为100/0、20/80、40/60、60/40、75/25、80/20 和 100/0 这几个配比。从结果可以看出,当nCe/nCo=75/25时效果最佳,样品Ce75-Co25-0.0017在通气50 min完全穿透,而更高负载量的样品Ce75-Co25-0.0051需要70 min完全穿透。由于进一步提高Ce和Co的负载量会导致前驱体Ce(NO3)3和Co(NO3)2太多而无法全部容纳于多孔二氧化硅微球的孔道中,因此没有尝试更高的Ce和Co的掺杂量,而nCe和nCo的最佳比例为75/25。
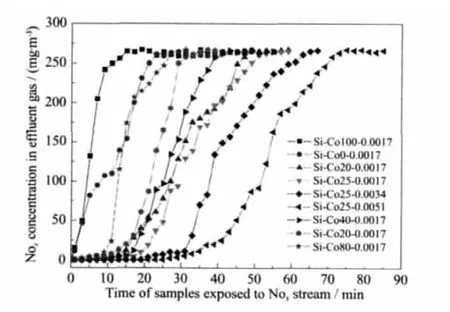
图2 不用样品对含NOx气体的流出曲线Fig.2 Effluent line of NOxstream under various samples
为了进一步提高催化剂的NOx吸附容量,我们在固定nCe/nCo最优比例为75/25的前提下、采用活性炭为载体制备了一系列NOx吸附剂。由于Ce和Co的催化氧化作用,活性炭会在300℃左右的空气中发生燃烧,因此以活性炭为载体的样品在负载Ce(NO3)3和Co(NO3)2后均在氮气气氛进行灼烧,灼烧温度选择300、400、500和600℃。其吸收结果如图3所示,可知样品AC-Co25-0.0017的NOx吸附容量明显高于Si-Co25-0.0017,在吸附剂用量减半(仅0.25 g)的情况下,400℃煅烧的样品需要120 min才能完全穿透,其NOx饱和吸附量为11.5 mg NO·g-1催化剂。
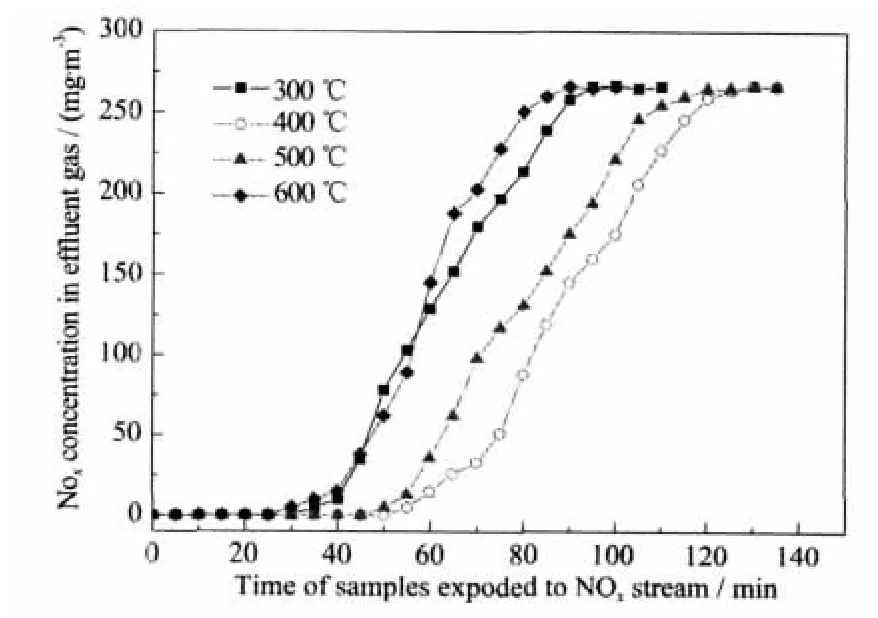
图3 样品AC-Co25-0.0017对含NOx气体的流出曲线Fig.3 Effluent line of NOxstream for AC-Co-0.0017
该结果可能有两个原因,第一,活性炭比表面远高于多孔二氧化硅,因此CeO2和CoOx可能以更加微小的晶簇状态散布于其表面,分散更加均匀,促进了NOx的氧化和吸收。第二:活性炭的表面活性基团很可能参与了NOx的贮存,因此在Ce和Co的掺杂量和掺杂比例不变的情况下,材料的NOx吸附量较样品Si-Co25-0.0017大幅度提高。在不同温度下灼烧的样品NOx有所差异的现象可以这样解释:当灼烧温度较低(如300℃)时,样品表面的Ce(NO3)3和Co(NO3)2可能没有完全分解,仍残留有部分硝酸盐物种,因此其NOx的吸附量不高;而当样品在400℃灼烧时,其表面硝酸盐物种被充分的分解去除,所以NOx吸附量提高。同时,惰性气体下灼烧活性炭有利于其表面碱性的增强[16],故400℃灼烧使材料表面的碱性官能团增多,因此这时材料的NOx吸附容量较高。当样品在500和600℃下灼烧时,过高的灼烧温度可能导致活性炭表面碱性基团脱氧而转化为相对惰性的基团,这不利于对NOx的吸收,因此其NOx吸附量反而下降。实验中还研究了空白活性炭对NOx的吸附效果,可知未经掺杂的活性炭对NOx的吸附能力低下,其原因可能在于空白活性炭对NO的氧化能力差,只能以物理吸附的方式吸收少量NOx。
基于上述考虑,从调控载体表面碱性基团数量的角度可以明显的提高样品的NOx吸附量。因此对活性炭载体进行HNO3预氧化处理,提高其表面的含氧活性基团数量,进而在负载Ce(NO3)3和Co(NO3)2后于氮气中400℃灼烧,使其表面含氧活性基团转化为碱性基团[16],则有望继续提高其NOx吸附量。该实验结果如图4所示:可知预氧化操作可以进一步提高样品的NOx吸附量至19.3 mg·g-1催化剂左右,是样品Si-Co25-0.0051吸附量的近6倍。同时在固定nCe/nCo=75/25的前提下研究了不同Ce、Co负载量对样品NOx吸附量的影响,由结果可知Ce和Co的负载量在0.5 mmol·g-1活性炭的情况下获得最优的NOx吸附效果,当负载过高和过低时,NOx的吸附容量都有所下降。
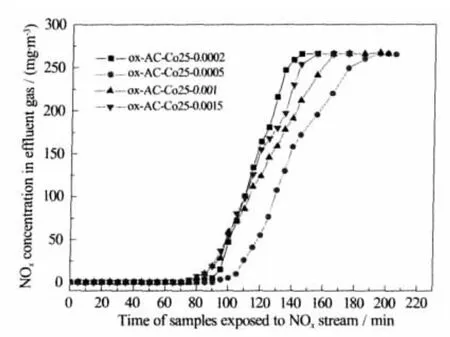
图4 以预氧化活性炭为载体的不同负载量样品对含NOx气体的流出曲线Fig.4 Effluent line of NOxstream for samples with pre-oxidized active carbon used as support under various doping amounts
为什么采用多孔二氧化硅微球为载体时样品的NOx吸附量随金属掺杂量的增大而增大,而采用活性炭为载体时样品的NOx吸附量在金属掺杂量为0.0005 mol·g-1活性炭时取得最大值?其原因很可能在于两种吸附剂不同的吸附机理:当采用二氧化硅为载体时,弱酸性的二氧化硅表面对NOx的吸附没有任何贡献,因此对NOx的吸收都来自CeO2/CoOx晶体团簇,由于Co掺杂的CeO2具有很好的催化氧化能力,使NO很快被氧化为NO2,进而与Ce的4f电子层空轨道相作用并被吸附于弱碱性的CeO2颗粒上[11],另外有少部分可能吸附于CoOx上,当CeO2/CoOx二元氧化物表面被NO2饱和时,样品便失去了氧化和吸附NOx的能力,因此样品的NOx吸附量和Ce、Co的掺杂量呈大致的线性正相关,其机理很可能如图5所示:
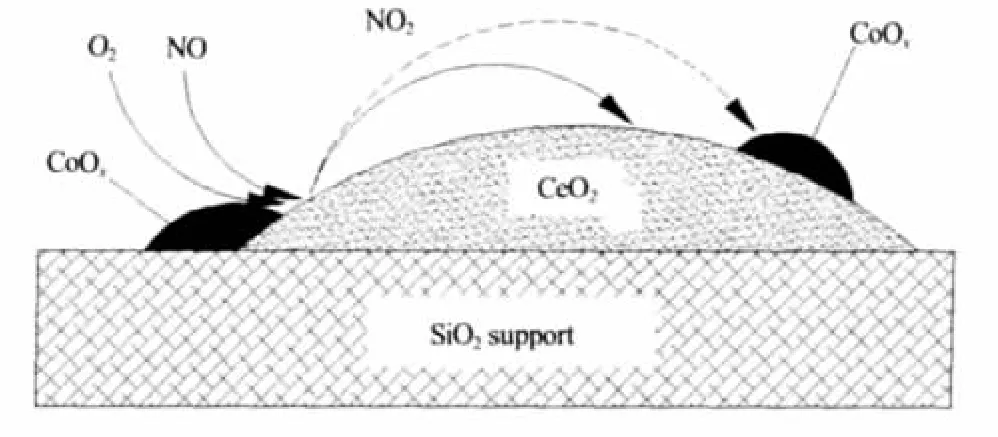
图5 以二氧化硅微球为载体的样品对NOx可能的吸附机理Fig.5 Proposed NOx-adsorption mechanism of the samples with silica sphere used as support
当采用活性炭作为载体时,反应气中的NO同样被CeO2/CoOx二元氧化物所氧化,但产生的硝酸盐物种很可能会从CeO2/CoOx的晶体团簇上扩散至临近的活性炭表面的碱性基团上去,从而减缓了CeO2/CoOx的晶体团簇失活的过程,因此材料的NOx吸附量显著提高。其可能的吸附机理如图6所示:当Ce、Co的负载量 较 低 时(如 图中 A,oxAC-Co25-0.0002),只有CeO2/CoOx晶体团簇附近的活性炭表面参与了NOx的吸附,因此吸附容量较低;当Ce、Co的负载量达最优值时(如图中 B,oxAC-Co25-0.0005),绝大部分的活性炭表面都参与了NOx的吸附,因此NOx吸附量达到极值;当Ce、Co的负载量过高时(如图中C,oxAC-Co25-0.001),大量的活性炭表面被CeO2/CoOx晶体团簇覆盖,而CeO2/CoOx二元氧化物对NOx吸附的贡献小于活性炭表面,因此其NOx吸附容量反而下降。
2.2 样品在NOx吸附后的还原效果
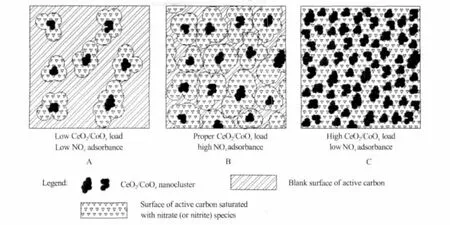
图6 以活性炭为载体时材料表面可能的NOx吸附机理Fig.6 Proposed NOx-adsorption mechanism on the surface of the sample when active carbon used as support
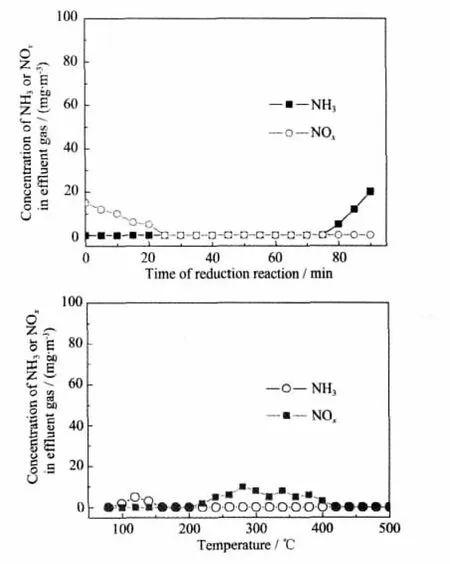
图 7 A:oxAC-Co25-0.0005 的 NH3还原结果;B:经还原后 oxAC-Co25-0.0005的 NOx-TPD 和 NH3-TPD曲线Fig.7 A:NH3reduction results of oxAC-Co25-0.0005;B:NOx-TPD and NH3-TPD profiles of reduced oxAC-Co25-0.0005
对吸附饱和NOx的样品oxAC-Co25-0.0005进行了NH3还原的研究,还原反应的温度为200℃,还原气体为NH3和N2的混合气,其中NH3含量为0.5 mL·L-1,样品量仍为 0.25 g,气体流量 7.2 L·h-1。还原过程中不断检测尾气中的NOx和NH3浓度。当尾气中 NH3含量达到 20 mg·m-3(即 0.026 ml·L-1)时停止还原实验。用Ar气吹扫床层至室温再以50 mL·min-1的N2为载气以5℃·min-1的升温速度进行程序升温脱附,并检测其出口当中的NH3和NOx浓度。其实验结果如图7A所示:在200℃下向吸附饱和的oxAC-Co25-0.0005中通入NH3时,尾气中的NH3浓度在反应的前85 min几乎检不出,这说明NH3和吸附在oxAC-Co25-0.0005的硝酸盐物种发生了生成N2的反应;同时可知,在反应的前20 min内有少量的NOx逸出,这可能是样品oxAC-Co25-0.0005单齿配位的硝酸盐物种在200℃轻微分解的结果。当还原反应进行到85 min时,尾气中NH3的浓度逐渐增加,很可能是因为oxAC-Co25-0.0005当中的大部分硝酸盐物种已经被NH3还原。对还原后的oxAC-Co25-0.0005进行的程序升温脱附结果如图7B所示,在100~140℃间出现了微小的NH3脱附峰,这可能是被活性炭孔道物理吸附的NH3在加热下脱附所致。在210~450℃之间出现了NOx的脱附峰,其峰高很低,这是单齿配位和双齿配位的硝酸盐物种分解的结果[11],该现象说明样品中仍然残留极少量未被还原的硝酸盐物种。从总的还原反应结果来看,>90%的NOx被还原。实验中还表征了经过还原反应的oxAC-Co25-0.0005的NOx吸附能力,结果表明其NOx吸附能力没有明显的变化,经过6次NOx的吸附/还原循环,样品都表现出了稳定的NOx吸附/还原能力。
2.3 样品的比表面分析
表1 给出了样品 Si-Co0-0.0017~Si-Co100-0.0017、Si-Co25-0.0026、Si-Co25-0.0034、Si-Co25-0.0051 的比表面分析结果。从结果可以看出,实验所采用的多孔二氧化硅微球载体具有较大的比表面和丰富的孔道,随着金属元素的掺杂,比表面有所下降。在掺杂的金属元素物质的量数相同的条件下,Ce的掺杂量越多,样品的比表面越低、且孔容越小,这是因为相对于Co而言,Ce的氧化物具有更高的密度和更大原子半径,而且其自身的比表面很低,当在多孔二氧化硅内部孔道分散时,Ce的氧化物更容易降低样品的比表面并占据更多的孔道空间。在相同的Ce/Co物质的量的比的条件下,掺杂的金属元素越多,样品的比表面和孔容也越低。
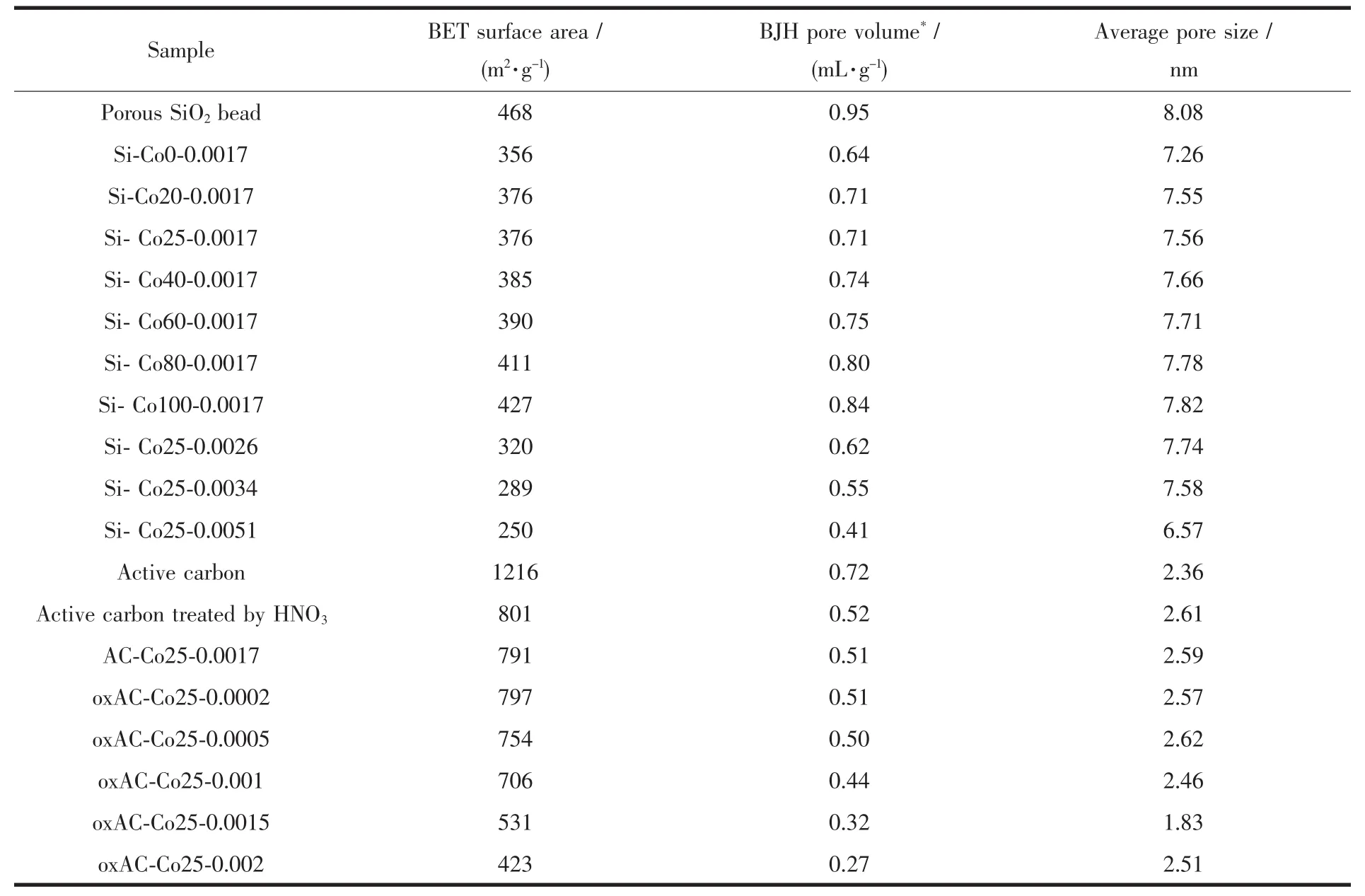
表1 样品的BET分析结果Table 1 BET results of the samples
测试可知空白活性炭载体的比表面为1216 m2·g-1,样品 AC-Co25-0.0017的比表面竟然降低至791 m2·g-1,这很可能有两个原因:第一是因为CeO2和CoOx的掺杂;第二是因为Ce和Co的硝酸盐在空气下烘干过程中已经表现出了较强的氧化能力,使活性炭载体的比表面因氧化而损失。空白活性炭样品在HNO3预氧化后比表面也锐减至801 m2·g-1,可见HNO3预氧化可明显破坏活性炭石墨相结构,显著降低其比表面和孔容。oxAC-Co25-0.0002~0.001的比表面积均在 700~800 m2·g-1之间,而样品oxAC-Co25-0.0015 和 oxAC-Co25-0.002 的比表面则分别降低至531和423 m2·g-1,这很可能是因为CeO2和CoOx掺杂量过高,导致载体表面严重氧化所致。结合前述的NOx吸收实验的结果可知,材料的NOx吸附容量不完全由比表面来决定,表面上酸、碱吸附基团的数量很可能是决定NOx吸附量的重要因素。
2.4 样品的SEM分析
图 8A、B、C 分别给出了样品 Si-Co25-0.0051 的颗粒扫描照片、断面扫描照片和空白二氧化硅载体的断面扫描照片。由图8A可知,样品Si-Co25-0.0051 为球形度很好的粒子, 尺寸在 200~500 μm之间。由图8C可知空白二氧化硅载体具有多孔的断面结构,其内部孔道比较发达;从图8B可以看出,由于CeO2和CoOx的掺杂量较大,样品Si-Co25-0.0051的断面上出现了明显的掺杂物。图8D、E分别给出了样品oxAC-Co25-0.0005的颗粒扫描照片和断面扫描照片,可知oxAC-Co25-0.0005为形状无规则的颗粒,由于其CeO2和CoOx的掺杂量不高,其断面仍然比较光滑,没有明显的掺杂物出现,这表明NOx的吸附容量不完全决定于CeO2和CoOx的掺杂量。

图8 A:二氧化硅载体SEM照片;B:Si-Co25-0.0051的断面SEM照片;C:二氧化硅载体断面SEM照片;D:oxAC-Co25-0.0005的 SEM照片;E:oxAC-Co25-0.0005的断面 SEM 照片Fig.8 A:SEM micrographs of the silica support;B:SEM of the transect of Si-Co25-0.0051;C:SEM of the transect of silica support;D:SEM of oxAC-Co25-0.0005;E:SEM of the transect of oxAC-Co25-0.0005
2.5 样品的XRD分析
图9给出了样品和多孔二氧化硅载体的XRD图,由图可知,二氧化硅载体为常见的无定形结构。样品Si-Co100-0.0017当中的Co元素主要以Co3O4的形式存在,由于其颗粒微小,而且分散在无定形二氧化硅颗粒的孔道内部,所以其衍射峰强度较弱,样品 Si-Co80-0.0017、Si-Co60-0.0017 和 Si-Co40-0.0017的XRD图中可以看到Co3O4和CeO2的衍射峰共存,其原因是两种氧化物互相掺杂。随着Co含量的减少和Ce含量的加大。比较上述几个样品可以看到:Co含量的增大导致CeO2的各衍射峰不断向高角度移动,计算可知CeO2的晶格参数从Si-Co80-0.0017 的 0.540 nm 降低至 Si-Co60-0.0017 的 0.533 nm,这表明Co3+和Co2+很可能对CeO2晶格中的Ce4+发生了部分替换,导致了CeO2晶格参数的降低,换言之,部分Co3O4和CeO2之间形成了固溶体。样品Si-Co25-0.0017 和 Si-Co20-0.0017 的 XRD 图中只存在单一的CeO2的衍射峰,其中Co元素很可能以固溶体的形式掺杂于CeO2中,其存在方式尚不能确定,结合NOx吸附实验结果可以推断:由Co3O4和CeO2组成的固溶体很可能对NO的氧化和NO2的吸附具有重要作用。
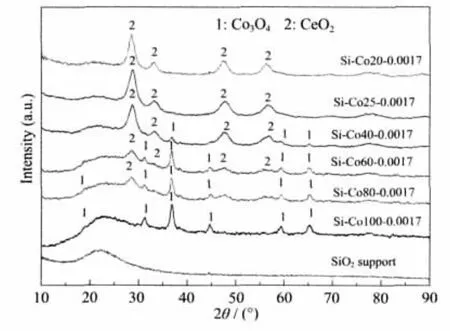
图9 以二氧化硅为载体的样品的XRD图Fig.9 XRD patterns of samples with silica used as support
图10给出了以活性炭为载体的样品的XRD图,由图可知,空白的活性炭载体在27°和45°附近分别出现了对应于石墨(002)面和(110)面的衍射峰,这是较为常见的活性炭衍射图。经过HNO3加热氧化后的活性炭的图中,石墨相(002)面和(110)面的衍射峰几乎完全消失,这表明HNO3加热氧化可以显著的破坏石墨相结构,并使活性炭的结构趋于无序,这和BET测试的结果非常一致;这种石墨相被严重破坏的活性炭虽然比表面有所下降,但对NOx的吸附能力却大大增加,原因很可能是HNO3氧化和N2下灼烧使其表面产生了对NOx吸附有贡献的活性基团。 oxAC-Co25-0.0005~oxAC-Co25-0.002 这 4 个样品的XRD图和Si-Co25-0.0017的图非常类似,其中的CoOx组分也可能因为形成固溶体而均匀分散在CeO2相中,因此不能在XRD图中找到其衍射峰。
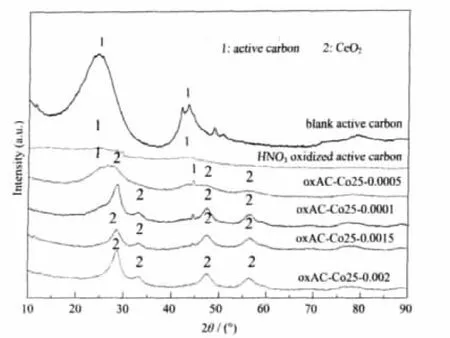
图10 以活性炭为载体的样品的XRD图Fig.10 XRD patterns of samples with active carbon used as support
3 结 论
制备了一系列以CoOx/CeO2二元氧化物为活性氧化组分的NOx吸附/还原催化材料。研究发现当Co和Ce的物质的量的比为25/75时,材料获得最佳的NOx氧化吸收性能。当采用多孔二氧化硅为载体时,材料的NOx吸附量随Co和Ce的掺杂增加而增加,当Ce和Co的掺杂达到0.0051 mol金属·g-1二氧化硅载体时,材料的NOx吸附量可达3.5 mg NO·g-1催化剂。当采用活性炭为载体时,材料的NOx吸附容量大大增加,其最优样品的NOx吸附量可达19.3 mg NO·g-1催化剂。研究了样品吸附饱和后的NH3还原性能,可知所吸收的NOx可以被NH3成功还原,样品在经过6次吸附/还原循环后其吸附和催化还原性能保持不变。样品通过BET和XRD分析研究了样品的比表面和晶型特征,发现CoOx和CeO2之间很可能有固溶体形成,当以活性炭为载体时,活性炭表面的碱性基团参与了NOx的储存。
[1]CHEN Yan-Guang(陈彦广),WANG Zhi(王 志),GUO Zhan-Cheng(郭占成).Chinese J.Process Engineering(Guocheng Gongcheng Xuebao),2007,7(3):632-638
[2]WU Bi-Jun(吴碧君),WANG Shu-Gang(王述刚),FANG Zhi-Xing(方志星).Thermal Power Generation(Reli Fadian),2006,35(11):59-60,64
[3]SHEN Bo-Xiong(沈伯雄),LIANG Cai(梁 材),GUO Bin-Bin(郭宾彬).Electric Power Environmental Protection(Dianli Huanjing Baohu),2006,22(6):37-39
[4]XIAO Jian-Hua(肖建华),LI Xue-Hui(李雪辉),XU Jian-Chang(徐建昌).Modern Chemical Industry(Xiandai Huagong),2005,25(8):15-19
[5]Gmez-Garcia M A,Pitchon V,Kiennemann A.Environ.Int.,2005,31:445-467
[6]Takahashi N,Shinjoh H,Iijima T,et al.Catal.Today,1996,27(1/2):63-69
[7]Katoh K,Kihara T,Harada J,et al.JSAE Review,1995,16(1):108-108(1).
[8]Corbos E C,Courtois X,Can F,et al.Appl.Catal.B,2008,84(3/4):514-523
[9]Kwak J H,Kim D H,Szanyi J,et al.Appl.Catal.B,2008,84(3/4):545-551
[10]Corbos E C,Haneda M,Courtois X,et al.Catal.Commun.,2008,10(2):137-141
[11]Machida M,Uto M,Kurogi D,et al.J.Chem.Mater.,2000,12:3158-3164
[12]Corbos E C,Courtois X,Can F,et al.Appl.Catal.B,2008,84(3/4):514-523
[13]KANG Shou-Fang(康守方),JIANG Zheng(蒋 政),HAO Zheng-Ping(郝郑平).Acta Phys.-Chim.Sin.(Wuli Huaxue Xuebao),2005,21(3):278-282
[14]NI Zhe-Ming(倪哲明),YU Wei-Hua(俞卫华),WANG Li-Geng(王力耕),et al.J.Chem.Eng.Chinese Univ.(Gaoxiao Huaxue Gongcheng Xuebao),2005,19(2):223-227
[15]CAO Gen-Ting(曹根庭),XIANG Fang-Fang(邢方方),FANG Cai-Ping(方彩萍),et al.Rare Metal Mater.Eng.(Xiyou Jinshu Cailiao yu Gongcheng),2008,37(suppl 2):406-408
[16]FENG Zhi-Yu(冯治宇).Technologies of Preparation and Application of Activated Coke(活性焦制备与应用技术).Dalian.Dalian University of Technology Press,2007.15
Preparation of CoOx/CeO2Binary Oxides for NOxStorage and Reduction at Low Temperature
LIU Hai-DiWEI Lian-QiYUE Ren-Liang CHEN Yun-Fa
(State Key Laboratory of Multi-Phase Complex Systern,Institute of Process Engineering,Chinese Academy of Science,Beijing 100190)
The preparation of NOxstorage and reduction catalyst using porous silica bead and active carbon as the support was studied.The optimized molar ratio of Co to Ce was obtained.The low temperature nitrogen adsorpdesorption was employed to measure the surface area and pore volume of the samples.The crystal structure of the metal element in the catalyst was investigated by XRD analysis.The results indicate that the best NOxadsorption performance is achieved when the nCe/nCo=75/25.When porous silica sphere is utilized as the support,the NOxis mainly adsorbed by the binary oxide composed of CoOxand CeO2;however,when the active carbon is used as the support,it makes obvious contribution in NOxadsorption,as a result,the NOxadsorption capacity of the sample is greatly increased.An adsorption mechanism upon NOxis also proposed and the NH3reduction behavior of the sample was investigated.
NOx;CeO2;CoOx;adsorption;reduction
O643
A
1001-4861(2010)05-0749-08
2009-12-07。收修改稿日期:2010-02-24。
国家高技术研究发展计划(863)(No.2007AA03Z439)资助项目。
*通讯联系人。 E-mail:liuhaidi@home.ipe.ac.cn
刘海弟,男,34岁,副研究员;研究方向:环境净化材料。

