纳氏试剂比色法测定水中氨氮的影响因素分析
高春燕
(迪庆州环境监测站,云南迪庆674400)
纳氏试剂比色法测定水中氨氮的影响因素分析
高春燕
(迪庆州环境监测站,云南迪庆674400)
就纳氏试剂比色法在测定水中氨氮的过程中各种影响测定的因素进行分析,并就实验时间对测定的的影响进行了研究。
氨氮;纳氏试剂;影响因素
1 前言
氨氮(NH3-N)以游离(NH3)或铵盐的形式存在于水中,两者的组成比取决于水的pH和水温。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例较高,水温则相反。
氨氮的测定方法中纳氏试剂比色法具操作简便、灵敏等特点,水中钙、镁和铁等金属离子、硫化物、醛和酮类、颜色、以及混浊等均会干扰测定,需作相应处理[1]。
水中氨氮的主要来源为生活污水中含氮有机物受微生物作用的分解产物,某些工业废水以及农田排水。氨氮是水体中的营养素,可导致水体富营养化现象产生,是水体中的主要耗氧污染物。水中氨氮含量高时,可使水中产生刺鼻的臭味,污染周围环境。鱼类对水中的氨氮比较敏感,当氨氮含量高时会导致鱼类死亡。测定水中的各种形态的氮化合物,有助于评价水体被污染和 “自净”状况。本文对氨氮的分析方法纳氏试剂比色法测定水中氨氮的过程中各种影响因素进行分析,以尽量将各种影响减小到最低,从而获得更为准确的监测数据。
2 试验
2.1 试剂仪器
2.1.1 仪器
北京普析通用仪器有限责任公司出品的T6-新悦可见分光光度计。
梅特勒-托利多仪器(上海)有限公司出品的LP115 FK型pH计。
2.1.2 试剂
配制试剂用水均应为无氨水,以下简称水。无氨水可选用下列方法之一进行制备:
(1)蒸馏法:每1L蒸馏水中加011ml硫酸,在全玻璃蒸馏器中重蒸馏,弃去50ml初馏液,接取其余馏出液于具塞磨口的玻璃瓶中,密塞保存。
(2)离子交换法:使蒸馏水通过强酸性阳离子交换树脂柱。
2.1.211 纳氏试剂
纳氏试剂可选择下列方法之一制备[1]:
(1)称取20g碘化钾溶于约25ml水中,边搅拌边分次少量加入二氯化汞(HgCl2)结晶粉末(约10g),至出现朱红色沉淀不易溶解时,改为滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不再溶解时,停止滴加氯化汞溶液。另称取60g氢氧化钾溶于水,并稀释至250ml,冷却至室温后,将上述溶液徐徐注入氢氧化钾溶液中,用水稀释至400ml,混匀。静置过夜,将上清液移入聚乙烯瓶中,密塞保存。
(2)称取16g氢氧化钠,溶于50ml水中,充分冷却至室温。另称取7g碘化钾和碘化汞(HgI2)溶于水,然后将此溶液在搅拌下徐徐注入氢氧化钠溶液中。用水稀释至100ml,贮于聚乙烯瓶中,密封保存[1]。
2.1.212 酒石酸钾钠溶液
称取50g酒石酸钾钠(KNaC4H4O6·4H2O)溶于100ml水中,加热煮沸以除去氨,放冷,定容至100ml。
2.1.213 铵标准贮备溶液
称取31819g经100℃干燥过的优级纯氯化铵(G.R.)溶于水中,移入1000ml容量瓶中,稀释至标线。此溶液每毫升含1100mg氨氮。
2.1.214 铵标准使用溶液
移取5100ml铵标准贮备溶液于500ml容量瓶中,用水稀释至标线,此溶液每毫升含01010mg氨氮。
212 试验方法原理
碘化汞和碘化钾的碱性溶液与氨反应生成淡红棕色胶态化合物,此颜色在较宽的波长内具强烈吸收,该化合物的色度与氨氮含量成正比。
最大吸收波长实验:在350nm~550nm测定最大吸收波长,结果如图1。
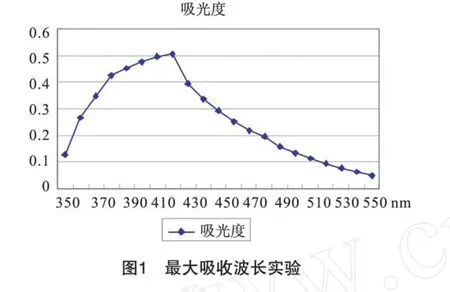
从图1可以看出在420nm处有最大吸收波长。因此实验在420nm波长处,用光程20mm比色皿,以水为参比,测量吸光度。
2.3 试验方法的适用范围
纳氏试剂比色法最低检出浓度为01025mg/L(光度法),测定上限为2mg/L。采用目视比色法,最低检出限为0102 mg/L。水样作适当的预处理后,本法可适用于地表水、地下水、工业废水和生活污水氨氮的测定[1]。
2.4 标准曲线的绘制
吸取0、0150、1100、3100、5100、7100和1010ml铵标准使用液于50ml比色管中,加水至标线,加110ml酒石酸钾钠溶液,混匀。加115ml纳氏试剂,混匀。放置10min后,在波长420nm处,用光程20mm比色皿,以水为参比,测定吸光度。由测得的吸光度,减去零浓度空白管的吸光度后,得到校正吸光度,结果见表1。
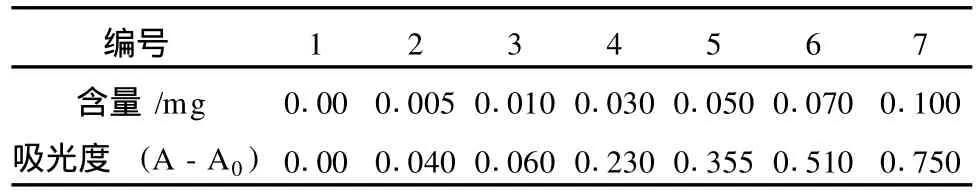
表1 标准曲线 空白值(A0):01020
2.5 计算
由水样测得的吸光度减去空白试验的吸光度后,从校准曲线上查得氨氮含量(mg)。
氨氮(N,mg/L)=m/V×1000
式中:m—从校准曲线上查得氨氮含量(mg);
V—水样体积(ml)。
2.6 试验数据处理
反应时间的影响。在本法测定氨氮的过程中,要求放置10min后测量吸光度。我们在不同反应时间下测定空白、标样及实验样品的吸光度,计算其浓度,进行比较,其结果见表2、表3、表4。

表2 不同时间对空白吸光度的影响
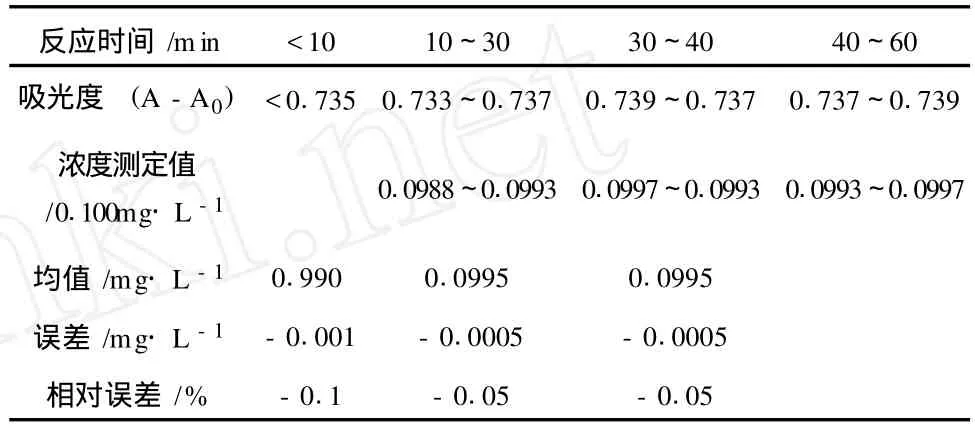
表3 不同时间对标准样品吸光度和浓度的影响
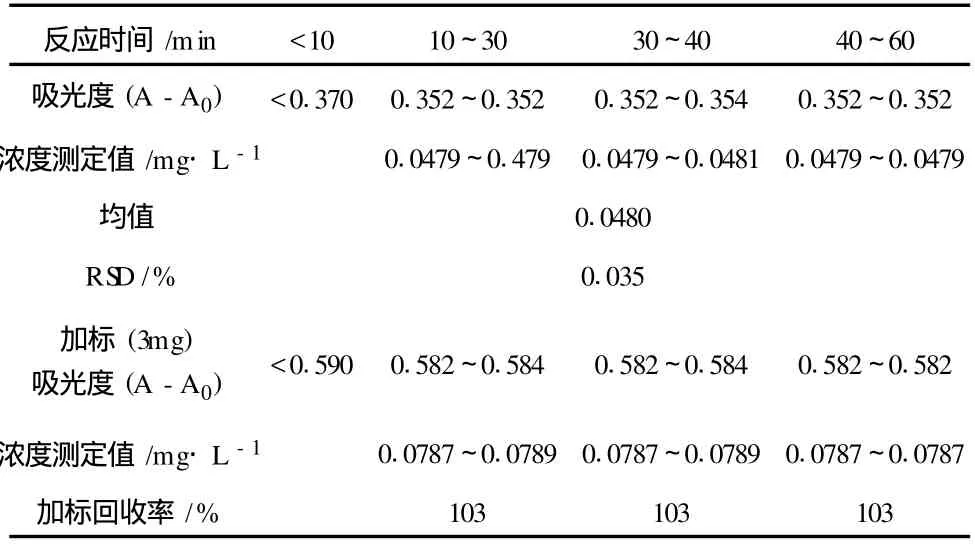
表4 不同时间对实验样品吸光度和浓度的影响
3 结果讨论
通过实验可以看出,<10min时,显色不完全,10~30min较稳定,30~60min颜色加深,吸光度呈增大趋势。但是对测定浓度的影响不大,空白及样品的吸光度同时上升与浓度呈线性关系。三个时段的误差、相对误差、加标回收率均没有明显差异,能达到实验要求。
4 影响因素及解决方法
(1)室验试剂的影响。本法实验所需试剂有纳氏试剂、酒石酸钾纳溶液。纳氏试剂有两种制备方法。第一种用碘化钾、二氯化汞和氢氧化钾配制。第二种用碘化钾、碘化汞和氢氧化纳配制。纳氏试剂配制后应避光低温冷藏保存在聚乙烯塑料瓶内,以防颜色加深,保证空白值的稳定性。酒石酸钾纳溶液的配制中应注意使用合格试剂,不合格试剂铵盐含量较大[2]。
(2)实验用水的影响。实验用水均应为无氨水。无氨水的制备有蒸镏法:每1L蒸镏水中加011L硫酸,在全玻璃蒸馏器中重蒸馏,弃去50ml初馏液,接取其余馏出液于具塞磨口的玻璃瓶中;还可用离子交换法制备无氨水。无氨水应密塞保存,空气中氨溶于水或有铵盐进入实验用水中,会导致实验空白达不到要求。
(3)水体中物质的影响。水样带颜色或混浊,含有其它一些干扰物质时,会影响氨氮的测定[3]。在实验中需对水样进行预处理,对较清洁的水,可采用絮凝沉淀法;对工业废水或严重污染的水,则用蒸馏法消除干扰。
(4)滤纸的影响。在实验中需要将水样通过滤纸过滤进行水样的预处理,滤纸中一般都含有铵盐,这是因为造纸工艺多采用铵法造纸,铵盐会残留滤纸中。有实验表明,通过对滤纸的洗涤次数的增加,吸光度呈下降趋势。因此在实验中应少量多次淋洗滤纸,以降低滤纸对测定的影响[4]。
(5)反应时间的影响。在本法测定氨氮的过程中,要求放置10min后,测量吸光度。我们在不同反应时间下测定空白、标样及实验样品的吸光度,计算其浓度,进行比较。通过实验可以看出,<10min时,显色不完全,10~30min较稳定,30~60min颜色加深,吸光度呈增大趋势。但是对测定浓度的影响不大,空白及样品的吸光度同时上升与浓度呈线性关系。
5 结论
在纳氏试剂比色法测定水中氨氮的实验过程中,我们应该注意实验用水、实验试剂、水体中物质的影响及滤纸的影响并避免新的影响因素,这样我们得到的实验数据才能准确可靠。
[1]本书编委会.水和废水监测分析方法(第四版)[M].北京:环境科学出版社,2002.
[2]温丽云,范朝.我国环境监测中的氨氮分析方法[J].分析实验室,2003,11(22).
[3]纪云峥.纳氏试剂比色法测定水中氨氮的干扰分析[J].分析实验室,2007,(S1).
[4]高春梅.浅谈水体中氨氮的测定方法[EB/OL].http://www.hjjc.ibicn.com/document/archive/200903/5060675579133731.html.
I mpacting Factors Analysis on Ammon ia Detection by Nessler′s Reagent Colorimetric M ethod
GAO Chun2yan
(Diqing EnvironmentalMonitoring Station,Diqing Yunnan 674400 China)
All kinds of impacting factors on ammonia detection by Nessler’s reagent colorimetric method are ana2 lyzed.The experimental time is focused on in the research.
ammonia;Nessler’s reagent;impacting factor
X83
A
1673-9655(2010)05-0092-03
2010-08-16

