市售不同产地丹参饮片中隐丹参酮、丹参酮Ⅰ及丹参酮ⅡA的含量比较
首都医科大学附属北京友谊医院(100050) 钟萌
北京市海淀区药品检验所(100083) 李东辉 杨帆
丹参是唇形科植物丹参的根及根茎,具有祛瘀止痛、活血通络、清心除烦的功效。丹参的有效成分包括脂溶性成分(二萜醌类)和水溶性成分(酚酸类),均具有一定的生理活性。由于受产地、品种、气候和生态环境及炮制方法等的影响,不同丹参饮片所含主要活性成分差异较大,《中华人民共和国药典》丹参项下脂溶性成分以丹参酮ⅡA作为质控指标[1]。近年来的研究表明,丹参脂溶性成分还包括隐丹参酮、丹参酮Ⅰ等,且含量较高,活性较强[2] [3]。
笔者收集了河北、山东、江苏、河南和安徽等主产地的丹参饮片,包括不同栽培方法的丹参饮片,用反相高效液相色谱法对其进行了隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的含量测定和比较,为丹参饮片的选优及临床用药提供一定的参考依据。
1 仪器与试药
LC-2010高效液相色谱仪(日本岛津公司),SPD-20A紫外可见检测器,CLASS-VP色谱工作站。KQ118超声波清洗器,BP211 1/10万电子分析天平。隐丹参酮(中国药品生物制品检定所,批号110852-200305,供含量测定用);丹参酮Ⅰ(中国药品生物制品检定所,批号0867-200205,供含量测定用);丹参酮ⅡA(中国药品生物制品检定所,批号110766-200417,供含量测定用);丹参饮片(购于不同饮片厂,1、2号:河北;3、4号:山东;5、6号:江苏;7、8号:河南;9、10号:安徽;丹参饮片均经北京市海淀区药品检验所韩杰副主任中药师鉴定)。

2 方法与结果
2.1 色谱条件的选择 色谱柱:kromasilTMC18分析柱(4.6mm×250mm,5μm);流动相甲醇-水(75:25),流速1ml·min-1,检测波长270nm,柱温30℃,进样量10μl[4][5]。在该色谱条件下,隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的保留时间分别为15.9min、17.3min和27.4min。
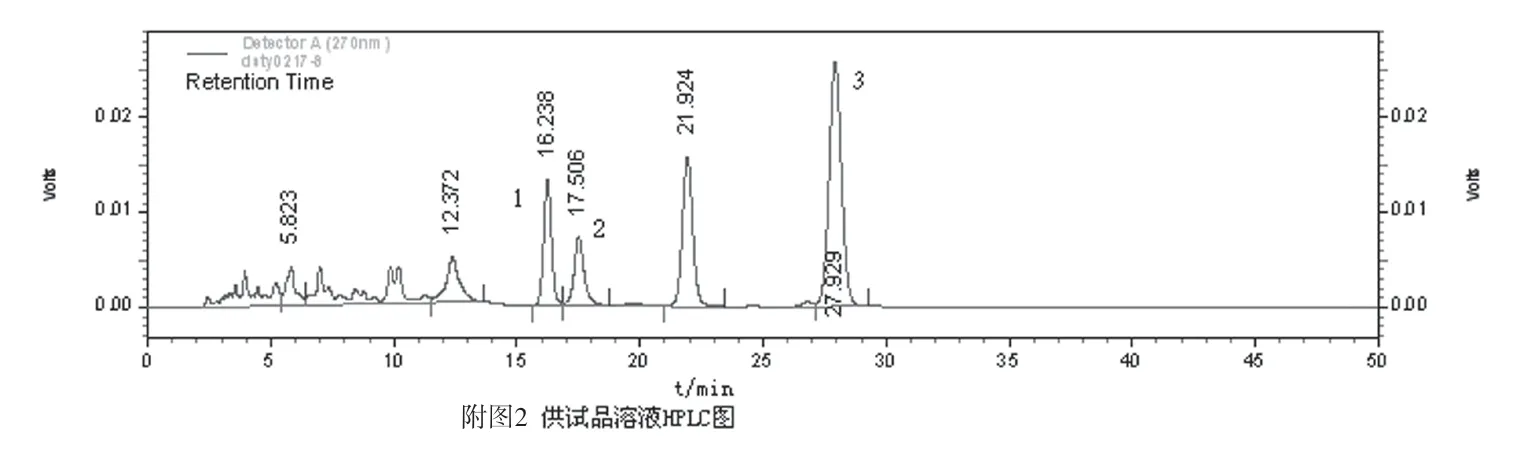
隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA与样品中其他组分分离良好,理论板数按隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA对照品峰计均大于5000。缺隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA阴性对照无干扰(结果见附图1,附图2)。
2.2 对照品溶液的制备 精密称取隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA对照品适量,加甲醇制成每毫升含隐丹参酮85μg、丹参酮Ⅰ102μg和丹参酮ⅡA107μg的混合溶液,然后至棕色瓶中,作为对照品储备溶液。
2.3 供试品溶液的制备 取供试品(丹参药材和饮片)粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,密塞,称定重量,超声处理(功率200W,频率40kHz),超声提取10分钟、20分钟、30分钟、40分钟、50分钟,放冷,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得[2]。
2.4 线性关系的考察 精密吸取隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA混合对照品溶液2、4、6、8、10、12μl,注入高效液相色谱仪,按上述色谱条件测定色谱峰面积,以对照品的进样量X(μg)对峰面积的积分值Y进行线性回归。
隐丹参酮:Y=5.2×105X+1.8×105,线性范围:1.45~10.19μg,R=0.9998;丹参酮Ⅰ:Y=5.3×105X-2.7×105,线性范围为2.16~15.12μg,R=0.9996;丹参酮ⅡA:Y=5.7×105X+1.0×105,线性范围为3.15~22.06μg,R=0.9997。
2.5 精密度试验 取隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA混合对照品溶液10μl,连续进样6次,测定峰面积,结果隐丹参酮的RSD为0.98%,丹参酮Ⅰ的RSD为1.08%,丹参酮ⅡA的RSD为0.86%,精密度良好。
2.6 重现性实验 取同一供试品,按2.3项下操作制备供试品溶液6份,按2.1项下色谱条件测定,结果隐丹参酮的RSD为1.13%,丹参酮Ⅰ的RSD为0.95%,丹参酮ⅡA的RSD为1.25%,重现性良好。
2.7 稳定性试验 取同一份供试品溶液,室温放置,分别在0、1、2、4、8、12、24 h进样,按2.1项下色谱条件测定,结果隐丹参酮的RSD为1.05%,丹参酮Ⅰ的RSD为0.85%,丹参酮ⅡA的RSD为1.15%,表明供试品在24 h内稳定。
2.8 加样回收率实验 取已知隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA含量的供试品(批号6174241)0.5g,6份,各加入一定量的隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA对照品。
按2.1项下色谱条件测定,计算隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA回收率分别为99.12%、98.96%、99.23%,RSD分别为1.21%、0.98%、1.05%。
2.9 样品测定 取不同产地的丹参饮片,按2.3项下操作制备供试品溶液,按2.1项下测定,结果见附表。
3 讨论
3.1 系统适用性试验 本试验曾参考中国药典2005年版一部丹参药材[2]项下含量测定方法,发现供试品色谱不仅有丹参酮ⅡA色谱峰,而且还有隐丹参酮、丹参酮Ⅰ色谱峰,通过查阅文献[2],确立了本试验的方法。
3.2 供试品溶液制备方法 供试品超声提取时间的考察,以甲醇为提取溶剂,实验结果表明,超声提取40分钟,隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的含量已基本保持不变,故确定超声提取时间为40分钟。
3.3 不同产地丹参饮片的隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA含量差别较大,山东的野生丹参饮片含量最高,安徽的栽培丹参饮片含量最低,而同一地区中野生品的含量普遍高于栽培品。这与丹参饮片的产地与加工方法有关,所以应对丹参药材的产地加以分类,同时饮片的加工方法应规范统一。

附表 不同产地丹参饮片中的隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA(n=3)

