纳米ZnO/SnO2粉体的制备及其光催化性能的研究
黄新友 邓悦欢 李晓毅
(江苏大学材料科学与工程学院,江苏镇江212013)
纳米ZnO/SnO2粉体的制备及其光催化性能的研究
黄新友 邓悦欢 李晓毅
(江苏大学材料科学与工程学院,江苏镇江212013)
以SnCl4·5H2O、ZnNO3·6H2O、HCl、NaOH为原料,采用共沉淀法制备出纳米ZnO/SnO2纳米复合催化剂粉体,以降解甲基橙溶液反应为模型,考察了不同比例ZnO/SnO2纳米粉体的光催化活性,探讨了煅烧温度对催化剂催化活性的影响。并用差热失重分析仪(TG/DSC)、透射电镜(TEM)、X-射线衍射(XRD)测试手段对其进行了表征。结果表明:ZnO复合SnO2后,光催化活性明显提高,其中以ZnO/SnO2在ZnO∶SnO2=4∶1的情况下复合催化剂光催化性能最优;热处理温度在650℃保温时间2h所得到的复合催化剂催化性能最好。
纳米ZnO/SnO2粉体,光催化,共沉淀,甲基橙
1 引言
自从1972年日本的fujishima[1]发现TiO2在光照的条件下能够水解制氢,揭开了光催化氧化技术序幕以来,纳米半导体光催化技术在多领域的应用得到迅速发展。其中纳米光催化剂在降解有机物,治理环境污染方面,得到研究者的广泛关注[2]。目前研究比较多的半导体光催化剂大多数都属于宽禁带n型半导体化合物,其中以TiO2、CdS和ZnO的催化活性最高[3]。但是由于单一半导体材料光催化剂,带隙能较大,空穴易与电子复合,所以光催化效率并不太高,需要对催化剂进行改性,以提高其光催化活性及可应用性[4]。目前,对于TiO2体系的改性已有较系统全面的研究,而ZnO在紫外和可见光区域都有一定的吸收[5],其禁带宽度与TiO2相近,且ZnO制备操作简单,因此近年来对ZnO的光催化性能的研究也越来越多[6]。本文采用共沉淀法制备出不同比例复合的ZnO/SnO2纳米粉体催化剂,以降解甲基橙反应为模型,考察了不同比例ZnO/SnO2纳米粉体的光催化活性,结果发现ZnO复合SnO2后,光催化降解甲基橙的活性明显提高,为复合纳米粉体在降解有机物的应用,奠定一定的基础。
2 实验
2.1 复合光催化剂粉体的制备
利用SnCl4·5H2O、ZnNO3·6H2O、HCl、NaOH(均为分析纯)为原料,采用共沉淀法制备ZnO/SnO2纳米复合光催化剂前驱体。按不同摩尔比 (ZnO∶SnO2=5∶1,4∶1,3∶1,2∶1,1∶1,1∶2,1∶3,1∶4,1∶5)将ZnNO3·6H2O和SnCl4·5H2O固体混合,加入适量的去离子水及少量浓HCl强烈搅拌下缓慢滴加一定浓度的NaOH溶液,调节溶液的pH值至7~8之间。得到的白色沉淀经离心、洗涤至洗液无Cl-然后用无水乙醇洗涤数次。此沉淀于100℃烘干,得到催化剂前驱体。将干燥的催化剂前驱体放在研钵里研磨至超微粉体,然后将粉体在不同温度条件下热处理,制得具有不同物相组成和晶粒尺寸的ZnO/SnO2复合光催化剂粉体。
2.2 复合催化剂粉体的表征
用德国耐驰STA449C综合热分析仪,分析ZnO/SnO2复合粉体前驱体热处理中的失重和热量变化,用日本理学D/max2500PC全自动粉末X射线衍射仪测定复合粉体的物相组成,用JEM-2100(HR)型透射电镜观察复合催化剂粉体形貌特征。
2.3 复合催化剂粉体催化活性的表征
以复合光催化剂粉体对甲基橙溶液的降解率评价其光催化性能。反应装置为自制,实验用灯为家用普通台灯(额定功率为40W)。
取不同条件下制备的催化剂粉体0.12g加入到100mL,浓度为10mg/L的甲基橙溶液中,超声振荡后于光催化装置中光照(溶液pH为6左右,温度为室温)。控制搅拌速度使催化剂粉体充分悬浮于溶液中,光照一定时间后,取样,离心分离,用UV2550型紫外可见分光光度计测定溶液吸光度。甲基橙的降解率用以下公式[7]表示:

3 结果与讨论
3.1 不同比例ZnO/SnO2纳米粉体的光催化活性的比较

从图1中可以看出纯纳米ZnO粉体的光催化性能最小而复合催化剂粉体的催化性能随着ZnO/SnO2比值的减小,复合光催化剂粉体对甲基橙的降解能力先增大,后减小。在摩尔比ZnO∶SnO2=4∶1时,复合光催化剂粉体对甲基橙的降解能力达到最大,在可见光照225min后复合光催化剂粉体对甲基橙的降解能力达到42.69%,而后复合光催化剂粉体对甲基橙的降解能力逐渐降低。这是因为在实验用灯光照射下,ZnO和SnO2受到光量子的激发,产生光生电子e-和光生空穴h+,它们在二者导带和价带之间的迁移可对复合光催化剂的催化活性产生两方面的影响[8]。一方面,这种迁移能够有效抑制电子和空穴的复合,提高产物的光催化活性。另一方面,产物的光催化活性与光生电子e-和光生空穴h+迁移的方向有关:由于SnO2价带的电极电位高于强于ZnO价带的电极电位导致SnO2价带的氧化能力强于ZnO价带的氧化能力,所以当光生空穴h+从ZnO价带向SnO2价带迁移时,催化剂的催化活性增强,反之,当光生空穴h+从SnO2价带ZnO价带迁移时,催化剂的催化活性减弱。在本实验中,复合光催化剂对甲基橙的光催化降解就是这两方面综合作用的结果,当复合光催化剂中SnO2的量较少时,一方面ZnO受到激发产生的较低电极电位的光生空穴h+数量较多,较低电极电位的光生空穴h+向较高电极电位迁移的几率大,从而一定程度上增强了催化剂的催化活性,对催化剂的催化活性产生了正作用;另一方面,高电极电位的光生空穴h+数量少,对催化剂的催化活性产生了负作用,随着SnO2量的增多,正负作用相互博弈,共同影响着催化剂的催化活性。当在摩尔比ZnO∶SnO2=4∶1时,达到极值,催化剂的催化活性最大。
3.2 煅烧温度对复合催化剂的催化活性的影响
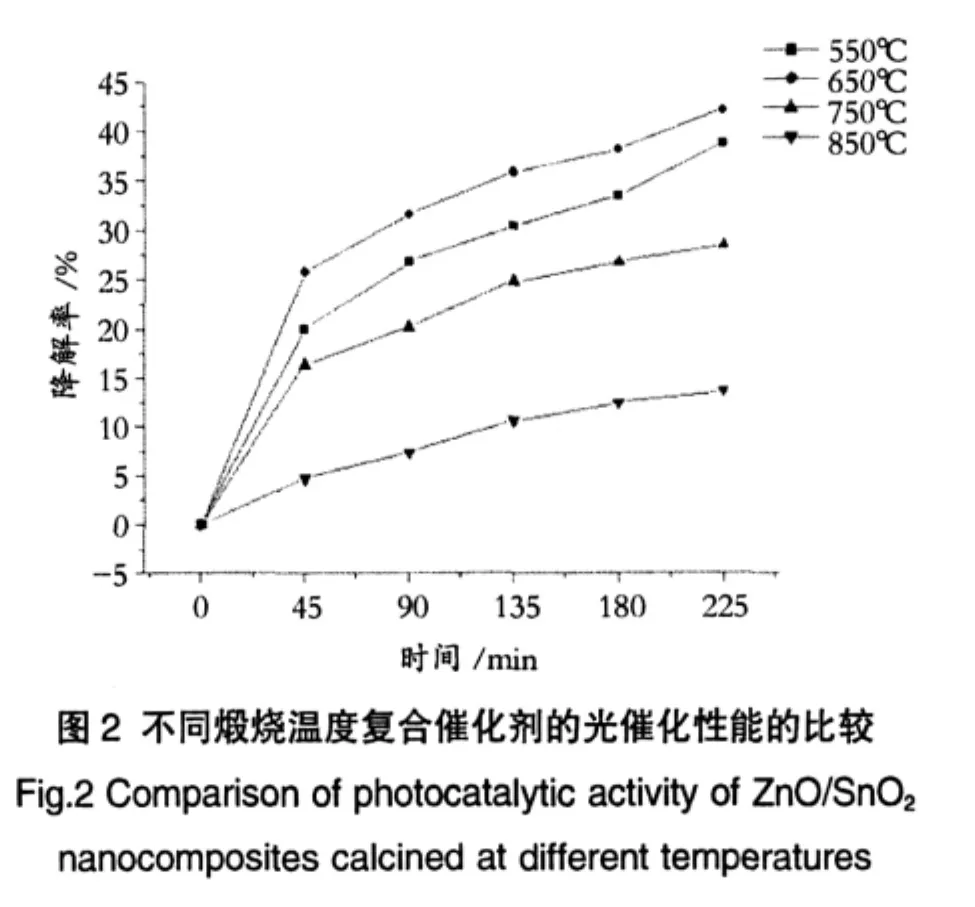
图2为ZnO∶SnO2=4∶1的复合催化剂前驱体在不同温度保温2h热处理得到的ZnO/SnO2复合催化剂在相同条件下降解甲基橙溶液的曲线图。从图中我们可以看出随着煅烧温度的提高,复合催化剂降解甲基橙溶液的能力也增大后减小,其中,以热处理温度为650℃保温2h的复合催化剂的降解能力最好。结合XRD衍射图样和TEM图样我们可以得知:当温度在550~650℃之间时,ZnO/SnO2的晶体开始生长并随着温度升高一方面晶体生长趋于完整,同时ZnO/SnO2晶体也逐渐增多,所以复合催化剂的催化能力随着温度的升高而升高。但是,当温度超过650℃时,随着温度的升高,一方面纳米粉体开始团聚,一方面减小了催化剂与溶液的接触面积,另一方面阻碍了光生电子e-和光生空穴h+游离到相界面进行有效的催化反应,因此降低了催化剂的催化性能。同时,在750℃时,ZnO和SnO2在高温的条件下生成了少量没有光催化性能的Zn2SnO4晶体[9],并且随着温度的进一步升高,ZnO和 SnO2进一步减少,Zn2SnO4晶体则逐渐增多,晶体亦生长完全。在这些因素协同作用下,复合催化剂粉体的催化性能下降。

3.3 复合催化剂粉体前驱体的TG-DSC分析
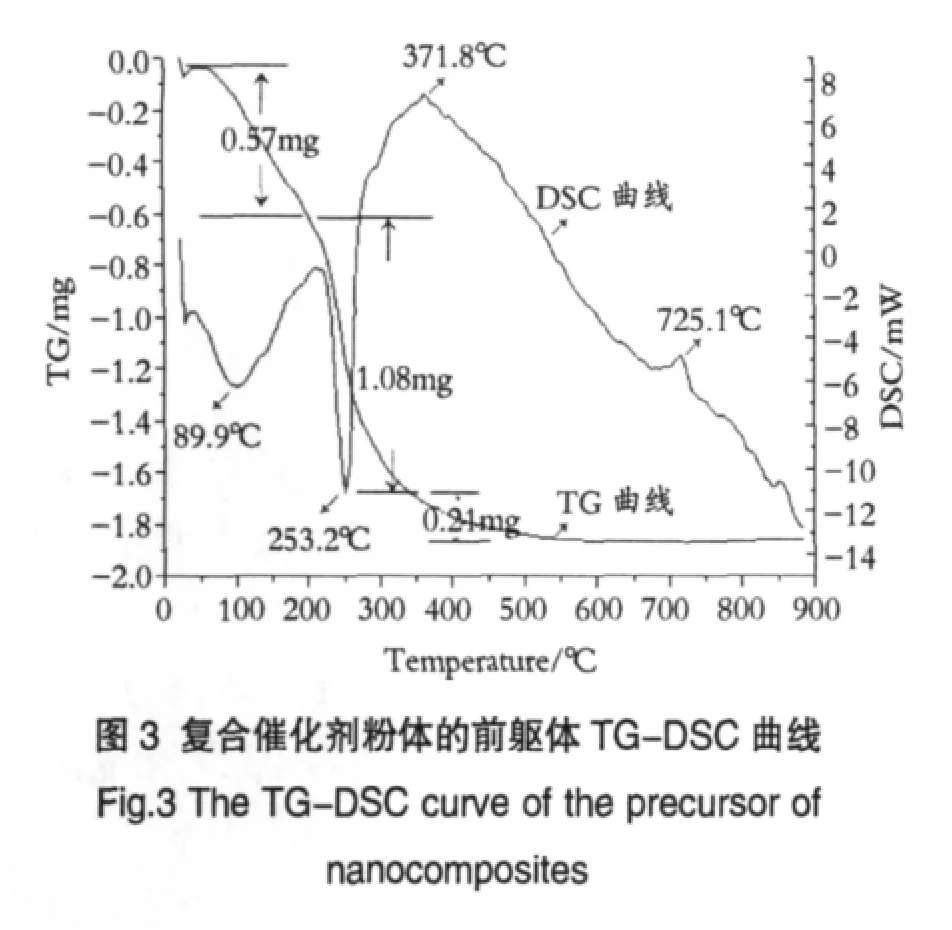
图3为ZnO∶SnO2=4∶1条件下制备的复合催化剂前躯体(14.277mg)的TG-DSC曲线。在TG曲线上,50~200℃失重 0.57mg,失重率为 3.86%,200~350℃失重1.08mg,失重率7.56%,350~600℃失重0.21mg,失重率1.47%,600℃以后几乎没有失重,并且在725.1℃附近也没有发生失重。在DSC曲线上89.8℃和253.2℃出现2个吸热峰。在371.8℃和725.1℃出现2个放热峰。结合TG-DSC曲线和XRD分析结果可知:89.8℃的吸热峰应该是由于前躯体表面的水,乙醇及附着物的挥发造成的,相应的有3.86%的失重率。253.2℃的吸热峰应该是由于前驱物Zn(OH)2和Sn(OH)4分解成ZnO和SnO2造成的,相应的有7.56%和1.47%的失重率。在371.8℃出现的放热峰应该是由于ZnO结晶放热造成的,725.1℃出现的放热峰应该是Zn2SnO4重结晶放热造成的。但是曲线上并未出现SnO2的结晶放热峰,可能是由于SnO2含量太少,放热与吸热中引起SnO2结晶放热峰不明显。
3.4 复合催化剂粉体的XRD分析
图4为ZnO∶SnO2=4∶1条件下的复合光催化剂前驱体在不同热处理温度保温2h所制备复合光催化剂粉体的XRD图。从图中可以看出,550℃焙烧时复合氧化物中检测到的强烈ZnO特征衍射峰,并且在2θ=27°和2θ=52°处检测到SnO2特征衍射峰,但衍射峰较弱。说明此时ZnO晶体已经形成并且生长完全,SnO2晶相已经形成,但是由于SnO2的量较少和晶体生长不完全,所以导致衍射峰较弱。650℃时,ZnO和SnO2衍射峰由弱变强,由宽变窄,说明在相同的保温时间2h下,650℃时,ZnO和SnO2结晶都趋于完整,晶粒尺寸变大。当温度达到750℃时,检测到有较弱的Zn2SnO4衍射峰,说明此时部分ZnO和 SnO2发生了反应,生成了 Zn2SnO4晶体,2θ=65~70°处三个ZnO的小峰变弱,也可以侧面说明上述结果。到850℃时,在2θ=35°处出现了Zn2SnO4的特征衍射峰,并且各处的衍射峰逐渐增多,而ZnO和SnO2的衍射峰量逐渐减弱,说明在850℃时,Zn2SnO4晶体逐渐增多,晶体生长趋于完整,但仍存在一定量的ZnO和SnO2晶体说明催化剂前躯体在850℃热处理后仍具有一定的催化能力。
3.5 复合催化剂粉体的TEM分析
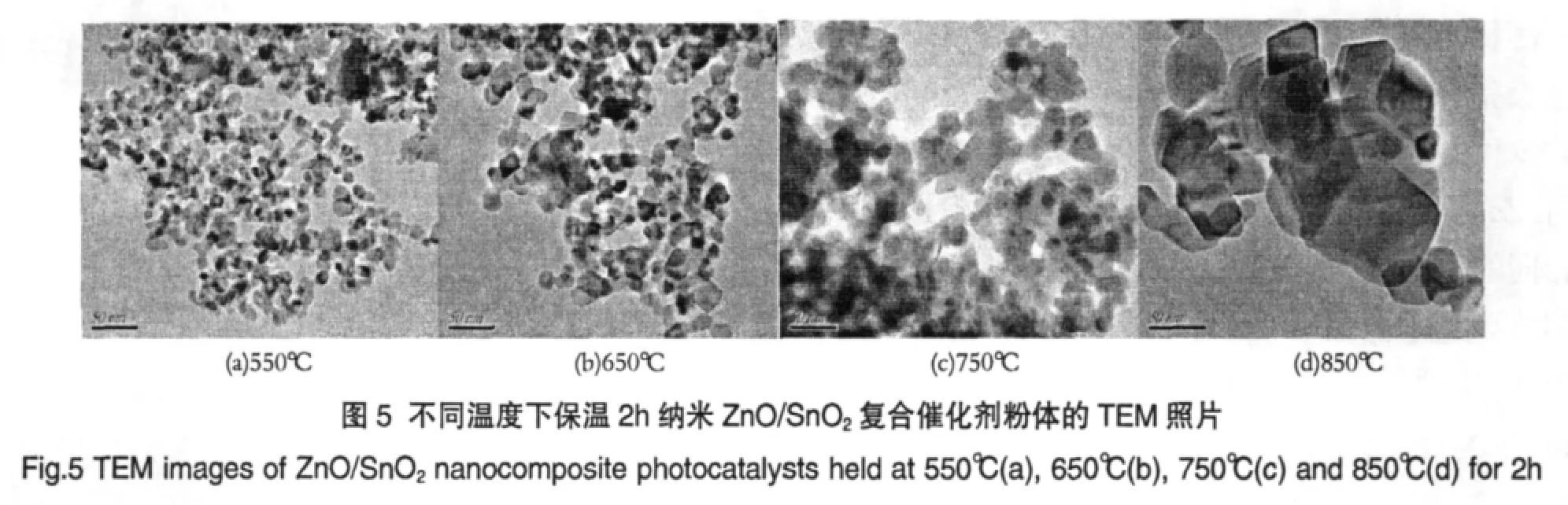
图5(a)、(b)、(c)和(d)分别为ZnO∶SnO2=4∶1条件下的复合光催化剂前驱体在550℃、650℃、750℃和850℃保温2h后热处理得到的纳米ZnO/SnO2复合光催化剂粉体的TEM照片。从图5(a)和(b)可以看出,复合氧化物粉体主要为球形状,随着温度升高,粒径逐渐增大但分散性仍然较好,主要分布在20~30nm。从图5(c)和(d)可以看出,复合氧化物的粒径较大,甚至超过100nm,并且团聚现象明显。表明温度升高后,复合氧化物的粒径变大,粒子分散性不好,容易团聚。
4 结论
(1)在本实验条件下,用ZnO/SnO2复合催化剂粉体,比同等条件下仅用纳米ZnO对甲基橙的降解率提高显著。
(2)在本实验条件下,ZnO/SnO2比例为4∶1,经650℃煅烧,保温2h后,所获得的样品的光催化活性最好,且其粉体颗粒粒径主要在20~30nm之间。
(3)随着热处理温度的升高,复合光催化剂的粒径增大,光催化活性先升高后降低,热处理温度为650℃时光催化活性达到最高,热处理温度高于750℃时,样品中出现Zn2SnO4晶体,ZnO/SnO2复合氧化物粉体的光催化活性逐渐降低。
1 Fujishima A and Honda K.Electrochemical photolysis of water at a semiconductor electrode.Nature,1972,238(5358):37~38
2桥本和仁,藤岛昭.图解光催化技术大全.北京:科学出版社, 2003
3高濂,郑珊,张青红.纳米氧化钛光催化材料及应用.北京:化学工业出版社,2002
4梁伟夏,莫伟彬.半导体光催化氧化技术的研究进展.化工新型材料,2009,37(3):18-20+33
5 Stakthivela S,Neppolianb B and Shankar M V.Solar Energy Materials&Solar Cells,2003,77(1):65~82
6 Akyol A,Yatmaz H C and Bayramoglu M.Applied Catalysis B: Environmental,2004,54(1):19~24
7周秉明,申利春,曹建新.纳米SnO2/ZnO复合氧化物的制备及制备条件对光催化性能的影响.化学研究与应用,2008,20(6): 705~709
8 J.Bandara,K.Tennakone and P.P.B.Jayatilaka.Composite tin and zinc oxide nanocrystalline particles for enhanced charge separation in sensitized degradation of dyes.Chemosphere, 2002,49(4):439~445
Abstract
ZnO/SnO2nanocomposites were prepared by coprecipitation method with SnCl4·5H2O,ZnNO3·6H2O,HCl and NaOH as raw materials,and characterized by TG-DSC,XRD and TEM.The photocatalytic activity of the nanocomposites with different ZnO/SnO2ratios and calcined at different temperatures was observed in their degradation of methyl orange.The results showed that the photocatalytic activity of ZnO was increased significantly when compounded with SnO2,and when the ratio of ZnO:SnO2was 4:1,the photocatalytic activity of the nanocomposite was the best;the nanocomposite calcined at 650℃for 2h had the best performance.
Keywords nanometer ZnO/SnO2powder,photocatalytic,coprecipitation,methyl orange
THE SYNTHESIS AND PHOTOCATALYTIC PROPERTIES OF ZNO/SNO2NANOCOMPOSITE
Huang Xinyou Deng Yuehuan Li Xiaoyi
(School of Materials Science and Engineering,Jiangsu University,Zhenjiang Jiangsu 212013,China)
TQ174.75
A
1000-2278(2010)04-0586-05
2010-06-28
邓悦欢,E-mail:dyhlvgyh@yahoo.com.cn

