1,2-二酮类化合物的合成研究进展
庄丹闻 崔冬梅
(浙江工业大学药学院,浙江 杭州310014)
1,2-二酮类化合物的合成研究进展
庄丹闻 崔冬梅
(浙江工业大学药学院,浙江 杭州310014)
1,2-二酮类化合物作为重要的有机合成中间体被广泛应用在高分子材料、农药、医药、化工原料等领域,在医药领域的应用主要是合成一些咪唑环、喹诺西林类的药物,也可以用于合成一些聚合物。本文概述了通过不同的原料,采用氧化、重排、亲核取代的方法得到1,2-二酮类化合物。
1,2-二酮;氧化;重排;亲核取代
1,2-二酮类化合物作为重要的有机合成中间体被广泛应用在高分子材料、农药、医药、化工原料等合成领域。如在高分子材料方面可用来合成一些导电聚合物[1]。在医药领域上主要用于合成一些含有咪唑环[2-4]、喹诺西林[5-6]等生理活性化合物。如1,2-二酮类化合物与醛、一级胺、醋酸胺在微波下可得到四取代咪唑环。咪唑基团作为组氨基侧链的一部分,起着多肽和蛋白质生物活性的主要作用。功能化的咪唑基团还有许多药理活性。如抗HIV、抗晕厥、钙拮抗剂和抑制剂、抗组胺、镇定等等作用。1,2-二酮类化合物也能与邻苯二胺类化合物反应可得到喹诺西林,喹诺西林是一种重要的含氮杂环化合物,有许多药理活性,如抗原虫、抗菌、抗真菌以及抗癌的药理活性。由于使用1,2-二酮类做为原料,克服了传统合成方法的催化剂昂贵、收率低、反应时间长、反应条件苛刻、操作步骤多等缺点。本文对1,2-二酮类化合物主要合成方法的相关文献进行综述。
1 合成方法
1.1 氧化法合成1,2-二酮
合成1,2-二酮的方法很多,主要方法是氧化法,通过不同的原料、不同的催化剂反应得到1,2-二酮。
1.1.1将带有α-活性氢单酮氧化成α-二酮
1.1.1.1利用PCC试剂氧化
SeO2是最早将单酮氧化成二酮的氧化剂,但作为还原产物的Se由于自身的性质,很容易形成硒化物,这样对反应带来不利的影响。而且Se元素有毒,如果处理不当会对环境造成影响[7]。
在1985年Carre M C[8]等人对该方法进行了改进,利用CuCl2-CuO做氧化剂将单酮氧化成二酮,用CH3COCH3做溶剂,但这种方法的缺点在于副产物太多。
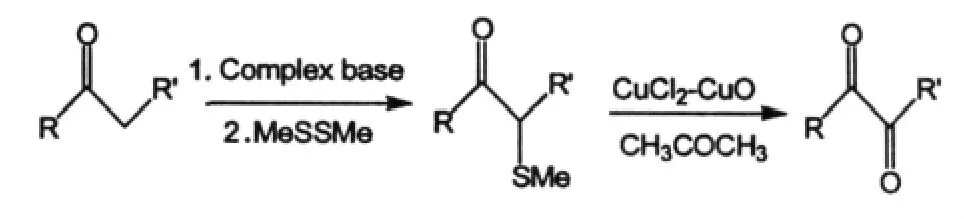
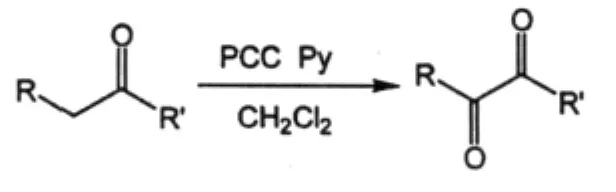
1988年Francesco Bonadies[9]等人采用了活性剂PCC氧化单酮得到二酮化合物。PCC是吡啶和CrO3在盐酸溶液中的络合盐,是橙红色晶体。它溶于CH2Cl2,使用很方便,在室温下便可将伯醇氧化为醛,而且基本上不发生进一步的氧化作用。
1.1.1.2 微波的无溶剂的氧化反应
2002年Jong Chan Lee等人[10]用吡啶N-氧化物和α-氧基酮在微波条件下进行了无溶剂的反应,发现这种方法反应条件温和,反应迅速,而且反应环境基本在中性条件下,收率也较高,普遍在80%以上。

1.1.2 1,2-二醇氧化得到1,2-二酮化合物
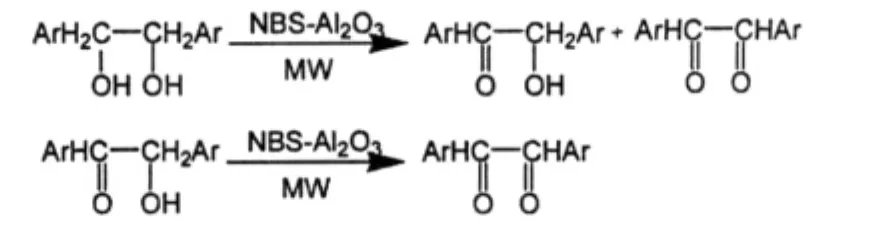
2008年Jitender M.Khurana[11]等人用NBSAl2O3在无溶剂的微波条件下,将1,2-二醇氧化得到1,2-二酮化合物。发现如果反应时间只有20 s,那么二醇中只有一个羟基被氧化成羰基,而将反应时间延长至3 min,就能得到二酮的产物,并且二酮收率都能达到98%~99%。
1.1.3氧化炔得到1,2-二酮化合物
1.1.3.1由氯化钯催化的由炔氧化得到二酮化合物
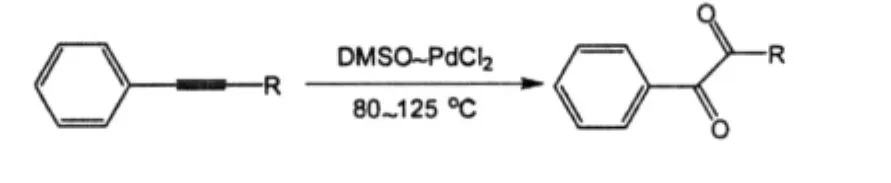
2001年M.S.Yusubov等人[12]用DMSO-PdCl2体系在80~125℃的温度范围下氧化炔,收率可达到55%~77%。该反应的作用机理主要是通过DMSO和Pd与三键配位,进而将炔氧化成1,2-二酮。
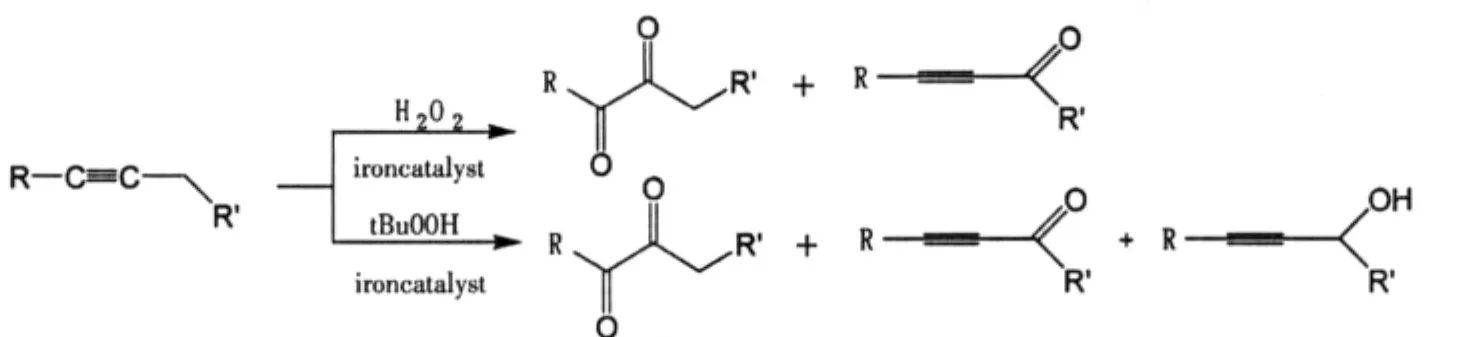
1.1.3.2由非血红素铁催化炔合成二酮化合物
2004年Ju Yeon Ryu等人[13]用非血红素铁配合物催化炔,发现二酮产物的形成与氧气的存在有很大的关系。在用过氧化氢或t-BuOOH做氧化剂时,在好氧条件下二酮为主要产物;但在厌氧条件下,与过氧化氢相比较,使用t-BuOOH作为氧化剂时,收率较低。
1.1.4氧化脱肟合成二酮化合物
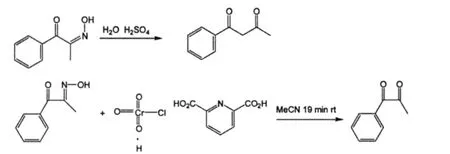
氧化脱肟合成二酮化合物的方法早在1943年就有报道,主要是在水中用硫酸做催化剂,收率为43%。
2002年Rahman Hosseinzadeh[14]等人开发了全新、快速、高效的脱肟催化剂2,6-二羧基吡啶氯铬酸盐。该氧化剂具有选择性好,收率高等优点,并且对原有羰基没有影响。
1.1.5联烯在纯态氧下的光氧化反应
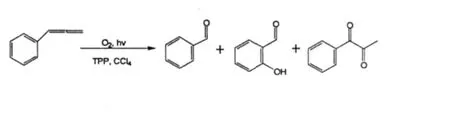
1991年Ihsan Erden等人[15]发现在钠灯的照射下,苯基联烯在四氯化碳卟啉的氧气饱和溶液下会缓慢发生反应,用1H NMR谱鉴定出所得的产物有3种。这个反应可能是经过1,2-,1,4-环加成模式进行反应,而且随着联烯结构的复杂化,产物的种类也会变多。
1.2 重排法合成1,2-二酮化合物
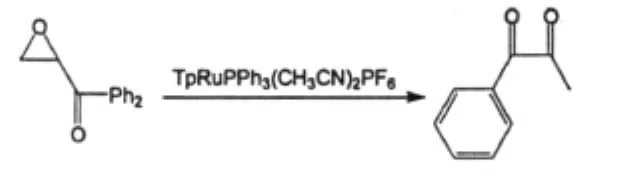
2003年Chang Chia-lung等人[16]用钌做催化剂对α,β-环氧酮进行重排反应,发现这个反应也可得到1,2-二酮产物。环氧化物在Lewis酸的存在下的重排可以得到醛酮。在大多数情况下由于开环的位置不同,会得到1,2-二酮和1,3-二酮两种产物。当使用常用的Lewis酸时,1,2-二酮的收率较低;而使用高氯酸镁时,1,2-二酮的收率可以达到80%以上,但催化剂要过量使用。
1.3 亲核取代合成1,2-二酮化合物
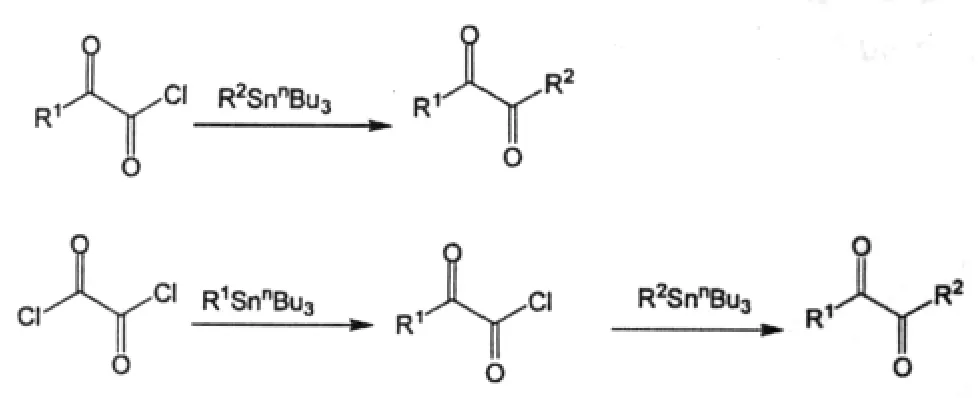
芳基-Sn键是一个良好的亲电取代试剂,芳基-氢化锡和酰氯能得到芳基酮,并且收率比较高。之前也有人做过用Pd催化的芳基-氢化锡试剂和酰氯的交叉耦连反应,但反应时间长,温度高,而且收率一般。在1980年和2004年,Tanaka M分别发表了用Bu3Sn-CN和Me3Sn-CONiPr2和酰氯在没有催化剂的条件下和酰氯发生交叉耦连反应得到酮。当Sn-C键在一定条件下可以激活α-杂原子,这样反应就可以在无催化剂条件下进行。但这两个方法只用在单酮的合成,于是,2008年Taigo Kashiwa bara和Masato Tanaka共同发现,酮酰氯和RSnnBu3不需要催化剂催化可得到二酮产物,并且该反应适用范围广泛,如以草酰氯为起始原料也可得到1,2-二酮化合物。
R1SnnBu3、R2SnnBu3分别为不同的R基取代的正丁基锡烷。
2 小结
综上所述,到目前为止,有关1,2-二酮类化合物的合成方法有一些报道,但存在一定的局限性,有的原料不易得到,有的选择性低并有副产物生成,有的要使用毒性较大的试剂及催化剂,限制了该类化合物的应用,所以针对1,2-二酮类化合物的高效率的合成方法有待进一步研究和开发。
[1]Arjan P Zoomblet,Jan Gilot,Marijin M Wienk,et al. Effect of extended thiophene segments in small band gap polymers with thienopyazine[J].Chem.Mater,2009,21:1663-1669.
[2]Mohammad R Mohammadizadeh,Alireza Hasaninejad, M Bahramzadeh.Trifluoroacetic acid as an efficient catalyst for one-pot,four-component synthesis of 1,2,4,5-tetrasubstituted imidazoles under microwave-assisted,solvent-free conditions[J]. Synthetic Communications,2009,39(18):3232-3242.
[3]Prashantha Kumar B R,Gyanendra Kumar,Sharma S Srinath,etal.Microwave-assisted,solvent-free,parallel synthesesand elucidation ofreaction mechanism forthe formation of some novel tetraaryl imidazoles of biological interest[J].Journal of Heterocyclic Chemistry,2009,46(2):278-284.
[4]NagalakshmiG.Synthesis and pharmacological evaluation of 2-(4-halosubstituted phenyl)-4,5-diphenyl-1H-imidazoles[J],E-Journal of Chemisrty,2008,5(3):447-452.
[5]Alireza Hasaninejad,Abdolkarim Zare,Mohammad Ali Zolfigol,et al.Zirconium tetrakis(dodecyl sulfate)[Zr(DS)4]as an efficientlewisacid-surfactantcombined catalystforthe synthesis of quinoxaline derivatives in aqueous media[J]. Synthetic Communications,2009,39:569-579.
[6]Zhao Zhijian,David D Wisnoski,Scott E Wolkenberg, et al.General microwave-assisted protocols for the expedient synthesis of quinoxalines and heterocyclic pyrazines[J]. Tetrahedron Letters,2004,45:4873-4876.
[7]Acheson R M.Some experiments with cyclopentanones [J].J Chem Soc,1956,11:4232-4237.
[8]Carre M C,Caubere P.A very efficient preparation of 1,2-diketones[J].Tetrahedron Letters,1985,26(26):3103-3106.
[9]Francesco Bonadies,Carlo Bonini.Oxidation of active methylene compounds by pyridinium chlorochromate[J]. Synthetic Communications,1988,18(13):1573-1580.
[10]Jong ChanLee,Hong-Jun Park,Jin Young Park. Rapid microwave-promoted solvent-free oxidation of αmethylene ketones to α-diketones,Tetrahedron Letters[J].2002, 43(32):5661-5663.
[11]JitenderM Khurana,ReemaArora.Microwave assisted solvent free oxidation of hydrobenzoins,benzoins and alcohols with NBS-Al2O3[J].ARKIVOC,2008:211-215.
[12]Yusubov M S,Filimonov V D,Chi Ki-Whan. Oxidation of alkylphenylacetylenes and diakylacetylences on palladium catalysts in DMSO [J].Russian Chemical Bulletin, 2001,50(4):649-653.
[13]Ju Yeon Ryu,Soonyoung Heo,Philsung Park,et al. Alkyne oxidation by nonheme iron catalysts and hydroperoxides [J].Inorganic Chemistry Communications,2004,7:534-537.
[14]Rahman Hosseinzadeh,Mahmood Tajbakhsh Moham mad,Yazdani Niaki.2,6-Dicarboxypyridinium chlorochromate:a mild,efficient,and selective reagent for oxidative deprotection of oximes to carbonyl compounds[J].Tetrahedron Letters,2002, 43(51):9413-9416.
[15]Ihsan Erden,Tomas R Martinez.Chemistry of singlet sxygen.dye-sensitized photooxygenation ofaylallenes[J]. Tetrahedron Letters,1991,32(16):1859-1862.
[16]Chang Chia-Lung,Manyam Praveen Kumar,Liu Rai-Shung.A highly efficient ruthenium-catalyzed rearrange ment of α,β-epoxyketones to 1,2-Diketones[J].Journal of Organic Chemistry,2003,69(8):2793-2796.
[17]Taigo Kashiwabara,Masato Tanaka.Synthesis of 1,2-diketones by the transition metal-catalyst-free reaction of αoxo acid chlorides or oxalyl chloride with organostannanes[J]. Journal of Organic Chemistry,2009,74:3958-3961.
The Synthesis Development of 1,2-Diketone
ZHUANG Dan-wen,CUI Dong-mei
(Zhejiang University of Technolgy,Hangzhou 310014,China)
1,2-diketones as an important synthetic intermediate is widely used in polymer materials, pesticides,pharmaceuticals,chemicals and other synthetic fields.It can be used to synthesize a number of drugs with imidazoles,quinoxalines,it also can be used to synthesize some conductive polymer.This note outlines the different synthesis methods by different reactants.
1,2-diketone;oxidation;rearrangement;nucleophilic substitution
1006-4184(2010)08-0013-04
2010-04-13
庄丹闻(1986-),女,浙江杭州人,浙江工业大学在读研究生,药物化学专业。

