基于MR图像的脑转移瘤计算机辅助检测
聂生东 刘兴昇 孙希文 陈兆学
1(上海理工大学医学影像工程研究所,上海 200093)
2(上海市肺科医院影像科,上海 200433)
引言
脑转移瘤系指原发于身体其他部位的肿瘤细胞转入颅内,占颅内肿瘤的10% ~15%。脑转移的肿瘤原发部位以肺、乳腺、消化道肿瘤及肾癌为常见,其中乳腺癌脑转移占16% ~25%,肺癌脑转移占30% ~40%。
脑转移瘤的生长速度非常快,其体积倍增时间平均只有25 d,如不迅速采取合适的治疗措施,患者的平均生存期一般不超过半年。除了能够迅速导致患者死亡,肿瘤细胞扩散到脑内后还会挤压、干扰甚至破坏正常的脑组织,引起一系列的症状,如头痛、癫痫、失语、偏盲、恶心、瘫痪等。脑转移瘤也可能会使患者感到疲劳乏力,还可能导致患者记忆方面的障碍,使患者的生存质量大打折扣。如果能够早期发现脑转移瘤,并对其进行治疗,可有效延长患者的生存时间,提高患者的生存质量[1-2]。
目前,能够对脑转移瘤进行有效诊断的工具为磁共振成像(MRI)[3]。为了早期诊断脑转移瘤,需要对全脑实施MRI的薄层扫描,这样就会产生大量MRI图像。由于脑转移瘤在早期较小(小于10 mm),即使在对比增强磁共振图像上,早期转移瘤与周围组织的对比度也不明显,在高分辨率的图像上也只出现在三四层厚度的图像,临床上很容易漏诊。另外,要从大量MRI图像中正确识别出较小的脑转移瘤,对放射科医生来说也是一项非常困难的工作,特别是在经历了长时间、高强度的读片之后,放射科医生难免会产生视觉疲劳,极易漏掉微小的病灶。
计算机辅助检测(computer-aided detection,CAD)技术的发展,为解决脑转移瘤的早期诊断问题奠定了基础。大量研究证明,CAD能够有效减轻放射科医生的读片负担,提高其诊断的正确率[4-5]。近年来,CAD已经在乳腺癌、肺癌及直肠癌的早期诊断中发挥着越来越重要的作用并有大量的文献报道,但在脑转移瘤早期诊断中的研究目前国内外均未见相关报道。为此,在国内外CAD研究的基础上,基于3 D模板匹配技术,本研究提出了一套基于MR图像的脑转移瘤计算机辅助检测的方法。首先,建立合适的脑转移瘤模板;然后,在MR序列图像数据中寻找与模板相似的区域,相似度较高的区域很可能就是脑转移瘤。采用12个病例数据对本方法的性能进行了测试,这12个病例共有27个直径不超过8 mm的脑转移瘤。利用本研究方法检测出其中的22个,检测正确率约为81.5%;假阳性共59个,假阳性率为每层图像平均0.0378个。从以上检测结果可以看出,本研究提出的基于MR图像的脑转移瘤计算机辅助检测方法为脑转移瘤的早期诊断奠定良好的基础。
1 脑转移瘤计算机辅助检测方法
基于MR图像的脑转移瘤计算机辅检测方法的具体流程如图1所示。基本步骤为:通过图像预处理,从MR序列图像中获取脑实质;建立脑转移瘤模板;利用模板匹配技术,计算归一化交叉相关系数(normalized cross correlation coefficient,NCCC);根据计算得到的NCCC值,确定疑似病灶,并给予标记。标记出的疑似病灶,可作为第二读者(second reader)意见提供给医生,最终由医生给出诊断结论。下面对各个步骤进行介绍。
1.1 图像预处理
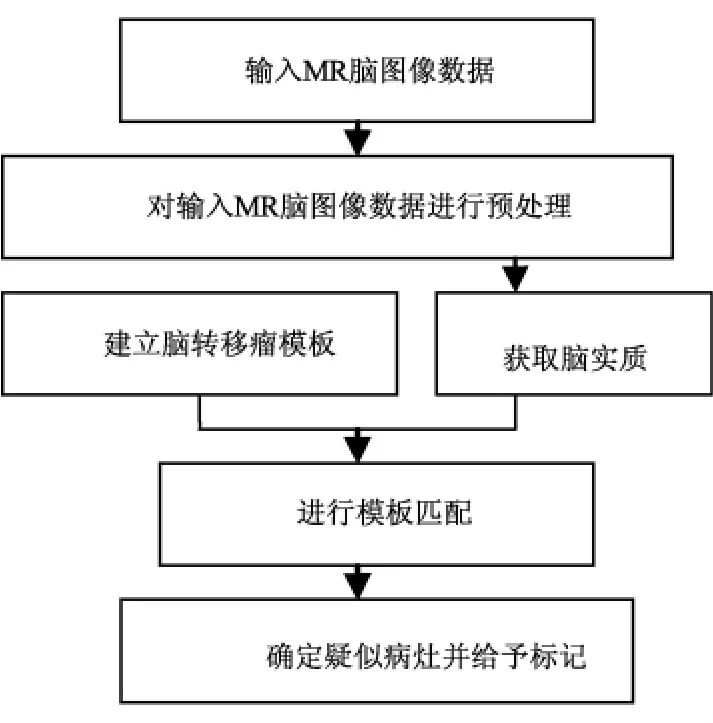
图1 本方法的流程Fig.1 The flowchart of our method
所处理的对象是3D MR脑图像数据,图像矩阵为250像素×250像素×130像素,因此处理的数据量非常大。检测对象是脑转移瘤,而脑转移瘤应处于脑实质区域。因此,为了减少处理时间,应将模板匹配的处理区域限定在脑实质中。本研究图像预处理的目的,就是从MR脑图像数据中把脑实质提取出来。
由于脑部图像结构复杂,到目前为止还没有一种全自动的图像分割方法,能从脑部磁共振图像中有效分割出脑实质。因此,采用半自动分割的方法,分4步从原始图像中分割出脑实质。首先,采用BET(brain extraction tool)对脑组织做一次自动分割[6],得到一个近似的脑实质模板;其次,以这个模板为初始条件,再次使用BET进行自动分割得到一个更为精确的结果;然后,使用Bioimage Suite读入原始图像与全脑模板[7],将模板作为objmap覆盖在原始图像之上,手动修改objmap使之恰好包含全部脑组织;最后,将手动修改过的模板作为二值图像输出,并用它从原始图像中提取出脑实质,最终得到仅包含脑实质的3 D图像。至此,预处理步骤结束,后续的处理步骤都在该3 D图像范围内进行。
1.2 建立脑转移瘤模板
在磁共振图像上观察到的脑转移瘤,从三维结构上看通常都表现为高亮的球形病灶,而且有明显的边界(margin)[8-9]。因此,建立的脑转移瘤模板应该具有这两个特征(球形和边界)。为了进一步提高边界的清晰度,借鉴文献[10]的方法在表示脑转移瘤的高亮度像素周围加上灰度为零的像素,由灰度为零的像素构成的区域称之为留白(padding)。为了将一个包含留白的球体体素化,首先要建立一个空间坐标系。假设坐标系原点也是球体的球心,那么整个模板空间就被该坐标系分成8个区域,如图2所示。这8个区域都关于原点、某个坐标轴或某个坐标平面对称,只要计算出其中的1/8,经过3次翻转就能得到整个模板。为直观起见,计算由x轴、y轴、z轴的正方向夹成的1/8部分。假设体素坐标为(x,y,z),坐标值以体素个数为单位;体素的长、宽、高分别为 a、b、c,则可以计算出每个体素的中心到坐标原点的距离

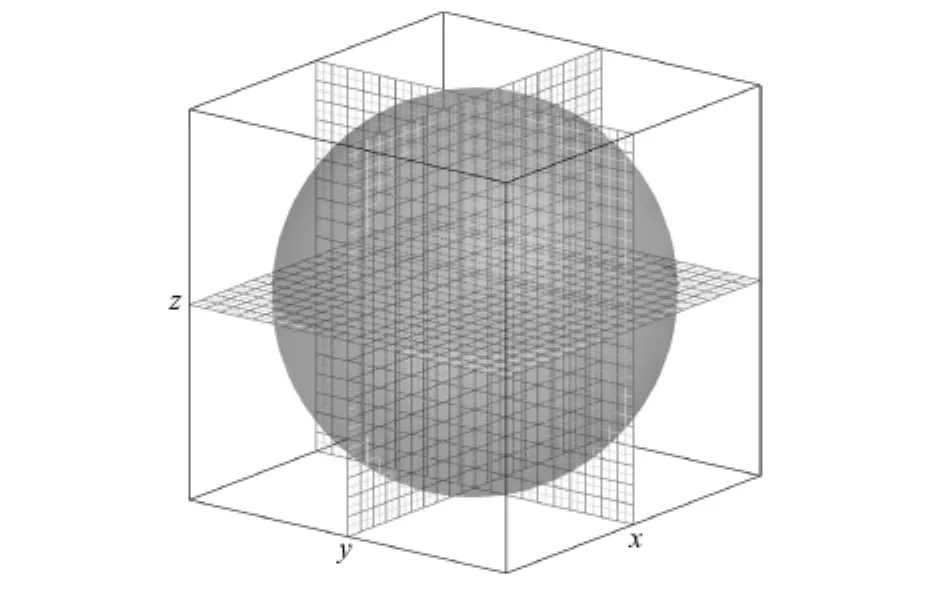
图2 模板所在坐标系Fig.2 The brain metastases template sketch map
另外,医学图像中,处于边界上体素的灰度值是同一体素中不同组织灰度值的加权平均[11],这就是医学图像中的部分容积效应(partial volume effect)。为降低部分容积效应对脑转移瘤检测的影响,所建立的脑转移瘤模板也应尽可能模仿出部分容积效应。
如果体素到球心的距离小于球体的半径,那么这个体素赋值为1,否则赋值为0,这样可确保球体内为高亮区域、球体外为黑色区域。x,y,z的定义域可以通过确定。
通过以上方式计算出来的模板虽然是一个球体,但却不能表现出部分容积效应。为此,可将体素的长、宽、高分别减少到原来的1/50,则一个原始体素即被分成50×50×50个体素。重新计算距离并赋值,然后再将分割过的体素合并。这样每一个合并后的体素包含125000个小体素,就能够模拟出部分容积效应。
图3给出了一个脑转移瘤球形模板的不同切片图,从中可以清楚地看到边界上的部分容积效应,球形模板的边界到图像边界的这段空白就是用来表示脑转移瘤与周围组织之间边界的留白。共建立了35个不同直径与留白的模板。直径的范围是2.4 ~ 8.0 mm,以 0.8 mm 递增,留白为 0.8 ~ 4.0 mm,也以0.8 mm递增。

图3 一个脑转移瘤模板的不同切片Fig.3 Different slice of one brain metastases template
1.3 模板匹配
模板匹配是本方法的关键步骤。检测图像特征的算法有很多种,如序贯相似性检测算法(sequential similarity detection algorithm,SSDA)梯度下降法、Snake(活动轮廓线)方法,以及一些基于小波的多分辨率算法等。但到目前为止,还没有出现一种被广泛认可且能够取代归一化交叉相关系数(normalized cross correlation coefficient,NCCC)的算法。NCCC的计算不需要额外的参数,在大多数情况下可作为模板匹配的默认算法[12]。本研究就采用NCCC来度量模板与图像上某一区域的相似程度。
使用交叉相关系数进行模板匹配的思想,来源于图像与模板间欧氏距离的测量[12],即
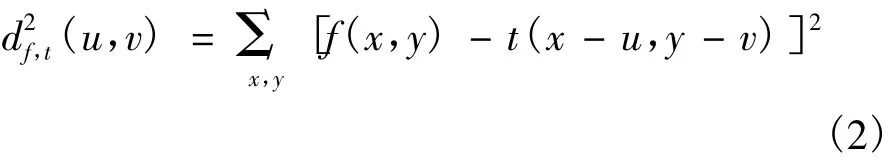
式中,f代表图像,u、v代表模板在图像上的当前位置;在每次计算模板与其在图像上所覆盖区域的相似度时,x、y用以表示模版与图像上的像素坐标。
式(2)变形后,可得
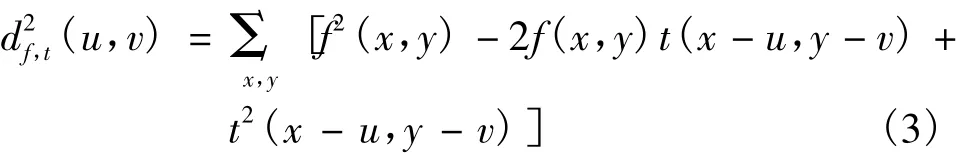
式中,t2(x-u,y-v)是常量,如果 f2(x,y)也可以近似地看作常量,那么剩下的交叉系数项

就可以作为图像与模板间相似性的度量。
使用式(4)作为模板匹配的标准有以下缺点:如果图像能量f2(x,y)随着位置改变,那么c(u,v)就会导致匹配失败。比如,一个和模板完全匹配的低亮度区域的得分可能会低于一个与模板并不相似的高亮度区域;c(u,v)的值域随着模板的大小而变化;式(4)会随着图像的强度而变化。将图像向量与模板向量归一化以后,就可以克服上述问题,有
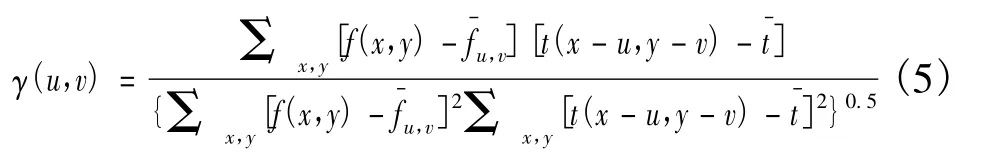
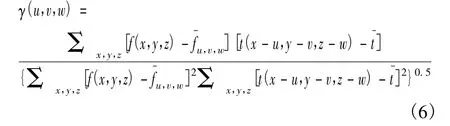
式(6)即为所采用的计算NCCC的公式。
图4为图像匹配前后的效果比较。图4(a)为原始3D数据中包含脑转移瘤的某层切片,图4(b)为图4(a)的NCCC图像,红色圆圈标记的是转移瘤。从图4(a)可以看出,原始图像中血管与脑转移瘤都是高亮区,难以识别出脑转移瘤;但在图4(b)中,NCCC图像中的脑转移瘤所在区域的亮度最高,很容易识别出脑转移瘤。
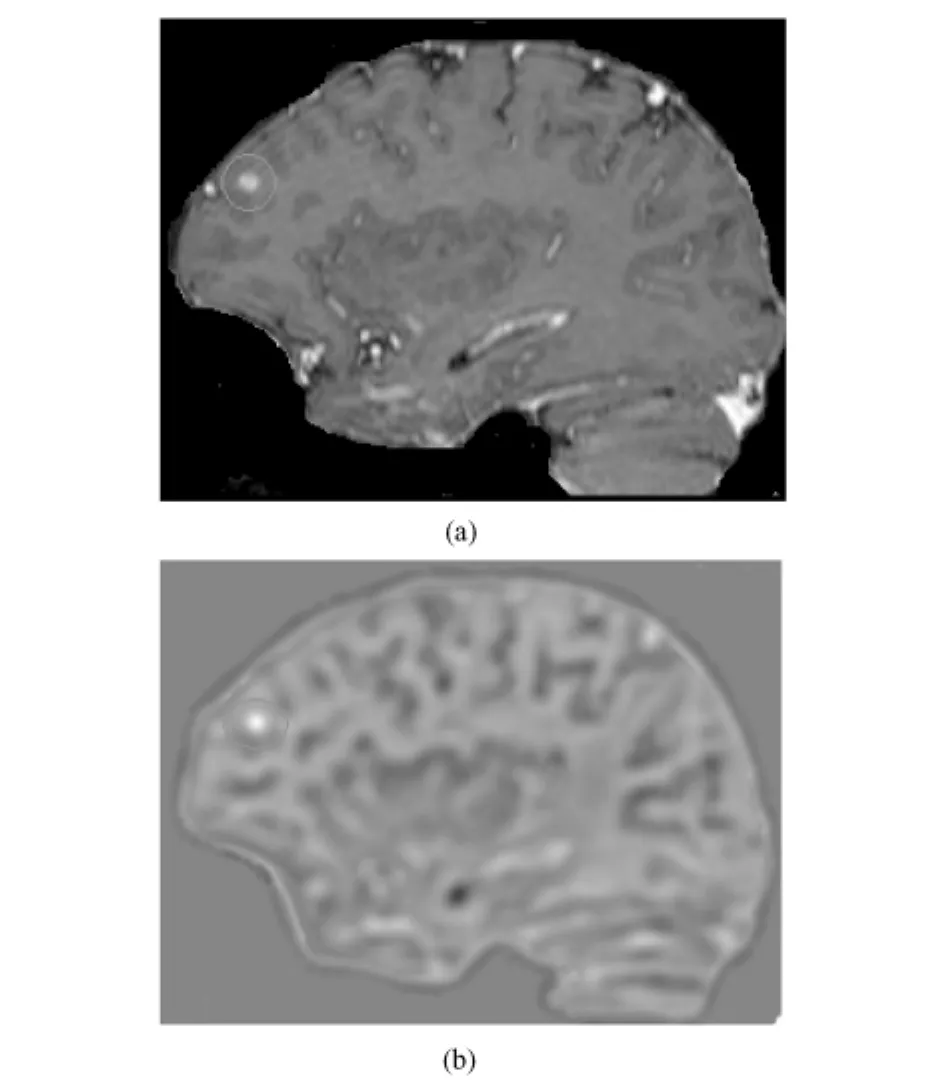
图4 图像匹配前后比较。(a)处理前;(b)处理后Fig.4 The result of before and after template matching processing.(a)before processing;(b)after processing
1.4 疑似病灶的检测并标记
模板匹配结束后,每一个病例都能得到一系列NCCC图像,只要设置合适的阈值,对其进行简单的阈值处理就能得到疑似病灶。由于相似的模板一定会重复检测出同一个病灶,这造成了在疑似病灶中会存在大量的冗余。因此,在计算脑转移瘤的个数与位置之前,首先要去除这些冗余。本研究将每一个病例阈值处理后所得到的二值图像进行逻辑与运算,通过这种方式来去除冗余。
包含疑似病灶的二值图像往往并不能引起医生的兴趣,医生感兴趣的是更为直观的信息,如疑似病灶的个数、位置等,这就需要利用连通成份标记算法从二值图像中提取这些信息。本研究使用的算法参考了文献[13],这种方法需要依次遍历图像两次,具体步骤如下:
在第一次遍历时,如果当前体素为1,则获取其邻域的体素值。如果邻域的体素值都为0,则赋予当前体素一个惟一的值,继续遍历;否则,将邻域中最小的体素值赋予当前体素,继续遍历。如果在某体素的邻域中发现了不同的体素值时,这些标记值就被称为等价标记,它们标记的是同一个对象,这种等价关系在第一次遍历时也需要记录下来。
第二次遍历主要处理等价标记,将所有等价标记用唯一的数值来重新标记,这样每一个检测对象就都被赋予了一个惟一的数值。通过这两次遍历,就能够得到脑转移瘤的个数,同时在第二次遍历的过程中也能很容易地计算出脑转移瘤。
2 参数优化选择
本方法涉及的参数有两个,一个是模板中留白的大小,另一个是检测疑似病灶时所设置的NCCC阈值。在测试过几个病例数据之后,发现随着阈值或留白的增大,本方法的敏感性与假阳性个数都有所下降。假阳性个数的下降是所希望的,但敏感性的降低是不愿看到的。因此,为了在降低假阳性的情况下,尽可能提高敏感性,有必要对所使用的两个参数进行优化选择。
所使用的图像数据均由上海市肺科医院影像科Philip 1.5 T磁共振成像扫描仪所得,扫描层厚为1 mm,图像矩阵为250像素×250像素×130像素。采用11个直径不超过8.0 mm的脑转移瘤病例(共有27个脑转移瘤)对上述两个参数进行测试,并绘制 了 FROC(free-response receiver operating characteristic)曲线,如图5所示。图中共有25个点,每一个点都代表一种留白与NCCC阈值的组合。对于每一条曲线来说,从左到右的5个点对应的阈值依次为 0.55,0.525,0.5,0.475,0.45。箭头所指为选定的最优参数。
从图5可以看出,阈值为0.5,留白为1.6 mm的点最靠近左上角。在这个点上,敏感性为83.2%,假阳性率为每层图像0.034645个。因此,这一组参数就被确定为最优参数。
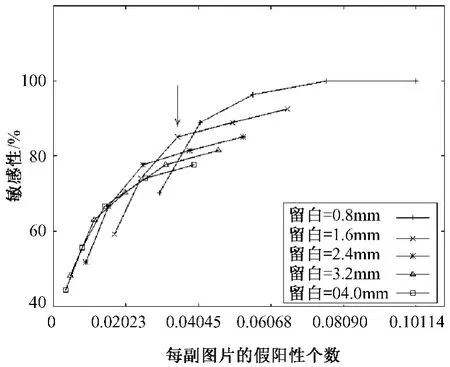
图5 FROC曲线Fig.5 The curve of FROC
3 性能评价与讨论
在确定最优参数后,使用12个病例数据,对所设计的脑转移瘤自动检测方法的性能进行了测试,这12个病例共有27个直径不超过8 mm的脑转移瘤。使用最优参数时,检测出22个脑转移瘤,整体检测的正确率约为81.5%;假阳性共59个,假阳性率为平均每层图像0.0378个。由于目前国内外均没有基于MR图像的脑转移瘤计算机辅助检测技术的文献报导,故该性能指标无法与相关文献进行比较。另外,还对直径大小不同的脑转移瘤进行检测实验,结果如表1所示。

表1 不同大小脑转移瘤的检出率Tab.1 The sensitivity for brain metastases of different size
从表1的统计结果可以看出,本方法对于小型脑转移瘤的识别正确率较高,对4 mm以下的脑转移瘤可以达到90% 以上的检测正确率,这对于脑转移瘤的早期诊断是非常有意义的。由表2可知,在总共出现的59个假阳性中,有21个是颅内静脉窦,而颅内静脉窦的直径一般大于4 mm。因此,之所以对4 mm以下脑转移瘤的检测准确率较高,可能的原因是在利用本方法对4 mm以上的脑转移瘤进行检测时,极有可能把颅内静脉窦错误地划分为脑转移瘤。而对4 mm以下的脑转移瘤进行检测时则不存在这个问题。因此,利用本方法对4 mm以下的脑转移瘤进行检测的准确率比较高,对于脑转移瘤的早期诊断是非常有意义的。
与近年来基于CT图像的肺结节计算机辅助检测的研究比较[14],本方法的检测正确率比较好,但假阳性相对偏高。根据对所产生的假阳性的分析,结果发现59个假阳性中的30个分布在颅内静脉窦与颅内颈动脉的分支(见表2)。这说明超过半数的假阳性出现在几个固定区域,如果能根据假阳性的这种分布特点设计相关方法加以去除,就能够进一步降低本方法的假阳性率。
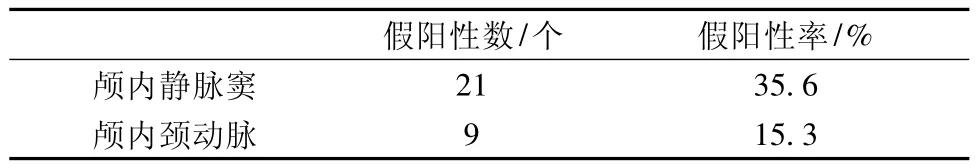
表2 颅内静脉窦与颅内颈动脉所占的假阳性比例Tab.2 The false positive rate of sinus and carotid
图6标示出假阳性常出现的区域,图6(a)圆圈标记的是被误认为脑转移瘤的颅内静脉窦,图6(b)圆圈标记的是被误认为脑转移瘤的颅内颈动脉。
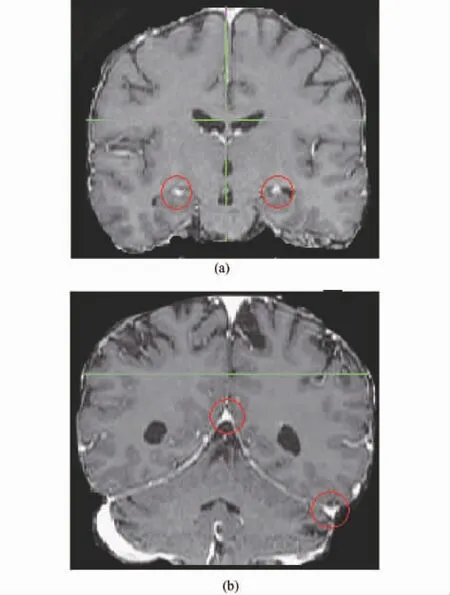
图6 假阳性常出现区域。(a)颅内静脉窦的位置;(b)颅内颈动脉的位置Fig.6 The area of the false positive frequent arisen.(a)the location of cerebral venous sinus;(b)the location of cerebral carotid.
4 结论
脑转移瘤是一种严重威胁患者生命的恶性肿瘤,对临床医生来讲,早期诊断存在很多困难。为此,基于3D模板匹配技术,本研究设计了一种基于MR图像的脑转移瘤计算机辅助检测方法。从实验结果看出,该方法的检测正确率较好,尤其对小于4 mm的微小脑转移瘤高达92.9%,这可为辅助放射科医生对脑转移瘤进行早期诊断奠定基础。本方法存在的主要问题是假阳性率偏高,但产生的假阳性超过半数分布在静脉窦与颅内动脉的分支上。因此,如果能够设计特定模式,将这些假阳性与脑转移瘤区分开来,就能够大大降低本方法的假阳性率,这将是笔者需要继续深入研究的内容。另外,在AMD3400+、DDR2667 MHz 1G的计算条件下,利用本方法处理一个病例(130幅250像素×250像素的图像序列)的时间约为5 min,进一步的工作是利用GPU并行计算技术实现相关算法,以便能大大缩短程序运行的时间。
[1]Charles JV,Hanny HR,Evert MN,et al.Treatment of single brain metastasis:radiotherapy alone or combined with neurosurgery[J].Annals of neurology,2004,33(6):583-590.
[2]Lohr F,Pirzkall A,Hof H,et al.Adjuvant treatment of brain metastases[J].Journal of Surgical Oncology,2001,20(1):50-56.
[3]李彦增.MRI诊断脑转移瘤的价值[J].实用医学影像杂志,2002,3(2):83-85.
[4]蒋红兵.计算机辅助诊断的应用简述[J].现代医学仪器与应用,2007,19(5):10-12.
[5]刘延彤,李茂星,叶建军.计算机辅助诊断在医学影像诊断中的新进展[J].西北国防医学杂志,2006,27(6):56-57.
[6]Smith SM.Fast robust automated brain extraction[J].Human Brain Mapping,2002,17(3):143-155.
[7]Papademetris X,Jackowski M,Rajeevan N,et al.BioImage Suite:An integrated medical image analysis suite[EB/OL].The Insight Journal,http://hdl.handle.net/1926/37,2005,1:3.
[8]Ranasinghe MG,Sheehan JM.Surgical management of brain metastases[J].Neurosurgical Focus,2007,22(3):1-7.
[9]Jagannathan J,Sherman JH,Mehta GU,et al.Radiobiology of brain metastasis: applications in stereotactic radiosurgery[J].Neurosurgical Focus,2007,22(3):1-5.
[10]Wang P,DeNunzio A,Okunieff P,et al.Lung metastases detection in CT images using 3D template matching[J].Medical Physics,2007,34(3):915-922.
[11]McRobbie DW,Moore EA,Graves MJ,et al.MRI from Picture to Proton[M].Cambridge: Cambridge University Press,2003.41-42.
[12]Lewis JP.Fast normalized cross-correlation[J].Circuits,Systems,and Signal Processing,2009,28(6):819-843.
[13]Stefano LD,Bulgarelli A.A simple and efficient connected components labeling algorithm[A].In: 10th International Conference on Image Analysis and Processing(ICIAP′99)[C].Venice:IEEE,1999.322-327.
[14]聂生东,孙希文,陈兆学.基于CT图像的肺结节计算机辅助检测技术的研究进展[J].中国医学物理学杂志,2009,26(2):37-41.

