反相高效液相色谱法测定注射用头孢美唑钠的含量
边 原,何 林,夏祺悦
(四川省医学科学院·四川省人民医院药剂科,四川 成都 610072)
头孢美唑钠(cefmetazole sodium)近年来广泛应用于临床,对革兰阳性菌和阴性菌均具有良好的抗菌效能,尤其是耐甲氧西林金黄色葡萄球菌(MRSA)、脆弱拟杆菌及厌氧菌[1],对各种"-内酰胺酶也有很强的耐受性和稳定性,体内分布好,不良反应少[2]。但头孢美唑钠的稳定性低,故笔者对其粉针剂用生理盐水配制为注射液后在常用试验条件下的稳定性进行了考察,以便为开展临床动物试验提供依据,现报道如下。
1 仪器与试药
2690型高效液相色谱仪,包括中央控制器、高压泵、全自动进样器、996二极管阵列检测器、Millennium Chromatography Manager色谱数据工作站(美国Waters公司);BP 211D型十万分之一电子分析天平(德国Sartorius公司)。头孢美唑对照品(美国Rockville公司,批号为1097782);注射用头孢美唑钠(辽宁海思科制药有限公司,批号为081001);甲醇为色谱纯,磷酸二氢铵、氢氧化四丁基铵、四氢呋喃为分析纯,试验用水为蒸馏水。
2 方法与结果
2.1 色谱条件
色谱柱:Diamonsil C18柱(150 mm ×4.6 mm,5μm);保护柱:Dikma Easy Guard C18柱(8 mm ×4 mm,5μm);流动相:以 10%磷酸调pH至4.5±0.1的磷酸二氢铵溶液(5.75 g磷酸二氢铵溶解在700 mL水中)-甲醇-四氢呋喃-10%四丁基氢氧化铵(700∶280∶25 ∶12.8);流速:1 mL/min;柱温:30 ℃ ;检测波长:272 nm;灵敏度:0.03921 AUFS。
2.2 溶液制备
取头孢美唑对照品适量,精密称定,加蒸馏水溶解并制成每1 mL中含0.2 mg的溶液,作为对照品溶液;取注射用头孢美唑钠适量,精密称定,加生理盐水溶解并制成每1 mL中含0.2 mg的溶液,作为供试品溶液;分别取头孢美唑对照品溶液0.05,0.5,1,2,3,4,5 mL,置10 mL量瓶中,以流动相稀释至刻度,即得质量浓度分别为 1,10,20,40,60,80,100μg/mL 的标准曲线工作液。
2.3 方法学考察
系统适用性试验:在上述色谱条件下,取对照品溶液和供试品溶液20μL分别进样。结果出峰时间均为5.17 min,色谱峰很好,拖尾因子为1.01,且无内源性杂质峰干扰。高效液相色谱图见图1。
标准曲线制备:取2.2项下各标准曲线工作液20μL进样测定,以峰面积积分值(Y)对质量浓度(X)进行线性回归,得回归方程(权重 W=1/C2)Y=2.65×104X-2.74×103,r=0.9999( n=7)。结 果 表明头孢美唑质量浓度在1~100μg/mL范围内与峰面积积分值线性关系良好。
精密度与准确度试验:配置质量浓度分别为10,40,80μg/mL的对照品溶液,分别于同日内连续测定5次和连续测定 5 d,计算日内、日间精密度和准确度。结果见表1。
加样回收试验:取头孢美唑对照品适量,精密称定,加生理盐水溶解并制成0.2 g/L的溶液,再分别配制成质量浓度为10,40,80μg/mL的对照品溶液,各取20μL进样,计算方法回收率,结果见表2。

图1 高效液相色谱图
表1 精密度与准确度试验结果()
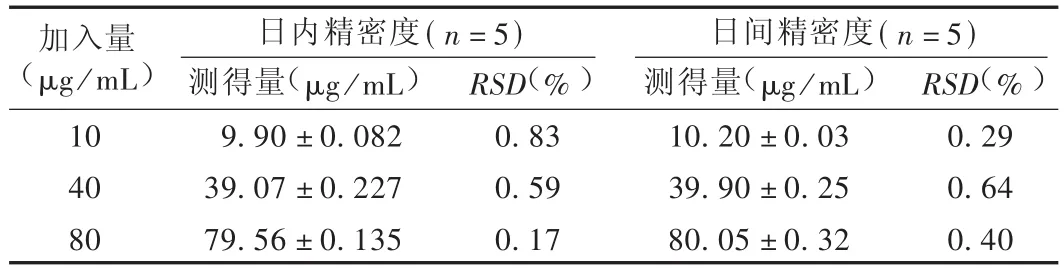
表1 精密度与准确度试验结果()
加入量(μg/mL)104080日内精密度(n=5) 日间精密度(n=5)测得量(μg/mL)9.90±0.08239.07±0.22779.56±0.135 RSD(%)0.830.590.17测得量(μg/mL)10.20±0.0339.90±0.2580.05±0.32 RSD(%)0.290.640.40

表2 加样回收试验结果(n=5)
2.4 样品含量测定
取2.2项下对照品溶液和供试品溶液各20μL,分别注入液相色谱仪,记录色谱图。按照外标法以峰面积进行计算。对3批样品分别同法测定5次,结果3批样品中头孢美唑的含量分别为标示量的 92.92%,93.90%,94.29%,平均 93.70%,RSD为 0.75%(n=5),符合《中国药典》所规定不低于86%的要求。
2.5 稳定性考察
取2.2项下新配制的对照品溶液,稀释成质量浓度分别为10,40,80μg/mL的溶液,依法进行检测。结果于4℃放置5 d后3种溶液的质量浓度分别为(10.17 ±0.05)μg/mL,(39.90 ±0.10)μg/mL,(79.05±0.89)μg/mL,RSD 分别为 0.05%,0.26%,1.12%,表明5 d内头孢美唑钠对照品溶液稳定性良好。
精密称取注射用头孢美唑钠适量,用生理盐水配制成临床动物试验所需3种质量浓度(33.5,67.0,134.0 g/L)的供试品溶液,分别于室温(20℃)和低温(4℃)下避光保存,临测前用流动相稀释成质量浓度分别为16.75,33.50,67.00μg/mL的供试品溶液,使其测量值在标准曲线的线性范围内。结果表明供试品溶液在两种存放条件下放置0~8 h稳定性良好,在室温避光放置3 d内、4℃下避光放置5 d后稳定性较好(表3、表4)。
表3 室温与低温放置0~8 h时稳定性考察结果(,n=3)
条件 理论值(μg/mL)室温(20℃)0 h 3 h 5 h 8 h低温(4℃)16.7533.5067.0016.7533.5067.00测得值(μg/mL)13.46±0.0627.07±0.1060.16±0.2613.86±0.0626.23±0.1158.98±0.07 RSD(%)0.450.360.430.440.190.13测得值(μg/mL)13.41±0.0427.29±0.3160.21±1.0213.80±0.0126.27±0.0259.07±0.03 RSD(%)0.291.131.690.080.060.05测得值(μg/mL)13.42±0.1027.00±0.2559.52±0.1313.79±0.0526.33±0.1558.99±0.06 RSD(%)0.720.930.210.330.570.10测得值(μg/mL)13.39±0.0527.23±0.7959.67±0.9613.67±0.0726.07±0.1658.45±0.08 RSD(%)0.372.911.610.510.620.14
表4 室温与低温放置1~5 d时稳定性考察结果(,n=3)
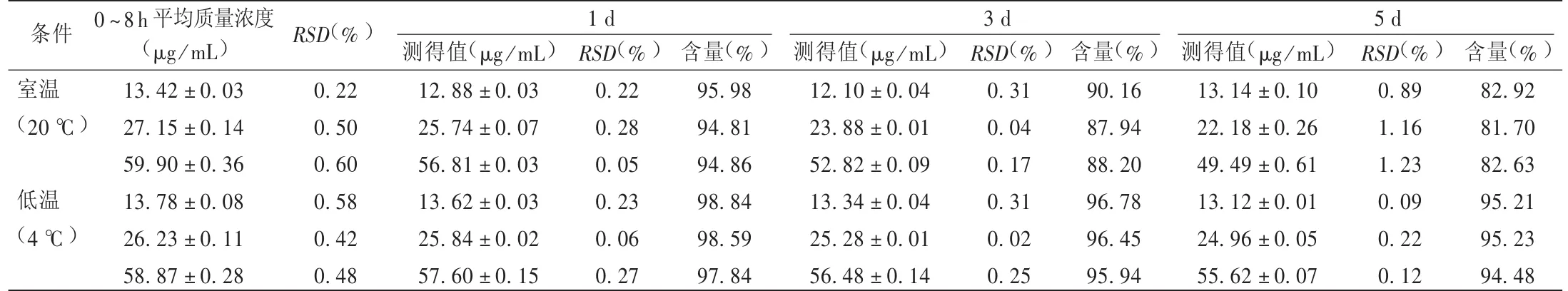
表4 室温与低温放置1~5 d时稳定性考察结果(,n=3)
条件 0~8 h平均质量浓度RSD(%)1 d 3 d 5 d(μg/mL) 测得值(μg/mL)RSD(%) 含量(%) 测得值(μg/mL)RSD(%) 含量(%) 测得值(μg/mL)RSD(%) 含量(%)室温13.42±0.030.2212.88±0.030.2295.9812.10±0.040.3190.1613.14±0.100.8982.92(20℃)27.15±0.140.5025.74±0.070.2894.8123.88±0.010.0487.9422.18±0.261.1681.7059.90±0.360.6056.81±0.030.0594.8652.82±0.090.1788.2049.49±0.611.2382.63低温13.78±0.080.5813.62±0.030.2398.8413.34±0.040.3196.7813.12±0.010.0995.21(4℃)26.23±0.110.4225.84±0.020.0698.5925.28±0.010.0296.4524.96±0.050.2295.2358.87±0.280.4857.60±0.150.2797.8456.48±0.140.2595.9455.62±0.070.1294.48
3 讨论
从表3和表4可知,注射用头孢美唑钠在室温条件下降解的速率较低温条件下大大增加,且有随时间延长而加快的趋势,这可能与降解过程中供试品溶液的内环境发生改变有关(pH改变以及降解产物的影响)。刘伟祥等[3]研究了头孢美唑与维生素C配伍的稳定性,发现头孢美唑与维生素C在0.9%氯化钠注射液中配伍后0~6 h内,其外观、pH无明显变化,含量变化不大。本试验结果显示,采用反相高效液相色谱法具有可行性,且为临床试验动物的准确给药及药代动力学研究提供了理论依据。
[1]黄兆好,谢翠刁.先锋美他醇的药理与临床应用[J].广东药学,2000,10(2):39.
[2]张春然,唐克慧.头孢美唑钠的质量与稳定性研究[J].国外医药·抗生素分册,2005,26(1):5-8.
[3]刘伟祥,曾 颖,罗宇芬.双波长紫外分光光度法考察头孢美唑与维生素C配伍的稳定性实验[J].中国医院药学杂志,1998,18(7):316.

