铕原子标记技术检验实验室移液器容量误差方法
沈 伟 张征军 孙 杰 邵平扬 王志刚/. 浙江省嘉兴市计量检定测试所;. 浙江省嘉兴市第二医院
建立铕原子标记技术对实验室移液器容量的比对与校准,能实现对小容量移液器容量准确度与精密度的有效监控。采用时间分辨荧光检测技术,检验移液器容量的误差来源。时间分辨荧光法检测批内重变性误差在0.17%~7.8%之间。铕标记法与蒸馏水称重法对移液器容量测定的比对试验,相对误差-3.9%~0.62%。时间分辨荧光进行移液器容量比对与误差评估,方法灵敏、精确、简便, 可适用于临床实验室移液器容量的误差识别及常规比对。
0 引言
移液器、进样器是利用空气排代原理的量出式加样器,是临床实验室定性与定量分析的常用工具,广泛应用于免疫学、分子生物学、色谱分析等技术领域,其容量的准确性直接关系到结果的可靠性、可比性与可重复性[1]。据报道新购置的移液器失准率为1.56%,则使用1万次以下的失准率为4%,(1~5)万次失准率为8.82%,(5~10)万次失准率为21.7%,10万次以上失准率为47.6%[2]。故对移液器进行误差检验,既是各实验室内部质量控制的必要条件,又是实现实验室之间检验、检查结果“一单通”的技术前提。
目前,移液器的容量检定有重量分析法和分光光度法两种[3、4],我们在实际工作中成功探索出用铕原子标记技术对移液器的容量进行误差识别,并获国家发明专利。该方法将铕标记技术的高灵敏性与高稳定性结合起来,不受气温、气压的影响,检测灵敏度达10-12~10-14g/L[5],精密度试验显示优异的性能,尤其适用于小容量移液器的容量比对。
1 原理与方法
1.1 实验原理
时间分辨荧光检测技术(time-resolved fluoroimmunoassay, TR-FIA)以镧系铕原子(Eu)作为示踪材料(原子序数63,原子半径2.56,原子体积28.9 cm3/mol),用β-萘甲酰三氟丙酮(β-NTA)为荧光增强液,336~337 nm为激发波长,610~613 nm为测定波长,利用这类荧光物质荧光寿命长及Stokes位移大的特点,荧光衰退时间730 μs,测定延时时间400 μs,通过波长和时间差两种分辨技术,有效排除非特异本底荧光的干扰,灵敏度高,标记物制备简单,稳定性好。鲁赫曼发射光谱由时间分辨荧光仪测定,测定载体为聚乙烯微孔板。以《移液器检定规程》(JJG 646-2006)为判断标准,建立起精确有效、简便快速的铕原子标记技术对移液器容量精确度进行比对与校准的方法。
1.2 仪器与材料
上海某生物技术有限公司的ANYTEST时间分辨荧光分析仪,配220 V电压、50 Hz频率的稳压电源;上海某仪器厂的TG-328A型光电分析天平;待检移液器若干。
1.3 实验准备
1)聚乙烯微孔板本底检测:空白聚乙烯微孔板在时间分辨荧光分析仪上进行本底测定。
2)铕原子标记液制备:上海某生物技术有限公司生产的铕标记试剂盒,取30 μL铕加3 mL稀释液混合成铕标记液。
1.4 移液器加样操作[6] :
1)温度平衡:先使移液器、吸液嘴与铕标记液温度平衡30 min后进行操作。
2)容量设定:转动移液器顶部调节旋钮,逆时针方向转动,增大加样量;顺时针方向转动,减少加样量,最终将移液器的容量调节到所需刻度。
3)预吸液:选择洁净、合适的滴头安置在移液器套筒上,稍加扭转压紧吸液嘴使与套筒之间无空气间隙。垂直握持移液器,预吸入铕标记液并排回原容器中,吸液、排液共重复3次。
4)吸液:垂直握持移液器,把按钮压至第一停点,滴头浸入液面下2~3 mm处,然后缓慢平稳地放松按钮,等1~2 s滴头完全吸满后,滴头离开液面,贴壁停留2~3 s,淌走多余的液体。
5)放液:将移液器移至聚乙烯微孔板侧壁,保持垂直状态,轻轻压下按钮至第一停点位置,等待1~2 s,移动滴头再贴试管壁,完全揿下按钮,以排尽滴头内的液体,然后将滴头沿试管内壁向上移开。
6)动作应柔和,避免按钮急速弹回;实验操作过程中,移液器始终保持垂直状态。
1.5 检测方法
1)按JJG 646-2006[7],用重量分析法确定1支移液器作为本次实验的标准移液器。
2)批内精密度试验:用标准移液器、待检移液器分别加铕标记液,进行批内精密度试验。
3)容量比对试验:标准移液器与待检移液器分别吸取同一铕标记液各10孔,混匀5 min,即时进行荧光时间分辨测定,计算均值、SD、CV%、相对误差R%。
4)稳定性检测:在即时、15 min、30 min、60 min,分别再次测定荧光强度值。
5)误差的识别:对CV%值超过《JJG 646 —2006》规定误差范围的移液器应弃用—随机误差;对CV%小,但R%超范围的待检移液器应当校正—系统误差。
6)允许误差范围设定:移液器容量允许误差范围和重复性判断标准,以JJG 646-2006规定为准。
1.6 统计学处理
相对误差采用成组设计的两样本均数的百分比。
2 试验结果
2.1 时间分辨荧光批内重复性试验
在最佳实验条件下,用已检定的移液器加铕标记液,进行批内重复性试验。实验结果显示50 μL、10 μL、5 μL、1 μL批内重复性误差 分 别 为 0.17%、0.96%~1.80%、1.67%~2.10%、4.80%~7.80%(表 1)。
2.2 稳定性检测
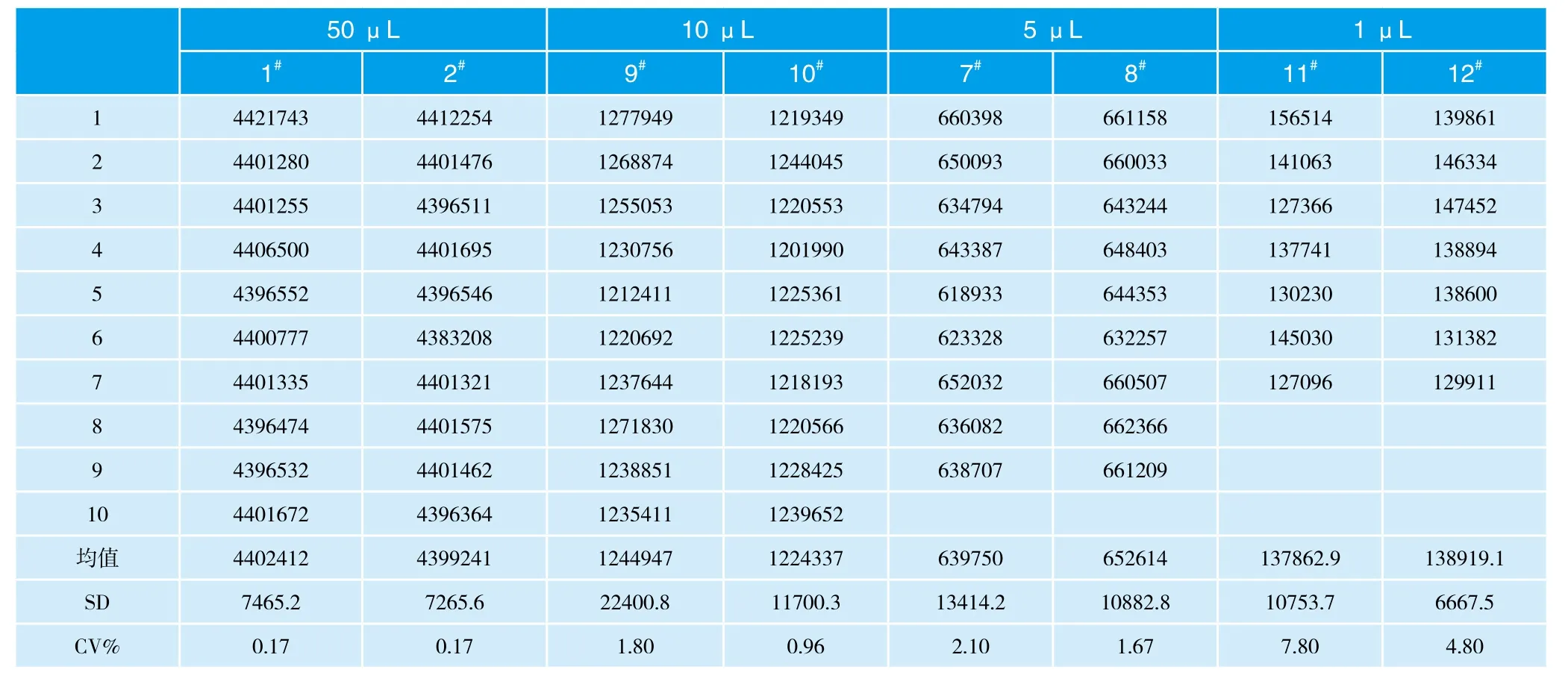
表1 铕标记法对标准移液器的重复性试验
在即时、15 min、30 min、60 min,分别再次测定荧光强度值,见图1。

图1 稳定性试验
2.3 铕标记法与称重法测定移液器容量比对
吸取同一铕标记溶液加样后进行测定,计算均值、SD、CV%及两者均数的相对误差R%(表2)。
2.4 非标准移液器的校准试验
对CV%值超过《移液器检定规程》(JJG 646-2006)规定误差范围的移液器应弃用;对CV%小,但R%超范围的待检移液器,先做好刻度记号,再用移液器专用扳手调节顶部旋钮,顺时针旋转,容量调大;逆时针旋转,容量调小,随后再进行10次标记溶液加样测定,直至R%小于《移液器检定规程》(JJG 646-2006)容量允许误差范围之内,即R%趋向于零。

表2 铕标记法与称重法比对试验
3 讨论
目前移液器容量比对与校准有两种方法[8-10]:①国家质量监督检验检疫总局推荐的蒸馏水称重法作为移液器容量校准的标准方法,但该实验须考虑到气温、气压条件,同时兼顾湿度与修正值等因素,整个操作比较繁琐,临床应用受到限制,其最大的缺陷还是灵敏度仅为0.1 mg/L,实验存在人为误差。②近年来,国内外学者提出分光比色法校准移液器,如重铬酸钾法、甲基橙法、曙红法等[11、12],由于此类方法采用“朗拜—比耳”定律,最适宜吸光度在0.05~0.65之间,而对高、低浓度溶液存在线性偏差,一般分光光度比色法的检测灵敏度为10-3~10-4g/L。
铕原子标记具有高特异性、高灵敏度、低本底、重复性好、示踪物稳定、标准曲线线性范围宽、不受样品自然荧光干扰、操作简便、可以无数次重复检测、无放射性污染等优点。通过荧光度或相对荧光强度比值,来判断反应体系中被分析物的浓度,达到定量分析之目的,深受生物医学研究工作者的青睐,已经广泛应用于临床医学检验和生物医学科学研究,成为最有发展前途的超微量分析技术,是当前标记免疫分析发展到新阶段的代表[13]。铕原子标记的发射光和激发光有较大的STOKES位移(200 nm),光谱间干扰小,同时,本底低(200~400cps)——特异性强;原子标记,位阻体积小,检测灵敏度高达10-12~10-14g/L;荧光寿命长,半衰期长,稳定性高;标准曲线线性范围宽——可测容量范围广。
根据标准移液器与待检移液器对同一放射性铕溶液各10次吸样荧光强度值,计算出各移液器的均值、SD、CV%。从CV%值的大小反映移液器精密度——移液器的随机误差。通过待检移液器与标准移液器的CPM均值比较,计算相对误差(R%),R%值大小反映被检移液器的准确度——移液器的系统误差。对CV%值超过规定者应弃用;对CV%值稳定、而相对R%值超出允许范围的非标准移液器,可通过移液器专用扳手调节顶部旋钮,最终达到对移液器的比对与校准目的。
总之,铕法进行移液器容量误差的鉴别,其方法灵敏、精确、简便与实用,可适用于临床实验室移液器的常规比对与校准。
[1] 韩志芳. 微量移液器在实验教学中的正确使用与校准[J]. 中国卫生检验杂志,2005,15:757-758.
[2] 李伟贤,杨新,吴勤如. 128支微量移液器容量准确性的连续检测报道[J]. 实用预防医学,2001,8:312.
[3] Djian R, Thibeault E, MacNamara. Optimization and cost analysis of a semi-automated pipette verification system in a clinical laboratory[J].Clin Chem, 2005, 51(6 Supple): A215.
[4] American society for testing and materials. Standard specifications for piston or plunger operated volumetric apparatus[J]. Designation:E,1993, 1154-1189.
[5] 许叔祥. 医学超微量分析方法和计量技术进展[J]. 上海计量测试,2002,29:4-6.
[6] Loria. A, Salas. R. Evaluation of pipertting systems, Part Ⅱ[J].Precision and accuracy of precision dispensers. Rev Invest Clin.1990,42:157-160.
[7] 全国流量容量计量技术委员会. JJG 646-2006[S]. 北京:中国计量出版社,2006.
[8] 刘李栋,谢云峥. 应用比色法检查自动加样仪的计算[J]. 检验医学,2004,19:168.
[9] 叶贤林,杨立新,周一炎. 应用甲基橙比色法测试移液器的精度[J]. 中国输血杂志,2003;16:406.
[10] 李凯,杨爱民,任娜等. 重视微量移液器的正确使用与校准[J].江西医学检验,2003,21:51.
[11] Curtis, RH. Performance verification of manual action pipettes[J].American Clinical Laboratory. 1994, 12:8.
[12] McGown E, Hafeman D. Multichannel pipettor performance verified by measuring pathlength of reagent dispensed into a microplate[J]. Anal Biochem,1998,258:155-157.
[13] 陶义训主编. 免疫学和免疫学检验[M]. 2版. 北京:人民卫生出版社,1999,156.

