2型糖尿病合并高血脂患者口服给药成本分析
姚德良,连文喜
糖尿病 (DM)是世界各国关注的公众健康问题,是一种累及多脏器的慢性终身性疾病,已成为仅次于脑血管和肿瘤之后,第 3位的常见病、多发病和慢性非传染性疾病。根据流行病学调查,糖尿病的发病率呈逐年上升的趋势。糖尿病是一种由于胰岛素生物活性或其效应绝对或相对不足,引起糖、蛋白质、脂肪代谢紊乱、血中葡萄糖升高而发生的疾病。DM已严重影响了人们的生活质量,并给个人、家庭政府带来了沉重经济负担。研究资料统计显示,美国至 2010和 2020年将分别达到 1560亿和 1920亿美元。随着我国糖尿病患者人数的增加,用于治疗糖尿病及其并发症的费用负担也将逐步增加。本研究对在现有医疗模式下二甲医院用规范化管理治疗 2型糖尿病合并高血脂患者的治疗成本进行分析。
1 资料与方法
1.1 一般资料 从本院病志管理系统提取 2007—2009年诊断为 2型糖尿病合并高脂血症的患者 30例。筛选标准及方式:(1)2型糖尿病的诊断均符合1999年 WHO糖尿病分型和诊断标准,均排除糖尿病急性并发症及严重脑血管意外、急性心肌梗死等合并症;无合并其他影响糖代谢的疾病,如库欣综合征、甲状腺功能亢进、肢端肥大症等;(2)高脂血症诊断标准:受检者均在清晨空腹时接受静脉采血 (禁食时间至少 >8 h),且近 3 d均为清淡饮食。以血清总胆固醇 >5.72 mmol/L和 (或)血清三酰甘油 >1.70 mmol/L,采用标准酶法测定。1.2 研究方法 空腹血糖 (FBG)、餐后 2 h血糖 (2 hPBS)采用葡萄糖氧化酶法测定;胆固醇 (TC)采用酶法测定;三酰甘油 (TG)采用酶法测定;高密度脂蛋白胆固醇 (HDLC)采用标准酶法测定;低密度脂蛋白胆固醇 (LDL-C)采用酶法测定;糖化血红蛋白 (HbAlc)采用高效液相色谱法。1.3 观察指标 治疗前后患者的体质指数 (BMI)、FBG、2 hPBG、 HbAlc、 TC、 TG、 HDL-C、 LDL-C。
1.4 药物种类 从数据库中直接检索记录药物的剂量及种类,本研究所涉及的药物种类为:(1)磺脲类:格列齐特 (达美康缓释片,施维雅制药有限公司),格列吡嗪 (瑞易宁,辉瑞制药有限公司生产),格列美脲 (亚莫利,安万特制药有限公司生产);(2)双胍类:二甲双胍 (格华止,施贵宝公司生产);(3)非磺脲类胰岛素促泌剂:瑞格列奈 (诺和龙,诺和诺德公司生产),那格列奈 (诺华制药有限公司生产);(4)噻唑烷二酮类:罗格列酮 (文迪雅,葛兰素史克公司生产 );(5)α-葡萄糖苷酶抑制剂:阿卡波糖 (拜糖苹,德国拜耳公司生产);(6)胰岛素:人胰岛素 (优泌林,美国礼来公司生产),赖脯胰岛素 (优泌乐,优泌乐 25,美国礼来公司生产),门冬胰岛素 (诺和,诺和 30R,诺和诺德公司生产),甘精胰岛素 (来得时,安万特制药有限公司生产)。
1.5 治疗费用计算 总治疗药物费用 (降糖药物费用 +降脂药物费用)和检查费。
1.6 代谢指标达标值 LDL-C≤100 mg/dl为血脂达标标准;糖化血红蛋白 (HbA1c)≤6.5%为血糖达标标准。
1.7 统计学方法 所有数据采用 SPSS13.0软件包处理,计量资料以 (x±s)表示,所有计量资料进行正态性检验和方差齐性检验,偏态分布的变量及方差不齐者,经自然对数 ln转换后分析,以 P<0.05为差异有统计学意义。
2 结果
2.1 30例 2型糖尿病患者治疗前后各观察指标比较 30例患者治疗后 FBG、2 hPBS、HbAlc、HDL-C检测结果与治疗前比较差异有统计学意义 (P<0.05);LDL-C、BMI、TG、TC检测结果与治疗前比较差异无统计学意义 (P>0.05,见表1)。
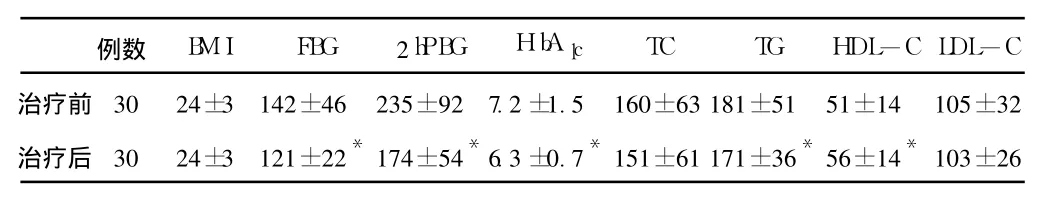
表 1 30例患者治疗前后各项观察指标的变化情况 (x ±s)Table 1 The variation of total index before and after the treatment on 30 patients
2.2 总人群代谢指标达标情况的分析 30例糖尿病合并高脂血症患者治疗后血糖达标人数为 18例 (占 60.0%),血脂达标人数为 11例 (占 36.7%)。总人群治疗药费平均为 6 307.1元/人·年,其中降糖费为 4 897.9元/人·年,合并高脂血症患者降脂费平均为 1 928.0元/人·年。在血糖达标组中每降1%HbA1c的降糖费用平均为 4 615.3元/人·年。由于收集的各项费用的数据呈非正态分布,故对变量 (费用)进行自然对数 ln变换,呈正态分布后统计分析,总人群与各达标组费用比较差异均无统计学意义 (P>0.05,见表 2)。
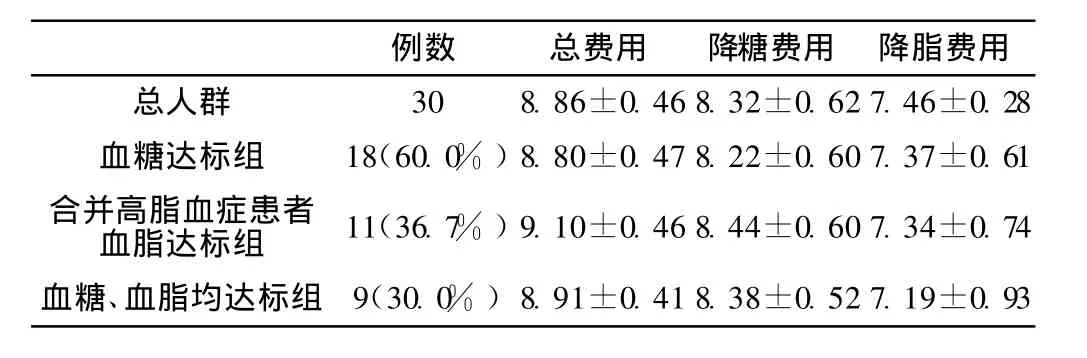
表 2 总人群及各达标组费用比较 (x ±s)Table 2 Medical expenditure comparation of the patients reaching goal and total crowd
3 讨论
有研究显示糖尿病患者常常伴有血脂异常,糖尿病患者高脂血症发生率明显高于非糖尿病患者[1];高脂血症不但加重了糖代谢紊乱,而且使糖尿病微血管、大血管并发症发生率及死亡率显著增高。目前认为高胰岛素血症可通过促进脂质合成及刺激动脉内膜平滑肌细胞增生,低胰岛素血症则通过减低脂质清除率及降低血管壁溶酶体脂肪酶系活性,均加速动脉粥样硬化的发生、发展[2-3]。糖尿病的病理生理机制是胰岛素抵抗和胰岛素分泌缺乏,二者都可引起脂类代谢紊乱导致血脂异常。2型糖尿病患者易发生致动脉粥样硬化性血脂异常,这与2型糖尿病多伴发中心性肥胖及胰岛素抵抗有关。此外,机体长期处于高血糖状态致使载脂蛋白 B(aPOB)的糖化率增加,使 LDL与受体的结合能力下降,从而延缓了其在血浆中的清除,增加巨噬细胞对其摄取,进一步促进泡沫细胞的形成[4]。
糖尿病患者的医疗成本包括直接医疗成本和间接医疗成本,直接医疗成本包括药品费用、给药途经费用、检查费用、治疗并发症的医疗费用等;间接成本包括患者误工费用、交通费,伙食费和因误工而带来的相关费用等。在本研究中所选择的 30例患者并未计算其间接医疗成本,而只对直接医疗成本进行统计。本研究显示患者就诊过程中支付治疗药物的费用平均为 6 307.1元/人·年,其中降糖药费用平均为 4 897.9元/人·年;平均每降低 1%HbA1c所需降糖药费用为 4 615.3元/人·年。这个成本从平均水平上来说,是国家统计局公布的2008年城镇居民平均年收入的 1/3(15 781元/人),应该说比较高。需要说明的是:(1)该组患者所用的药物均为原研究厂家的药物比同类仿制品的价格会高。(2)该研究的随访期仅一年半左右使该组资料仅能评估代谢指标的达标率,尚无法评估并发症的发生率与心血管事件率和减少并发症治疗而节约的费用,因此会出现效益不足而成本过高。有待后续进一步~100倍,与 CsA相比,最大的优势是肝脏毒性小,适用于肝功能异常的移植病人。他克莫司可逆转已发生的排斥反应,使器官移植的存活率大大提高[1-2]。
当他克莫司出现肾毒性、高血压、高血钾、高血糖、腹泻、头痛、震颤、癫痫等不良反应时,或在器官移植术后常常发生颅内真菌感染,肺部感染、神经精神系统等并发症,或患者合并关节病、胃溃疡、高血压等其他疾病时,常需合并用药,因而可能会发生药物相互作用。他克莫司主要通过肝脏细胞色素 P450 3A酶系统广泛代谢,进行脱甲基作用或羟化作用。可与许多经此酶代谢的药物发生相互作用,从而导致血药浓度升高或下降,药效增强或减弱,甚至诱发严重不良反应。因此联用时要权衡利弊和血药浓度监测。现将具体药物的相互作用综述如下。
1 抗生素
1.1 大环内酯类 根据大环内酯类抗生素对 CYP3A4的结合力及抑制作用的差别,可将其分为三类:一类为红霉素及其前体药物、醋竹桃霉素,它们能与 CYP3A4形成 P450-MI(metabolite intermediate complex)并紧密结合在一起,从而抑制CYP3A4活性;另一类为克拉红霉素、氟红霉素、麦迪霉素、交沙霉素、罗红霉素等,它们与 CYP3A4能产生中度结合;而阿奇霉素、地红霉素、螺旋霉素等是与 CYP3A4结合力较弱的一类,一般对 CYP3A4无抑制作用[3]。体外实验证明 14元环的大环内酯类抗生素和细胞色素 P450 3A同工酶会形成非活性复合物,抑制他克莫司在肝脏和小肠中的代谢,从而升高了他克莫司的血药浓度,同时两类药的相互作用还会导致急性肾功能损害。红霉素和他克莫司均为大环内酯类,它们均对人类淋巴细胞的增殖有抑制作用。体外实验证实:红霉素能够增强他克莫司对淋巴细胞增殖的抑制作用。合用时红霉素对他克莫司的影响较大,可使其口服生物利用度增加,血浓度升高6倍以上并出现毒性反应。其机制为红霉素既抑制他克莫司肝代谢,同时也影响他克莫司的肠代谢。15元环的阿奇霉素不能诱导或激活 CYP450系统,因此相对较安全,但两药合用时仍要密切监测他克莫司的血药浓度和肾功能[4]。
1.2 抗结核药 他克莫司通过 CYP3A4代谢,同时也是 P-糖蛋白 (P-glycoprotein)介导的转运的底物,而利福平是CYP和 P-糖蛋白的强效诱导剂,它对 CYP1A2、CYP3A4和CYP2C均能产生诱导作用。它诱导他克莫司在肝、肠CYP4503A酶系统和 P-糖蛋白的代谢,显著增加他克莫司的消除,减少他克莫司的生物利用度,使他克莫司血药浓度达不到治疗范围,引起器官排异。利福平停用 1~3周后 CYP代谢才会恢复至正常。1例肝移植儿童,应用他克莫司 4 mg,2次/d,谷浓度为 10μg/L,给予利福平 150 mg,2次/d,此时他克莫司血药浓度低于治疗范围,必须增大他克莫司的剂量至 8 mg,2次/d,才能达到治疗效果。6例男性健康志愿者在合用利福平之前及合用过程中分别口服 (0.1 mg/kg)和静脉注射(0.025 mg·kg-1·4h-1)他克莫司,两药共合用 18 d,通过观察他克莫司体内药代动力学的改变,发现利福平能显著增加他克莫司的清除率 (由 36.0 ml· h-1·kg-1增加至 52.8 ml·h-1·kg-1),并能显著减少他克莫司的生物利用度 (由14.4%减少至7.0%)。有时必须将他克莫司剂量提高 10倍,才能继续维持他克莫司的临床疗效,但如此做法可能会导致移植肾功能的损害[5-6]。利福布丁也可以降低他克莫司的血药浓度,但作用小于利福平。
1.3 其他 氯霉素通过抑制 CYP450酶系统,减慢了他克莫司的消除,延长其半衰期 (t1/2),使其血药浓度升高,增加其毒性。1例万古霉素耐药肠球菌感染 (VRE)的青年肾移植患者,给予氯霉素 600 mg,每 6 h一次,给药 2 d,出现他克莫司的毒性,同时他克莫司的血谷浓度上升,t1/2延长,药时曲线下面积 (AUC)是正常的 7.5倍,他克莫司剂量须减少83%才降至基础水平[7-8]。林可霉素抑制他克莫司强度是红霉素的一半。
2 抗真菌药
抗真菌药是器官移植术后常用的一类咪唑类药物,包括氟康唑、克霉唑、酮康唑、伊曲康唑等,通过抑制 CYP450酶系统,显著抑制他克莫司的代谢,使他克莫司的血药浓度升高,且两类药物合用有肾毒性增强的趋势。1例肝移植患者应用克霉唑治疗时,他克莫司的血谷浓度从 0.6μg/L上升到 1.5 μg/L,AUC从 18 μg· h-1· L-1增加至 33 μg· h-1· L-1,影响显著,但 t1/2从 10.5 h延长至 11.3 h,没有显著改变。其机制可能也是克霉唑同他克莫司结合竞争空肠黏膜细胞上的P450酶,导致他克莫司吸收增加,代谢减少;同时克霉唑在一定程度上减少了肝脏 P450酶系统对他克莫司的代谢,使他克莫司的血药浓度升高。这一相互作用有助于减少他克莫司剂量而达到理想的他克莫司的血药浓度。在临床上应密切监测他克莫司血药浓度,根据血药浓度调整剂量,必要时停用克霉唑以减少毒性或降低由于剂量低于治疗范围而产生的急性排斥反应[9]。19例肾移植患者,静脉注射他克莫司 0.04 mg/kg,24 h后,1次口服酮康唑 400 mg,他克莫司的生物利用度 (F)平均提高 118%,同时分布容积 (Vss)从 104.77 L降至80.44 L。其机制是酮康唑影响他克莫司的肠代谢导致生物利用度升高,而 Vss的改变与手术后 α-1-酸性糖蛋白 (AAG)变化有关。他克莫司在体内仅 77%与 AAG结合,而酮康唑与血浆蛋白高度结合。同样,应用伊曲康唑时,也会引起他克莫司的血药浓度上升,增加不良反应的发生率。因此在移植患者中使用伊曲康唑,应降低他克莫司的剂量,从而可降低治疗费用而不会引起排斥反应[10]。20例器官移植患者口服氟康唑100 mg/d或 200 mg/d,他克莫司的血谷浓度分别上升 1.4倍和 3.1倍,并产生急性肾损害,同时 t1/2延长,其相互作用呈剂量依赖性。但静脉给予大剂量的氟康唑 (400 mg),对他克莫司的血浓度影响并不显著。其可能机制是氟康唑通过影响他克莫司的肠代谢过程而增加其吸收,因为 P450除主要存在于肝脏外,还分布于肺、肾、小肠等部位[11]。
伏立康唑抑制 P450同工酶 CYP2C19、CYP2C9、CYP3A4的活性,使血药浓度升高。两者合用时他克莫司剂量需减量2/3,然后按监测后谷浓度调整剂量。据报道,随机 22周安慰剂对照动力学研究表明,1例肝移植患者服用他克莫司 2 mg,加伏立康唑 200 mg,2次/d,加后第 3天他克莫司血药浓度由合并用药前 2.3μg/L升至 12.5μg/L,第 5天升至 23.4μg/L,他克莫司浓度升高 10倍。停用伏立康唑后他克莫司血药浓度回至基线。
泊沙康唑 (posaconazole,POS,商品名:noxafil)由于酶抑作用使他克莫司血药浓度升高,健康志愿者研究显示[12],当他克莫司与泊沙康唑 400 mg,2次/d,7 d后,他克莫司的AUC增加358%,Cmax升高 121%,故当二者合用时,他克莫司剂量应减为原剂量的 1/3。泊沙康唑的药代动力学则不受影响。
卡泊芬净 (caspofungin acetate,cancidas)是新型葡聚糖合成酶抑制剂类抗真菌药,是 CYP3A系列酶诱导剂,可降低他克莫司血药浓度,从而降低其效应。卡泊芬净可使他克莫司的 AUC减少约 20%,血药浓度峰值降低约 16%,12 h后血药浓度降低约 26%,合用时应监测他克莫司的血药浓度并及时调整剂量。他克莫司对卡泊芬净的药物动力学参数无影响。
阿尼芬净 (anidulafungin,VER2002,LY303366)是第三代棘白菌素类的半合成抗真菌药,是两性霉素 B的衍生物。阿尼芬净不通过肝脏代谢,因此不存在与其他药物相互作用。一项评价阿尼芬净和他克莫司安全性和药代动力学相互作用的研究[13],健康受试者于第 1天和第 13天口服他克莫司 5 mg,并于第 4天静脉给予阿尼芬净 200 mg,从第5天开始连续13 d给予阿尼芬净 100 mg,阿尼芬净和他克莫司合用组与单个用药组相比,其主要药代动力学参数 Cmax、AUC、t1/2、CL、Vss无显著性差异。阿尼芬净与他克莫司合用无药代动力学相互作用,两药耐受性良好,无严重不良反应。
3 抗病毒药
蛋白酶抑制剂能抑制由 CYP450代谢的他克莫司,其中抑制强度最强的是利托那韦 (ritonavir)。Jain等[14]在他克莫司合用 Kaletra(一种抗病毒药,含洛匹那韦 (lopinavir)和利托那韦 (ritonavir))相互作用的研究中,Kaletra使他克莫司的血药浓度显著升高,患者出现肾毒性和 (或)神经毒性的风险[15-16]。Kaletra与他克莫司合用的患者,他克莫司剂量低于1 mg/周就足以维持其血药浓度。刚合用 Kaletra的患者依据肝功能 3~5周内无需增加剂量。非核苷逆转录酶抑制剂奈韦拉平 (nevirapine)诱导肝 CYP450酶系统。应避免利托那韦、奈韦拉平和他克莫司合用。给予齐多呋啶、拉米呋啶、茚地那韦将是相对安全的,但需常规监测他克莫司的血药浓度和肌酐(Cr)。他克莫司本身是 CYP450 3A4同工酶的抑制剂,当他克莫司与蛋白酶抑制剂合用时,后者的血药浓度也会升高。
4 硝基唑类药物
本类药物有甲硝唑、替硝唑。由于 CYP3A4和 P-糖蛋白的抑制作用增强他克莫司血清效应和增加毒性,据报道1例给予甲硝唑 500 mg,2次/d,口服,14 d后他克莫司血药浓度由7~10μg/L升至 26.3μg/L,血肌酐值由 1.6~1.8 mg/dl升至3.3 mg/dl,停用甲硝唑后恢复至基线。另 1例为加用甲硝唑400 mg,3次/d,口服,第 9天他克莫司血谷浓度由 9.0μg/L升至 17.9μg/L,血肌酐值也相应升高,也在停用甲硝唑后恢复至基线[17]。
5 钙离子拮抗剂
高血压是器官移植术后的常见并发症,其发病率为 47%,而钙拮抗剂是治疗高血压的常用有效药物。二氢吡啶类钙拮抗剂 (CCB)是 CYP450同工酶的强抑制剂,通过抑制他克莫司在肝脏的代谢,减慢其消除,并且可减少他克莫司的肾毒性。Huntress等研究表明 CCB通过抑制 Ca2+介导的淋巴细胞的增殖,导致发生急性排斥反应减少。但目前尚无 CCB和他克莫司在免疫调节方面的相互作用研究。硝苯地平是他克莫司代谢的强抑制剂,抑制肝脏和其他部位的 CYP450 3A4酶系统。研究提示他克莫司和硝苯地平存在剂量依赖型不良反应。对 50例肝移植患者经过 1年对比研究,合用硝苯地平,他克莫司的绝对日剂量、累积剂量与不用硝苯地平相比,两者均降低,并存在显著差异。合用硝苯地平后,他克莫司血浓度升高 55%(从 8.9μg/L上升至 13.8μg/L)且肾功能显著改善,这一现象,对接受免疫抑制剂治疗导致高血压的移植病人将是十分有益的。其可能作用机制为硝苯地平抑制他克莫司经细胞色素P450的代谢过程,同时通过扩张肾血管,降低血清肌酐,促进肾功能的改善。如合用硝苯地平,他克莫司应减量 1/3左右。
其他的钙拮抗剂如硫氮卓酮、维拉帕米等也通过竞争CYP3A4酶影响他克莫司的代谢,同时其扩血管效应对他克莫司的肾毒性有防治作用[18]。
6 神经系统药物
6.1 苯妥英钠 苯妥英也为肝微粒体酶诱导剂,对 CYP1A2、CYP3A4和 CYP2C均能产生诱导作用。和他克莫司合用后,他克莫司血药浓度下降,在正常的血清蛋白浓度下游离型的苯妥英钠浓度不断升高。其机制是苯妥英诱导他克莫司代谢,而他克莫司通过与苯妥英竞争性地与血浆蛋白结合,致使游离的苯妥英浓度上升,因此两药合用时,必须监测两者的浓度。1例肾移植患者因癫痫发作而长期服用苯妥英 (600/500 mg,1次/d)进行治疗,后因慢性排斥反应而用他克莫司替代 CsA,在治疗过程中,几次增加他克莫司的剂量以提高其血浓度(由 14 mg,2次/d增加至 17 mg,2次 /d),认为两药之间可能存在相互作用,使他克莫司的血药浓度难以快速上升[3]。
6.2 奈法唑酮 奈法唑酮 (nefazodone,商品名:Serone)为选择性 5-羟色胺再摄取抑制剂类 (SSRIs)抗抑郁药,与他克莫司合用时抑制他克莫司的代谢,使他克莫司的血药浓度升高,易出现毒性反应,因此两药合用时,必须监测他克莫司的血浓度。1例女性患者肾移植 2年后因抑郁症口服抗抑郁药奈法唑酮 (50 mg,2次/d),1周后出现头痛、意识模糊、视觉“灰区”(gray areas),未发现眼部异常,他克莫司谷浓度明显升高 (>30μg/L)。由于他克莫司和奈法唑酮均通过 CYP3A4代谢,而奈法唑酮是 CYP3A4的抑制剂,因此抑制了他克莫司的肝代谢[3]。
7 生殖及内分泌系统调节药
己烯雌二醇对他克莫司的代谢具有和 CsA同样强的抑制作用。达那唑具有弱雄激素作用,抑制促性腺激素的分泌。1例肾移植患者,因特发性血小板减少性紫癜用泼尼松 50 mg/d治疗无效,采用口服达那唑 400 mg,3次/d治疗。4 d后他克莫司的血谷浓度从 0.7μg/L上升至 2.7μg/L,11 d后上升至4.9μg/L,减少他克莫司的剂量,其血浓度仍然偏高,只有停用达那唑后,他克莫司的血浓度才降至基础水平,血清肌酐也恢复正常。其作用机制是他克莫司通过脱甲基和羟基化代谢,而达那唑则能抑制其代谢。
8 非甾体类抗炎药 (NSAID)
他克莫司能促进收缩血管的前列腺素 (PG)类产生,从而导致肾血管阻力增加,肾血流量减少,最终降低肾小球滤过率,引起肾毒性。完全正常的前列腺素系统可以减弱他克莫司的这种肾毒性。当他克莫司与 NSAID合用时后者会抑制前列腺素合成,从而减弱前列腺素系统的保护作用,使得他克莫司肾毒性增强。尤其是对于肝功能不全或移植器官功能不正常的患者施救援疗法应用他克莫司时,不应给予 NSAID。如合用需检测血尿肌酐及记录尿量,若肾毒性确实存在,需立即停用他克莫司,用前列腺素 (PGE)治疗,将有助于加速肾功能的逆转。据报道 2例患者用布洛芬和他克莫司发展为急性可逆性肾衰竭。停用他克莫司,给予静脉 PGE1,患者的肾功能和精神症状均随之显著改善。两者合用时并不会升高他克莫司的血药浓度[4]。
9 免疫抑制剂
9.1 CsA CsA通过激活正常人外周血淋巴细胞,在体外抑制植物血凝素、抗 CD3抗体、混合淋巴细胞反应 (MLR)刺激及 IL-2的增殖,和他克莫司产生药理上的拮抗作用。同时他克莫司和 CsA及其代谢物 M17在抗过敏方面可起到协同作用。两药均经 CYP3A4酶代谢,当两者合用时,竞争 CYP3A4代谢酶结合点。CsA可抑制他克莫司的代谢,使他克莫司血药浓度升高,同时他克莫司也抑制 CsA代谢,延长 CsA的 t1/2,从而产生协同/加成性的肾毒性效应。
9.2 硫唑嘌呤 可使他克莫司的血药浓度降低到治疗范围以下,还有可能导致过度免疫抑制[4]。
9.3 类固醇激素 可诱导 CYP3A酶和 P-糖蛋白的活性,而他克莫司是 CYP3A酶和 P糖蛋白的底物,当两种药物合用时,可发生药理学和药动学方面的相互作用。即使是类固醇激素的用量很低,其相互作用还是存在,因此临床同时使用两种药物时应谨慎,低剂量的类固醇激素也可能会导致他克莫司的肾毒性[19]。
9.4 霉酚酸酯 (MMF) MMF和他克莫司存在药动学相互作用。MMF对他克莫司的药动学影响很微小。接受他克莫司和 CsA同时治疗的患者霉酚酸 (MPA)浓度比接受 CsA和MMF的患者有显著的升高。10例接受 CsA+MMF+甲泼尼龙(MEP)进行免疫抑制治疗的肾移植患者,用他克莫司代替CsA后,尽管预先减少了 MMF的剂量 (1.7 g/d减至 1.5 g/d),血浆霉酚酸谷浓度仍然由 1.87 mg/ml上升至 3.4 mg/ml。提示肾移植患者他克莫司和 MMF合用能够产生比预计还要大的免疫抑制强度,应对 MMF剂量进行适当调整,并进行血药浓度监测[20]。
9.5 西罗莫司 当他克莫司与 2~5 mg/d西罗莫司 (雷帕鸣)合用时 AUC减少 30%,Cmin也下降 30%,合用西罗莫司 1 mg/d,他克莫司的 AUC减少 3%,Cmin下降 11%。因此不推荐合用,如必需合用应监测他克莫司血药浓度。
9.6 巴利昔单抗 巴利昔单抗 (BASI,Basiliximab,商品名舒莱)是兼有人源性和鼠源性的嵌合性单克隆抗体。能抑制白介素 -2介导的 T淋巴细胞激活,抑制排斥反应过程中细胞免疫的关键通道,具有较强的互补免疫抑制作用。临床应用耐受性较好,用于预防首次肾移植术后早期急性器官排斥反应。舒莱使他克莫司血浆谷浓度升高并增加其毒性。12例肾移植患者采用他克莫司和舒莱诱导治疗 (移植当天及移植后第 4天 20 mg),二者合用后第 3天血谷浓度升高 63%(与抗胸腺细胞球蛋白相比)。6/12例他克莫司谷浓度 >20μg/L,3/6例呈急性肾小管坏死 (肾活检),故移植后 1周内经历了 2次血透[21]。机制是细胞因子诱导 CYP3A介导他克莫司代谢改变。9.7 粟精胺 粟精胺 (castanospermine,CAST)是一种能破坏淋巴细胞和内皮细胞结合的新型免疫抑制剂,其作用机制可能包括对 T细胞增殖的抑制。为了解粟精胺和他克莫司之间的相互作用,Grochowicz等[4,22]建立了大鼠心脏移植模型,分别用他克莫司 (0.05、0.1、0.2和 0.5 mg/kg 4种剂量)、CAST(50、100、200和 300 mg/kg 4种剂量)、他克莫司与 CAST合用 (0.05 mg/kg+100 mg/kg和 0.1 mg/kg+100 mg/kg)进行免疫抑制治疗,并观察大鼠模型存活率的变化。结果两药合用时大鼠模型存活率中位值明显延长,显示两者有协同作用,如果两药合用,可能要减少他克莫司的剂量,减轻其毒性反应[3]。
10 各种含铝、镁药物
属于本类药物有氢氧化铝、磷酸铝、甘羟铝、氢氧化镁、氧化镁、三硅酸镁。该类药物增加他克莫司暴露量,机制不详,临床需谨慎合用,检测他克莫司血药浓度及暴露量,检测他克莫司不良反应症状包括肾毒性、高血糖、高血钾等。
11 保钾利尿剂
高血钾症是他克莫司的另一副作用,也主要由肾小球滤过率下降引起。因此,在与保钾利尿剂如安体舒通、氨苯蝶啶、阿米洛利合用时,也将增加他克莫司的肾毒性。
12 紫锥花
紫锥花 (Echinacea)属紫苑家族,是北美地区极受欢迎的天然草药。大量研究证实,紫锥花能增强及刺激人体免疫系统,有助消炎杀菌,抵抗病毒。紫锥花直接降低他克莫司免疫抑制作用,从而降低他克莫司抗排异效应。由于本品能增强粒细胞、单核细胞、淋巴细胞效应,增强吞噬细胞活性和自然杀伤细胞功能。动物研究证明本品体内可增强抗原免疫效应,吞噬活性和免疫刺激作用,故不可与他克莫司合用。
13 利纳西普
利纳西普 (Rilonacept)能有效缓解反复发作的慢性痛风患者的疼痛及病情的严重程度,还用于治疗 CAPS(与Cryopyrin蛋白相关的一种遗传性炎症疾病,包括家族性寒冷型自身炎症综合征 (FCAS)和多系统炎症综合征 (MWS,荨麻疹、淀粉样变性、肾炎和耳聋综合征))[23]。利纳西普是白介素受体 -1拮抗剂,可使 CYP450系列酶形成恢复正常,从而加速他克莫司代谢,降低其血浆浓度,故应用利纳西普时需监测他克莫司血浆浓度及作出相应剂量调整。
14 其他药物
青藤碱和他克莫司可产生抗细胞增殖的协同作用。他克莫司能抑制 T细胞激活后信息传递中早期的 Ca2+依赖性活动,将改善心肌细胞对阿霉素的耐受性。
动物实验表明汉防己碱和他克莫司的联合使用在治疗和预防糖尿病试验中,可产生强大的协同作用减少糖尿病的发生率。
现知他克莫司可与近 150种 (类)药物发生相互作用,加之移植患者病情重,并发症多,合并用药种类多,潜在的新的药物相互作用还会被不断认识。故在实行抗排异治疗中应严密观察,加强检查,及时发现潜在相互作用造成的病情发展,实现临床合理、安全、有效地应用免疫抑制剂以保障患者健康是广大医务工作者的责任。
1 Jing H,Kobayshi M.Difference between cyclosporine A and tacrolimus in organ transplantation[J].Transplant Proc,1999,31:1978-1986.
2 丁春雷,刘丽宏,马萍,等 .他克莫司治疗药物监测研究进展[J].中国药房,2008,19(20):1580-1583.
3 陆志城.他克莫司的药物相互作用 [J].国外医学泌尿系统分册,2001,21(5):239-242.
4 张弋,呼自顺,高仲阳.他克莫司的药物相互作用 [J].中国医院药学杂志,2002,22(2):106-108.
5 Hebert MF,Fisher RM,Marsh CL,et al.Effects of rifampin on tacrolimus pharmacokinetics in healthy volunteers[J].J Clin Pharmacol,1999,39(1):91-96.
6 Chenhsu RY,Loong CC,Chou MH,et al.Renal allograft dysfunction associated with rifampin-tacrolimus interaction[J].Ann Pharmacother,2000,34(1):27-31.
7 Schulman SL,Shaw LM,Jabs K.Interaction between tacrolimus and chloramphenicol in a renal transplant recipient[J].Transplantation,1998,65(10):1397-1398.
8 Bakri R,Breen C,Maclean D,et al.Serious interaction between tacrolimus and chloramphenicol in a kidney-pancreastransplant recipient[J].Transpl Int,2003,16(6):441-443.
9 Vasquez EM,Shin GP,Sifontis N,et al.Concomitant clotrimazole therapy more than doubles the relative oral bioavailability of tacrolimus[J].Ther Drug Monit,2005,27(5):587-591.
10 Shitrit D,Ollech JE,Ollech A,et al.Itraconazole prophylaxis in lung transplant recipients receiving tacrolimus(FK 506):efficacy and drug interaction[J].J Heart Lung Transplant,2005,24(12):2148-2152.
11 缪海均,刘皋林.他克莫司与其它药物的相互作用 [J].中国医院用药评价与分析,2001,1(3):167-168.
12 Sansone Parsons A,Krishna G,Martinho M.Effect of oral posaconazole on the pharmacokinetics of cyclosporine and tacrolimus[J].Pharmacotherapy,2007,27(6):825-834.
13 Dowell JA,Stogniew M,Krause D,et al.Lack of pharmacokinetic interaction between anidulafungin and tacrolimus[J].J Clin Pharmacol,2007,47(3):305-314.
14 Jain AB,Venkataramanan R,Eghtesad B,et al.Effect of coadministered lopinavir and ritonavir(Kaletra)on tacrolimus blood concentration in liver transplantation patients[J].Liver Transpl,2003,9(9):954-960.
15 Schonder KS,Shullo MA,Okusanya O.Tacrolimus and lopinavir/ritonavir interaction in liver transplantation[J].Ann Pharmacother,2003,37(12):1793-1796.
16 Schonder KS,Shullo MA,Okusanya O.Tacrolimus and lopinavir/ritonavir interaction in liver transplantation.Ann Pharmacother,2003,37(12):1793-1796.
17 Page RL,Klem PM,Rogers C.Potential elevation of tacrolimus trough concentrations with concomitant metronidazole therapy[J].Ann Pharmacother,2005,39(6):1109-1113.
18 Krahenbuhl S,Menafoglio A,Giostra E,et al.Serious interaction between mibefradil and tacrolimus[J].Transplantation,1998,66(8):1113-1115.
19 Anglicheau D,Flamant M,Schlageter MH,et al.Pharmacokinetic interaction between corticosteroids and tacrolimus after renal transplantation[J].Nephrol Dial Transplant,2003,18(11):2409-2414.
20 Hubner GI,Eismann R,Sziegoleit W.Drug interaction between mycophenolate mofetil and tacrolimusdetectable within therapeutic mycophenolic acid monitoring in renal transplant patients[J].Ther Drug Monit,1999,21(5):536-539.
21 N.M.Sifontis,E.Benedetti,E.M.Vasquez.Clinically Significant Drug Interaction Between Basiliximab and Tacrolimus in Renal Transplant Recipients[J].Transplantation Proceedings,2002,34:1730-1732.
22 P.M.Grochowicz,A.D.Hibberd,K.M.Bowen,et al.Synergistic Interaction Between Castanospermine.a Rat Heart Allograft Model[J].Transplantation Proceedings,1997,29:1259-1260.
23 Hoffman HM,Throne ML,Amar NJ,et al.Efficacy and safety of rilonacept(interleukin-1 Trap)in patients with cryopyrin-associated periodic syndromes:results from two sequential placebo-controlled studies[J].Arthritis Rheum,2008,58(8):2443-2452.

