原子荧光光度法中湿法消解、微波消解、干灰化前处理法测定水产品中总砷含量的比较
宋洪强,郝云彬,吴益春,罗海军,祝世军
(舟山市渔业检验检测中心,浙江舟山 316000)
砷及其化合物已被国际癌症机构确认为致癌物,自然界的砷以不同化学形式存在,包括无机砷(三价砷和五价砷)以及有机砷 ,毒性顺序为 AsH3>As3+>As5+﹥R—As—X[1]。
砷是食品中的有害元素,是重要的食品、卫生检测项目,各个国家对食品中砷都有严格的限量要求[2],加强水产品中总砷的检测,是保证初级水产品安全的重要保障。然而,在利用原子荧光法检测总砷的实际工作中,湿法消解、微波消解和干灰化法三种不同前处理方法使同一产品的检测结果常常不一致,有时候会相差甚远[3]。究竟哪一种方法适合,不同水产品应选择哪一方法更适宜呢?本文应用氢化物原子荧光法中三种不同的消解方法测定贻贝粉、海带粉标准物质中总砷含量,对三种消解方法所测得的结果进行了初步探讨。
1 材料与方法
1.1 仪器和试剂
AFS-930原子荧光光度计(北京吉天仪器有限公司)、专用砷编码空心阴极灯、WX-4000微波快速消解仪、DKQ-3B智能控温电加热器(上海屹尧分析仪器有限司)、DB-3电热板(嘉兴市新胜东城仪器厂)、2.5-10马弗炉(沈阳市节能电炉厂)、玻璃仪器(所用玻璃仪器均在40%硝酸溶液中浸泡24 h以上)。
使用试剂除特殊规定外均为分析纯,实验用水为超纯水。
硝酸、盐酸、硫酸、高氯酸均为优级纯(GR)。载流液(5%HCl):量取50 mL盐酸,慢慢倒入1 000 mL超纯水中,混匀。硼氢化钾溶液(10 g/L):准确称取2.50 g氢氧化钠,溶于超纯水中,彻底溶解,再称取5.00 g硼氢化钾溶于氢氧化钠溶液中,定容至500 mL。硫脲溶液(50 g/L):准确称取5.00 g硫脲,溶于100 mL超纯水中,溶解混匀(现用现配)。
1.2 仪器参数
光电倍增管负高压270 V;原子化器高度8 mm;灯电流60 mA;载气流量400 mL/min;屏蔽气流量800 mL/min;读数时间 7 s;延时时间 1.5 s。
2 样品前处理及标准曲线绘制
2.1 湿法消解前处理
准确称取固体试样0.50 g,置入50~100 mL锥形瓶中,同时做4份试剂空白。加硝酸30 mL,硫酸1.25 mL,摇匀后放置过夜,然后置于电热板上加热消解。加入1mL高氯酸,继续加热至消解完全,再持续蒸发至白烟散尽,冷却,加入50 g/L硫脲2.5 mL,定容至25 mL比色管中,样品稀释20倍待测。加热消解温度梯度为150℃1 h,200℃1 h,300℃消解至未有未分解物质或色泽几乎无色透明,消解赶酸至白烟散尽[4]。
2.2 微波消解前处理
A:准确称取固体试样0.50 g左右,置于消解罐中,同时做4份试剂空白,加入7 mL硝酸和2 mL过氧化氢摇匀,放置4 h。然后参照表1条件消解,消解完毕,150℃赶酸、冷却,转移至25 mL比色管中,加入2.5 mL盐酸、5 mL 50 g/L硫脲溶液,用纯水定容,稀释20倍待测。
B:消解同A,消解完毕冷却后,加入1.25 mL硫酸和1 mL高氯酸分别于150℃、200℃、300℃赶酸处理,冷却,转移至25 mL比色管中,加入2.5 mL盐酸,5 mL 50 g/L硫脲溶液,用纯水定容稀释20倍待测[8]。

表1 微波消解程序Tab.1 Microwave digestion process
2.3 干灰化前处理
准确称取固体试样0.50 g,同时做4份试剂空白,加入150 g/L硝酸镁10 mL混匀,低热蒸干,将氧化镁0.5 g仔细覆盖在干渣上,于电炉上碳化至无烟,移入500℃高温炉灰化4 h,取出冷却,加入(1+1)(V/V)盐酸 10 mL,移入 25 mL比色管中,加入 2.5 mL 50 g/L硫脲溶液,用(1+9)(V/V)硫酸分次刷洗坩埚合并,定容25 mL稀释20倍待测[4]。
2.4 标准曲线绘制
砷标准储备溶液(100 mg/L),由国家环境保护总局标准样品研究所提供。将储备液逐级稀释到10 μg/L,采用仪器自动稀释功能,测量 2.000、4.000、6.000、8.000、10.000 μg/L 五点的荧光值,绘制标准曲线。
3 结果与讨论
3.1 三种消解方法的原理及应用
湿法消解是通过氧化性酸和氧化剂,在加温加热条件下对有机质进行氧化、水解,达到无机化的目的。微波消解技术,现在已被广泛地应用到各行业的检测分析方法中,它通过加压加热来达到破坏有机质的目的,有着快速、安全、有效及使用试剂少、污染小的优点[5]。干灰化法是在供给能量的前提下,利用高温下空气中氧将有机物升温氧化(450~800℃)和碳化,有机物燃尽除去,挥发掉易挥发性组分,待测物保留在干灰中[6]。
3.2 水产品中总砷的消解条件
动物性海产品中均含有很大比例的砷甜菜碱和砷胆碱,植物性海藻中砷糖很丰富,但不存在砷甜菜碱。砷甜菜碱和砷胆碱在硝酸中加热会转化为三甲基胂氧化物,接着转化为二甲基胂酸(DMA)。植物性海藻中的砷糖在酸碱条件下会发生糖水解形成基础糖元[7]。
在硝酸氧化体系中,单甲基胂酸(MMA)在小于140℃条件下和二甲基胂酸(DMA)在小于200℃条件下稳定,二甲基胂酸(DMA)在300℃时放置90 min后才可完全转化为五价砷离子;砷糖在100℃加热10 min未发生显著改变,在60℃水浴中用6 mol/L盐酸提取18 h,砷糖部分或全部转化为DMA[9-11]。常用的消解方法湿法消解和微波消解的温度均不能使MMA和DMA完全转化为砷,但是达到300℃的消解条件,方法均可使用。
3.3 实验结果
3.3.1 湿法消解(按 2.1 处理)
由表2可知,贻贝粉和海带粉均符合标准。由此可见,湿法消解处理中加热达到300℃的条件,可破坏砷甜菜碱和砷胆碱,进行彻底的无机化消解,可以得到所要结果。此方法常用酸有硝酸、高氯酸、硫酸以及盐酸,在实际应用中常以混合酸形式在消化以提高消化效率。常压下,硝酸的沸点为86℃,高氯酸的沸点为200℃左右,硫酸沸点为338℃,盐酸沸点为108℃。国标中总砷的湿消化是以硝酸-硫酸体系、硝酸-硫酸-高氯酸体系来消化样品,该方法对大部分砷存在形式比较简单的样品尚能满足前处理要求,在样品中砷存在形态复杂的时候结果基本偏低,分析原因除了挥发损失外,最主要的还是温度过低,有些稳定的砷存在形态不能被完全无机化造成在仪器上无响应或者响应偏低。该方法耗费时间长,耗费试剂多,并需要专人看护以观察试剂的量值和避免碳化。
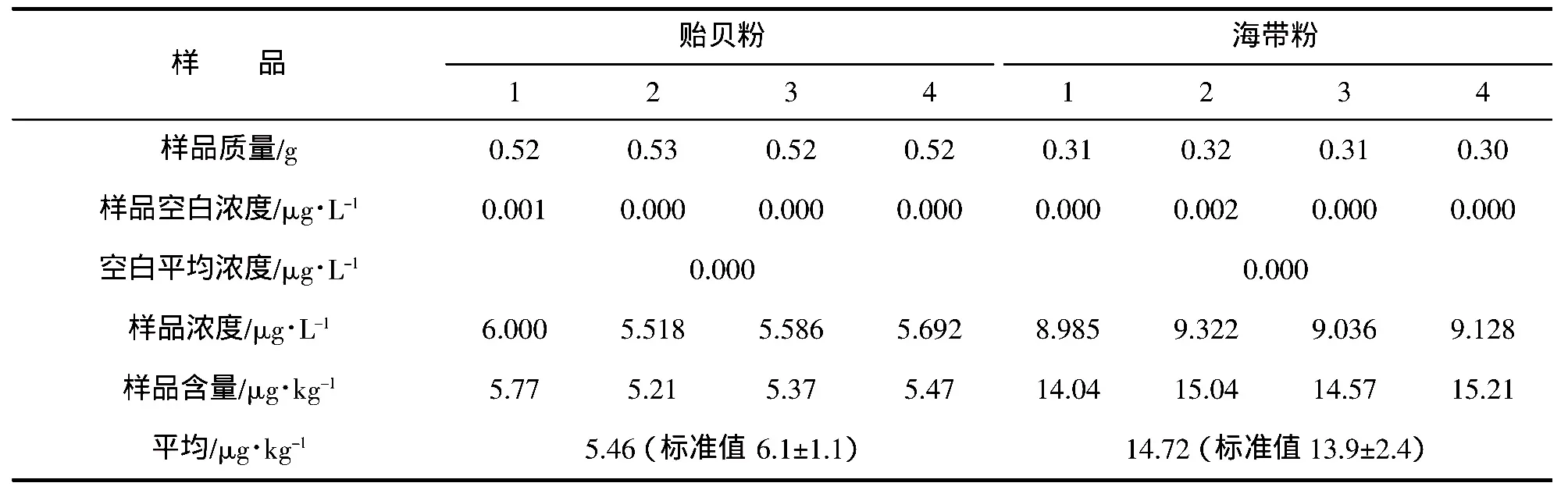
表2 湿法消解结果Tab.2 The results of wet digestion
3.3.2 微波消解(A)(按 2.2A 处理)
由表3可知,贻贝粉和海带粉均未符合标准,可知简单的微波消解无法彻底消解掉样品中所含的砷,即由于消解仪器对酸的使用的限制(众多的消解仪器不允许使用硫酸和高氯酸),即使加压加热,仍无法破坏掉砷的组织形态,而且微波消解仪器的加热温度限制在200℃无法达到要求。在微波消解的应用中发现对于不同类别的样品,所得结果满意度也不尽人意。微波消解系统对含有复杂形态的砷的水生生物样品消解不完全,部分物理化学性质稳定的砷化物不能被消解成无机砷形态,从而引起总砷的测定偏低。
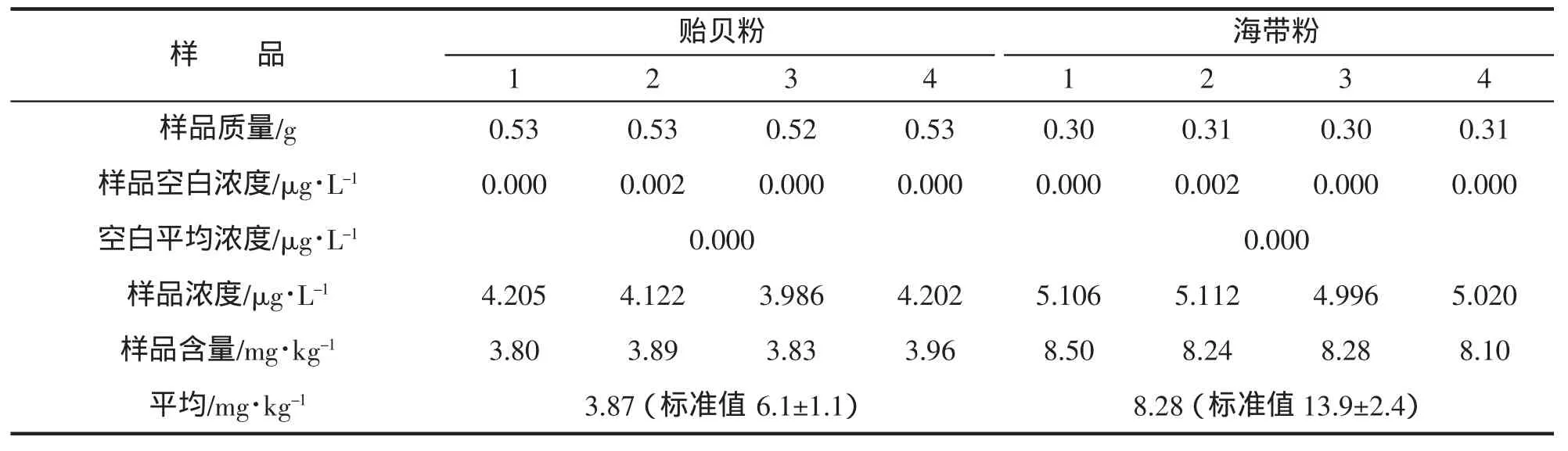
表3 微波消解(A)结果Tab.3 The results of microwave digestion(A)
3.3.3 微波消解(B)(按 2.2B 处理)
由表4可知,贻贝粉和海带粉所测结果符合标准,与(A)相比,(B)弥补了微波消解的缺陷,即微波消解+湿法消解的应用,弥补了微波消解对酸和温度的限制,好处就是缩短了湿法消解前处理的时间以及前期对酸的用量。此方法摆脱了酸和温度的限制,使水产品得到彻底消解,减少了污染,对批量不大的样品是个很好的选择。
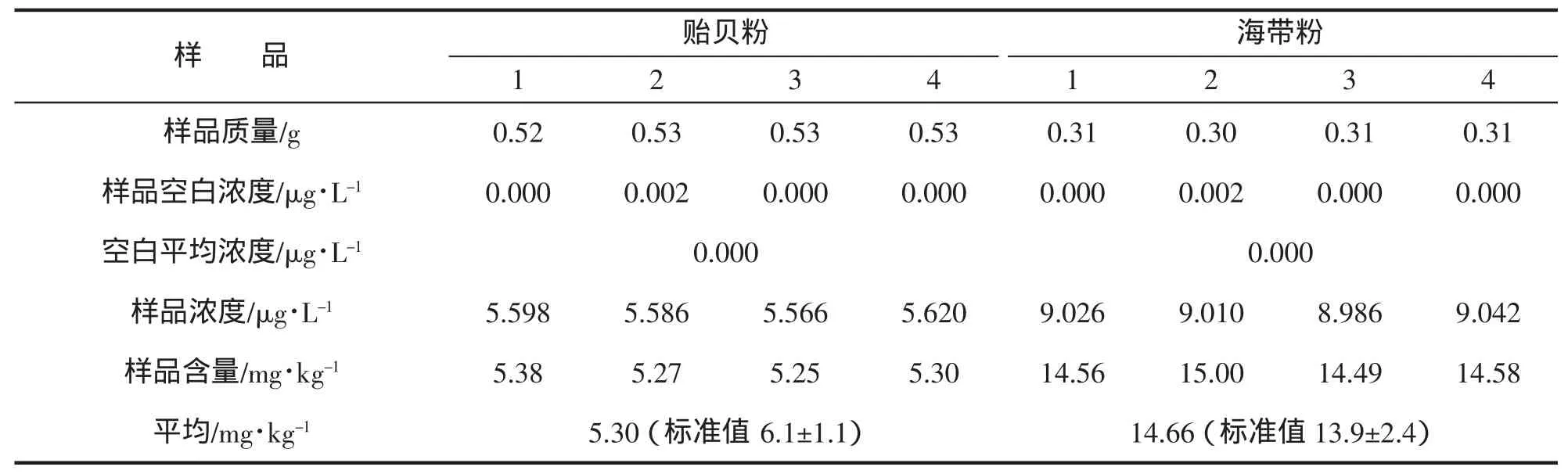
表4 微波消解(B)结果Tab.4 The results of microwave digestion(B)
3.3.4 干灰化(按 2.3 前处理)
由表5可知,贻贝粉所测结果符合标准,海带粉所测结果偏低。分析原因为海带粉是一种易燃的轻质粉末,在碳化过程中非常容易造成燃烧速度过快而导致样品飞溅,而且容易造成砷吸收剂轻质氧化镁覆盖层的破坏,在此情况下于500℃马弗炉灰化时会导致砷的严重损失。
干灰化法是一种日常样品元素分析中常用的前处理方法,尤其对挥发性温度比较高的元素。相对于湿法消解和微波消解,干灰化法简便,对湿法消解和微波消解由于消解温度低而不能消解的砷存在形态可以有效地进行无机化处理。该方法操作简便快捷,用酸种类少、用量少,时间短,不过对实验的空白要求高,低热蒸干、碳化对温度要求相对高,空白做出往往较高。因此对实验中的操作步骤要谨慎、注意。

表5 干灰化结果Tab.5 The results of dry ash
3.4 三种消解方法的试剂消耗及时间消耗
由表6可知,三种消解方法中湿法消解消耗酸试剂最多,消耗时间最长,干灰化次之,微波消解用酸量最少,时间最短。

表6 试剂消耗及时间消耗Tab.6 Reagent and time consumption
4 小结
由以上结果数据可知,对水产品的前处理,酸和温度是消解彻底与否的关键因素。
三种消解方法,湿法消解耗费时间最长,用酸种类多,用量大,但数据稳定,对实验操作要求较低,依据溶液的颜色可判断消解的程度且同时可处理大批量样品,是目前实验室使用最多的消解方法。微波消解(A),操作最简单,所用溶液最少,但是由于微波消解仪自身原因,使其对酸和温度的控制达不到彻底消解的条件,所测结果偏低,均不符合要求。微波消解(B),实际上是微波消解(A)和湿法消解的共同处理,相比湿法消解时间少,溶液用量少,结果符合要求。对于干灰化,温度过高会造成元素的损失,过低会导致无法彻底消解,而且受马弗炉空间要求的影响,一批测量的样品,数量相对较少,对空白要求高,现在大多实验室未采用此方法测量水产品。
因此,从对仪器的要求,对实验样品数量的要求,湿法消解是最易达到的条件,对大批量样品使用适宜。较少量样品且挥发温度高或油脂含量高的样品可采用干灰化处理,而微波消解可处理砷的存在形态结构相对简单的样品。
[1]陈 国,凌建刚,许秀琴,等.原子荧光法测定水产品中的无机砷[J].宁波农业科技,2006(4):5-8.
[2]张 静,彭新然,何弘水.微波消解原子荧光法测定食品中的砷[J].中国卫生检验杂志,2006,16(9):1 066.
[3]李 宏,陈 莉,杨汉卿.不同前处理方法对饲料中总砷测定的影响[J].饲料广角,2004(18):23-24.
[4]强卫国,杨惠芬,毛 红,等.GB/T 5009.11-2003 食品中总砷及无机砷的测定[S].北京:中国标准出版社,2004.
[5]郭 健,范稚莉,赵乃曼.氢化物原子荧光光度法测定水产品中的总砷[J].中国卫生检验杂志,2005,15(1):69.
[6]刘明钟,闫 军,陈志新,等.原子荧光应用手册[Z].北京吉天仪器有限公司,2007.
[7]孙建璋,孙庆海.海带(Laminaria japonica Aresch)含砷问题的探讨[J].现代渔业信息,2004,19(12):25-27.
[8]贺广凯,马永安,马新东,等.微波消解-原子荧光法测定海洋生物中As[J].海洋环境科学,2007,26(4):194-196.
[9]王雪芹.氢化物发生—原子荧光法快速测定食品中痕量砷[D].杭州:浙江大学,2008.
[10]郭莹莹.海藻中砷化物检测技术研究及食用安全性评价[D].青岛:中国海洋大学,2008.
[11]蒋瑾华,温巧玲,胡 思.动物源性食品中痕量无机砷的测定[J].光谱实验室,2006,23(4):751-754.

