4-酰基吡唑啉酮过渡金属配合物的合成、表征及生物活性研究
张彦翠,刘新文,董文魁
(1.兰州交通大学化工学院,甘肃 兰州 730070;2.天水师范学院生命科学与化工学院,甘肃 天水 741001)
4-酰基吡唑啉酮是一类重要的杂环β-二酮螯合剂,具有活性的双酮配体结构,可以与多种金属离子形成配合物,是金属离子良好的萃取剂和配位剂,同时具有一定的抗菌、抗病毒性能,广泛应用于药理、生物活性试剂、冶金、染料、发光材料等领域[1~7]。
近年来,研究发现酰基吡唑啉酮过渡金属配合物具有明显的抑菌活性,但对真菌类的抑菌性研究几乎没有。作者在此合成了4-酰基吡唑啉酮及其过渡金属新型配合物,并针对不同的细菌、真菌进行了抑菌活性测试,对进一步研究该类化合物在生物中的应用具有指导意义[8,9]。
合成路线如下:

M=Cu2+、Zn2+、Ni2+、Mn2+
1 实验
1.1 试剂与仪器
1-苯基-3-甲基-5-吡唑啉酮,分析纯,天津市科密欧化学试剂有限公司;苯甲酰氯,分析纯,国药集团化学试剂有限公司;二氧六环,分析纯,天津市化学试剂六厂;其它试剂均为市售分析纯。
2400型元素分析仪、FTIR-1730型红外光谱仪(KBr压片)、CS-9301PC型差热-热重分析仪、Lambda35型紫外可见分光光度计,美国铂金埃尔默有限责任公司;970CRT型荧光分光光度计,上海分析仪器总厂;X-4型显微熔点测定仪(温度未经校正);DDS-307型电导率仪,上海精密科学仪器有限公司。
1.2 1-苯基-3-甲基-4-苯甲酰基-5-吡唑啉酮配体(L)的合成[10]
称取20 mmol 1-苯基-3-甲基-5-吡唑啉酮加入到20 mL二氧六环中回流加热溶解,当反应体系温度上升至52℃左右时加入无水氢氧化钙3.0 g,摇匀,缓慢滴加2.4 mL(21 mmol)苯甲酰氯到二氧六环溶液中,升温继续回流1 h左右,得黄色浊液,温度控制在70~80℃。冷却后加入50 mL 2 mol·L-1HCl,搅拌,立即有黄色沉淀生成,过滤,水洗,用无水甲醇重结晶,干燥,得黄色片状晶体,m.p.92~92.7℃。
1.3 过渡金属配合物(ML2)的合成[11]
称取2 mmol配体L溶于10 mL热三氯甲烷中,1 mmol 的金属盐溶于适量无水乙醇中;加热回流配体L,滴加金属盐溶液出现沉淀,继续加热回流2~3 h,得有色溶液,温度控制在62~63℃。静置冷却,有沉淀析出,过滤,用无水乙醇洗涤数遍,用DMF重结晶,60℃真空干燥得有色晶体。
1.4 抑菌活性测定
1.4.1 培养基的制备[12]
细菌用牛肉膏蛋白胨培养基,真菌用马铃薯培养基。
1.4.2 试液的配制
以N,N-二甲基甲酰胺作溶剂,将配体及配合物配制成试液,质量浓度分别为2.0 mg·mL-1、2.5 mg·mL-1、3.0 mg·mL-1、3.5 mg·mL-1、4.0 mg·mL-1,备用。
1.4.3 方法
(1)将活化后的菌种制备成菌悬液,备用。
(2)在铺有培养基的培养皿中,注入0.1~0.2 mL的菌悬液,用涂布棒涂布均匀,备用。
(3)将吸取不同浓度试液的Φ=6.0 mm中性滤纸片置于涂有不同类型微生物的平板培养基上,每皿呈三角形摆放相同浓度药液的3个滤纸片,细菌、真菌分别在37℃、28℃恒温培养箱倒置培养5~7 d,测量抑菌圈直径。求3个抑菌圈的平均值。根据抑菌圈的大小可初步判断配合物的抑菌能力[13]。以上操作均在无菌条件下进行。
2 结果与讨论
2.1 元素分析与理化性质
称取0.05 g配合物于烧杯中,用1∶1的HClO4和HNO3混合回流分解后,产物溶于pH=10的氨水缓冲溶液中,以铬黑T作为指示剂,EDTA溶液滴定至终点,测定金属元素M、C、H、N的含量及配合物的摩尔电导率Λm,结果见表1。

表1 配体及配合物的元素分析及摩尔电导率数据
由表1可知,合成的配体L及配合物组成符合C17H14N2O2、MC34H26N4O4的化学式。在25℃、1×10-3mol·L-1的DMF溶液中配合物的摩尔电导率在8.8~18.9 S·cm2·mol-1之间,均属非电解质范围[7]。配合物可在空气中稳定存在,易溶于DMF、DMSO、丙酮、氯仿、乙腈等,微溶于冷乙醇、乙醚等,难溶于水。
2.2 红外光谱分析
配体和配合物的红外光谱特征吸收数据见表2。
由表2可知,配合物相互间各峰位移差别不大,但与配体吸收峰有明显差别。游离配体在中红外区出现吡唑酮环羰基、酰基羰基伸缩振动ν(C=O)、ν(C=O(1))的1759 cm-1和1498 cm-1吸收峰,形成配合物后,分别蓝移至1774~1783 cm-1和1522~1534 cm-1。在3100~3000 cm-1未发现烯醇式羟基氢键缔合峰ν(O-H…N),说明配体主要以酮式结构存在。配位后β-双酮产生互变作用,其吡唑啉酮环的ν(C=C)由1415 cm-1位移至1424~1441 cm-1,并在1350~1365 cm-1出现吡唑啉酮螯合环伸缩振动ν(C-O)。说明配体以烯醇式去质子形式参与配位。这表明,由于配位原子的成键作用,影响了相关基团键力常数,致使振动频率改变。此外,配合物在474~484 cm- 1附近的新峰,可归属为ν(M-O)。根据上述分析,可初步推测配合物中酰基羰基氧和吡唑啉酮环上互变烯醇式氧与过渡金属离子配位[14]。

表2 配体及配合物的红外光谱特征吸收数据(4000~400 cm-1)
2.3 差热-热重分析(表3)
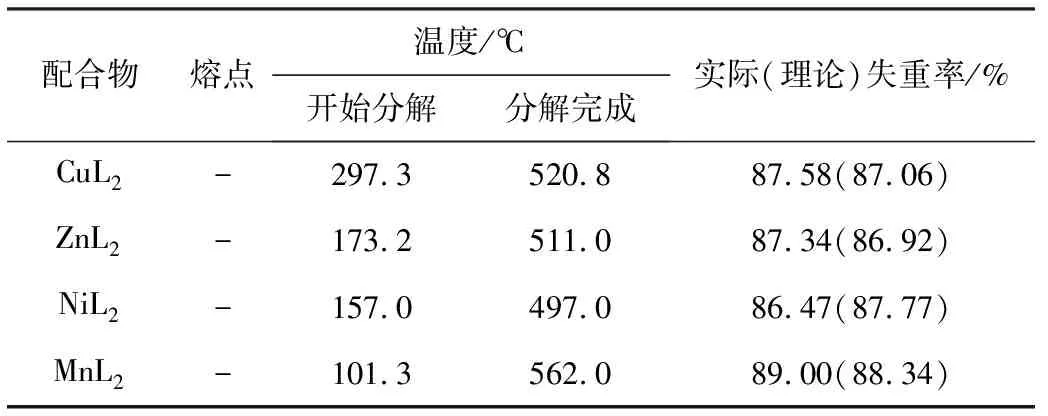
表3 配合物的差热-热重数据
以配合物CuL2为代表分析配合物的热稳定行为。由表3可知,CuL2从室温到297.3℃时化学组成稳定,相应的TG曲线基本没有失重,而DTA曲线在此温度区间无熔融吸热峰,因此配合物CuL2无固定熔点。CuL2在297.3℃开始氧化分解,在297.3~520.8℃,TG曲线有一系列的失重峰,而与此对应的DTA曲线则有一系列的放热峰,归属为配合物有机配位体的氧化分解以及中间产物的氧化分解等一系列变化,最终产物为CuO[15]。当温度高于520.8℃时,DTA和TG曲线均不再变化,累计失重率为87.58%,与理论值87.06%在实验误差范围内相符。
2.4 紫外光谱分析
以三氯甲烷为溶剂,将配体及配合物配制成浓度为1×10-5g·mL-1的溶液,在190~500 nm范围内测定紫外吸收光谱,结果见表4。

表4 配体及配合物在三氯甲烷溶液中的主要紫外吸收数据
由表4可知,所有配合物基本体现配体的吸收,在上述区域出现相应位移的吸收峰。配体的三氯甲烷溶液在紫外区240 nm、282 nm处出现2个强宽峰,分别对应于配体中共轭羰基和苯环的π-π*电子跃迁峰。与自由配体相比,配合物第一吸收峰基本落在配体两吸收峰之间,这可能和配体羰基的氧原子与中心离子发生配位作用引起C=O键极化,并影响了相关共轭分子轨道的状态有关,从而产生红移现象。第二吸收峰基本不变,说明配合物的吸收主要来自配体中共轭羰基的π-π*电子跃迁,配合物的生成对配体苯环的π-π*跃迁影响不大[15]。上述区域出现的两组吸收峰是配体与中心离子配位成键后,影响了配位原子周围的电子云密度,发生电荷迁移而影响相关共轭分子轨道的能级状态所致的[11]。
2.5 抑菌活性(表5)
抑菌圈是指平板培养基上微生物无法生长的透明圈。随着抑菌剂的不断扩散,浓度不断下降,达到临界抑菌浓度时,微生物开始生长,最终形成抑菌圈,这个临界浓度应为最佳抑菌浓度。但研究者一般认为随着抑菌剂浓度的不断增大,抑菌圈直径也不断增加,当两个相邻浓度的抑菌圈直径接近时,较低的浓度即为样品最佳抑菌浓度,这样判断既经济又有效。
由表5可知,同一种化合物对大肠杆菌、金黄色葡萄球菌、黑曲霉菌、米曲霉菌、白地霉菌、热带假丝酵母菌达到最佳抑菌效果时的质量浓度(mg·mL-1)分别为:L 2.5、3.5、3.0、2.5、3.5、3.5;CuL22.0、3.0、4.0、3.0、3.5、3.5;ZnL22.0、4.0、2.0、3.5、2.5、4.0;NiL24.0、3.0、3.0、3.0、3.0,对热带假丝酵母菌没有抑菌性;MnL24.0、3.5、3.5、2.5、3.5、3.5。
同样,不同物质对同一菌类抑菌效果不同。L、CuL2、ZnL2、NiL2、MnL2对同一菌类达到最佳抑菌效果时的质量浓度(mg·mL-1)分别为:大肠杆菌2.5、2.0、2.0、4.0、4.0;金黄色葡萄球菌3.5、3.0、4.0、3.0、3.5;米曲霉菌2.5、3.0、3.5、3.0、2.5;白地霉菌3.5、3.5、2.5、3.0、3.5;热带假丝酵母菌3.5、3.5、4.0、无、3.5;配体与配合物对黑曲霉菌的抑菌效果不是很明显。
总而言之,配合物比配体的抑菌效果明显,对细菌抑菌效果较好的配合物是ZnL2,而对真菌抑菌效果明显的配合物是CuL2、NiL2,配合物MnL2对细菌和真菌的抑菌效果一般。
3 结论
合成了4种4-酰基吡唑啉酮过渡金属配合物,对其抑菌活性进行了研究。结果表明,对细菌和真菌而言,配合物的抑菌效果好于配体的抑菌性[16];配体及配合物对细菌都具有一定的抑制作用,大部分的配合物对真菌有抑制作用,尤其对米曲霉菌和白地霉菌的抑制作用较明显。为进一步研究新型杀菌剂和防腐剂提供了理论依据,在医学、农业等领域有一定的影响意义。

表5 配体及配合物的抑菌圈数据
[1] 竹学友,俞志刚,刘洲亚,等.一种新型席夫碱及其铜配合物的合成与抑菌活性的研究[J].化学与生物工程,2008,25(4):43-45.
[2] 张姝明,贾永金,王瑾玲,等.1-苯基-3-甲基-4-三氯乙酰基-5-吡唑啉酮缩水杨酰肼席夫碱的合成表征及抑菌活性[J].天津师范大学学报,2003,23(2):4-6.
[3] 江强明,陈绍辉.新型稀土配合物发光材料的合成及性能研究初探[J].闽西职业技术学院,2008,10(2):96-98.
[4] 张有娟,魏少红,陈静.酰基吡唑啉酮席夫碱及其配合物的研究进展[J].商丘师范学院学报,2007,23(9):63-67.
[5] 李锦州,蒋礼,安郁美.酰基吡唑啉酮缩氨基酸席夫碱的合成及稀土配位性能和生物活性研究[J].中国稀土学报,2004,22(2):189-192.
[6] 李锦州,俞志刚,安郁美,等.酰基吡唑啉酮缩β-氨基酸稀土配合物的合成与光谱表征[J].光谱学与光谱分析,2005,25(9):1482-1485.
[7] Geary W J. Use of conductivity measurements in organic solvents for the characterization of coordination compounds[J]. Coord Chem Rev,1971,7(1):81-84.
[8] 何其庄,马树芝,许东芳.稀土酰基吡唑啉酮邻菲咯啉配合物的合成、表征及其生物活性[J].无机化学学报,2007,23(10):1723-1725.
[9] 乔永锋,董学畅,张莉.吡唑啉酮类配体及配合物的合成和抑菌活性[J].云南民族大学学报(自然科学版),2005,14(4):333-335.
[10] 吴宇雄,周尽花,赵鸿斌.1-苯基-3-甲基-4-苯甲酰基-5-吡唑啉酮的合成与结构表征[J].上饶师范学院学报,2004,24(6):47-49.
[11] 李琴,周德建,周永芬,等.铕与4-烷基酰代吡唑啉酮配合物的合成、表征与荧光性能[J].北京大学学报(自然科学版),1996,32(6):680-682.
[12] 沈萍,范秀容.微生物学实验(第四版)[M].北京:高等教育出版社,2003:35-75.
[13] 胡志和,庞广昌,陈庆森,等.不同条件下水解酪蛋白所得到的抗菌肽抑菌效果比较[J].食品科学,2003,24(2):130-133.
[14] 俞志刚,李锦州,刘双全.二苯基呋喃甲酰基吡唑啉酮及金属配合物的合成与电化学行为[J].应用化学,2004,21(12):1301-1305.
[15] 李琴,周德建,黄春辉,等.铽与1-苯基-3-甲基-4-异丁酰基吡唑啉酮-5和中性配体混配配合物的合成、表征及荧光性能[J].中国稀土学报,1997,15(4):297-298.
[16] 李锦州,于文锦,蒋礼.酰基吡唑啉酮缩邻苯二胺稀土配合物的合成,表征及生物活性[J].无机化学学报,2001,17(6):888-892.

