四丁基碘化铵催化合成螺[4.4]壬烷-1,6-二酮
螺[4.4]壬烷-1,6-二酮(化合物Ⅰ)分子具有C2对称性,分子中二个螺结的五元环基本相互垂直,整个分子不易扭变,刚性很强,是制备一些手性催化剂的前体[1]。外消旋的螺二酮经过不对称还原,可以得到光学纯螺二醇,可用于合成促进迪尔斯-阿德尔反应的路易斯酸配体。用它作为手性骨架的手性配体,可用于双键(C=C、C=O、C=N)的不对称催化氢化反应以及环氧化反应、硅氢化反应和氢转移反应等[2]。
Cram等[3]于1954年以丙二酸二乙酯为起始原料合成了外消旋化合物Ⅰ,操作过程较为复杂,产率很低,而以环戊酮-2-羧酸乙酯为原料,经过取代、脱羧、环化得到化合物Ⅰ的产率较高,其关键步骤是环戊酮-2-羧酸乙酯与4-溴丁酸乙酯的取代反应,需要以昂贵的KH[4,5]或是经过特殊处理的K2CO3[2]作为碱,在严格无水无氧条件下操作。
作者在文献[5]的基础上,对化合物Ⅰ的合成方法进行了改进:以廉价易得的碳酸钾为碱、以四丁基碘化铵(TBAI)为催化剂,在温和条件下以较高产率制备了4-(1-乙氧羰基-2-氧代环戊基)丁酸乙酯(化合物Ⅱ)。该反应不需要在低温无水条件下进行,原料价廉易得,反应时间短,简化了化合物Ⅰ的合成步骤。其合成路线见图1。
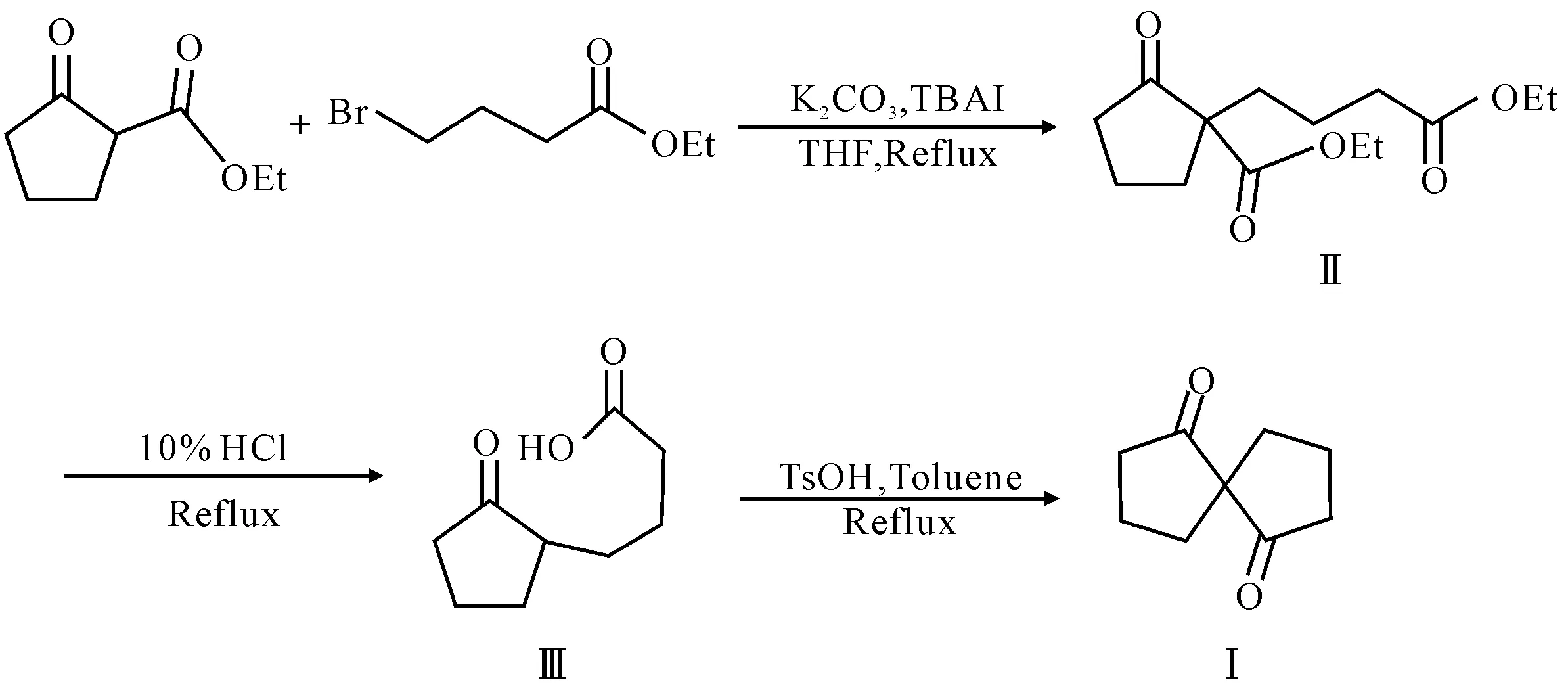
图1 螺[4.4]壬烷-1,6-二酮的合成路线
1 实验
1.1 试剂及仪器
环戊酮-2-羧酸乙酯和4-溴丁酸乙酯经重蒸纯化,其它试剂均未经处理。
Varian Unity INOVA 600型(600 MHz)核磁共振仪(氘代氯仿或DMSO为溶剂,TMS 为内标);PE-Spectrum One型红外光谱仪(KBr压片)。
1.2 方法
1.2.1 4-(1-乙氧羰基-2-氧代环戊基)丁酸乙酯(化合物Ⅱ)的合成
将环戊酮-2-羧酸乙酯(0.132 g,0.849 mmol)、4-溴丁酸乙酯(0.182 g,0.934 mmol)、碱(1.0 mmol)、四丁基碘化铵(摩尔分数0%~50%)、溶剂 (4.5 mL) 加入到三颈烧瓶中,加热回流,TLC监测原料环戊酮-2-羧酸乙酯消耗完后,真空去除溶剂,加入10 mL水,分别用氯仿和无水乙醚萃取。有机相用无水Na2SO4干燥,过滤,去除溶剂。粗品经硅胶柱层析纯化得无色油状液体0.192 g,产率87%。1HNMR (CDCl3,600 MHz),δ:4.18~4.15 (q,J=7.2 Hz,2H),4.14~4.10(q,J=7.2 Hz,2H),2.55~2.39 (m,2H),2.32~2.24 (m,3H),2.02~1.91 (m,4H),1.71~1.54 (m,3H),1.26~1.24 (t,J=7.2 Hz,6H)。
1.2.2 4-(2′-环戊酮基)-1-丁酸(化合物Ⅲ)的合成[5]
在圆底烧瓶中,加入化合物Ⅱ(1.078 g,4.0 mmol)和10% HCl(32 mL),加热回流12 h。反应混合物用无水乙醚萃取,乙醚层再用饱和NaHCO3溶液洗涤。饱和NaHCO3层用稀盐酸酸化至pH值≤2,再用无水乙醚萃取。有机相用无水Na2SO4干燥,过滤,去除溶剂。粗品经硅胶柱层析纯化得无色油状液体0.558 g,产率78%。
1.2.3 螺[4.4]壬烷-1,6-二酮(化合物Ⅰ)的合成[5]
在圆底烧瓶中,加入化合物Ⅲ(0.405 g,2.637 mmol)、TsOH (0.223 g,1.174 mmol)、甲苯(18 mL), 加热回流,用油水分离器分水,TLC监测反应完成后,加入饱和NaHCO3溶液,剧烈搅拌15 min。水相用无水乙醚萃取,合并有机层,用无水Na2SO4干燥,过滤,去除溶剂。粗品经硅胶柱层析纯化得白色固体0.248 g,m.p.38.5℃(文献值[5]m.p.38~40℃),产率69%。IR:1746 cm-1(-C=O)。1HNMR (CDCl3,600 MHz),δ:2.42~2.34,(m,4H),2.32~2.27 (m,2H),2.22~2.15 (m,2H),1.94~1.87 (m,2H),1.84~1.80 (m,2H)。
2 结果与讨论
在以TBAI为相转移催化剂合成化合物Ⅱ的过程中,溶剂选择、碱、催化剂用量对产率和反应时间的影响见表1。
从表1可以看出,当以极性较小的二氯甲烷或三氯甲烷作溶剂时,在回流温度下,反应几乎不发生或产物成分复杂、难以分离;以极性较强的乙腈或THF作溶剂时,能够分离得到目标产物, 且以THF作溶剂更好,此时反应时间短(4 h),产率高(77%)。
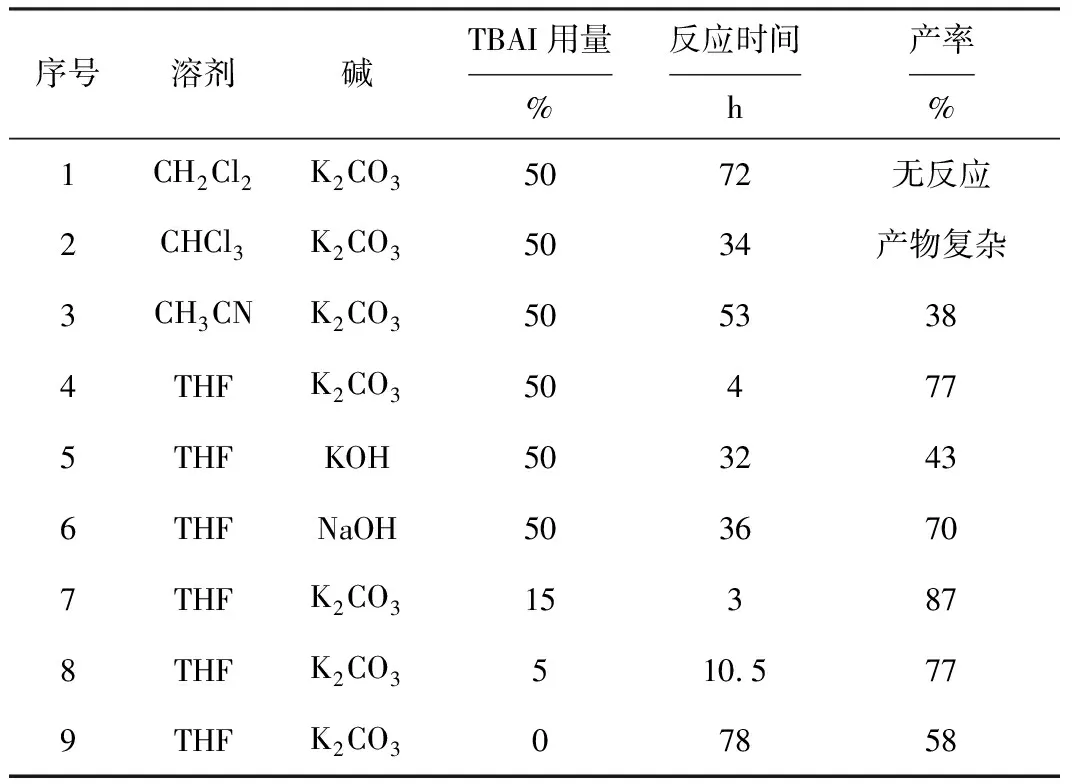
表1 在不同反应条件下化合物Ⅱ的产率
从表1还可以看出,常用的三种碱KOH、NaOH和K2CO3相比较,以碳酸钾为碱时,产率最高(77%),反应时间最短。这可能是因为使用KOH、NaOH时,反应体系中OH-浓度大,更容易与4-溴丁酸乙酯反应生成副产物,导致化合物Ⅱ的产率偏低。
考虑到TBAI在反应中除作为相转移催化剂外,还可能与4-溴丁酸乙酯反应生成4-碘丁酸乙酯,从而加快反应速度。所以,研究中首先加入较大量的TBAI(50%);进一步研究表明,TBAI用量为15%比较好,此时不仅反应时间短(3 h),而且产率很高,达到87%。
3 结论
改进了螺[4.4]壬烷-1,6-二酮的合成方法。以四丁基碘化铵(15%)作为相转移催化剂、碳酸钾(1.0 mmol)作为碱、THF作为溶剂,在环戊酮-2-羧酸乙酯和4-溴丁酸乙酯摩尔比为1∶1.1时,合成了4-(1-乙氧羰基-2-氧代环戊基)丁酸乙酯,将其进一步水解脱羧和关环反应得到了螺[4,4]壬烷-1,6-二酮,三步总产率为47%。该法条件温和,操作简便,不仅缩短了反应时间,而且降低了原料成本、简化了实验步骤。
参考文献:
[1] Nakazaki Masao,Chikamatsu Hiroaki,Asao Masaaki.Microbial s-tereodifferentiating reduction of l,6-spiro[4.4]nonanedione,a gyrochiral diketone with two homotopic carbonyl groups[J].Journal of Organic Chemistry,1981,46(6):1147-1151.
[2] 张毅,韩晓燕,郝金库.外消旋螺环二酮的合成工艺条件研究[J].天津化工,2006,20(1):17-19.
[3] Cram Donald J,Steinberg Howard.Synthesis and properties of derivatives of spiro[4.4]nonane[J]. J Am Chem Soc,1954,76(10):2753-2757.
[4] Nieman James A,Parvez Masood,Keay Brian A.An improved s-ynthesis and resolution of (±)-cis,cis-spiro[4.4]nonane-1,6-diol[J].Tetrahedron:Asymmetry,1993,4(9):1973-1976.
[5] Nieman James A,Keay Brian A.An efficient synthesis and resolution of (±)-cis,cis-spiro[4.4]nonane-1,6-diol[J].Synthetic Commun,1999,29(21):3829-3840.

