脑出血合并急性肺损伤 IFN-γ表达的研究
冯维龙,高先彬,葛恒超
脑出血后出现的急性肺损伤 (acute lung injury,ALI)是一个较为的严重并发症,可使肺的通气和换气功能受损,增加患者的病死率和致残率。大量研究证实这种损伤与脑出血导致的全身非特异性炎症反应有关,这种炎症反应引发多种炎性细胞过度激活及多种炎性介质的过度释放,并产生连锁反应,导致肺组织及多个器官功能受损,严重时出现多器官功能衰竭。IFN-γ是一种由 CD和 CD的 T淋巴细胞生产的炎性细胞因子,具有多种生物学活性,本实验旨在研究 IFN-γ是否在急性肺损伤中起作用。
1 材料与方法
1.1 动物及分组 正常成年 SD大鼠 (由贵阳医学院实验动物中心提供)80只,体质量在 250~300g。分为两组:脑出血组 (A组)与对照组 (B组)。
1.2 用自体血注入法建立动物模型 以 10%的水合醛腹腔注入麻醉动物,大鼠固定在江湾 I型立体定向仪 C上,切开皮肤、颅骨钻孔,A组大鼠从尾部取自体血 50μl,在 3~5min内注入尾状核 (沿钻孔垂直进针 7mm);B组用 0.9%氯化钠溶液 50μl注入尾状核。
1.3 检测方法 常规灌注,石蜡包埋,切片,厚度为 5μm,用免疫组化法 (SABC法)检测 IFN-γ的表达情况。一抗为多克隆兔抗大鼠 IFN-γ抗体,二抗为山羊抗兔 IgG,过氧化酶标记。
1.4 结果判定 A组大鼠采用 Longa四分法进行神经功能缺损评分,评分在 1~3分,即术后出现对侧前爪不能伸展,行走时向偏瘫侧转圈或行走时向偏瘫侧倾倒者为成功模型。观察在 400倍光学显微镜下采集免疫组化图像并输入 Biomias99图像分析系统 (四川大学图像图形研究所研制),每张切片随机选取 5个视场,取视场面积为:443268mm2,每个视场进行阳性细胞计数。
2 结果
2.1 实验动物一般情况 出血组动物术后出现体质量下降毛皮晦涩,并出现不同程度的偏瘫,轻度者出现前爪不能伸展,严重时出现行走向偏瘫侧倾倒。对照组动物则仅出现术后一过性懒动倦怠,无偏瘫的出现。
2.2 肺组织的大体改变 A组大鼠可见双侧肺组织肿胀,重量增加,呈淡红色,严重者实变成暗红色,双肺散在大小不一的出血点,切面上可挤出淡红色浆液。对照组肺组织无肿胀,呈白色,无出血点,切面无浆液渗出。
2.3 IFN-γ表达阳性细胞结果的测定 在出血组大鼠肺组织中可发现 IFN-γ表达阳性细胞,胞浆呈棕黄色,胞膜表达少。
2.4 细胞计数及统计学分析见表1。
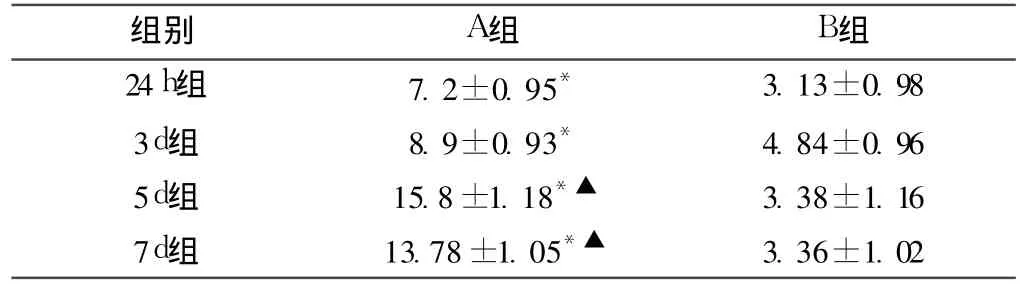
表1 各组阳性细胞计数Table1 The number of postive macrophages in different group
3 讨论
机体在脑出血等严重创伤打击下,会引发一种非特异性炎症反应,这种炎症反应可以是从局部逐渐发展致全身,也可以是一开始就是全身性的,人们将这种非特异性的炎症反应定义为全身炎症反应综合征 (systemic inflammatory response syndrome SIRS)。SIRS通过炎性细胞的过度激活及炎性递质的过度释放损伤机体的器官,出现急性肺损伤,严重时出现多器官功能衰竭 (multiple organ failure MOF)。
3.1 炎症反应的发生与转归 炎症反应发生较早,脑出血后24h即可出现,但程度较轻,此时肺组织出现轻度的充血,少量炎性细胞浸润,炎性细胞因子 IFN-γ表达开始增加;出血发生后 3~7d炎症反应明显加强,肺泡内出现大量的浆液渗出,较多的炎性细胞浸润,主要以单核一巨噬细胞为主,炎性细胞因子 IFN-γ表达进一步增强。
3.2 炎性细胞因子 IFN-γ作用及与肺损伤的关系 IFN-γ是一种重要的炎性细胞因子,本次实验发现在脑出血合并肺损伤时 IFN-γ表达增强,与肺损伤严重程度有明显的相关性。IFN-γ主要是由 CD4和 CD8 T淋巴细胞产生,该因子发挥生物学作用必须与相应的受体结合,IFN-γ受体存在于单核-巨噬细胞,NK淋巴细胞。IFN-γ的生物学效应:能广泛使各种类型的炎性细胞表达 MHC-II类抗原,放大了免疫应答的识别阶段,IFN-γ还是一种强有力的单核-巨噬细胞激活剂。激活的炎性细胞可直接损伤肺组织,还可释放炎性递质如过氧化物,蛋白酶破坏肺部细胞和组织,导致肺脏结构和功能受损。
1 龚非力.医学免疫学 [M].北京:中国医药科技出版社,2000:125-129.
2 Cong C,Hoff JT,Keep RF.Acute inflammatory reaction following experimental intracerebral hemorrhage in rat[J].Brain Res,2000,14(1):57-65.
3 王松.急性脑血管病患者伴全身炎症反应综合征和多器官功能衰竭综合征的临床观察 [J].脑与神经疾病杂志,2004,12(2):130-133.
4 Wu S,Fang CX,Kim J,et al.Enhanced pulmonary inflammation following experimental intracerebral hemorrhage[J].Exp Neurol,2006,200(1):245-249.

