镁离子掺杂对Li4Ti5O12/C结构和电化学性能的影响
尹艳红,范志娟,闫林林,谷继峰,杨书廷
(1.河南师范大学化学与环境科学学院,河南新乡 453007;2.河南省动力电源及关键材料工程技术研究中心,河南新乡 453007)
随着锂离子电池在电子产品中的广泛应用,它已成为具有优良性能的可充电电池。负极材料在锂离子电池中有着举足轻重的地位。目前锂离子电池的负极材料大多采用各种嵌锂碳材料。但是碳电极的电位与锂离子的电位很接近,当电池过充电时,碳电极表面易析出金属锂,会形成枝晶引起短路;温度过高时易引起热失控等。因此,寻找能在比碳负极电位稍正的电位下嵌入锂,廉价易得、安全可靠和高比容量的新的负极材料是很有意义的课题。
尖晶石结构的钛酸锂Li4Ti5O12是一种“零应变”插入材料[1-4],它以优良的循环性能和极其稳定的结构而成为锂离子电池负极材料中受到广泛关注的一种材料。另外,Li4Ti5O12有很好的充放电平台[5];相对于Li/Li+电对的还原电位高达1.5 V,不与电解液反应;价格比较便宜,更容易制备且成本更低。但Li4Ti5O12中锂离子导电性和电子导电性很低,成为影响其应用于实践的瓶颈。为提高材料的离子导电性和电子导电性,人们做了大量研究工作[6-8]。当前,通过碳掺杂在一定程度上来弥补Li4Ti5O12电子导电性差这一缺陷,通过金属离子的掺杂在一定程度上来弥补Li4Ti5O12中锂离子导电性差的缺陷。但少量碳的掺杂也会使材料的振实密度降低[9]。
所以,本工作在以葡萄糖为碳源的基础上,以乳酸镁为高价离子掺杂源和部分碳源,葡萄糖为碳源,采用高温固相法合成掺杂Mg2+的Li4Ti5O12/C复合负极材料。目前为止,还没有对乳酸镁为高价离子掺杂源和部分碳源,高温固相法合成Li4Ti5O12/C复合负极材料这方面的报道。
1 实验
1.1 材料的制备
将Li2CO3、TiO2(均为分析纯)按 4︰5(质量比,其中 Li过量8%以弥补高温下的挥发)称重后溶于无水乙醇中,加入10%(摩尔分数)的葡萄糖作为碳源,高速球磨2 h,待原料混匀干燥后,在氮气气氛下马弗炉中,先以10℃/min升温到600℃恒温6 h,再以5℃/m in升温到800℃恒温12 h,反应完成后随炉冷却至室温,研磨后得灰白色样品,记为Sample b;在混料时加入9%的葡萄糖和1%的乳酸镁,按照上述合成方法制备掺杂样品,记为Sample c;按上述方法制备的纯样品,记为Sample a。
1.2 Li4Ti5O12/C复合正极材料的物理性能表征
XRD测试所用仪器为德国布鲁克AXS公司生产的D8X射线衍射仪,管压 40 kV,管流 40 mA,Cu靶 Kα射线(λ=0.154 06 nm)。FESEM测试采用日本日立公司生产的S-4800型号场发射电子显微镜,加速电压25 kV。粒度分析采用珠海欧美克科技有限公司生产的LS-POP(Ⅲ)型激光粒度测试仪,水为分散剂,超声分散5m in。比表面积测试用JW-004型全自动氮吸附比表面积仪 (北京精微高博科技有限公司),液氮为吸附质。材料的振实密度按照国家标准GB5162-85测量。
1.3 Li4Ti5O12/C复合正极材料的电化学性能表征
所合成的材料为活性物质,乙炔黑为导电剂,聚四氟乙烯(PVDF)为粘合剂,按质量比85︰10︰5溶解在溶剂N-甲基吡咯烷酮(NMP)中混合均匀形成浆料,将浆料均匀涂在铝箔上,涂层的厚度约为100μm,将涂好的电极片裁剪成大小面积为1 cm2的工作电极,110℃干燥后0.3MPa下压片,测试电池采用常规的扣式电池,以金属锂为对电极及参比电极,聚丙烯celgard2400为隔膜,lmol/L的LiPF6-EC+DEC(1︰1)为电解液。在充满氮气的手套箱(ZKX3,南京大学仪器厂)中组装模拟电池。用LAND电池测试系统(武汉兰电电子有限公司)室温下在不同倍率进行充放电循环测试,电压范围为2.1~1.0 V。交流阻抗(AC Impedance)测试在电化学工作站(CHI660B,上海辰华仪器公司)上进行。
2 结果与讨论
2.1 物理性能表征
图1为掺杂前后的XRD图。经过800℃热处理12 h后所得的样品a,样品b和样品c的结晶度都很高。与标准的Li4Ti5O12衍射谱相比可以看到,样品a、b、c是基本上结晶比较完全,表现为 2θ=18.37°、35.60°、43.27°、47.38°、57.23°、62.86°、66.09°时出现的几个强的特征峰。由于掺杂量很少并没有改变Li4Ti5O12的晶体结构,与文献[10]报道一致。物相分析表明,三种材料的XRD图与钛酸锂的标准JCPDS卡片(26-1198)相符,为尖晶石结构,没有观察到其它杂相的存在,说明Mg2+已进入Li4Ti5O12晶格内部。

根据图1中衍射峰计算a、b、c三个样品的晶胞参数a值分别为0.835 8、0.835 6、0.837 2 nm,比较可知,碳包覆后晶胞参数几乎没有变化。碳元素的加入未改变Li4Ti5O12的晶胞参数,是因为碳仅包覆在材料的表面,而乳酸镁为高价离子掺杂源和部分碳源制备的Li4Ti5O12/C复合负极材料的晶格常数稍微变大。因为Mg2+与Li+的半径非常相近,高价态Mg2+取代Li+,实现了有效高价掺杂,镁掺杂(Mg2+取代Li+)后的效应是产生了一个更接近于导带低的载流子,从而提高了材料的体相导电性能。其次,也可能是因为二价镁离子捕获材料中的电子来补偿其正电荷缺陷,一方面使材料中电子有效密度降低,另一方面提高了材料的空穴,有利于充放电过程中Li+的插入和脱插。
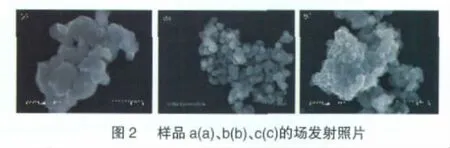
图2所示为样品的FESEM照片。样品a颗粒堆积无序,大小不均;碳包覆样品b和掺杂样品c颗粒半径减小、大小均一且呈明显的椭球状堆积,说明碳材料的添加有助于抑制颗粒的长大,增加粒子与粒子之间的电接触,与Guerfi[7,11]等报道相一致,这样既有利于得到高的振实密度同时也有利于电解液与材料之间的充分接触,提高活性物质的插脱锂深度。
对镁掺杂前后样品的粒度、比表面积、振实密度进行了研究,结果见表1。由表1可见,掺杂材料的比表面积增大,振实密度明显提高,这和FESEM照片显示结果是一致的。其中样品b和样品c颗粒大小相近,样品c的比表面积稍大于样品b的且有团聚现象,可能是因为高比表面积的小颗粒更容易趋向于团聚在一起,以减少比表面结合能,获得稳定结构。掺杂后材料的振实密度由掺杂前的1.13 g/cm3增加到1.35 g/cm3和1.40 g/cm3。合适的比表面积和振实密度使材料与电解质接触紧密,提高Li4Ti5O12材料的活性颗粒插脱锂深度,提高材料的电化学性能,同时有利于材料的电极加工。

表1 样品a、b、c的粒度、比表面积、振实密度
2.2 电化学性能表征
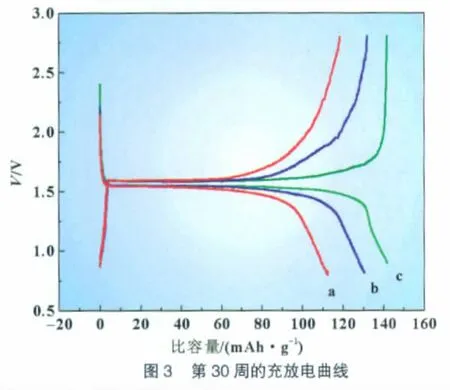
图3是样品a、b、c第30周的充放电曲线。对三种电极活性材料在0.7~2.7 V和1/3C的条件下进行了充放电测试。从图可知,三种材料的充放电曲线都在1.55 V左右有一个比较长的放电平台,即Ti4+被还原为Ti3+,电极活性材料由Li4Ti5O12转化为Li7Ti5O12,进行了正常的可逆反应[5,12]。镁掺杂的Li4Ti5O12/C复合材料第30周的放电比容量为142mAh/g,比没有镁掺杂的Li4Ti5O12/C材料(130mAh/g)提高了12mAh/g,比纯Li4Ti5O12(112mAh/g)提高30mAh/g。且镁掺杂的Li4Ti5O12/C复合材料平台区域更长、电压更稳定,材料性能更优,说明掺杂后减小了充放电过程中的极化现象。Li4Ti5O12充放电过程是受锂离子扩散以及电荷转移步骤所控制的[13-14]。镁离子掺杂后,为了保持电荷平衡,在贫锂和富锂两相中均存在一定量的Ti4+/Ti3+混合价态[10],这有助于改善锂离子脱嵌过程中两相界面的电子导电性,从而降低电荷转移阻抗,减小极化。这一点也可以从图5所示的交流阻抗谱图中得到证实。
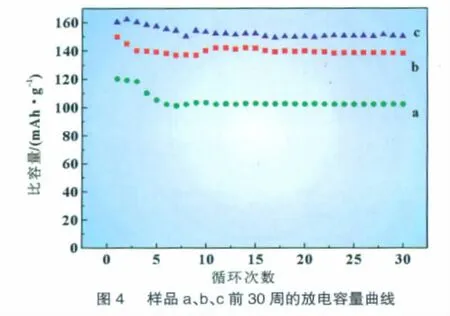
图4为镁掺杂前后材料的前30周的循环性能。起始的几次循环中两种材料存在衰化过程,在第10次循环均有活化过程且以后的循环稍有衰减。样品b在第11次循环达到最大比容量140.2mAh/g,随后的循环几乎一直保持最大容量;样品c在第9次循环达到最大值151.2mAh/g,随后的循环一直保持最大容量且有活化过程。这表明掺杂前后材料均表现良好的循环性能,特别是掺杂Mg2+循环性能更优,后20次循环后容量无衰减现象。充放电性能研究结果表明,掺杂乳酸镁为Mg2+的掺杂源和部分碳源不仅能提高Li4Ti5O12/C充放电容量,对其循环性能也有所改善。

为了进一步探讨乳酸镁的加入在合成Li4Ti5O12/C中所起的作用,本工作用交流阻抗法考察了乳酸镁的加入对于材料电导率的影响。图5为掺杂镁前后样品的阻抗性能的变化图谱,图中显示三条曲线均由高频区的半圆和低频区的直线组成,高频区的小半圆反映的是电解质/氧化物电极界面的电荷传输所引起的阻抗,低频区的直线则反映了锂离子在氧化物电极界面扩散所引起的Warburg阻抗[15]。掺杂碳材料后,Li4Ti5O12在充放电过程中的电荷转移阻抗值大幅度降低,材料Rct从180Ω左右降低为约45Ω,尤其是掺杂乳酸镁后,虽然Rct值同样降低约45Ω,但直线斜率更大,反应了掺杂Mg2+后插锂过程的快速动力学机制,有利于克服充放电过程中的动力学限制,使Li4Ti5O12活性颗粒中的嵌锂深度得到提高,并降低活性颗粒表面与内部存在的Li+浓度差,从而降低电池极化,提高放电容量,改善循环性能。这与图4中放电容量活化相一致。
3 结论
以乳酸镁作为Mg+的掺杂源和部分碳源制备的材料,采用二步固相合成反应法制备了Li4Ti5O12尖晶石材料,掺杂后增大了晶胞参数,但未引起尖晶石结构的变化。对掺杂前后样品a、b、c进行电化学性能对比测试表明,掺杂后材料充放电过程中的电荷转移阻抗显著减小,有利于克服充放电过程的动力学限制,降低电池极化,提高材料的可逆容量和循环性能;尤其是乳酸镁掺杂的电极材料效果最明显,碳包覆提高了材料的电子导电性,而镁掺杂后的效应是产生了一个更接近于导带低的载流子,使Li+可快速嵌入和脱出,同时提高了材料的离子导电性和电子导电性,掺杂后获得了较好的可逆容量和循环性能。掺杂后的材料在比表面积增大的情况下振实密度比掺杂前增加了0.27 g/cm3。
[1] OHZUKU T,UEDA A,YAMAMOTO N J.Zero-strain insertion material of Li[Li1/3Ti5/3]O4for rechargeable lithium cells[J].Electrochem Soc,1995,142:1431-1435.
[2] 唐致远,阳晓霞,陈玉红,等.钛酸锂电极材料的研究进展[J].电源技术,2007,31(4)332-336.
[3]WANG G X,BRADHURSTD H,DOU SX,etal.Spinel Li[Li1/3Ti5/3]-O4asan anodematerial for lithium ion batteries[J].JPower Sources,1999,83:156-150.
[4]TSUTOMU O,ATSUSHIU.Why transitionmetal(di)oxidesare the mostattractivematerials for batteries[J].Solid State Ionics,1994,69:201-205.
[5] NAKAHARA K,NAKAJIMA R,MATUOHIMA T.Preparation of particulate Li4Ti5O12having excellent characteristics as an electrode activematerial for power storage cells[J].JPower Sources,2003,117:131-136.
[6]HUANG SH,WEN Z Y,ZHU X J,eta1.Preparation and electrochem ical performance of Ag doped Li4Ti5O12[J].Electrochem Commun,2004,6:1093-1097.
[7] GUERFIA,CHAREST P,KINOSHITA K,et a1.Nano electronically conductive titanium-spinel as lithium ion storage negative electrode[J].JPower Sources,2004,126:163-168.
[8]GUERFIA,SEVIGNY S,LAGACEM,eta1.Nano-particle Li4Ti5O12spinel as electrode for electrochem ical generators[J].J Power Sources,2003,ll9-l2l:88-94.
[9] CHEN Z,DAHN JR.Reducing Carbon in LiFePO4/C Composite Electrodes to Maxim ize Specific Energy,Volumetric Energy,and Tap Density[J].JElectrochem Soc,2002,149:A1184-A1189.
[10] CHEN C H,VAUGHEY J T,JANSEN A N,et al.Studies of Mg-substituted Li4–xMgxTi5O12spinel electrodes(0≤x≤1)for lithium batteries[J].Electrochem Soc,2001,148(1):A102-A104.
[11]GUERFIA,SEVIGNY S,LAGACEM,eta1.Nano-particle Li4Ti5O12spinelas electrode for electrochemical generators[J].JPower Sources,2003,ll9-l2l:88-94.
[12]HUANG SH,WEN Z Y,ZHU X J,eta1.Preparation and electrochemicalperformance of Ag doped Li4Ti5O12[J].Electrochem Commun,2004,6:1093-1097.
[13] SCROSATIB,PANERO S,REALE P,etal.Investigation of new types of lithium-ion battery materials[J].JPower Sources,2002,105:161-168.
[14]SINGHAL A,SKANDAN G,AMATUCCIG,et al.Nanostructured electrodes for nextgeneration rechargeable electrochem ical devices[J].JPower Sources,2004,129:38-44.
[15]CHUNG S Y,CHIANG Y M.M icroscale measurements of the electrical conductivity of doped LiFePO4[J].Electrochem Solid StateLett,2003,6(12):A278-A281.

