酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠的影响
张 锐,姚芳芳,何 伟*
(1.郑州大学公共卫生学院,河南 郑州 450001;2.河南省医药科学研究院,河南 郑州 450052)
酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠的影响
张 锐1,姚芳芳1,何 伟2,*
(1.郑州大学公共卫生学院,河南 郑州 450001;2.河南省医药科学研究院,河南 郑州 450052)
目的:研究酪蛋白磷酸肽(CPPs)、钙粉及二者复合物对高尿酸血症大鼠血清尿酸(UA)、总胆固醇(TC)、黄嘌呤氧化酶(XOD)、腺苷脱氨酶(ADA)及肝脏XOD和ADA的影响。方法:用腺嘌呤(100mg/(kg bw·d))+乙胺丁醇(250mg/(kg bw·d))给大鼠灌胃3周,造成高尿酸血症模型,再在饲料中加入酪蛋白磷酸肽、钙粉以及二者复合物对其进行干预28d。结果:干预前造模大鼠的血尿酸水平高于空白组;和模型组相比,各干预组大鼠血清UA和TC水平均降低,同时各组肝脏中XOD、血清和肝脏中ADA活性均低于模型组,其中复合组的效果最为明显(P<0.05)。结论:酪蛋白磷酸肽结合钙粉可相对更好地促进尿酸降低。
高尿酸血症;酪蛋白磷酸肽;钙;尿酸;总胆固醇
Abstract:Objective:To study the effects of casein phosphopeptides (CPPs), high-calcium diet and their combination on uric acid (UA), total cholesterol (TC), xanthine oxidase (XOD) and adenosine deaminase (ADA) in the serum and XOD and ADA in the liver of hyperuricemic rats. Methods:Hyperuricemic model rats were induced by intragastric administration with adenine(100 mg/(kg bw·d)) and ethambutol (250 mg/(kg bw·d)) for 3 weeks. The model rats were then treated with foods containing CPPs, high-calcium diet and their combination for 28 days. After intervention for 28 days, UA, TC, XOD and ADA in serum and XOD and ADA in liver were determined. Results:Serum uric acid level of rats induced by intragastric administration was significantly higher than that in the control group before intervention. Compared with the model rats, each intervention group exhibited an obvious decrease in UA and TC levels. The XOD activities in all the intervention groups were all lower than those in the liver of the model group, and the ADA activities in all the intervention groups were lower than those in both the serum and liver of the model groups, especially in high-calcium diet and their combination intervention groups (P< 0.05). Conclusion:CPPs and high-calcium diet exhibit a high potential to decrease uric acid level.
Key words:hyperuricemic;casein phosphopeptides;calcium;uric acid;total cholesterol
大量调查研究发现乳制品的摄入与血清尿酸水平呈负相关,喝奶或摄入发酵乳制品的人比没有摄入相应乳制品的人血尿酸低,推测可能是由于乳制品中的血清蛋白、酪蛋白等生物活性物质具有促尿酸排泄的作用[1]。本实验根据每日推荐的牛奶摄入量换算牛奶中酪蛋白磷酸肽和钙含量,并研究二者及其复合物对高尿酸血症大鼠血清尿酸(UA)、总胆固醇(TC)、黄嘌呤氧化酶(XOD)和腺苷脱氨酶(ADA)等的影响,为进一步开发酪蛋白磷酸肽和改善高尿酸血症患者的膳食结构提供实验室依据。
1 材料与方法
1.1 材料、试剂与仪器
雄性SD大鼠50只,体质量140~160g,北京维通利华实验动物技术有限公司提供,合格证号:0143435,动物使用许可证编号:SCXK(京)2007-2001。
清洁级鼠料 北京科澳协力饲料有限公司;腺嘌呤北京索莱宝科技有限公司;盐酸乙胺丁醇 上海医药(集团)有限公司信谊制药总厂;酪蛋白磷酸肽 北京惠康源生物科技有限公司;UA、HDL-C试剂盒 上海科华生物工程股份有限公司;XOD、ADA试剂盒(批号20090627) 南京建成生物工程研究所。
DS-671型电子天平 上海寺岗电子有限公司;DTS-3低速自动平衡离心机 北京时代北利离心机有限公司;ADVIA1200全自动生化分析仪 德国拜耳公司;KY-2000半自动生化分析仪 Hitachi公司;DY89-1型电动玻璃匀浆机 上海新诺仪器设备有限公司;漩涡混匀器 英国Vision公司。
1.2 方法
实验动物在本实验室适应性喂养一周后,按体质量随机抽取10只作为空白组,用蒸馏水灌胃,余下的以腺嘌呤(100mg/(kg bw·d))+乙胺丁醇(250mg/(kg bw·d))灌胃3周,造成高尿酸血症模型[2]。造模成功后按尿酸水平随机分成4组,即CPPs组(1.82g CPPs/(d·只))、Ca粉组(0.96 g Ca HPO4/(d·只))、复合剂量组((1.82g CPPs+0.96g CaHPO4)/(d·只))、模型组。各组喂以25g/d的基础饲料,干预喂养28d后,断头采血。按试剂盒说明测定血清中UA和TC水平以及XOD和ADA的活性;取其肝脏称质量,制成匀浆,按试剂盒说明测定其中XOD、ADA活性[3]。
2 结果与分析
2.1 SD大鼠造模期间血清UA水平
表1 SD大鼠造模期间血清UA的水平比较(±s)Table 1 Serum uric acid level in rats during model establishment period (±s) mmol/L

表1 SD大鼠造模期间血清UA的水平比较(±s)Table 1 Serum uric acid level in rats during model establishment period (±s) mmol/L
注:*.与空白组比较有显著性差异P<0.05。
组别 只数 第7天 第14天 第21天空白组 10 1.729±0.3959 1.860±0.3155 1.831±0.3581模型组 40 1.845±0.5926 2.038±0.3155 2.255±0.4386*
由表1可知,在造模过程中,大鼠的血清UA水平不断升高,但在第7、14天UA水平并没有显著变化,只有在第3周模型组和空白组大鼠的血清UA出现的差异才具有统计学意义(P<0.05)。
2.2 高尿酸血症大鼠在干预期间的血清UA水平
由表2可知,在干预期间,模型组大鼠的血清UA有降低的趋势,但并不明显。除Ca组在干预的一周内并没有表现出明显的降低血清UA的作用,其余各组大鼠的血清UA水平在各时期均表现出了较为明显的降低,与模型组相比,差异有统计学意义(P<0.05或P<0.01)。
表2 高尿酸血症大鼠在干预期间的血清UA水平比较(±s)Table 2 Serum uric acid level in hyperuricemic rats during intervention period (±s) mmol/L
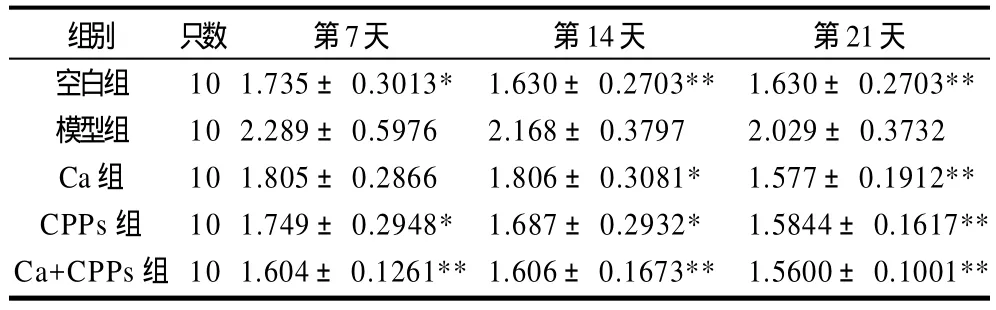
表2 高尿酸血症大鼠在干预期间的血清UA水平比较(±s)Table 2 Serum uric acid level in hyperuricemic rats during intervention period (±s) mmol/L
注:*.与模型组相比有显著性差异,P<0.05;**.与模型组相比有极显著性差异,P<0.01。下同。
组别 只数 第7天 第14天 第21天空白组 101.735±0.3013* 1.630±0.2703** 1.630±0.2703**模型组 102.289±0.5976 2.168±0.3797 2.029±0.3732 Ca组 101.805±0.2866 1.806±0.3081* 1.577±0.1912**CPPs组 101.749±0.2948* 1.687±0.2932* 1.5844±0.1617**Ca+CPPs组 101.604±0.1261**1.606±0.1673** 1.5600±0.1001**
2.3 各组大鼠在干预28d后血清中UA和TC水平
表3 酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠血清UA、TC的影响(±s)Table 3 Effects of CPPs, high-calcium diet and their combination on serum UA and TC in hyperuricemic rats (±s)
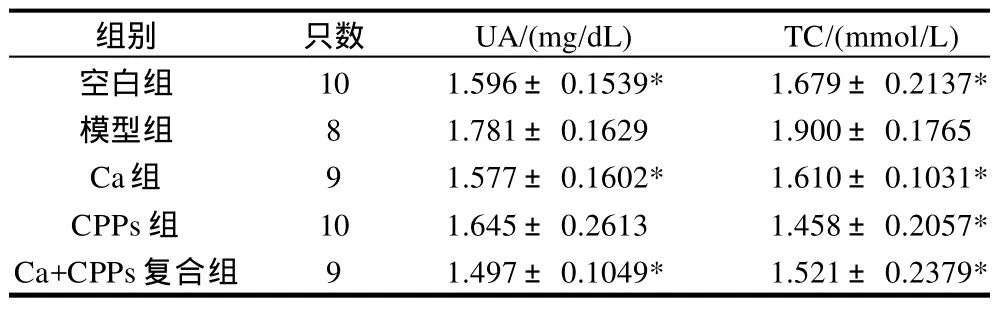
表3 酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠血清UA、TC的影响(±s)Table 3 Effects of CPPs, high-calcium diet and their combination on serum UA and TC in hyperuricemic rats (±s)
组别 只数 UA/(mg/dL) TC/(mmol/L)空白组 10 1.596±0.1539* 1.679±0.2137*模型组 8 1.781±0.1629 1.900±0.1765 Ca组 9 1.577±0.1602* 1.610±0.1031*CPPs组 10 1.645±0.2613 1.458±0.2057*Ca+CPPs复合组 9 1.497±0.1049* 1.521±0.2379*
如表3所示,和模型组相比,各干预组的UA水平均降低。其中Ca组和复合组同模型组大鼠的血清UA水平的差异有统计学意义(P<0.05),而CPPs组大鼠血清UA虽有降低却不明显,各干预组间没有差异;空白组和各干预组的TC水平均低于模型组,差异有统计学意义(P<0.05)。
2.4 各组大鼠血清和肝匀浆中XOD、ADA活性比较
表4 酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠血清XOD、ADA的影响(±s)Table 4 Effects of CPPs, high-calcium diet and their combination on XOD and ADA activities in serum of hyperuricemic rats (±s)

表4 酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠血清XOD、ADA的影响(±s)Table 4 Effects of CPPs, high-calcium diet and their combination on XOD and ADA activities in serum of hyperuricemic rats (±s)
组别 只数 XOD/(U/L) ADA/(U/mL)空白组 10 41.109±3.834 5.286±1.597模型组 8 41.945±3.509 6.063±3.649 Ca组 9 42.019±4.243 5.344±1.986 CPPs组 10 44.449±5.231 4.750±2.264 Ca+CPPs复合组 9 46.418±3.609* 5.472±1.730
表5 酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠肝XOD、ADA的影响(±s)Table 5 Effects of CPPs, high-calcium diet and their combination on the activities of XOD and ADA in liver of hyperuricemic rats (±s)
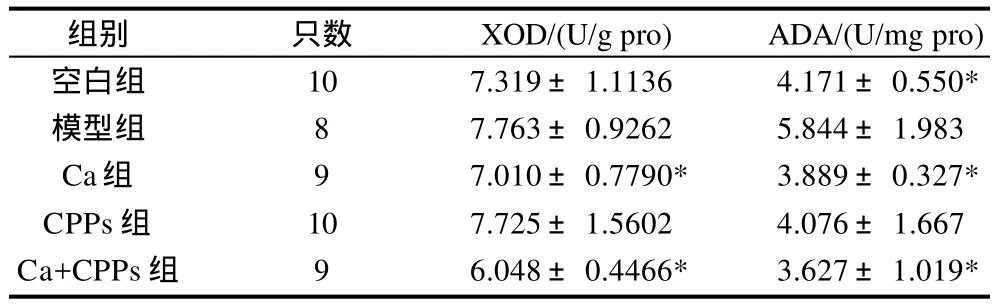
表5 酪蛋白磷酸肽、钙粉及二者复合物对高尿酸血症大鼠肝XOD、ADA的影响(±s)Table 5 Effects of CPPs, high-calcium diet and their combination on the activities of XOD and ADA in liver of hyperuricemic rats (±s)
组别 只数 XOD/(U/g pro) ADA/(U/mg pro)空白组 10 7.319±1.1136 4.171±0.550*模型组 8 7.763±0.9262 5.844±1.983 Ca组 9 7.010±0.7790* 3.889±0.327*CPPs组 10 7.725±1.5602 4.076±1.667 Ca+CPPs组 9 6.048±0.4466* 3.627±1.019*
如表4、5所示,在膳食干预的第28天,3个干预组大鼠的血清XOD活性高于模型组,肝脏中该酶的活性低于模型组。在3个干预组中,以Ca+CPPs组的干预效果最为明显,血清中该酶活性与模型组相比较高,且差异有统计学意义(P<0.05),肝脏中该酶的活性低于其他各组,尤其是模型组,但是各干预组间差异没有统计学意义(P>0.05)。
通过干预,各干预组大鼠血清中ADA活性低于模型组且高于空白组,但不明显,其中,以Ca组和Ca+CPPs组较接近空白组,各组与模型组的差异没有统计学意义;相对于模型组,各干预组大鼠肝脏中该酶的活性均较低,其中以CPPs组较为接近空白组,但是与模型组的差异没有统计学意义,而Ca组和混合干预组大鼠肝脏中该酶的活性低于空白组也明显低于模型组(P<0.05)。
3 讨 论
酪蛋白磷酸肽(CPPs)是从牛奶酪蛋白中分离提纯的生物活性肽,可在pH值呈中性至微碱性的动物小肠内与Ca2+、Fe2+和Zn2+等金属离子结合,阻止金属离子与磷酸根产生沉淀,增加了这些金属离子的溶解度,促进这些金属离子的吸收和利用[4]。目前已有大量实验研究致力于CPPs的加工生产,使其成为促进钙吸收的保健品或食品添加剂。在美国第三次全国健康与营养调查的诸多结果[1,5-8]中,通过横断面调查发现乳制品的摄入与血清尿酸水平呈负相关,喝奶或摄入发酵乳制品的人比没有摄入相应的乳制品的人血尿酸低,差别有统计学意义。这与之前的研究结果一致[9]。
目前,关于酪蛋白结合钙粉对高尿酸血症影响的研究国内外未见相关报道。塑造一个与人类高尿酸血症临床表现相近的动物模型是研究这一膳食干预效果的基础。本研究在众多造模方法[10-15]中选取易于操作又高效持久的方法,即选用雄性SD大鼠作为实验动物,用腺嘌呤(100mg/(kg bw·d))+乙胺丁醇(250mg/(kg bw·d))作为造模剂对实验动物连续灌胃21d,其中,腺嘌呤促进尿酸的合成,增加体内核酸、蛋白质的代谢含量,乙胺丁醇则增加了尿酸在体内的蓄积[2]。通过以上实验可以看出,与空白组相比,造模期间,模型组大鼠的血尿酸水平不断升高,且在干预期两组之间的差别仍较为明显,说明造模成功。
将造模成功的大鼠按血清尿酸水平随机分为4组,即模型、Ca组、CPPs组和Ca+CPPs组。在干预的前两周,个别大鼠出现死亡。这几只大鼠在实验过程中出现了持续的摄食相对较少、体质量相对较轻的现象,其死亡原因可能是较高的尿酸值对机体造成了不可逆的损伤。
根据以上实验可以看出,通过干预,各干预组血清尿酸水平相对于模型组均有明显的降低,其中以酪蛋白磷酸肽结合钙粉的复合物组干预效果最为显著,同时该组大鼠TC水平也表现出更有利于健康的趋势。
非嘌呤类前体物质在体内经过一系列的生物转化,生成嘌呤类核苷酸,继续分解生成次黄嘌呤和黄嘌呤,再经过XOD的连续氧化生成尿酸。XOD是尿酸代谢的关键酶,直接调控着体内尿酸水平的高低[16]。ADA是尿酸代谢的重要酶之一,它能够催化脱氧腺嘌呤核苷和嘌呤核苷脱氨,生成氨、脱氧次黄嘌呤核苷和嘌呤核苷,再由嘌呤核苷磷酸化酶的催化生成的次黄嘌呤氧化生成尿酸[17]。根据本实验的研究结果,推测酪蛋白磷酸肽结合钙粉的降尿酸作用的机理之一可能是降低了肝脏的XOD、肝脏和血清中ADA的活性。
根据以上实验可以得出结论:1)使用腺嘌呤和乙胺丁醇可以成功造出高尿酸血症大鼠模型; 2) 酪蛋白磷酸肽结合钙粉复合干预相对于单纯的酪蛋白磷酸肽干预和钙粉干预,能够更明显地降低血清UA、TC的水平;3) 酪蛋白磷酸肽结合钙粉复合干预降低血清尿酸的机制可能是降低了肝脏XOD、血清和肝脏中ADA的活性。
[1] CHOI H K, EARL S F. Prevalence of the metabolic syndrome in individuals with hyperuricemia[J]. The American Journal of Medicine,2007, 120(5):442-447.
[2] 熊湘明, 曲竹秋. 大鼠高尿酸血症模型的建立[J]. 天津中医学院学报, 2001, 20(4):28-29.
[3] 孔悦. 菊苣提取物防治高尿酸血症的作用及机理探讨的实验研究[D].北京:北京中医药大学, 2003.
[4] 范江平. 酪蛋白磷酸肽(CPPs)在食品工业中的应用[J]. 食品工业,2004(3):22-23.
[5] CHOI H K, CURHAN G. Coffee, tea, and caffeine consumption and serum uric acid level:The Third National Health and Nutrition Examination Survey[J]. Arthritis Rheum, 2007, 57(5):816-821.
[6] CHOI H K, LIU S, CURHAN G. Intake of purine-rich foods, protein,and dairy products and relationship to serum levels of uric acid:The Third National Health and Nutrition Examination Survey[J]. Arthritis Rheum, 2005, 52(1):283-289.
[7] HAK A E, CHOI H K. Menopause, postmenopausal hormone use and serum uric acid levels in US women:The Third National Health and Nutrition Examination Survey[J]. Arthritis Res Ther, 2008, 10(5):120.
[8] CHOI H K, CURHAN G. Beer, liquor, and wine consumption and serum uric acid level:The Third National Health and Nutrition Examination Survey[J]. Arthritis Rheum, 2004, 51(6):1023-1029.
[9] GARREL D R, VERDY M, PETITCLERC C, et al. Milk-and soyprotein ingestion:acute effect on serum uric acid concentration[J]. Am J Clin Nutr, 1991, 53(3):665-669.
[10] 李莉. 高嘌呤饮食诱发大鼠高尿酸血症临床观察[J]. 河北医学, 2007,13(9):1060-1062.
[11] DEHGHAN A, van HOEK M, SIJBRANDS E J G, et al. High serum uric acid as a novel risk factor for type 2 diabetes [J]. Diabetes Care,2008, 31(2):361-362.
[12] BLEYER A J, HART T C. Genetic factors associated with gout and hyperuricemia[J]. Adv Chronic Kidney Dis, 2006, 13(2):124-130.
[13] 孙玉萍. 原发性高尿酸血症相关基因和环境因素及与代谢性疾病关系的研究[D]. 乌鲁木齐:新疆医科大学, 2007.
[14] 林伟青, 谢建祥. 高尿酸血症动物模型研究进展[J]. 中国药物与临床, 2005, 5(2):115-118.
[15] 王宗涛, 管春梅, 车会莲, 等. 高尿酸血症大鼠模型的实验研究[J].中华内分泌代谢杂志, 2004, 20(5):474-475.
[16] 孔悦, 张冰, 刘小青, 等. 黄嘌呤氧化酶活性在高尿酸血症动物模型中的变化[J]. 北京中医药大学学报, 2004, 27(6):38-41.
[17] 刘春红, 刘新郑. 三种肝病患者血清黄嘌呤氧化酶的变化[J]. 河南医科大学学报, 1998, 33(1):81-82.
Effects of Casein Phosphopeptides, High-calcium Diet and Their Combination on Hyperuricemic Rats
ZHANG Rui1,YAO Fang-fang1,HE Wei2,*
(1. College of Public Health, Zhengzhou University, Zhengzhou 450001, China;2. Medical Research Institute of Henan Province, Zhengzhou 450052, China)
R151.3
A
1002-6630(2010)21-0332-03
2010-03-17
张锐(1985—),女,硕士研究生,研究方向为营养与疾病。E-mail:zhangrui-2085@163.com
*通信作者:何伟(1963—),男,研究员,博士,研究方向为营养与疾病。E-mail:weibho@163.com

