超临界流体技术制备微细颗粒的方法及装置
乔 培 陈 岚 李广田 可 嘉 陆 璐
(上海理工大学医疗器械与食品学院,上海 200093)
1 引言
微细颗粒,特别是纳米级粒子的制备,在当前的高新技术中已成为一个热门领域。由于微细颗粒特殊的物理化学性能,在微电子学、表面科学、材料科学、生物学等领域越来越受到重视[1,2]。
传统制备微粒的方法如:喷雾干燥、超细研磨等方法所制备的颗粒的粒径大小、均匀程度、流动性等方面均难以达到许多产业技术所要求的标准[3]。因此,寻求制备结晶纯度高、粒度均匀、流动性好的微细颗粒的方法成了当前的研究热点[1-4]。
超临界流体(Supercritical Fluid,SCF)技术是一种新型的微细颗粒的制备方法,近年来在化工、材料和制药等许多领域的研究迅速展开,引起了许多研究者的重视[16,21]。本文主要对超临界流体技术制备微粒的重要方法及其各自的装置特点进行了介绍,并对超临界流体技术发展中存在的问题和应用前景进行了分析和展望。
2 超临界流体的特性
SCF指处于临界温度(TC)和临界压力(PC)以上状态的流体。处于超临界区的流体与常温常压流体相比,具有很显著的特点:从临界点起始,气—液界面消失,体系性质均一。密度和液体相近,黏度与气体接近,扩散系数比液体大,有着优越的传递特性[2]。
在超临界情况下,降低压力可以导致溶液过饱和,固体溶质沉淀析出。此过程在准均匀介质中进行,能够较好的控制沉析过程,是一种很有前途的新技术[4]。常用的SCF有CO2、戊烷、乙醇、水等。其中超临界CO2因其临界温度(31.1℃)和临界压力(7.38 MPa)相对较低,且具无毒、安全、环保、价廉等优点而应用最广。
3 超临界流体制备微细颗粒的方法
根据SCF在微细颗粒制备过程中所起的作用,一般将SCF制备颗粒的方法分为:作为溶剂的超临界流体快速膨胀法(Rapid Expansion of Supercritical Solution, RESS);作为抗溶剂的超临界流体抗溶剂法(Supercritical Anti-Solvent, SAS);作为溶质的气体饱和溶液沉析法 (Precipitation from Gas Saturated Solution,PGSS)等。
3.1 RESS法
RESS法由Krukonis在1984年首次提出,并且成功运用了此方法处理难以粉碎的固体颗粒[5]。RESS法因其流程简单、无溶剂残留、产生的颗粒粒径小且分布均匀、微粒成分不易被破坏等优点而受到普遍重视,并显示出了其巨大的应用前景。
3.1.1 RESS法原理及特点
溶质在SCF中具有一定的溶解度是RESS过程得以进行的必要条件。首先将溶质溶解在SCF中,然后使超临界溶液在非常短的时间内(10-8~10-5s)通过一个细微的喷嘴进行减压膨胀。膨胀过程中因压力、温度的突然变化使溶质的过饱和度骤然升高,析出大量微核,并在极短的时间内快速生长,形成粒度均匀的微米或纳米级颗粒[4]。
传统制粒过程中,溶液的过饱和是通过降温过程实现,释放热量时则会在溶液中形成温度梯度,造成不同程度的过饱和,所析出的颗粒尺寸分布较广[3]。而RESS工艺的显著特点就是快速的机械扰动和快速降压所产生的极高的过饱和度。前者使成核介质均一化,从而形成很窄的粒径分布;后者则使所得的粒径变小而形成微细颗粒,从而获得粒径均匀的超细微粒[6]。
3.1.2 RESS过程装置
RESS法的过程装置可分为三部分:使溶剂达到超临界状态的溶剂输送部分、溶解固体溶质形成超临界溶液的萃取部分和快速膨胀形成微粒的制粒部分。其基本装置如图1所示。钢瓶中的CO2经过制冷器和预热器加热到所需温度,然后由高压泵打入高压恒温反应釜中,并加压到预定压力后保压。在高压恒温反应釜中对已装填好的原料进行充分溶解。在沉积单元,含溶质的SCF通过一个特制的喷嘴快速膨胀,压力骤然下降,溶质瞬间达到过饱和,形成微小的、粒度均匀的颗粒在膨胀室沉积。喷嘴须预热至适当温度,以避免溶质突然大量析出而堵塞喷嘴。
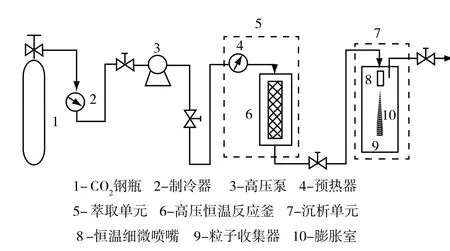
图1 RESS过程装置图
喷嘴是RESS过程的特色部件,它由长度短(<5 mm)和内径小(6 µm~100 µm)的不锈钢毛细管制成。喷嘴决定了流体的膨胀特性,进而最终决定产物的形态和质量。Matson等将SCF在RESS过程中的膨胀过程分为三个阶段:近似绝热区的亚音速膨胀、等熵区超音速自由膨胀和射流、膨胀区内的周围气体的相互作用,并研究了每个阶段的物理化学和流体力学特征[4]。
3.1.3 RESS过程的影响因素
RESS过程中影响微粒粒径和形态的因素较多。实验研究大多集中在工艺参数对产品特性的影响,如萃取温度和压力、溶质的浓度、膨胀前后的温度、溶液喷射的距离、共溶剂的种类、喷嘴的结构等,通过控制这些条件可制备出微米级甚至纳米级颗粒[7]。
3.1.4 RESS技术的改良方法
RESS法虽然具有过程简易、产物有机溶剂残留量低等优点,但由于CO2没有偶极矩,内聚能密度低,除氟代聚合物、聚硅氧烷及低分子量的聚合物之外,大多数聚合物及极性化合物在超临界CO2中的溶解度均很低,而RESS过程仅应用于能溶解于SCF的材料,故限制了RESS方法的使用。近年出现了一些RESS法的改良方法,如超临界流体快速膨胀-非溶剂法 (Rapid Expansion from Supercritical Solution with a Non-solvent,RESS-N)[8];超临界流体快速膨胀至液体溶剂法 (Rapid Expansion of a Supercritical Solution into a Liquid Solvent, RESOLV )[9]、超临界流体快速膨胀-固态共溶剂法 (Rapid Expansion of Supercritical Solution with Solid Cosolvent, RESSSC)[10]、超临界流体快速膨胀共沉析法 (Co-precipitation during the Rapid Expansion of Supercritical Solution, CORESS)[11]等,这些方法都针对RESS方法的局限性进行改进并获得了一定的效果。
3.2 超临界抗溶剂法(SAS)
3.2.1 SAS法制粒原理及特点
超临界抗溶剂法(SAS)首先由Gallagher等在1989年提出,用于炸药的重结晶中[12]。这种不同于RESS法的操作被称为抗溶剂法。SAS法的提出和应用大大拓展了RESS的研究领域,而且可以在较大范围内控制微粒的尺寸、形状和结构,使得超临界流体技术呈现出了更大的发展和应用前景。
SAS法是以SCF为抗溶剂,将需要制备颗粒的材料溶解在某种有机溶剂中制成溶液,将此溶液与超临界流体相混合。超临界流体虽然对溶液中的溶质基本不溶,但是溶液中的溶剂却能和此种超临界流体互溶。当溶液与超临界流体互溶时,溶液会发生体积膨胀,导致原溶剂的溶解能力大大降低,从而使溶质析出[4]。
SAS法最大的特点在于选择适合的超临界流体和操作条件,溶液中的溶剂会被超临界流体完全溶解,析出的溶质可以是无污染的干燥颗粒,此外,通过控制超临界流体与溶液的混合速率可以控制溶质的析出速率,从而控制析出颗粒的形状和大小。
SAS法有多种工艺过程,如气体抗溶剂法(Gas Anti-solvent, GAS),气溶胶溶剂萃取法(Aerosol Solvent Extraction System,ASES),也叫压缩流体及溶剂沉析工艺(Precipitation with a Compressed Fluid Antisolvent,PCA),超临界流体强化溶液分散法(Solution Enhanced Dispersion by Supercritical Fluids,SEDS)等。
3.2.2 SAS法相关过程及其装置
3.2.2.1 GAS法
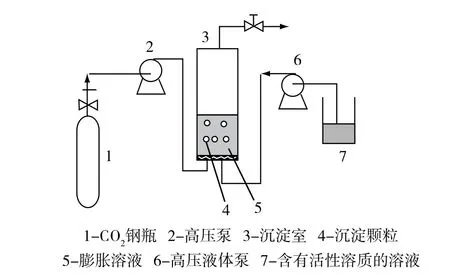
图2 GAS过程装置图
GAS法的基本装置如图2所示,首先在沉淀室中放入含溶质的溶液,再加入超临界CO2直至达到最终压力,为了使CO2与溶液充分混合,通常使CO2在沉淀室中保持一定的停留时间,同时使用磁力搅拌器,以加强CO2在有机溶剂中的溶解,使得溶剂发生膨胀,溶解能力下降,有机溶剂中原有溶质因短时间的过饱和而形成微细颗粒。在沉淀操作的最终阶段,设定压力下,向沉淀室中继续通入SCF带走有机溶剂。
GAS法的特点是借助有机溶剂提高了溶质的溶解度,可以解决工业生产中遇到的生产能力问题。GAS法制粒过程操作简单,设备要求较低,但缺点是高压釜中通入CO2时溶液较难达到均匀的体积膨胀,难以实现均一的过饱和度。另外,GAS法只能分批操作,限制了该法在工业生产中的广泛应用[13]。
3.2.2.2 ASES法
ASES法的基本装置如图3所示。ASES法是对GAS法的改进。主要是利用特制的喷嘴在一定压力下将含有溶质的溶液喷射到沉淀室内已有的超临界CO2中,超临界流体向溶液内部扩散使溶液发生膨胀,液体溶剂能量减少,引起液体混合物过饱和度的急剧上升,导致微粒析出。当收集到足够的微粒之后,首先关闭液体泵,SCF继续通入釜中以去除粒子中的残留溶剂[14]。
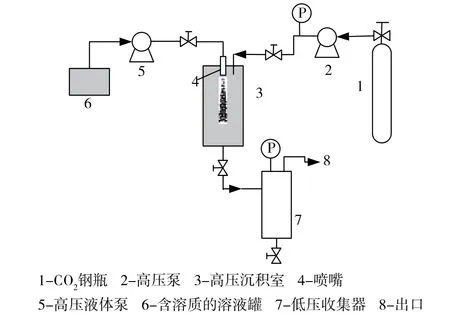
图3 ASES过程装置图
与GAS法相比,利用喷嘴将溶液喷入沉淀室中是ASES法的特色,可得到更细小的微粒。要充分发挥ASES法的优点,有机溶液需以较高的压力喷入高压釜中,使溶液得到充分雾化[15]。
3.2.2.3 SEDS法
SEDS法的基本装置如图4所示。SEDS法是一种特殊的ASES方法,是ASES法的改进,将ASES法中的喷嘴改为同轴式喷嘴,此同轴喷嘴也是SEDS法不同于其他方法的最大特点。此喷嘴由二、三或多个不同口径的微孔管共轴组装在一起,在此操作过程中,将SCF与液体溶液同时由同轴喷嘴的内、外侧喷孔以一定的流速差喷入高压沉淀室中,高速的SCF把溶液粉碎成非常细小的液滴,且在分散的同时,SCF作为抗溶剂从液滴中萃取出有机溶剂,使微粒析出。
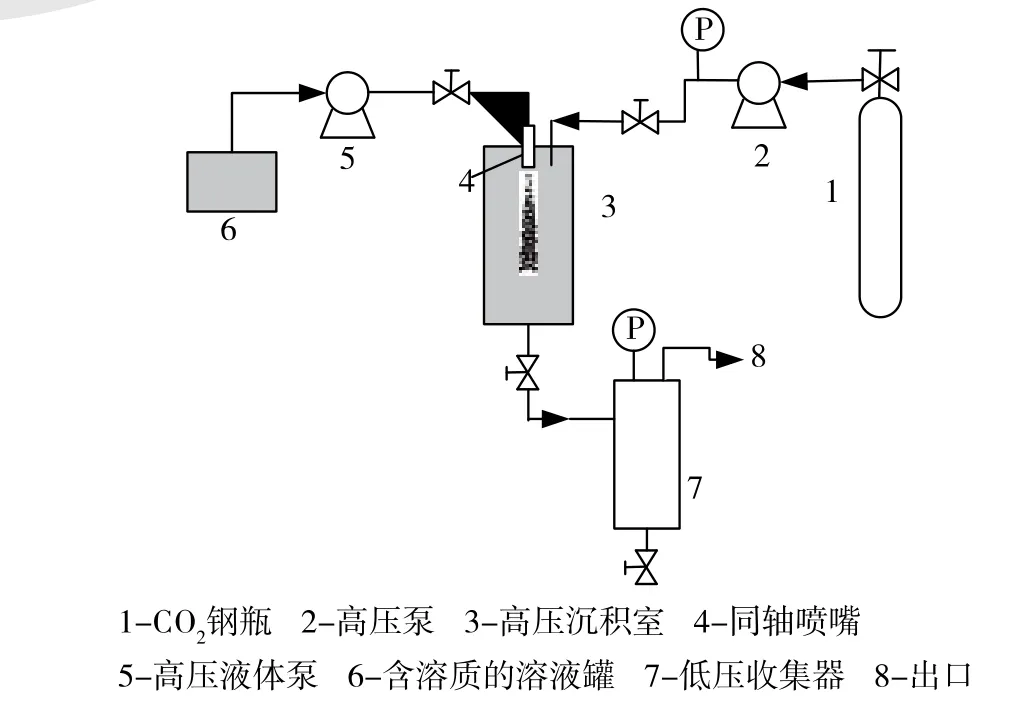
图4 SEDS过程装置图
将溶液与SCF同时引入至同轴喷嘴中,可增强SCF和溶液的混合度,增强传质速率,从而在高压釜内形成巨大的扰动度,有利于雾化后形成细小和混合均匀的液滴,因此两相间的传质速率大大提高,调节两种液体间的相对流速可控制颗粒的大小和粒径分布,产生的液滴比纯液相溶液喷射得到的液滴尺寸更小[16,17]。
3.2.3 SAS法的影响因素
对SAS法的影响因素也较多,研究主要集中在操作压力及温度、溶质浓度、CO2的摩尔分数等对颗粒形态结构的影响[18]。此外,喷嘴结构特征[19]、CO2的流率、溶液的流率、有机溶剂的选择及操作过程的选择(间歇式,连续式)等因素也是影响颗粒制备结果的重要参数。
3.3 气体饱和溶液沉析法(PGSS)
3.3.1 PGSS过程原理及特点
PGSS法与RESS法具有相似之处,都是使超临界溶液快速通过喷嘴,达到溶质沉积析出的目的。而PGSS法是将超临界CO2溶入液态溶质中或溶质的悬浮液,达到饱和后,这一高压的气液或气液混合物经过一个喷嘴快速膨胀降压后,形成气溶胶,气溶胶中CO2和H2O经膨胀室的高温挥发,溶质沉析,制得微细颗粒[20]。
PGSS工艺的最大特点是可以应用于能溶于水溶液的溶质中,操作温度较低,能降低压缩气体操作压力并减少用量,同时不使用有机溶剂,具有连续化生产的优势。PGSS法可用于处理高浓度溶质的超临界溶液,并可得到较高的产率,主要用于低熔点和耐热微细颗粒的制备。
3.3.2 PGSS过程装置
PGSS过程装置如图5所示。PGSS工艺得以实现的一个重要原因是压缩气体在熔融(混悬、溶液)状态的物料中溶解度远高于熔融(混悬、溶液)物料在压缩气体中的溶解度(RESS法的原理)[21]。
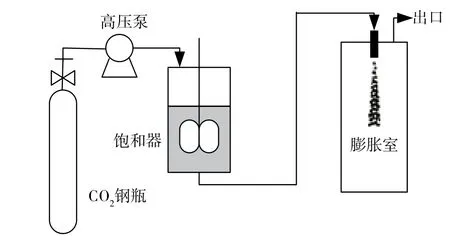
图5 PGSS过程原理图
图6是一个PGSS装置的示意图。超临界CO2和溶液在T字型喷嘴内混合,混合物从毛细管喷出雾化成小液滴。雾化的小液滴在膨胀室里沉析出颗粒。微粒的尺寸可以通过初始溶液的浓度与雾化有关的参数(温度,压力,流速,毛细管的尺寸)等来控制。
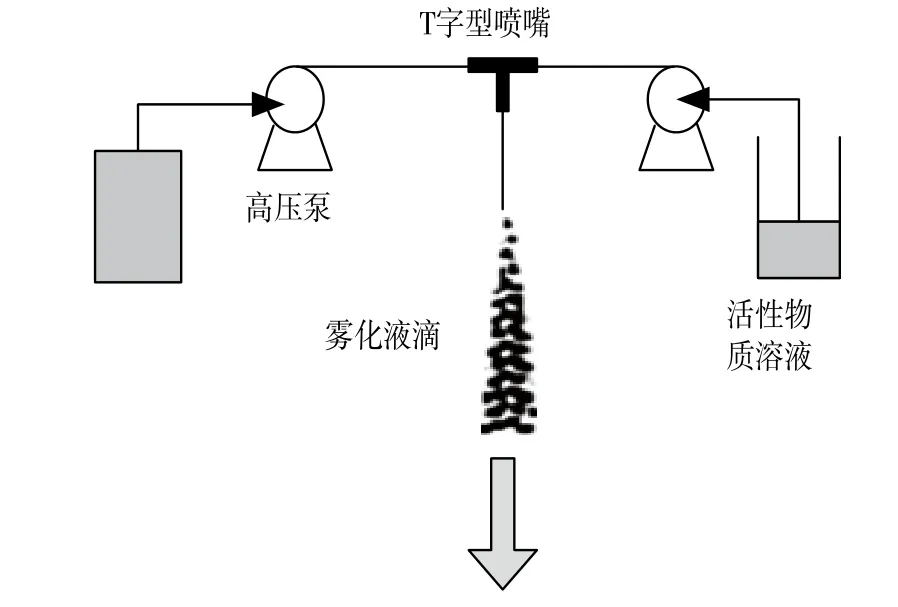
图6 PGSS装置示意图
3.3.3 PGSS法的衍生技术
基于PGSS法为基础,其衍生出来的方法有二氧化碳辅助雾化及泡式干燥法 (CO2-Assisted Nebulization with Bubble Drying, CAN-BD)及超临界辅助雾化法(Supercritical Assisted Atomization,SAA)[22],液态有机溶液降压膨胀法 (Depressurization of an Expanded Liquid Organic Solution, DELOS)[23]等。
4 结语
RESS法装置简单,在生产少量物质时只使用一个喷嘴就可以实现。但RESS法最大的限制是SCF对大多数物质的溶解度太小。SAS法的应用更为广泛,特别是生产质量要求高的药品、食品添加剂、化妆品等,通过控制操作条件来控制这些物质的性质和组成,但这些方法存在过程相对复杂、投资费用大等缺点。PGSS法原理简单,装置费用低,应用范围较广,但制备的粒子尺寸不可控,颗粒粒径较大。在选择一种方法来制造微细颗粒时,要综合考虑各种因素,如:溶质的溶解度、需制备得到的微粒尺寸、形状、设备造价等,选择合适的方法。
总的来说,超临界流体技术是制备微细颗粒的具有很好发展前景的一种新技术。在制备过程中颗粒的生物活性及物性损失较小,且制备出的微粒粒径均匀,粒径分布窄。但目前超临界流体技术制备微细颗粒技术还处于实验研究阶段,现有的研究工作主要集中在过程的影响因素及工艺的可行性,在过程放大和工业化应用方面仍有许多基础理论问题需要解决。
近年来,对超临界流体沉析理论尤其是其过程机理和颗粒生长机理的研究也在深入开展中,但是由于该技术是一项多学科交叉的新技术,在产品的形态与性质控制、相平衡基础数据、晶体成核和生长模型等方面还有待进一步研究和完善。随着相关学科的发展和该项技术理论及应用研究的进一步深入, 超临界流体技术在微细颗粒制备领域中必将具有广阔的应用前景。
[1] Byrappa K, Ohara S, Adschiri T. Nanoparticles synthesis using supercritical fluid technology – towards biomedical applications. Advanced Drug Delivery Reviews, 2008, 60(3): 299–327.
[2] Pasquali I, Bettini R, Giordano F. Supercritical fluid technologies: An innovative approach for manipulating the solid-state of pharmaceuticals. Advanced Drug Delivery Reviews, 2007, 28(6): 1-12.
[3] 张立德, 牟季美. 纳米材料和纳米结构[M] . 北京: 科学出版社,2001: 25-139.
[4] 朱自强. 超临界流体技术—原理和应用[M] . 北京: 化学出版社,2000: 516-538.
[5] 廖传华,柴本银. 超临界流体与新材料制备[M]. 中国石化出版社,2007:87-116.
[6] Martín A, Cocero M J. Micronization processes with supercritical fluids: Fundamentals and mechanisms. Advanced Drug Delivery Reviews, 2008,60(3): 339-350.
[7] Yildiz N, Tuna S, Doker O, et al. Micronization of salicylic acid and taxol (paclitaxel) by rapid expansion of supercritical fluids(RESS). J. of Supercritical Fluids, 2007, 41(3): 440-451.
[8] Meziani M J, Pathak P, Beacham F, et al. Nanoparticle formation in rapid expansion of water-in-supercritical carbon dioxide microemulsion into liquid solution. J. Supercritical Fluids, 2005, 34(1): 91–97.
[9] Thakur R, Ram B, et al. Rapid expansion of supercritical solution with solid cosolvent (RESS-SC) process: Formation of 2-aminobenzoic acid nanoparticle. J. of Supercritical Fluids, 2006, 37(3): 307-315.
[10] Turk M, Upper G, Hils P. Formation of composite drug-polymer particles by co-precipitation during the rapid expansion of supercritical fluids. J. of Supercritical Fluids, 2006,39(2): 253-263.
[11] Matsuyama K, Mishima K, Hayashi K I, et al. Formation of microcapsules of medicines by the rapid expansion of a supercritical solution with a nonsolvent. Journal of Applied Polymer Science, 2003, 89(3): 742-752.
[12] Tai C Y, Cheng C S. Supersaturation and crystal growth in gas antisolvent crystallization. Journal of Crystal Growth, 1998, 183: 622-628.
[13] Mishima K. Biodegradable particle formation for drug and gene delivery using supercritical fluid and dense gas. Advanced Drug Delivery Reviews, 2008, 60(3): 411–432.
[14] Kim M Y, Yoo K Pm, Lim J S, Preparation of poly(L-lactic acid) submicron particles in aerosol solvent extraction system using supercritical carbon dioxide. J. Chem. Eng., 2007, 24(5): 860-865.
[15] Lee S, Nam K, Kim M S, et al. Preparation and Characterization of Solid Dispersions of Itraconazole by using Aerosol Solvent Extraction System for Improvement in Drug Solubility and Bioavailability. Arch Pharm Res, 2005, 28(7): 866-874.
[16] Jung J, Perrut M. Particle design using supercritical fluids: Literature and patent survey. J. of Supercritical Fluids, 2001, 20(3): 179–219.
[17] Yeo S D, Kiran E. Formation of polymer particles with supercritical fluids: A review. J. of Supercritical Fluids, 2005, 34(3): 287-308.
[18] Reverchon E, Adami R, Caputo G, et al. Spherical microparticles production by supercritical antisolvent precipitation: Interpretation of results. J. of Supercritical Fluids, 2008, 47(1): 70–84.
[19] Boutin O, Badens E, Carretier E, et al. Co-precipitation of a herbicide and biodegradable materials by the supercritical anti-solvent technique. J. of Supercritical Fluids, 2004, 31(1): 89–99.
[20] M. Rodrigues M, Peiriço N, Matos H, et al. Microcomposites theophylline/hydrogenated palm oil from a PGSS process for controlled drug delivery systems. J. of Supercritical Fluids, 2004, 29(1-2): 175–184.
[21] Davies O R, Lewis A L, Whitaker M J, et al. Applications of supercritical CO2in the fabrication of polymer systems for drug delivery and tissue engineering. Advanced Drug Delivery Reviews, 2008, 60(3): 373–387.
[22] Reverchon E, Adami R, Cardea S, et al. Supercritical fluids processing of polymers for pharmaceutical and medical applications. J. of Supercritical Fluids, 2009,47(3): 484–492.
[23] Ventosa N, Sala S, Veciana J. DELOS process: a crystallization technique using compressed fluids. J. of Supercritical Fluids, 2003, 26(1): 33-45.

