硫与铋比例对水热合成Bi2S3粉体形貌的影响
刘 运, 谈国强, 朱刚强
(1.陕西科技大学电子与信息工程学院, 陕西 西安 710021; 2.陕西师范大学物理学与信息技术学院, 陕西 西安 710062)
0 引言
纳米材料具有特殊的结构和性能,可广泛应用于化学、物理学、电子学、光学、机械和生物医学等领域[1-3],其中一维或准一维纳米结构体系的研究既是研究其它低维材料的基础,又与纳米电子器件及微型传感器密切相关,是近年来国内外研究的前沿[4,5],并已经在通信﹑微波﹑电子开关或光电器件方面得到了广泛应用[6,7].一维纳米材料主要包括纳米管﹑纳米线﹑纳米带以及纳米棒等.目前,制备一维纳米材料的方法主要有:气相沉积法﹑模板法﹑高温分解法﹑溶胶凝胶法﹑微胶模板法以及水热(溶剂热)法等.
Bi2S3是一种重要的直接带系半导体材料.纳米尺度的Bi2S3不仅能引起吸收波长与荧光发射发生蓝移,还能产生非线性光学响应,并增强纳米粒子的氧化还原能力,具有更优异的光学催化活性,在发光材料、非线性光学材料、光催化材料等方面有着广泛的应用前景[8,9].由于Bi2S3是一种具有典型层状结构的晶体,具有很强的向C轴生长的趋势,因此Bi2S3易于形成一种高长径比的一维晶体结构[10,11].近年来,研究者通过水热法、溶剂热法、模板法和气相沉积法制备了大量一维的Bi2S3纳米线﹑纳米棒和纳米带[12-15].纳米管具有特殊的结构特征,跟其它的一维纳米结构相比,已报道过的Bi2S3纳米管制备方法很少,而此前我们已报道了利用水热法在120 ℃低温下制备了尺寸均匀的纳米管[11].
本实验以硫化钠和硝酸铋为原料,尿素为矿化剂,通过在反应溶液中加入不同比例的S/Bi,研究了不同硫与铋的比例对Bi2S3纳米管形貌和尺寸的影响.
1 实验部分
1.1 原料
本实验采用的试剂:硝酸铋(Bi(NO3)3·5H2O,分析纯,天津市化学试剂公司);硫化钠(Na2S·9H2O,分析纯,天津市化学试剂公司);尿素(CO(NH2)2,分析纯,天津市化学试剂公司);乙二醇(C2H6O2,分析纯,天津市化学试剂公司);去离子水(自制).
1.2 实验过程
将3份0.73 g Bi(NO3)3分别加入5 mL的乙二醇中,用搅拌子搅拌5 min,完全溶解得到澄清溶液A1﹑A2﹑A3,分别将3份质量为1.5 g, 1.9 g, 2.3 g 的Na2S·9H2O溶于10 mL去离子水中,得到溶液B1﹑B2﹑B3;将溶液B1﹑B2﹑B3分别缓慢逐滴地滴入A1﹑A2﹑A3中,同时不断快速搅拌,形成黑色前驱物;最后,分别向前驱物中加入0.76 g的CO(NH2)2并配成30 mL溶液(去离子水与有机溶液的体积比为5∶1),倒入容量为50 mL带聚四氟乙烯内衬的不锈钢反应釜中,再将反应釜放置在120 ℃的恒温箱里进行恒温加热12 h.反应结束后,产物用去离子水清洗数次,然后在80 ℃干燥6 h.
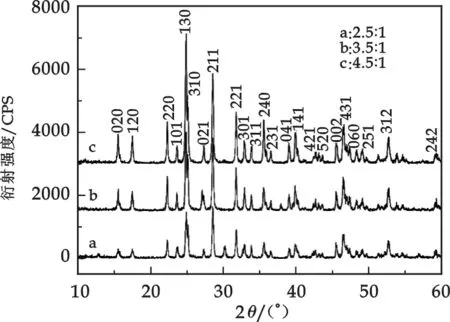
图1 不同硫与铋比例所制备的Bi2S3粉体的XRD图谱( (a) 2.5∶1 ;(b)3.5∶1; (c) 4.5∶1)

图2 (a) Bi2S3 纳米管的SEM照片; (b) Bi2S3 纳米管的TEM照片; (c) 高放大倍数Bi2S3 纳米管的TEM照片; (d) Bi2S3 纳米管的HRTEM照片, 插图为Bi2S3 纳米管的选区电子衍射照片
1.3 结构表征
采用日本理学D/max2550/PC 型X射线衍射仪对Bi2S3粉体进行物相定性和结构分析,测试条件为:铜靶辐射源(λ=0.154 06 nm),石墨单色器,管压40 kV,管流50 mA, 扫描速度10°·min-1,狭缝宽10 mm,步长0.02°,测量范围为10°~60°;用荷兰FEI Quanta 200型扫描电镜(SEM)和日本JEM-3010型透射电镜(TEM)以及高倍透射电镜(HRTEM)观察粉体的颗粒形貌和尺寸;用美国Perkin-Elmer Lambd 950型紫外-可见近红外光谱仪测量粉体的吸收光谱.
2 结果与讨论
2.1 XRD分析
图1显示的是不同硫与铋的比例(S/Bi=2.5∶1、3.5∶1、 4.5∶1),乙二醇-去离子水为反应溶剂, 以尿素为矿化剂,在 120 ℃保温12 h反应得到的硫化铋纳米粉体的XRD图谱.XRD图谱中所有衍射峰与正交相的Bi2S3(JCPDS: 17-0320)的衍射峰相对应,并由图1a中XRD计算出Bi2S3纳米管的晶胞参数为:a=1.115 0 nm,b=1.130 6 nm,c=0.398 1 nm,与标准卡中的晶格参数符合得很好.从XRD图可以看出没有其它的杂质,并且随着硫与铋比例的增大衍射峰的强度也相应增强.
2.2 SEM和TEM分析

图3 (a) Bi2S3纳米管的SEM照片,(b) 低放大倍数Bi2S3纳米管的TEM照片, (c) 单根Bi2S3纳米管的大倍数TEM照片

图4 (a) Bi2S3纳米管的SEM照片, (b) 高放大倍数Bi2S3纳米管的SEM照片,(c) Bi2S3纳米管的TEM照片, (d) 高放大倍数单根Bi2S3纳米管的TEM照片
图2a为硫与铋的比例为2.5∶1时在120 ℃条件下反应12 h所制备的Bi2S3纳米管的SEM图.由图中可以看出,所得到的产物是由大量直径为纳米尺寸的棒状产物组成,线的表面光滑均匀,外径在100~300 nm之间,长达1~5μm,并可以清楚地观察到部分末端中空的产物.图2b TEM照片可更清楚地观察到Bi2S3的形貌.从照片中还可以看出,所制备的产物由大量的Bi2S3纳米管组成,进一步验证了Bi2S3纳米管的存在.图2c是大倍数的TEM照片,纳米管的外径为200 nm,内径为80 nm,管壁为60 nm.图2d是Bi2S3纳米管管壁上的HRTEM图,从图中可以清晰看到晶格的排列,并测出了两个方向的相邻晶格间的间距分别为0.375 nm和0.312 nm,对应着Bi2S3正交相(101)和(211)晶面的间距.图2d中的插图是Bi2S3纳米管的选区电子衍射图样,从图中可以看到明亮的电子衍射斑点,并且这些衍射斑点呈线状排列.由于从同一根纳米管的不同位置得到了同样的结果,因此说明所制备的纳米管为单晶.
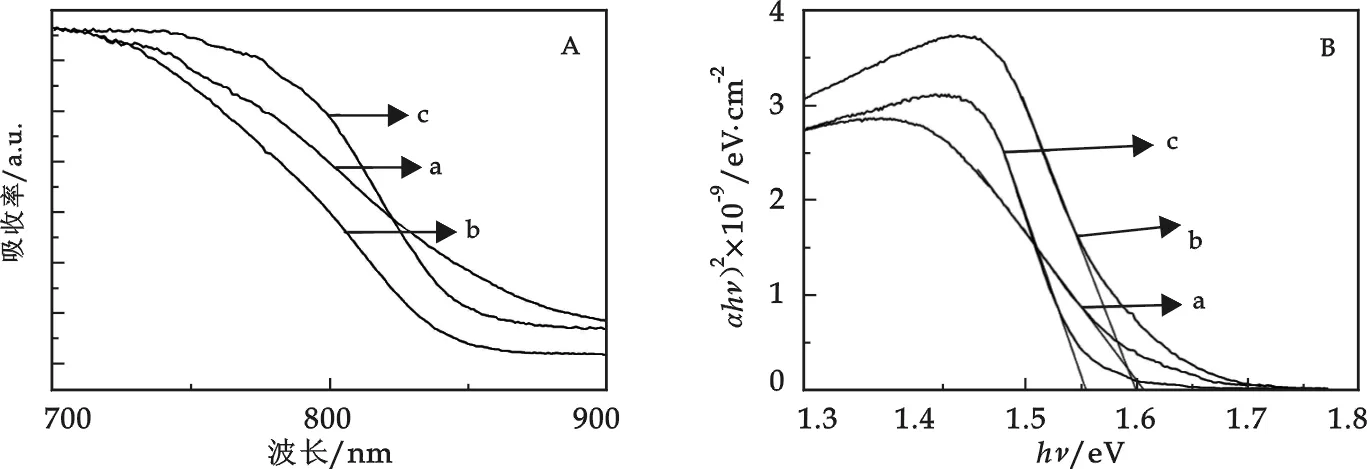
图5 (A) 不同硫和铋的比例所制备的Bi2S3粉体的紫外-可见吸收光谱:a: 2.5∶1; b: 3.5∶1; c: 4.5∶1;(B) 由(αhv)2与hv的关系作出的带隙宽
图3是硫与铋的比例为3.5∶1时在120 ℃反应12 h所制备的Bi2S3粉体的SEM和TEM图.从图3a可以看出,所制得的产物是由大量直径为纳米尺寸的线状产物组成,线的表面光滑均匀,外径为200~700 nm,长度为2~10μm.图3b和图3c是产物的TEM照片,从图中可清楚地观察到产物是由Bi2S3纳米管组成.图4是硫与铋的比例为4.5∶1时在120 ℃反应12 h所制备的Bi2S3粉体的SEM和TEM图.从图4a可以看出,所制得的产物是由大量尺寸不均的线状产物组成,线的表面光滑均匀,外径为500 nm~2μm,长度为5~15μm.图4b为大倍数的SEM图片,从图中可以看到一根末端并没有生长完整的微管,其直径为1μm,图4c是Bi2S3微管的透射电镜照片,由于管壁较厚,因此并没有在图中观察出中空的特征,而从图4d可以看出这个Bi2S3微管端口中空的特征.从图2~图4的SEM和TEM照片可以看出,Bi2S3产物随着硫与铋比例的增大,其长度和直径都增大,而且长度和直径大小分布也越来越不均匀,但是从图中可见不同硫与铋的比例并没有影响到Bi2S3管状特征的变化,而只是对其长度和直径有影响,且所得产物Bi2S3纳米管均为单晶.其原因在于Bi2S3是具有典型层状结构的晶体,具有很强的向C轴生长的趋势;在本实验中所制备的Bi2S3纳米管是由“自我卷曲”形成的,即先形成Bi2S3纳米薄片,然后随着时间的延长纳米薄片自我卷曲形成Bi2S3纳米管[11].而溶液中硫化钠的增加会导致溶液的粘度增加,不利用离子的流动,因此在溶液中晶体的生长速率大于成核速率,最终导致晶体的尺寸变大.
2.3 UV-vis光谱分析
图5A是硫化铋纳米粉体的紫外-可见吸收光谱,由于纳米粉体的尺寸分布不均可能导致吸收带变宽.曲线a、b和c分别是硫和铋的比例为2.5∶1、3.5∶1和4.5∶1时所制备的粉体的吸收谱线, 根据公式α=k(hv-Eg)n/2/hv可以算出粉体的带隙宽度,以hv为x轴,(αhv)2为y轴可以作出图5B,通过其切线得到粉体的带隙宽分别为1.55 eV、1.60 eV和1.61 eV,其带隙相对于块体的Bi2S3(1.32 eV)均发生了明显的蓝移.结合前面硫化铋粉体尺寸的变化我们认为正是纳米结构和尺寸的变化造成了吸收峰的蓝移.
3 结论
以硫化钠和硝酸铋为原料,尿素为矿化剂,去离子水为反应溶剂,采用水热合成法在120 ℃下反应12 h 制备了高长径比的Bi2S3纳米管,并通过X-射线粉末衍射、扫描电子显微镜、透射电子显微镜、选区电子衍射、高分辨透射电镜和UV-vis光谱对其结构和形貌进行了表征.测试结果表明,所制备的产物是单晶正交相Bi2S3纳米管;随着硫与铋的比例增大,合成的Bi2S3纳米管的长度和直径都增大,因此通过控制不同硫与铋的比例可以很好地控制纳米管的形貌和尺寸.
[1] Patzke G R, Krumeich F, Nesper R. Oxidic nanotubes and nanorods-anisotropic modules for a future nanotechnology[J]. Angew Chem Int Ed, 2002, 41: 2 446-2 461.
[2] Alfredo M. Morales, Charles M. Lieber. A laser ablation method for the synthesis of crystalline semiconductor nanowires[J]. Science, 1998, 279(9): 208-211.
[3] Banerjee S, Dan A, Chakravorty D. Review synthesis of conducting nanowires[J]. Journal of Materials Science, 2002, 37(20): 4 261-4 271.
[4] Shen X P, Liu H J, Fan X,etal. Construction and photoluminescence of In2O3nanotube array by CVD-templates method[J]. Journal of Crystal Growth, 2005, 276: 471-477.
[5] Chen C C, Yeh C C, Chen C H,etal. Catalytic growth andcharacterization of gallium nitride nanowires[J]. American Chemical Society, 2001, 123(12): 2 791-2 798.
[6] Young-wook Jun, Sang-Min Lee, Nam-Jung Kang,etal. Controlled synthesis of multi-armed CdS nanorod architectures using monosurfactant system[J]. Journal of American Chemistry Society, 2001, 123(21): 5 150 -5 151.
[7] Christopher Ma, Daniel Moore, Jing Li,etal. Nanobelts, nanocombs and nano-windmills of wurtzite ZnS[J]. Advanced Material, 2003, 15: 228.
[8] Hongmei Cuia, Hong Liua, Xia Lia,etal. Synthesis of Bi2Se3thermoelectric nanosheets and nanotubes through hydrothermal co-reduction method [J].Journal of Solid State Chemistry, 2004, 177: 4 001-4 006.
[9] D Arivuoli, F D Gnanam, P Ramasamy. Growth and microhardness studies of chalcogneides of arsenic, antimony and bismuth[J]. Journal of Materials Science Letters, 1988, 7: 711-713.
[10] Yee Wee Koh, Chian Sing Lai, An Yan Du,etal. Growth of bisumth sulfide nanowire using bismuth trisxanthate single source precursors[J]. Chemistry Letters, 2003, 15: 4 544-4 554.
[11] Liu Yun, Miao Hongyan,etal. Effect of reaction solvents on morphology of Bi2S3[J]. Chinese Journal of Inorganic Chemistry, 2008, 2: 240-243.
[12] Jyoti R Ota, Suneel K Srivastava. Low temperature micelle-template assisted growth of Bi2S3nanotubes[J]. Nanotechnology, 2005, 16: 2 415-2 419.
[13] Zhang H, Ji Y J, Ma X Y,etal. Long Bi2S3nanowires prepared by a simple hydrothermal method[J]. Nanotechnology, 2003, 14: 974-977.
[14] Michael B. Sigman, Jr., Brian A. Korgel. Solventless synthesis of Bi2S3(bismuthinite) nanorods, nanowires, and nanofabric[J]. Chemistry Letters, 2005, 17: 1 655-1 660.
[15] Xingfu Zhou, Xin Zhao, Danyu Zhang,etal. Hollow microscale organization of Bi2S3nanorods[J]. Nanotechnology, 2006, 17: 3 806~3 811.

