Ru-Co/SiO2催化剂的 TPR还原动力学
高海燕,相宏伟,李永旺
(1.江南大学化学与材料工程学院,江苏无锡214122;2.中国科学院山西煤炭化学研究所煤转化国家重点实验室,山西太原030001)
担载型钴基催化剂被广泛应用于由天然气经合成气转化为重质烃的反应中,所得的重质烃经加氢裂解可制得优质的环保型柴油[1-2]。研究已表明,钴的氧化物不具备催化活性,只有还原状态下金属钴才是反应的活性相,因此催化剂的还原度对其反应活性起着很重要的作用[3]。
Ru在世界各大石油公司开发的钴催化剂中常用作助剂,许多学者[3-6]研究了 Ru对钴基催化剂还原度的影响,发现少量 Ru的加入可以提高钴催化剂的还原度,从而提高催化剂的反应活性和重质烃选择性。关于 Ru的加入提高钴催化剂的还原度的原因,他们主要是集中在催化剂微观结构的表征方面进行了研究。
笔者首次用 TPR法研究 Co3O4粉末、Co/SiO2催化剂、Ru-Co/SiO2催化剂的还原动力学,求出了这几种物质的还原活化能。
1 实验部分
1.1 试剂及仪器
硝酸钴,分析纯,北京化工试剂厂产品;B型粗孔硅胶,青岛海洋化工集团公司产品;硝酸钌,质量分数6%,昆明贵金属研究所提供。
采用自制的 U形石英反应管进行 TPR实验。催化剂装量50 mg,载气为5%H2-95%N2混合气, N2吹扫温度373 K,TCD检测,纯 H2还原,还原压力0.2 MPa,体积空速1000 h-1。
1.2 催化剂的制备
1.2.1 Co3O4粉末的制备
用一定浓度的硝酸钴于723 K下焙烧4 h,得到Co3O4粉末。
1.2.2 Co/SiO2催化剂的制备
用 150 mL一定浓度的 NH4NO3溶液处理100 g粗孔硅胶载体,在 363 K下加热回流 2 h,固、液分离,并用去离子水洗涤载体,然后在373 K下干燥12 h,粉碎过筛,取20~40目的改性硅胶。用一定浓度的硝酸钴溶液等体积浸渍改性硅胶,放置12 h,在红外灯下烘干,723 K下焙烧4 h,即制得 Co/SiO2氧化态催化剂。催化剂中的Co质量分数为18%。
1.2.3 Ru-Co/SiO2催化剂的制备
将一定量的硝酸钴溶液与不同硝酸钌含量的溶液混合均匀,然后等体积浸渍20~40目的改性硅胶,放置24 h,在373 K下烘烤4 h,再在马福炉内623 K下焙烧4 h,制得Ru质量分数为2%、Co质量分数为18%的Ru-Co/SiO2催化剂。
2 结果与讨论
催化剂的还原动力学研究采用 TPR的速率方程式(1)[8]。
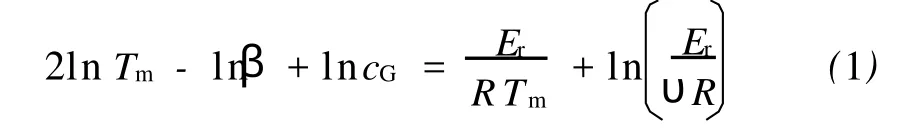
式(1)中,Tm为最大还原速率所对应的温度,K; β为线性升温速率,K/min;cG近似看成是 H2的平均浓度,mol/L。以2 lnTm-lnβ对1/Tm作图,从所得直线斜率可求得还原反应活化能 Er,从直线截距和 Er可求得指前因子υ。按照上述方法分别求出了 Co3O4粉末、Co/SiO2和 Ru-Co/SiO2催化剂的还原活化能。它们的 TPR还原动力学参数列于表1,不同升温速率下的 TPR谱示于图1。
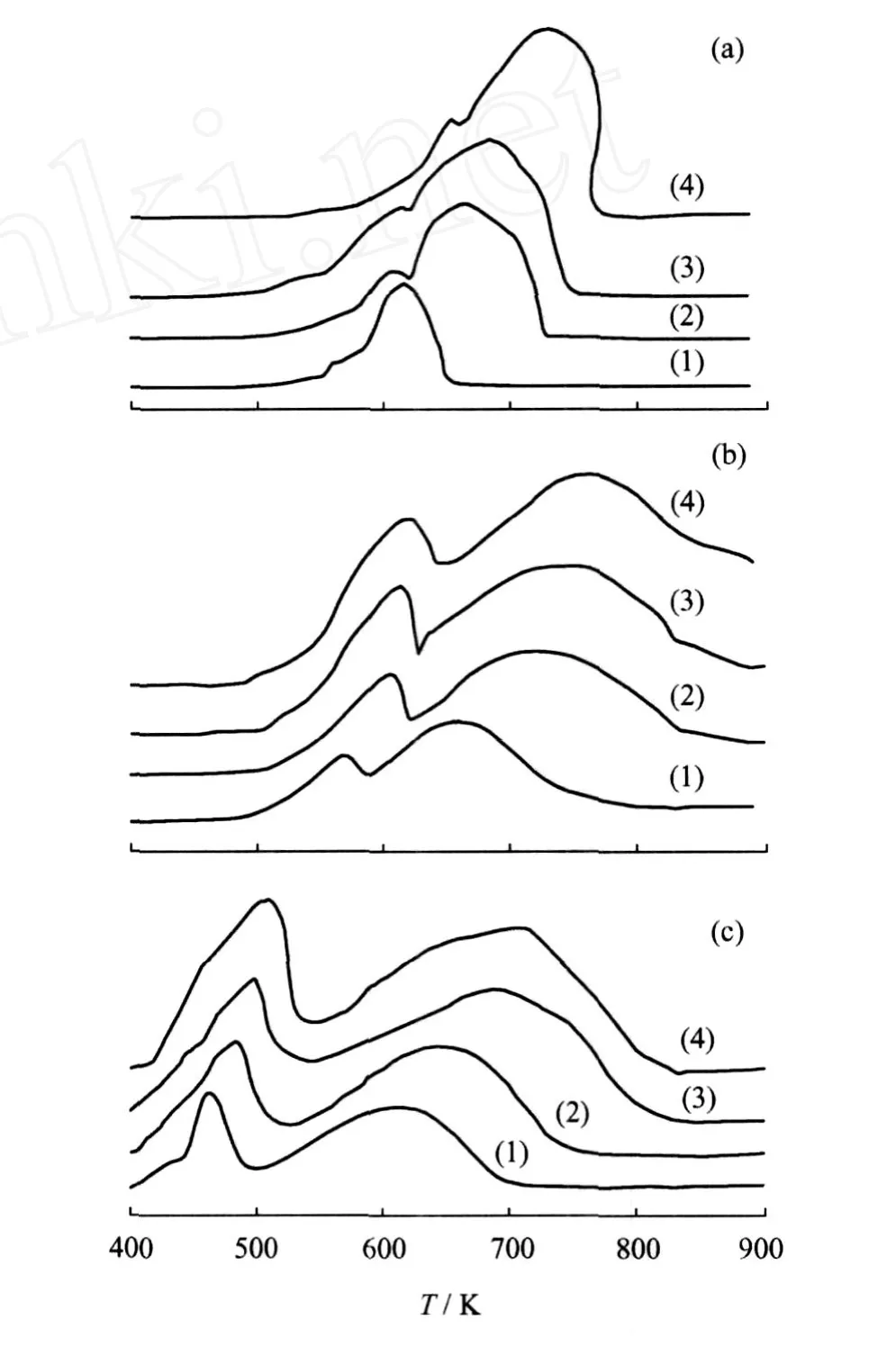
图1 不同升温速率下Co3O4粉末、Co/SiO2和 Ru-Co/SiO2催化剂的TPR谱图Fig.1 TPR profiles of Co3O4,Co/SiO2and Ru-Co/SiO2 catalyst at different heating rates(a)Co3O4;(b)Co/SiO2;(c)Ru-Co/SiO2Heating rate/(K·min-1):(1)5;(2)10;(3)15;(4)20
研究表明[3,5],Co3O4的还原分 2步进行: Co3O4→CoO→Co。从图1和表1可以看出,Co3O4粉末对应于第1个峰的Co3O4→CoO的还原活化能为39.195 kJ/mol,对应于第2个峰的CoO→Co的还原活化能为37.081 kJ/mol。

表1 Co3O4粉末、Co/SiO2和 Ru-Co/SiO2催化剂的 TPR还原动力学参数Table 1 The kinetic parameters of TPRreduction of Co3O4,Co/SiO2and Ru-Co/SiO2catalyst
氧化态Co/SiO2催化剂中 Co物种均以 Co3O4形式存在[5-6]。Co/SiO2催化剂中,对应于第1个峰的Co3O4→CoO的还原活化能为62.698 kJ/mol,对应于第 2个峰的 CoO→Co的还原活化能为42.585 kJ/mol,均大于 Co3O4粉末样品,表明存在着Co3O4与载体SiO2间的相互作用。
但是当 Co3O4负载在 SiO2载体上后,在所有升温速率下,Co/SiO2催化剂的最大还原温度均向低温偏移。一方面这是由于 Co/SiO2催化剂中Co氧化物与载体 SiO2之间的相互作用,使其还原活化能增大,还原速率减慢;另外,纯Co3O4化合物由于其表面积小,不易吸附 H2,当 Co3O4被分散到 SiO2载体时,Co3O4处于高分散状态,减小了 H2在催化剂上扩散效应的影响,故比较容易被还原。
Ru-Co/SiO2催化剂中,Co3O4→CoO的还原活化能为42.002 kJ/mol,CoO→Co的还原活化能为32.840 kJ/mol。与 Co3O4粉末相比,Ru-Co/SiO2催化剂还原过程中 Co3O4→CoO的还原活化能增大,而CoO→Co的还原活化能降低。这是因为, (1)Ru-Co/SiO2催化剂中Co氧化物与载体 SiO2之间的相互作用,使其还原活化能增大;(2)Ru的氢溢流作用[5]使氢原子参与了还原过程,使得 Co氧化物的还原活化能降低。
从图1还可知,Ru-Co/SiO2催化剂比 Co3O4粉末的还原温度显著降低,这是因为 Ru的还原温度较低,因此在较低的温度下即可发生氢溢流现象,使得Co物种还原;另一方面,由于Co前驱体负载在SiO2载体上,减少了扩散效应。与 Co/SiO2催化剂相比,Ru-Co/SiO2催化剂还原过程中两步的活化能均有所降低,可以认为还原过程中反应物由H2变成了活化 H原子,即在 Ru助剂的作用下, Co/SiO2催化剂的还原路径发生了变化。
Co3O4粉末、Co/SiO2催化剂、Ru-Co/SiO2催化剂中,Co3O4→CoO 的还原活化能均高于CoO→Co的还原活化能。但是实验发现,在纯 H2、673 K、6 h的工业还原条件下,几乎所有的 Co3O4可以还原为CoO,但CoO还原为金属Co的程度随载体的不同而不同[7]。这个现象可以解释为, Co3O4还原为CoO后,一部分 CoO与载体发生反应,形成难还原的化合物;另一部分CoO在 H2的作用下还原为金属 Co,这部分 CoO的还原相对较易。在 Ru助剂的作用下,Co/SiO2催化剂中Co3O4→CoO的还原活化能降低程度大于CoO→Co的还原活化能的降低程度,使得催化剂可以在低温下还原。低温下的还原可以减少随后的CoO与载体SiO2的相互作用程度,因此可以增加 Co/SiO2催化剂的还原度。
3 结 论
(1)Co3O4粉末、Co/SiO2催化剂、Ru-Co/SiO2催化剂中,Co3O4→CoO的还原活化能均高于CoO→Co的还原活化能。
(2)Co/SiO2催化剂中,对应于 Co3O4→CoO和CoO→Co的两步还原过程的活化能均大于Co3O4粉末,表明Co物种与 SiO2载体存在着相互作用力。其中第1步的还原活化能增加较多,而第2步次之,这是因为 Co3O4在还原过程中已经克服了其与载体的相互作用,一些CoO可以比较容易被还原为Co。
(3)Ru-Co/SiO2催化剂还原过程与 Co/SiO2催化剂相比,Co3O4→CoO 的还原活化能降低20.696 kJ/mol,而 CoO→Co的还原活化能降低9.754 kJ/mol。这是由于 Ru可以在低温下还原,还原后的金属Ru上的氢溢流作用,使活化 H原子参与了还原过程,改变了 Co/SiO2催化剂的反应历程。
[1]WEI C,PETR A C,LÉON G.Cobaltspecies in promoted cobalt alumina-supported Fischer-Tropsch catalysts[J].Journal of Catalysis,2007,252(2):215-230.
[2]AHMAD T,REZA M,MAL EK A,et al.Fischer-Tropsch synthesis overcobaltcatalystsupported on carbon nanotubesin a slurry reactor[J]. Applied Catalysis A:General,2008,345(2):134-142.
[3]LI P,LIU J,NAG N,et al.In situ synthesis and characterization of Ru promoted Co/Al2O3Fischer-Tropsch catalysts[J].Applied Catalysis A:General, 2006,307(2):212-221.
[4]REINIKAINENA M,NIEMELAÉA M K,KAKUTAB N, et al.Characterisation and activity evaluation of silica supported cobalt and ruthenium catalysts[J].Applied Catalysis A:General,1998,174(1):61-75.
[5]GL ESIA E,SOL ED S L,FIATO R A,et al.Bimetallic synergy in cobalt-ruthenium Fischer-Tropsch synthesis catalysts[J].Journal of Catalysis,1993,143(2):345-368.
[6]KOGELBAUER A,GOODWIN J G,OU KACI R.Ru promotion of Co/Al2O3F-T catalysts[J].Journal of Catalysis,1996,160(1):125-133.
[7]MING H,BAKER B G.Characterization of Co F-T catalysts[J].Applied Catalysis,1995,123(1):23-34.
[8]杨锡尧.固体催化剂的研究方法[J].石油化工,2001, 30(12):952-959.(YANG Xiyao.The study method to solid catalyst[J].Petrochemical Technology,2001,30 (12):952-959.)

