肤康涂膜剂处方优选的实验研究*
盛国荣
(江苏省南通市皮肤病性病防治所,江苏 南通 226006)
肤康涂膜剂处方优选的实验研究*
盛国荣
(江苏省南通市皮肤病性病防治所,江苏 南通 226006)
目的筛选肤康涂膜剂处方的最佳药物用量。方法采用正交试验设计法,考察不同处方的肤康涂膜剂对实验性小鼠的镇痛作用和对豚鼠皮肤石膏样毛癣菌感染模型的治疗作用,根据考察数据设计最佳处方。结果最佳处方为1 000 mL肤康涂膜剂中含水杨酸30 g,酮康唑20 g,薄荷脑20 g,氯霉素10 g。结论正交试验设计法优选肤康涂膜剂的处方,方法可行,效果满意。
正交设计;肤康涂膜剂;处方优选;镇痛试验;石膏样毛癣菌感染模型
皮炎、湿疹及其合并真菌感染在临床上较常见,外用药物仍以皮质激素类制剂或激素加抗真菌药物的复方制剂为主,但由于皮质激素的多种不良反应,使其临床使用受限。为此,笔者以水杨酸、酮康唑、薄荷脑、氯霉素为主要配方,研制了非激素类皮肤科外用制剂肤康涂膜剂[1]。为选择处方的最佳药物用量,达到临床疗效好、不良反应小的治疗目的,笔者采用正交试验设计法[2],并以对实验性动物的镇痛作用和对豚鼠皮肤石膏样毛癣菌感染模型的治疗作用为评价指标进行了研究,报道如下。
1 试验材料
试药:水杨酸(北京燕京药业有限公司,批号为071101);酮康唑(批号为 KE070406),氯霉素(批号为CH080329)均由南京白敬宇制药有限责任公司生产;薄荷脑(南通薄荷厂有限公司,批号为070323);肤康涂膜剂(本所制剂室,批号为080525)。
动物:昆明种小鼠,18~22 g,雌性;白色豚鼠,300 ~400 g,雌雄各半。由南通大学医学院实验动物中心提供,生产许可证为SCXK2002-0019。
菌种和培养基:石膏样毛癣菌(中国医学科学院皮肤病研究所);培养基(中国药品生物制品检定所)。
2 方法与结果
2.1 因素水平确定
根据临床用药经验、预试验及肤康涂膜剂处方,选择水杨酸(因素 A)、酮康唑(因素 B)、薄荷脑(因素 C)、氯霉素(因素 D)用量(每1 000 mL涂膜剂中药物g数)为考察因素。前3种药物起主要治疗作用,试验时每个因素安排4个水平;氯霉素主要起预防搔抓所致皮肤继发性感染的作用,试验时安排2个水平。各因素水平见表1。表1是一个43×21的试验,拟选用L16(43×26)的正交表。因表1中每个因素的水平都是由小到大按顺序排列,按正交表试验,所有因素的1水平要碰在一起,这种极端的组合易增加试验误差,因此对起主要治疗作用的前3个因素的水平进行了随机化处理,见表2。

表1 因素水平表

表2 随机化后各因素水平表
2.2 热板法镇痛试验[3]
选择昆明种雌性小鼠,置(55±0.5)℃恒温水浴上的金属盆底热板上,测定小鼠从开始放置于热板到受热板刺激后第1次出现舔后足的时间(s),即为该小鼠痛阈值。选用痛阈在20~30 s(剔除疼痛反应不规律如过敏、迟钝或喜跳动的小鼠)的小鼠80只,随机分成16组,每组5只,分笼存放并编号。试验前1 d给各组小鼠腹部剃毛,面积1 cm2。根据人体常用推荐剂量0.05 mL/cm2,按体表面积折算出小鼠用量为0.032 mL/cm2[4],取表3试验号对应处方用量制备的肤康涂膜剂,给上述相应编号的每只小鼠涂药,共4次,前2次涂腹部去毛皮肤,后2次涂四足掌,用药面积约1 cm2,每次用量0.032 mL/cm2,每次用药间隔为30 min。给药前测各小鼠痛阈值2次,取其平均值为正常痛阈值。各组动物在末次涂药后90 min分别测定痛阈值,求出给药后的痛阈提高百分率。
2.3 豚鼠皮肤毛癣菌感染模型治疗试验
菌液制备:取石膏样毛癣菌种,恢复其致病力,接种于沙堡琼脂斜面试管,26℃培养7 d后,用接种钩取成熟菌落,加到含0.1%吐温-80的0.9%无菌氯化钠溶液中,制成约(1~5)×106CFU/mL的孢子混悬液,备用[5]。
豚鼠感染模型制备与分组:取白色豚鼠120只,用10%硫化钠霜背部脱毛,脱毛面积约5 cm×6 cm,24 h后用细砂纸轻轻磨擦去毛皮肤,在去毛区中央制备有轻微出血的粗糙面,面积约2 cm×2 cm,将已制备好的石膏样毛癣菌混悬液用棉签均匀地涂抹于破损皮肤区,每天观察皮肤感染情况。接种菌液5~7 d后,选择接种部位出现类似人体体癣症状(如局部红肿、渗出、皮肤出现鳞片样改变)的豚鼠,真菌学检查(包括直接镜检和培养)阳性为造模成功。挑选其中造模质量较高的80只豚鼠,随机分成16组,每组5只,分笼存放并编号。
试验方法:根据人体常用推荐剂量0.05 mL/cm2,按体表面积折算出豚鼠用量为0.05 mL/cm2[4],取表3试验号对应处方药物用量制备的肤康涂膜剂,给上述相应编号的每只豚鼠皮损处涂药,用量为0.05 mL/cm2,2次/d。局部涂药时,至少应超过皮损边缘0.5 cm,共给药4周。治疗期间每隔1周记录感染部位的皮损程度,同时观察受试动物的反应。
2.4 评价指标与标准
镇痛试验量化评分:5只小鼠的痛阈总和为痛阈总值,以小鼠痛阈提高百分率(%)=[(给药后痛阈总值-给药前痛阈总值)/给药前痛阈总值]×100%为评价指标,评价肤康涂膜剂局部止痛、止痒效果,以 y1表示。优为 y1≥60%,良为 60%>y1≥50%,中为50%>y1≥25%,差为 y1<25%。
豚鼠感染模型皮损分级评分:以豚鼠皮肤感染的损害程度为判断标准,分为4级。0级,去毛皮肤无任何感染迹象,皮损分数记为0分;!级,接种真菌部位出现少量红斑与丘疹,色泽淡,皮损分数记为1分;"级,红斑面积大,伴脱屑或丘疹范围大,皮损分数记为2分;#级,炎症反应明显,有严重红斑,局部渗出或脓肿,有鳞屑样改变,皮损分数记为3分。5只豚鼠的分值总和为积分值。以疗效指数=[(治疗前积分值-治疗后积分值)/治疗前积分值]×100%为评价指标,评价肤康涂膜剂的抗真菌效果,以 y2表示。优为 y2≥90%,良为90% >y2≥60%,中为60% >y2≥30%,差为y2<30%。
2.5 正交试验结果
正交试验方案与结果:见表3。
直观分析:由表3可见,以镇痛作用为评价指标时,各因素影响大小顺序为C>A>B>D,不同因素内各水平影响强弱为A1>A4>A2>A3,B4>B3>B1>B2,C3>C1>C2>C4,D2> D1,最佳因素水平组合为A1B4C3D2,以对豚鼠感染模型的治疗效果为评价指标时,各因素影响大小顺序为B>A>C>D,不同因素内各水平影响强弱为A1>A3>A2>A4,B1>B4>B3> B2,C4> C1> C2>C3,D1> D2,最佳因素水平组合为A1B1C4D2。两个指标的差异为因素 B、因素 C、因素 D,即酮康唑、薄荷脑和氯霉素的用量。

表3 正交试验方案与结果
方差分析:结果见表4。可见,以镇痛作用为评价指标时,因素C和A影响有显著性差异,影响强度与直观分析结果相一致;以对豚鼠感染模型的治疗效果为评价指标时,因素A和B影响均有显著性差异,影响强度也与直观分析结果相符。在镇痛试验中,由表3中值可知,B4与B1无显著性差异,都能满足试验要求,结合镇痛试验和对豚鼠感染模型治疗试验,取B1较合适。在豚鼠感染模型治疗试验中,由表3中值可知,C3与C4也无显著性差异,都能满足试验要求,结合镇痛试验和豚鼠感染模型的治疗试验,取C3较合适。考虑到D的2个水平虽对结果有一定的影响,但直观分析和方差分析显示差异都很小,根据临床用药经验,D因素选取第1水平。综合直观分析和方差分析,最佳因素水平组合为A1B1C3D1。

表4 方差分析结果表
2.6 优选处方验证试验
根据优选结果,按最佳处方A1B1C3D1制备5批肤康涂膜剂,验证对小鼠的镇痛作用和对豚鼠感染模型的治疗效果。结果见表5。可见,最佳处方制备的肤康涂膜剂镇痛作用明显,痛阈提高百分率均高于60%;对豚鼠皮肤石膏样毛癣菌感染模型具有良好的治疗作用,疗效指数均高于90%。
表5 优选处方的验证(±s,n=5)
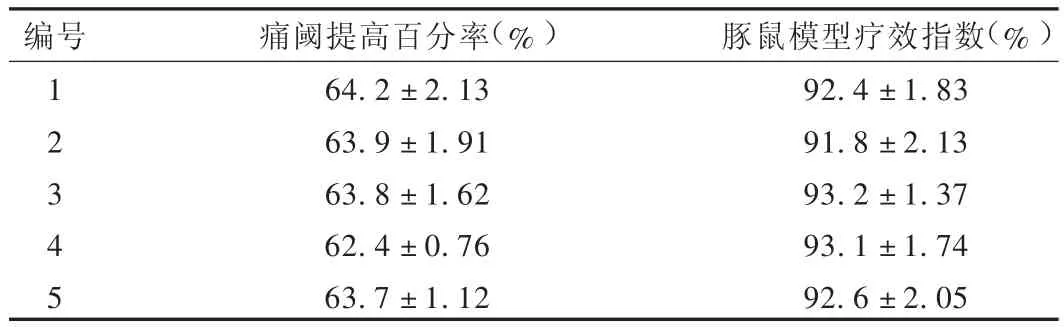
表5 优选处方的验证(±s,n=5)
编号1 2 3 4 5痛阈提高百分率(%)64.2±2.13 63.9±1.91 63.8±1.62 62.4±0.76 63.7±1.12豚鼠模型疗效指数(%)92.4±1.83 91.8±2.13 93.2±1.37 93.1±1.74 92.6±2.05
3 讨论
结果显示,最佳处方为每1 000 mL肤康涂膜剂中含水杨酸30 g,酮康唑20 g,薄荷脑20 g,氯霉素10 g。各因素选出的最佳水平,除氯霉素在试验中只安排了2个水平,评定时2者选1外,其余对治疗起主要作用的3个因素的最佳水平都处于试验方案的中间,说明各因素水平的确定合理。
处方中所含的水杨酸具有镇痛、抗炎、止痒和抗菌(包括真菌)作用[6],薄荷脑作为复方制剂局部使用可产生清凉、止痒、消炎作用[7],两药配伍使用,可使镇痛、止痒作用进一步增强。酮康唑对许多致病真菌的深部、浅部感染均有良好的抗菌作用[8],与水杨酸配伍使用可发挥协同作用。薄荷脑能抑制3!-羟类甾醇脱氢酶,促进生成更多氢化可的松,发挥抗炎作用[7]。因此酮康唑与薄荷脑配伍使用,对皮肤真菌感染所致的红斑、水肿等症状有很好的治疗作用。氯霉素抗菌谱广,可发挥低浓度抑菌、高浓度杀菌的作用[8],与具有温和防腐、抑菌作用的薄荷脑[9]配伍使用,对于防止搔抓所致继发性皮肤细菌感染具有良好的作用。透皮促进剂氮酮的加入,可使本制剂的镇痛、止痒、抗菌作用进一步增强。
在进行小鼠痛阈试验时,应采用导热良好、底部平整光洁的金属盆。本试验只选用雌性小鼠,因为雄性小鼠阴囊受热会下垂而与热板接触,受热刺激而跳动,影响试验进行。
本试验采用正交试验设计法较好地筛选出肤康涂膜剂的最佳处方,方法可行,效果满意,为临床应用提供了实验依据。
[1]盛国荣,谢 勇.肤康涂膜剂质量控制标准研究[J].中国药房,2004,15(5):283.
[2]方积乾.医药数理统计方法[M].第2版.北京:人民卫生出版社,1995:267.
[3]冯穗生,谭毓治,何 冰,等.骨友灵贴膏药效学研究[J].广东药学院学报,2004,20(1):42.
[4]徐叔云,卞如濂,陈 修.药理实验方法学[M].第3版.北京:人民卫生出版社,2002:202.
[5]郭宁和,吴绍熙,沈永年,等.特比萘芬治疗豚鼠皮肤癣菌感染的疗效[J].新药与临床,1996,15(6):339.
[6]芮耀诚.现代药物学[M].北京:人民军医出版社,1999:1 364.
[7]王浴生.中药药理与应用[M].第2版.北京:人民卫生出版社,2000:1 240.
[8]陈新谦,金有豫,汤 光.新编药物学[M].第16版.北京:人民卫生出版社,2007:125,84.
[9]王筠默.中药药理学[M].上海:上海科学技术出版社,1985:126.
Experimental Study of Formula Optimization for Fukang Plastics
Sheng Guorong
(Nantong Institution for Dermatosis and Venereal Disease,Nantong,Jiangsu,China 226006)
ObjectiveTo screen the best formula for Fukang Plastics.MethodsThe orthogonal experiment was used to study the abirritation effect on rats and the treating effect on infection model caused by trichophyta gypseum.The best formula was designed according to the result of this study.ResultsThe optimal formula was salicylic acid 30 g,ketoconazole 20 g,menthol 20 g,chloramghenicol 10 g per 1 000 mL.ConclusionThe formula optimized by orthogonal experiment is reasonable with satisfactory effect.
orthogonal design;Fukang Plastics;formula optimization;abirritating test;trichophyta gypseum induced infection model
R285.5
A
1006-4931(2010)04-0017-03
*南通市指令性社会发展科技计划项目,项目编号:S2007026。
盛国荣,男,主任药师,主要从事医院新制剂研发工作,(电子信箱)ntsgr@126.com。
2009-02-13)

