科学家优化遗传变异筛选技术推动疾病精准诊断
近年来,随着测序技术和群体研究的进展,加上大型生物样本库的建立,疾病相关变异的检测与解释得到了完善。
然而,许多遗传病患者仍难以确定其致病变异,影响了治疗选择、临床试验参与和家庭规划。
基因治疗的兴起使得寻找准确诊断更加关键,但由于生物数据库中非欧洲裔个体数据的不足,疑义变异的鉴定仍然存在困难。
深度突变筛选,能够通过高通量功能测定生成对突变的功能评分。然而,深度突变筛选的高成本和复杂性限制了其广泛应用。
已建立的饱和诱变方法如程序性等位基因系列(PALS)虽成本低,但是操作烦琐。
此外,功能测定方法如生长富集方法和流式细胞方法也面临成本和准确性挑战。因此,优化深度突变筛选技术对于更好地理解与疾病相关的基因变异至关重要。
为了实现了无需专用试剂、设备或烦琐步骤的饱和诱变,来自美国耶鲁医学院的团队基于程序性等位基因系列的核心概念进行了改进,开发出一种名为程序性等位基因系列一通用流程的方法。
实现深度突变筛选在罕见遗传病中的新突破
耶鲁医学院的马凯玥博士是本次成果的主要研究人员。2019年初,他刚结束博士一年级的三轮轮转,面临选择实验室的抉择。
其中,一个是他熟悉的基因组学方向,课题也与他的兴趣契合;另一个是本次论文共同通讯作者耶鲁医学院蒙科尔·莱克教授的实验室,研究方向是他不太熟悉的罕见遗传疾病的诊断与治疗。
在做出决定前,后者对他说:“我家有3只令人喜受的宠物狗,而吉姆(另一个课题组的负责教授)家只有一只。”正是这句轻松的话语让他做出了最终的选择。
尽管当时他对罕见病研究的挑战和机遇还不够了解,但综合多方因素后,最终正式加入了该团队。
事实上,蒙科尔本人是一名肢带型肌营养不良症患者(由肌联蛋白帽基因TCAP变异引起)。正因为自身的经历,蒙科尔非常关注诊断的速度和准确性,同时致力于开发新的治疗方法。
确定致病基因和致病突变是患者接受基因特异性疗法或参与临床试验的前提条件。然而,对于罕见病患者,获得准确诊断通常需要漫长的时间。
据统计,罕见病患者在发达国家平均需三到四年才能确诊。可以想象在发展中国家,这一过程更为艰难。
临床上常见的一类致病突变是单基因的单核苷酸变异。
尽管当前测序技术的进步使检测这些突变变得更加容易,但其中超过一半的变异仍被分类为“致病性不确定的基因突变”
这是因为每个人无论健康与否,都存在大量基因突变。这使得突变的临床后果难以得到简单直接的解析。因此,关键在于理解这些突变与疾病的相关性。
就a-抗肌萎缩相关糖蛋白病而言,它是一类由多种基因突变引起的罕见疾病,包括FKRP和LARGE1基因的突变。
目前,针对这些基因变异导致的疾病,已有多种疗法正在开发中,包括小分子药物和基因治疗。
因此,帮助更多患者获得确诊,从而使其有机会接受新疗法或参与临床试验,成了课题组的主要工作方向之一。
当前在研究突变致病性的领域中,深度突变筛选是一种广泛使用的方法。
它通过在细胞模型中饱和式地创造出目标基因的所有可能突变,并通过功能筛选对这些突变进行定性分析,以高通量获取突变的功能性信息。
该课题组研发的饱和诱变强化功能分析(SMuRF)就是一种适用于深度突变筛选的工作框架。
在开发过程中,该团队采用了多种新方法来降低成本和操作复杂性。
由于罕见病研究的实验室通常资金有限,但也往往拥有基因特异性的功能检测手段,因此研究人员希望通过简化工作流程,鼓励更多实验室参与深度突变筛选研究。
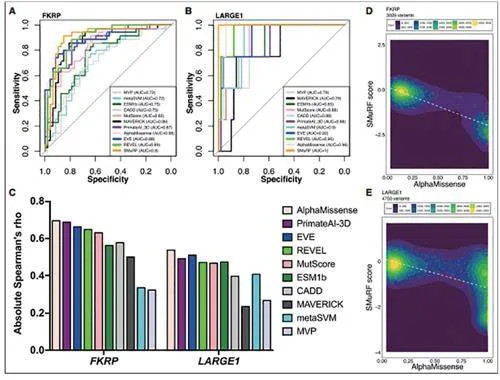
而通过应用SMuRF,研究团队对FKRP和LARGE1基因的单核苷酸突变进行了饱和式的功能评分,为这些基因的临床诊断提供了额外的参考依据。
SMuRF工作框架的开发与精准医学的未来探索
深度突变筛选,包含饱和诱变和功能测定两部分。该团队在开发SMuRF时,目标是创建一套通用工作流程,适用于多种饱和诱变和功能测定方法。
如前所述,在本次研究中他们开发了程序性等位基因系列一通用流程饱和诱变方法,并将其与流式细胞仪的高通量功能测定方法相结合。
另外,他们还探索了一种基于生长富集的功能测定方法。
SMuRF的开发经历了以下历程,首先,2015年发表在杂志上的程序性等位基因系列方法的相关论文引起了课题组的兴趣。
但该团队发现尽管其潜力巨大,实际应用却很少。
他们认为原因在于技术难度较高,因此他们基于程序性等位基因系列开发了更简便的程序性等位基因系列一通用流程,保留了其优势但只需使用更常规的实验室试剂。
继而,对于功能测定,a-抗肌萎缩相关糖蛋白病的分子表型是糖基化不足。
尽管已有流式细胞仪方法可检测患者成纤维细胞的糖基化,但课题组发现其灵敏度达不到深度突变筛选的要求,于是对染色条件和载体进行了优化。
此外,他们还发现,酶突变研究中基因表达量的控制至关重要,过高的表达可能掩盖突变影响,因此使用了较弱的泛素C启动子(UbC)。

此外,该团队结合深度突变筛选方法,开发了一整套从测序数据到功能打分的分析管线,并将其公开于GitHub,简化了数据处理流程。
团队协作是本研究获得成功的关键。研究中,一款关键的商用抗体停产,其他品牌的替代商用抗体无法实现预期效果。
此时,美国霍华德·休斯医学研究所研究员凯文·坎贝尔教授提供了大量实验室制备的抗体,使项目得以继续推进。
坎贝尔实验室的抗体借助爱美国荷华大学的平台向各处研究者廉价分享,保证了后续实验的可重复性。
而为了开发基于假型水疱性口炎病毒(ppVSV)的生长富集功能方法,美国乔治亚大学的梅琳达·布林达利教授为课题组提供了必要的实验材料及技术指导。
对于该成果的应用前景,该团队称提供的功能打分为临床诊断提供了额外的证据,已成功帮助来自德国和英国的医生与患者提升诊断准确性。
同时,课题组正在积极开发FKRP相关的基因治疗方法,功能打分也将作为额外的支持证据,助力患者参与临床治疗。
此外,研究人员正在与生物医药公司合作,计划采用SMuRF工作流程及改进后的功能方法,以检测小分子药物对不同突变的治疗效果,旨在推动精准医学的发展,确保患者获得更有效的治疗选择。
日前,相关论文以《疾病相关基因的饱和诱变强化功能进行分析》为题发表在期刊上。
马凯玥是第一作者,马凯玥和蒙科尔·莱克担任共同通讯作者。
总的来说,SMuRF提供了一个灵活的工作框架。
未来,课题组将通过多种方式增强其功能和易用性,具体计划包括:
1.开发基于精确编辑的饱和诱变方法,以实现高通量的内源饱和诱变。
2.研发适用于其他多重疾病基因的功能方法,扩展框架的应用范围。
3.改良现有脚本,使程序性等位基因系列一通用流程的设计与功能打分生成过程更为简便。
同时,该团队期待与遗传学、分子生物学、进化生物学、比较基因组学和罕见病临床研究等领域的同行进行广泛合作,以推动研究的深入与创新。(综合整理报道)(策划/克珂)
