二维层状麦克烯材料Nb2C催化改性Mg(BH4)2储氢性能研究


摘" 要: 硼氢化镁(Mg(BH4)2)因具有14.9%的储氢量,被认为是一种具有良好前景的高容量储氢材料.考虑到二维层状过渡金属碳化物麦克烯材料(MXene)对Mg(BH4)2的放氢过程具有显著的催化效果,文中采用酸刻蚀法制备了微观表征为二维层状的MXene材料碳化铌(Nb2C),并通过机械球磨法将所制备的Nb2C掺杂到Mg(BH4)2中,以此来催化改性Mg(BH4)2的放氢性能.由程序控温放氢(TPD)测试可得:在Mg(BH4)2-x%Nb2C(x= 20,30,40)催化改性体系中,当x= 40时,Mg(BH4)2-40%Nb2C体系的起始放氢温度可降至130 ℃左右,且升温至500 ℃后,可释放出12.8% H2,而未添加Nb2C的纯Mg(BH4)2约在285 ℃才开始放氢.除此之外,该体系在等温放氢测试中也表现出良好的放氢动力学性能,且由该体系改性后的放氢动力学性能可以在随后的第二和第三次吸放氢循环中保留下来,表现出良好的循环性能.
关键词: 硼氢化镁;Nb2C麦克烯;储氢性能;" 放氢动力学
中图分类号:TK91""" 文献标志码:A""""" 文章编号:1673-4807(2024)01-036-06
DOI:10.20061/j.issn.1673-4807.2024.01.006
收稿日期: 2022-03-31""" 修回日期: 2021-04-29
基金项目: 江苏省自然科学基金青年项目(BK20210884);江苏科技大学科研启动基金项目(1142932003)
作者简介: 郑家广(1992—),男,博士,讲师,研究方向为轻质金属基配位储氢材料的吸放氢性能调控及机理分析.E-mail: jgzheng@just.edu.cn
引文格式: 郑家广,张智,张焱,等.二维层状麦克烯材料Nb2C催化改性Mg(BH4)2储氢性能研究[J].江苏科技大学学报(自然科学版),2024,38(1):36-41.DOI:10.20061/j.issn.1673-4807.2024.01.006.
Study on the hydrogen storage property of two-dimensional layeredMXene material Nb2C catalytically modified Mg(BH4)2
ZHENG Jiaguang1, ZHANG Zhi1, ZHANG Yan1, ZHANG Haoyu1,WU Fuying2, ZHANG Liuting1
(1.School of Energy and Power, Jiangsu University of Science and Technology, Zhenjiang 212100, China)
(2.Testing and Analyzing Center, Jiangsu University of Science and Technology, Zhenjiang 212100, China)
Abstract:Magnesium borohydride is considered to be a promising high-capacity hydrogen storage material due to its hydrogen storage capacity of 14.9%. Considering that transition metal carbides have a significant catalytic effect on the hydrogen evolution process of Mg(BH4)2, acid etching method was used to prepare MXene material Nb2C microscopically characterized as two-dimensional layers, and the niobium carbide (Nb2C) was prepared by mechanical ball milling. The as-prepared Nb2C was doped into Mg(BH4)2 by the method to catalyze the modification of the hydrogen release properties of Mg(BH4)2. It can be obtained from the programmed temperature desorption (TPD) test: in the catalytic modification system of Mg(BH4)2-x%Nb2C(x=20, 30, 40), when x=40, the initial hydrogen desorption temperature of the Mg(BH4)2-40% Nb2C system can be reduced to about 130 ℃, and 12.8% H2can be released after heating to 500 ℃. Nevertheless, the pristine Mg(BH4)2 without Nb2C addition starts to release hydrogen at about 285 ℃. Furthermore, the isothermal hydrogen desorption test also showed favorable dehydrogenation kinetics. Moreover, the kinetic performance of hydrogen desorption modified by this system can be retained in the subsequent second and third hydrogen absorption and desorption cycles, showing excellent cycle performance.
Key words:Mg(BH4)2, Nb2CMXene, hydrogen storage property, dehydrogenation kinetics
当今世界,随着化石能源的不断消耗及其造成的污染,开发并研制出一种新型无污染能源迫在眉睫.氢能作为一种清洁可持续能源,具有高热值、燃烧产物仅生成水、可获取资源丰富、应用领域宽广等优势.然而,如何实现安全高效的储氢仍是氢能大规模应用的关键难题[1].
储氢方式目前主要有高压储氢、液化储氢和固态储氢,相对于其他两种储氢方式,固态储氢因具有储氢密度高、安全性能好、便于使用及运输等优点,受到了国内外学者的广泛关注[2].其中,硼氢化镁(Mg(BH4)2)因具有14.9%的高储氢量,被认为是一种具有良好前景的固态储氢材料,但由于自身的放氢动力学性能缓慢、放氢过程复杂、可逆性能差等弊端,限制了其在实际领域的应用[3].因此,需要通过适当的技术方法来改善其性能.
目前,对硼氢化镁主要的改性手段有氢化物复合[4]、催化掺杂[5]、纳米化[6]、反应失稳等[7].其中,使用催化剂掺杂性可以显著提升Mg(BH4)2的吸放氢动力学性能,这是一种简单有效的改善Mg(BH4)2储氢性能的方法.文献[8]中将Ti纳米颗粒通过球磨的方式掺杂到Mg(BH4)2中,在等温放氢实验中,掺杂该催化剂的样品氢气释放量均高于未加催化剂的Mg(BH4)2,被催化的Mg(BH4)2的吸放氢动力学也比未催化的Mg(BH4)2表现出更好的效果.过渡金属基催化剂被认为是一类能够有效提升Mg(BH4)2放氢性能的催化组元,但传统的过渡金属基催化剂不能有效地改善Mg(BH4)2的放氢性能,且表现出较差的可逆性,其主要原因是由于颗粒状的催化剂并不能很好地抑制硼氢化物颗粒在吸放氢过程中的团聚,且催化剂和硼氢化物需要更加有效地接触以获得更好的催化性能[9].因而找到一种可有效改善Mg(BH4)2储氢性能的催化剂材料非常重要.
MXene材料是一类过渡金属碳化物或氮化物,其作用于硼氢化物时表现出显著的纳米限域作用和催化效果.MXene材料也是最近发现的一种二维材料,已被应用于电池、复合材料、传感器和医疗设备等多个行业[9].MXene材料Nb2C是一种新型的二维功能化碳材料,具有良好的多排层状结构和高比表面积[10].Nb2C作为催化组元既可以提供具有良好催化能力的Nb位点,也能为Mg(BH4)2配位氢化物提供高比表面积的层状负载基体.文中将酸刻蚀法制备的Nb2C通过机械球磨掺杂到Mg(BH4)2中,并对其储氢性能进行了详细地研究.
1" 实验
1.1" Mg(BH4)2的制备
采用湿化学球磨法制备Mg(BH4)2.选用无水MgCl2和NaBH4作为原料,无水乙醚作为溶剂,将MgCl2和NaBH4按照摩尔比1∶2称取后置于球磨罐中,密封后充入1 MPa氢气作为保护气,并在行星式球磨机以450 r/min转速干磨12 h.球磨时在无水乙醚溶液中发生复分解反应以制备Mg(BH4)2,其反应方程式为:
MgCl2+2NaBH4→Mg(BH4)2+2NaCl
因反应产物Mg(BH4)2可溶于无水乙醚,而NaCl不溶于无水乙醚,故向干磨后的球磨罐中加入无水乙醚并再密封湿磨24 h以分离Mg(BH4)2和NaCl.接下来将湿磨后的泥巴状产物通过真空抽滤分离,取抽滤得到的清液.将清液置于耐高温的不锈钢容器中在动态真空下升温至200 ℃后,保温2~3 h以彻底去除乙醚溶剂和与Mg(BH4)2络合的乙醚.去除溶剂后所获得的白色粉末即为Mg(BH4)2.
1.2" Mxene材料Nb2C的制备
Nb2C通过酸刻蚀MAX相陶瓷Nb2AlC的方法制得.具体操作步骤如下,取1 g Nb2AlC粉末和10 ml HF(49%浓度)溶液,将HF加入至聚四氟乙烯内衬后,再将Nb2AlC粉末缓慢多次加入至HF中,然后将内衬置于磁力搅拌器中55 ℃搅拌40 h.随后将生成的溶液转移到离心管中,离心速度设为3 500 r/min,用去离子水洗涤多次至样品的pH值达到7.得到的湿沉淀物用微孔保护滤纸(0.22 μm)真空过滤,最后将产物在真空干燥箱中50 ℃烘干18 h.该方法总回收率可达98%[11].
1.3" Mg(BH4)2-x% Nb2C催化改性体系的合成
将制备好的Nb2C在不锈钢球磨罐中与Mg(BH4)2分别按照20、30、40的质量比进行掺杂,然后将样品在1 MPa的氢压下,以400 r/min 的转速球磨10 h时,球料比为40∶1.为保护样品不被空气污染,该掺杂过程在充满高纯度氩气的手套箱中进行,随后向球磨罐中充入氢气作为保护气.
1.4" 样品表征
XRD测试使用的是荷兰PANalytical公司生产的X'Pert Pro型X射线衍射仪.辐射源为Cu Kα(λ=0.154 05 nm)辐射,工作电压电流分别为40 kV和34 mA. XRD测试的扫描范围为5~80°,扫描速率为4°/min和0.02°/step.使用日本Hitachi公司生产的SU-70型场发射扫描电镜(SEM)观测样品的微观形貌,工作电压为3.0 kV.此外,对储氢材料的差示扫描量热法(DSC)测试可以得到其放氢初始和峰值温度.文中使用德国Netzch公司生产的Netzch STA 449C Jupiter型热分析测试仪进行DSC测试.Mg(BH4)2-x%Nb2C催化改性放氢体系是在实验室自制的Sievert型储氢性能测试仪上进行的.对于程序控温放氢(TPD)测试,样品在室温下以5 ℃/min 的升温速率升至500 ℃以获取放氢数据.样品的等温放氢测试是在室温下快速升至指定温度,并在此温度下保温3 h以记录该温度下的等温放氢性能. 循环性能测试是将样品升温至280 ℃进行放氢,然后在同一温度下以9 MPa氢压吸氢10 h,循环操作此步骤3次,记录每一次的放氢数据.放氢量的计算不包含催化剂的质量.
2" 结果与讨论
2.1" MXene材料 Nb2C的结构组成及形貌
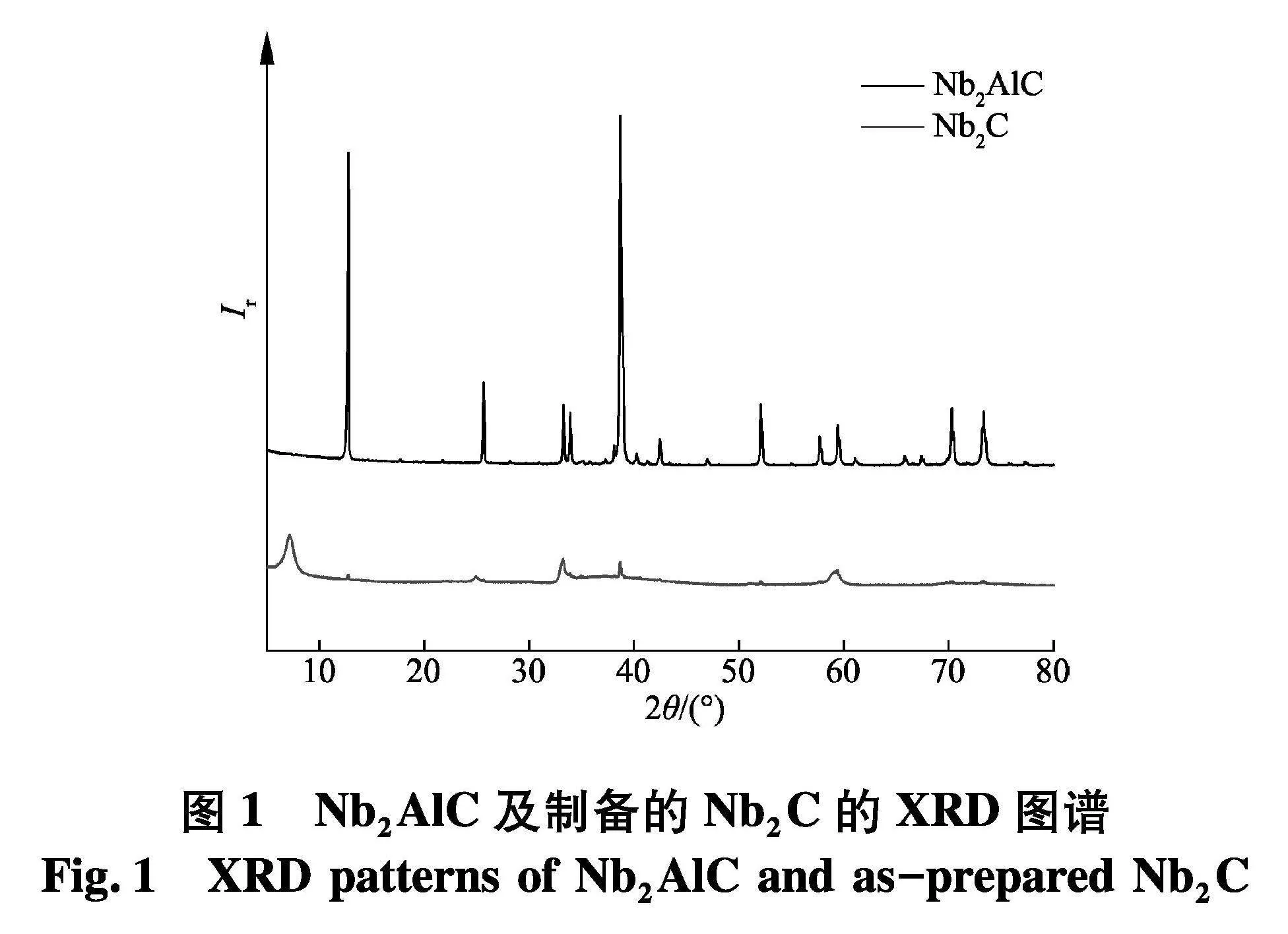
图1为刻蚀前的原料Nb2AlC以及使用 HF 刻蚀后生成的Nb2C的XRD图谱.
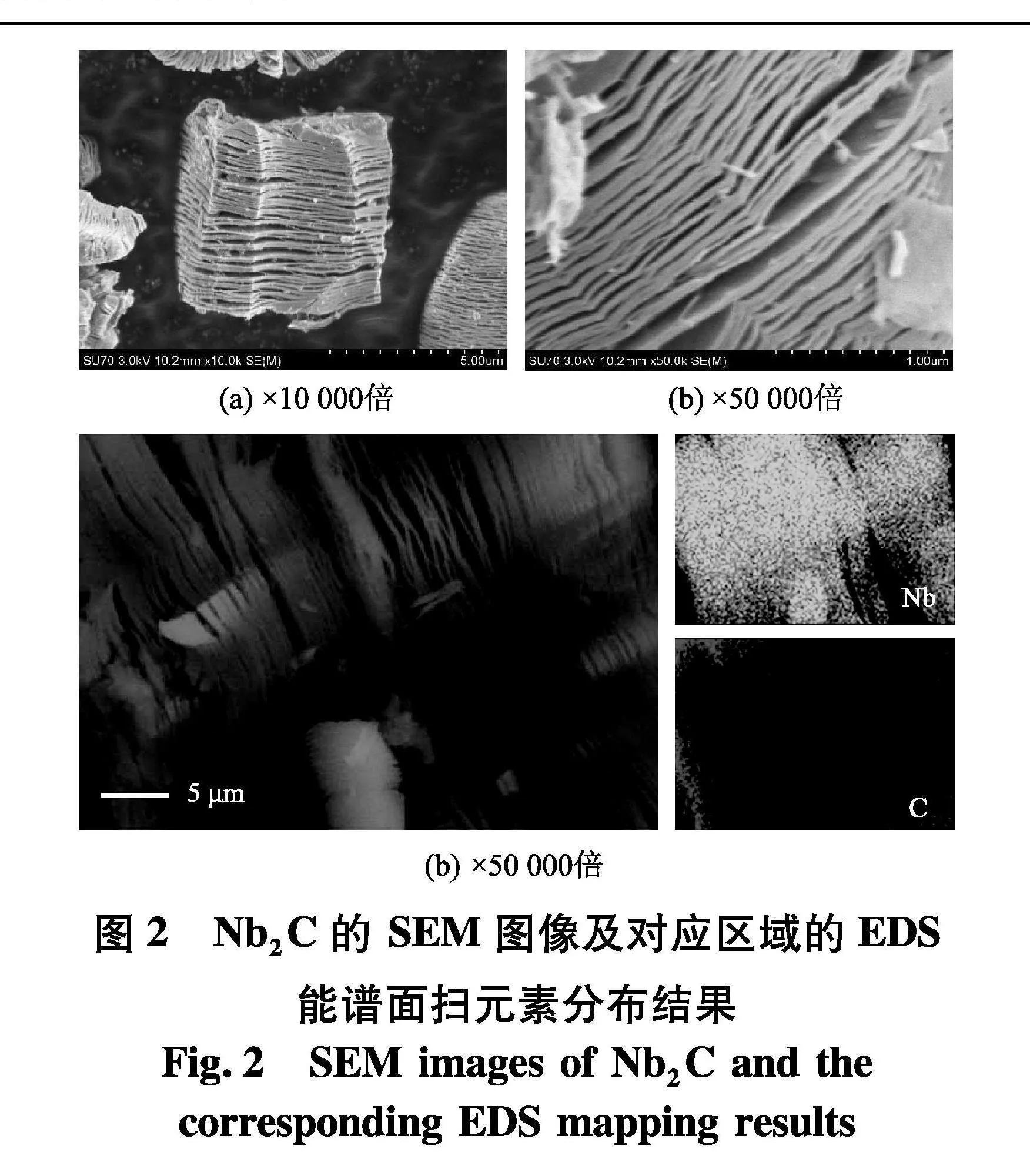
从图谱中可明显看出,反应前的Nb2AlC在12.8°、38.7°有两处强度较高的衍射峰,而在反应后Nb2AlC的特征衍射峰消失,同时产物Nb2C在7.2°、33.2°、38.7°、59.3°形成了4处衍射峰.图2(a,b)为反应后生成的Nb2C在不同倍率下的SEM图像,可以看出,刻蚀后的Nb2C呈明显的多排层状结构,其层间间距保持在0.5~3 μm,且层间厚度均在1 μm左右.图2(c)为Nb2C的暗场SEM照片及对应区域的EDS能谱面扫元素分布结果,通过EDS的结果可看出Nb元素大量且均匀地分布着,C元素则因测试过程中使用碳导电胶而无法清晰分辨.XRD中Nb2AlC特征衍射峰的消失,SEM图像中Al层被反应刻蚀以及相对应的EDS能谱面的元素分布,三者的结果共同证实了Nb2C已成功制备.
2.2" Mg(BH4)2-x% Nb2C体系的结构组成及形貌分析
为确定球磨掺杂后的Mg(BH4)2-x% Nb2C催化体系的成分组成,对不同掺杂比(x=20,30,40)的样品进行XRD表征.如图3,未添加催化剂的纯Mg(BH4)2在 17.4°、18.6°、19.1°、19.8°、21.5°有5处明显的衍射峰,经文献[12]对比其全部属于Mg(BH4)2的特征衍射峰,说明制备的Mg(BH4)2纯度较高.Mg(BH4)2-x%Nb2C催化体系的成分组成可从图3中得出:Mg(BH4)2和Nb2C的衍射峰依然存在于Mg(BH4)2-x%Nb2C催化体系的衍射图谱中,证明经过长时间的球磨两者没有发生明显的反应.
其次,Mg(BH4)2在掺杂Nb2C球磨后,其特征衍射峰大幅降低,且随Nb2C催化剂含量的增加,其衍射峰越不明显.这说明Mg(BH4)2晶粒在掺杂球磨过程中被大幅细化,这可能源于Mg(BH4)2颗粒的细化,而Nb2C自身的结构在球磨后可能保持了稳定.
通过SEM对Mg(BH4)2-x%Nb2C体系进行微观形貌观测.图4(a)为纯Mg(BH4)2的SEM图像,可看出纯Mg(BH4)2呈较大的颗粒状,且颗粒尺寸普遍超过15 μm.图4(b~d)为不同质量比的Mg(BH4)2-x%Nb2C样品的SEM图像,可看出球磨后的Mg(BH4)2颗粒尺寸普遍在3~8 μm,并且均匀地负载在Nb2C的层状表面,这说明掺杂球磨后的Mg(BH4)2颗粒被大幅度细化,且Nb2C的层状结构在球磨后得到了保留,这与前文的XRD结果相对应.
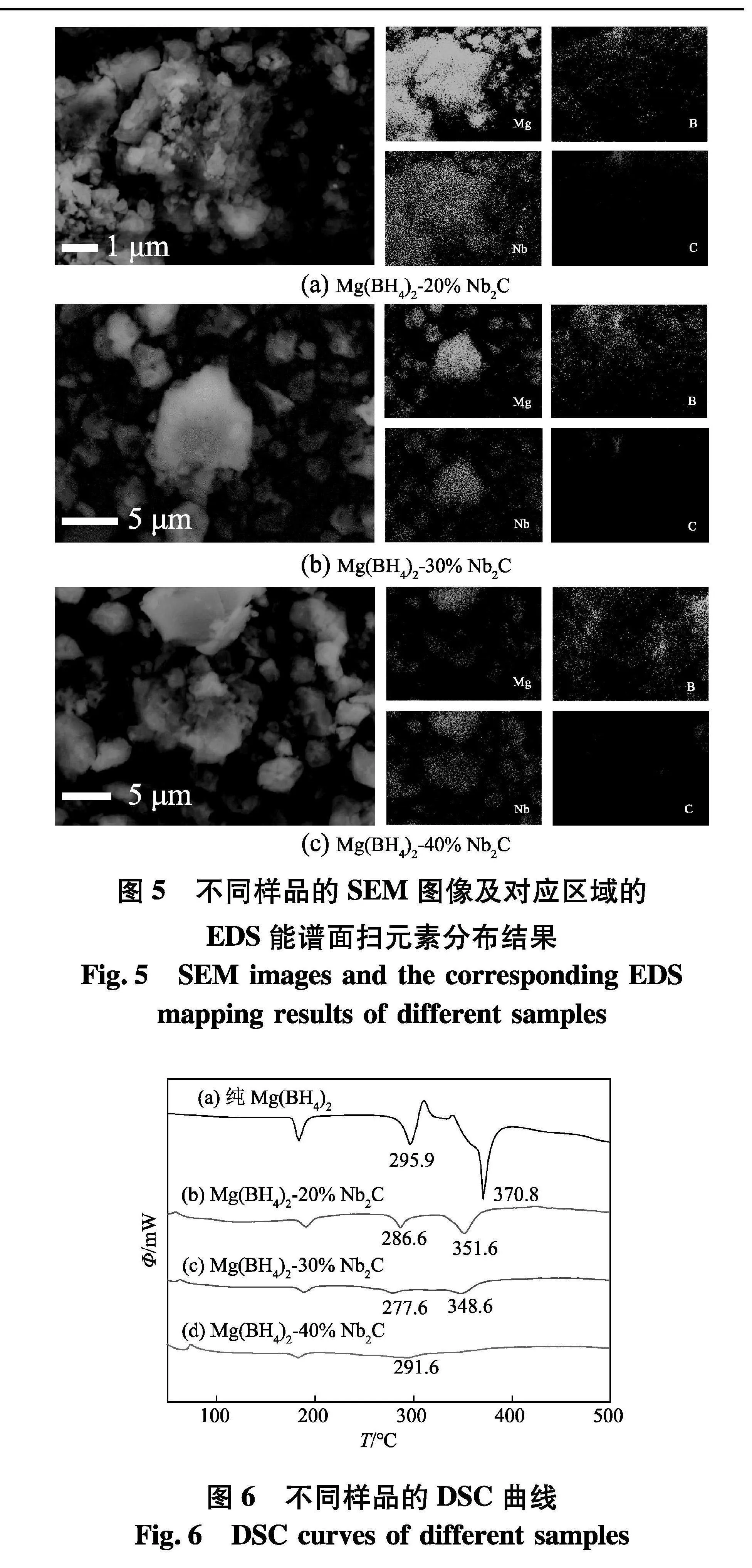
同时使用了暗场SEM及其对应的EDS能谱分析来确定不同质量比样品中各元素的分布情况.其结果如图5,除了因碳导电碳胶在测试中的使用,而导致C元素无法明显观察到之外,在不同质量比的Mg(BH4)2-x% Nb2C样品中,Mg,Nb和B元素均呈现均匀分布状态,且Nb元素的分布覆盖了大部分区域,Mg与B元素弥散分布区域与Nb元素区域相同.通过EDS能谱分析结果进一步说明了经过球磨后的Mg(BH4)2细小颗粒在Nb2C片层表面均匀存在,同时也证实了前文SEM分析得到的结论.
2.3" Mg(BH4)2-x% Nb2C体系的升温放氢性能
DSC测试可用于确定储氢材料的放氢峰值温度,文中采用5 ℃/min的升温速率对不同质量比的样品进行了DSC测试,结果如图6.在图6中,纯Mg(BH4)2在295.9 ℃和370.8 ℃出现两处明显的吸热峰,这对应了Mg(BH4)2两次不同的放氢过程(曲线a).图6中曲线(b~d)为Mg(BH4)2-x%Nb2C催化体系对应的DSC曲线,可以看出Nb2C催化剂的加入使得Mg(BH4)2放氢峰值温度明显提前.当Nb2C的添加量为20%时,Mg(BH4)2的两步放氢温度分别提前至286.6 ℃和351.6 ℃,并且随Nb2C含量的增加,Mg(BH4)2的放氢峰值温度逐渐降低,这表明Nb2C的加入有效改善了Mg(BH4)2的放氢动力学性能.
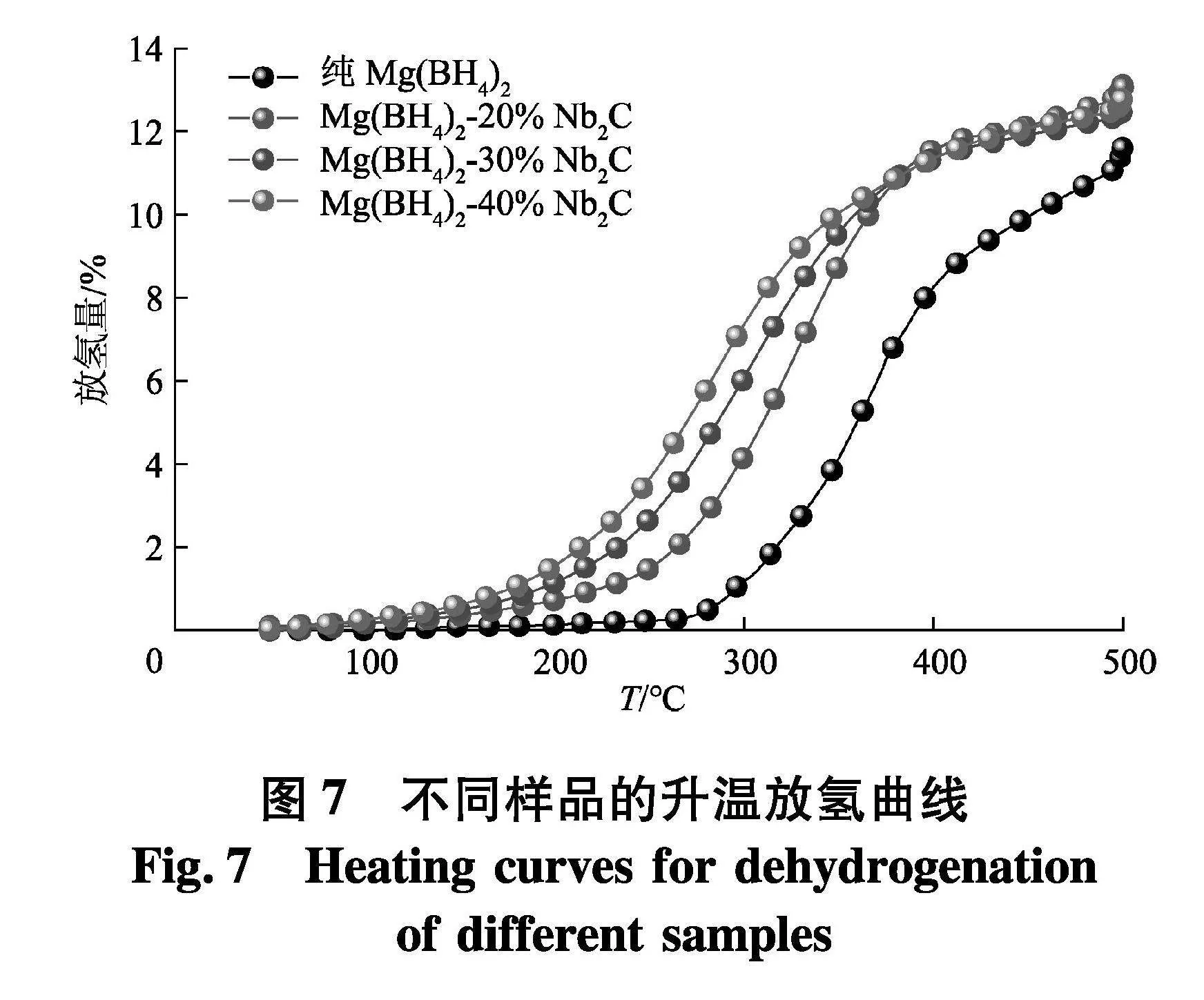
通过TPD测试得到了Mg(BH4)2-x%Nb2C体系的升温放氢温度及放氢量,其结果如图7.在该测试中,温度从室温以5 ℃/min的升温速率升到500 ℃.从图7中可以得知,纯Mg(BH4)2的起始放氢温度约为285 ℃,且在500 ℃也无法完全放氢,其在500 ℃下总放氢量为11.4%.较高的起始放氢温度和较晚的放氢终止点说明纯Mg(BH4)2的放氢性能需要改善.为了将Mg(BH4)2-x%Nb2C体系的放氢量和纯Mg(BH4)2的放氢量进行更直观地对比,计算时将放氢量归一化处理.根据图7中测试结果,Mg(BH4)2-20%Nb2C样品的起始放氢温度为163.1 ℃,Mg(BH4)2-30%Nb2C样品的起始放氢温度为145.4 ℃,而Mg(BH4)2-40%Nb2C样品能在132.7 ℃的较低温度就开始放氢.掺杂Nb2C的Mg(BH4)2样品的起始放氢温度相对于纯Mg(BH4)2均有大幅降低,且随着Nb2C添加量的增加,Mg(BH4)2-x%Nb2C体系的起始放氢温度逐渐降低,这说明增加Nb2C的质量比能够使得Mg(BH4)2获得更好的放氢性能.同时,可以从图中看出,该体系的最终放氢量均超过12%,这说明Nb2C的添加有效提升了Mg(BH4)2的放氢动力学性能和放氢量.但需要指出的是,如果考虑该体系的实际放氢量,Mg(BH4)2-x%Nb2C体系(x=20,30,40)的实际放氢量为10.5%、8.7%和7.7%.
2.4" Mg(BH4)2-30% Nb2C样品的等温放氢及循环放氢性能
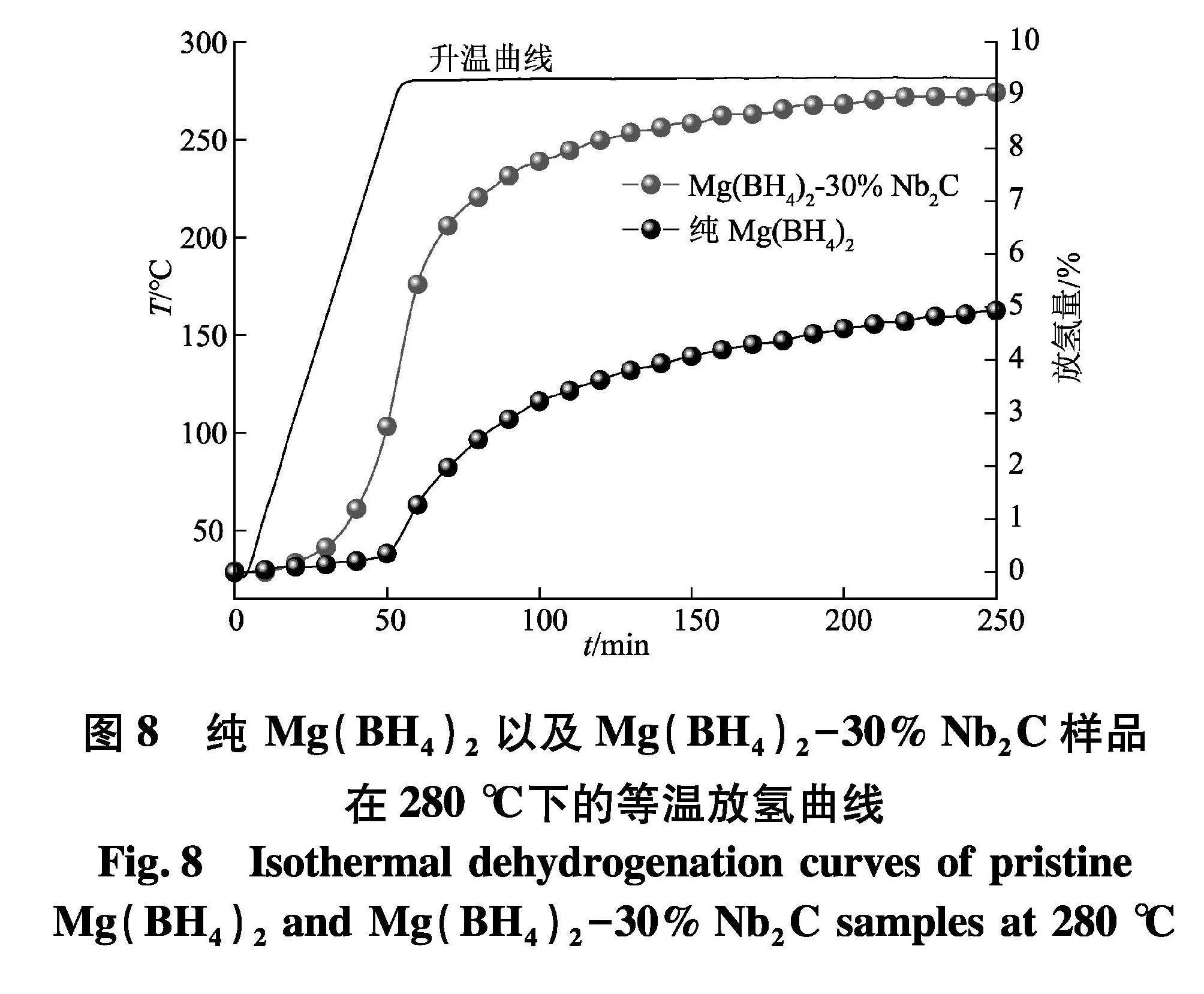
综上所述,Mg(BH4)2-30% Nb2C样品具有较低的放氢起始温度和峰值温度,并且综合考虑实际放氢量,故选取该比例样品进行等温放氢和循环放氢性能测试.在280 ℃下对Mg(BH4)2-30% Nb2C样品和纯Mg(BH4)2进行等温放氢测试对比,其结果如图8.
Mg(BH4)2 and Mg(BH4)2-30% Nb2C samples at 280 ℃
在测试过程中,温度从室温快速升至280 ℃,然后在该温度下保温3 h并记录样品的放氢量.从图8可以看出,纯Mg(BH4)2在280 ℃的温度下只能缓慢放氢,保温3 h后仅释放4.9%H2.而Mg(BH4)2-30%Nb2C样品在280 ℃下1 h之内就能迅速释放8.1% H2,且保温3 h后能够放出9.0%H2.需要补充的是,该样品最终的实际放氢量为6.4%,相对于纯Mg(BH4)2有了较为明显的提升.等温放氢测试进一步证明,Nb2C催化剂的加入显著提升了Mg(BH4)2的放氢动力学性能.
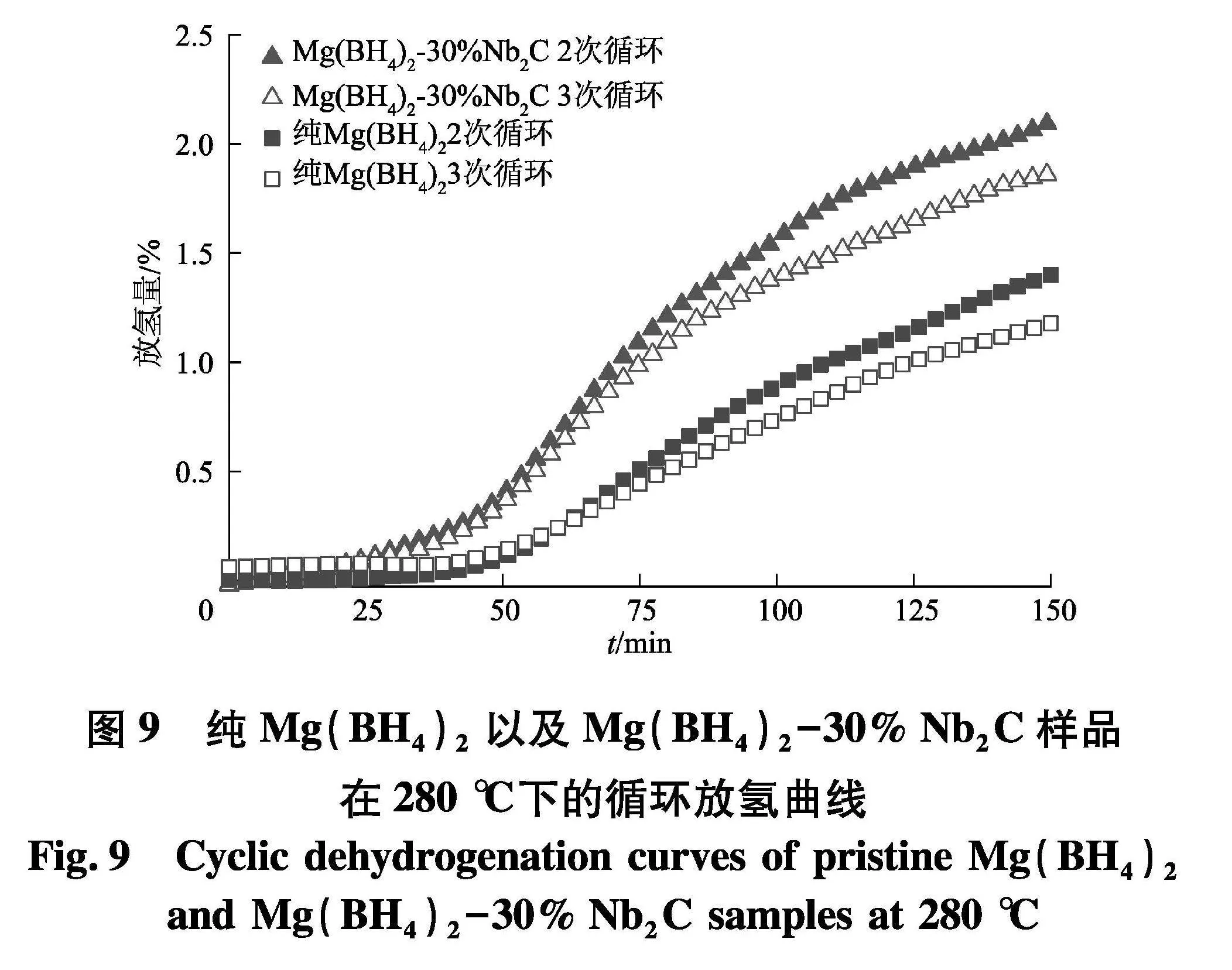
吸放氢循环测试是衡量储氢材料性能的一项重要指标.本测试对Mg(BH4)2-30% Nb2C样品和纯Mg(BH4)2进行了3次循环放氢测试.测试过程中,样品升温至280 ℃后保温一段时间,然后在同一温度下以90 bar氢压吸氢10 h,重复此操作3次,同时记录其每一次的放氢曲线,结果如图9.从图中可以看出,纯Mg(BH4)2在第2次和第3次循环后,其放氢量分别只有1.4%和1.2%.而掺杂了Nb2C的Mg(BH4)2-30% Nb2C样品在第2次和第3次循环后分别能放出2.1%和1.8%H2,相对于纯Mg(BH4)2的放氢量有较大提升.循环放氢测试结果说明:第一,在一定程度上,Nb2C的加入对Mg(BH4)2放氢动力学的提升作用在循环放氢过程中得到了维持;第二,Nb2C的加入能够提升Mg(BH4)2在同一温度下的循环放氢容量.
在280 ℃下的循环放氢曲线
and Mg(BH4)2-30% Nb2C samples at 280 ℃
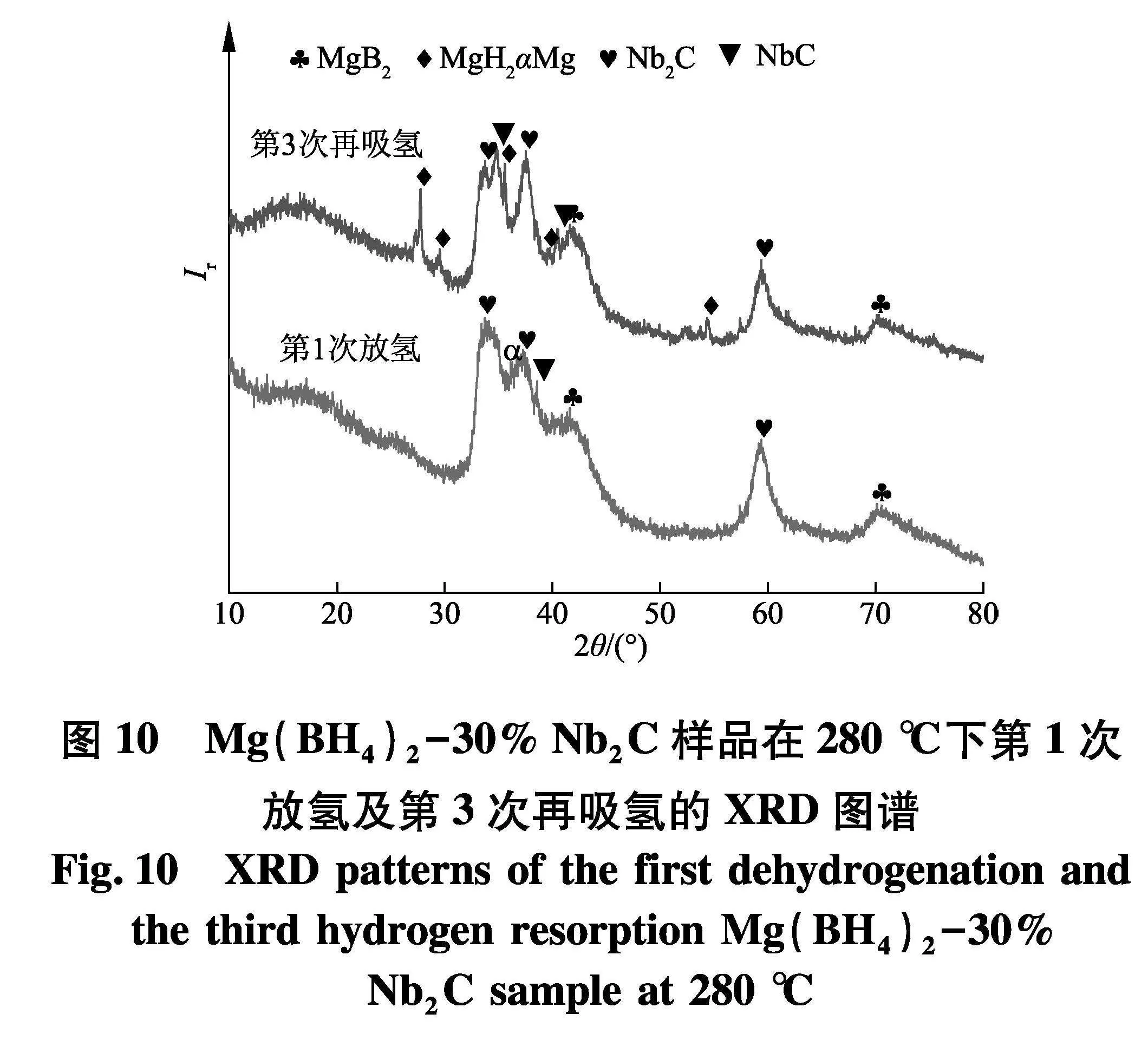
为进一步确定Nb2C的加入对Mg(BH4)2可逆储氢性能的影响机制,对Mg(BH4)2-30% Nb2C样品的放氢和再吸氢产物进行了XRD测试,其结果如图10.由图10中可以得出,Mg(BH4)2-30% Nb2C样品在280 ℃第1次放氢后的最终放氢产物为MgB2以及Nb2C和由Nb2C原位生成的NbC[13],结合图Mg(BH4)2-30% Nb2C样品在第3次吸氢后的XRD 图谱,说明了Nb2C以及NbC 在Mg(BH4)2吸放氢循环过程中起到了协同催化的作用.同时,由第3次再吸氢后样品的XRD图谱可知,再吸氢生成物中出现了较强的MgH2的特征衍射峰,这说明Mg(BH4)2-30% Nb2C样品在放氢后生成了少量的Mg,且生成的Mg在样品加压吸氢的过程中转变为MgH2.由于再吸氢产物主要由MgH2和MgB2组成, 说明可逆放氢容量的来源主要为MgH2,以及Mg(BH4)2只能实现部分可逆,这导致了Mg(BH4)2的可逆储氢性能下降以及循环放氢量的减少.
3" 结论
文中成功制备了二维层状MXene材料Nb2C以及纯度较高的Mg(BH4)2,并将Nb2C用于催化改性Mg(BH4)2的储氢性能.Nb2C的催化作用大幅提升了Mg(BH4)2的动力学性能,且Mg(BH4)2-40% Nb2C样品相对于纯Mg(BH4)2,放氢温度提前了近150 ℃,且最终放氢量也得到了提升.Mg(BH4)2放氢性能的大幅度提高归因于催化剂Nb2C的层状结构,而且Nb2C的层状结构在球磨掺杂后也得到了保留.这说明Nb2C一方面作为载体负载了细小的Mg(BH4)2颗粒防止其团聚,另一方面在吸放氢过程中又能原位生成NbC以达到协同催化的效果.这种负载-协同催化机理是Nb2C改善Mg(BH4)2储氢性能的关键.
参考文献(References)
[1]" 张刘挺,颜年华,陆雄, 等.TiH1.971催化Mg纳米晶储氢性能研究[J].江苏科技大学学报(自然科学版),2021,35,(1):46-50.
[2]" WANG Z Y, ZHANG X L,REN Z H, et al. In situ formed ultrafine NbTi nanocrystals from a NbTiC solid-solution MXene for hydrogen storage in MgH2[J]. Journal of Materials Chemistry A,2019, 23: 14244-14252.
[3]" WANG X, XIAO X, ZHENG J, et al. In-situ synthesis of amorphous Mg(BH4)2 and chloride composite modified by NbF5 for superior reversible hydrogen storage properties[J]. International Journal of Hydrogen Energy, 2020, 45(3): 2044-2053.
[4]" GRUBE E, JENSEN S R H, Nielsen U G, et al. Reactivity of magnesium borohydride-Metal hydride composites, γ-Mg (BH4)2-MHx, M=Li, Na, Mg, Ca[J]. Journal of Alloys and Compounds, 2019, 770: 1155-1163.
[5]" SALDAN I, FROMMEN C, LLAMAS-JANSA I, et al. Hydrogen storage properties of γ-Mg(BH4)2modified by MoO3 and TiO2[J].International Journal of Hydrogen Energy, 2015, 40(36): 12286-12293.
[6]" JAVADIAN P, SHEPPARD D A, BUCKLEY C E, et al. Hydrogen storage properties of nanoconfined LiBH4-Ca (BH4)2[J]. Nano Energy, 2015, 11: 96-103.
[7]" YING B,ZI W P,FENG W, et al. Role of Metal Electronegativity in the dehydrogenation thermodynamics and kinetics of gomposite metal borohydride-LiNH2 hydrogen storage materials[J]. Acs Applied Materials amp; Interfaces, 2018, 10(11):9514-9521.
[8]" WANG X, XIAO X, ZHENG J, et al. The dehydrogenation kinetics and reversibility improvements of Mg(BH4)2 doped with Ti nano-particles under mild conditions[J]. International Journal of Hydrogen Energy, 2021, 46(46): 23737-23747.
[9]" MALAKI M, MALEKI A, VARMA R S. MXenes and ultrasonication[J]. Journal of Materials Chemistry A, 2019, 7(18): 10843-10857.
[10]" GUL S, SERNA M I, ZAHRA S A, et al. Un-doped and Er-adsorbed layered Nb2CMXene for efficient hydrazine sensing application[J]. Surfaces and Interfaces, 2021, 24: 101074.
[11]" GUL S, SERNA M I, ZAHRA S A, et al. Un-doped and Er-adsorbed layered Nb2CMXene for efficient hydrazine sensing application[J].Surfaces and Interfaces, 2021, 24: 101074.
[12]" JENNY G,VITILLO,SILVIA B, et al. Spectroscopic and structural characterization of thermal decomposition of γ-Mg(BH4)2:Dynamic vacuum versus H2 atmosphere[J]. The Journal of Physical Chemistry C, 2015, 119(45), 25340-25351.
[13]" VISHWANADH B, MURTHY T S R C, ARYA A, et al. Synthesis and phase transformation mechanism of Nb2C carbide phases[J]. Journal of Alloys and Compounds, 2016, 671: 424-434.
(责任编辑:顾琳)

