不同黄芪甲苷含量测定法对玉屏风颗粒质量控制的影响


【摘 要】 目的:研究参考2020版《中国药典》黄芪项下的加氨提取法测定玉屏风颗粒中黄芪甲苷含量对其质量控制的影响。方法:分别通过加氨提取法和氨洗法对玉屏风颗粒中黄芪甲苷进行含量测定,考察不同测定方法下黄芪甲苷的转移率,并优化加氨提取黄芪甲苷含量测定方法。结果:玉屏风颗粒以加氨提取法测得的黄芪甲苷含量高于氨洗法所测含量,两种方法测得的转移率存在明显差异,优化的黄芪甲苷测定法各方法学考察试验RSD<4%。结论:参考2020版药典的黄芪甲苷测定法适用于玉屏风颗粒,该法具有操作简便、黄芪甲苷转化率高的特点,优于氨洗法,作为玉屏风颗粒的质量控制方法可广泛推广。
【关键词】 玉屏风颗粒;黄芪甲苷;含量测定;加氨提取法;氨洗法
【中图分类号】R284.2
【文献标志码】A 【文章编号】1007-8517(2024)12-0047-04
DOI:10.3969/j.issn.1007-8517.2024.12.zgmzmjyyzz202412010
Influence of Different Astragali Radix Assay Method on Quality Control of Yupingfeng Granule
LIU Lu FU Chuhan MEI Yan
Guangdong Food And Drug Vocational-technical School,Guangzhou 510663, China
Abstract:Objective To studythe influence of 2020 Chinese pharmacopoeia astragaloside Ⅳassay methodunder Astragali radixitem on quality control of Yupingfeng Granule.Methods The content of astragaloside Ⅳ in Yupingfeng Granule was determined by ammonia-added extraction method and ammonia-washed method. Transfer rate of astragaloside Ⅳ measured by different methods was investigated. The ammonia-added extraction astragaloside Ⅳ assay method of Yupingfeng Granule was optimized.Results Astragaloside IV content of the ammonia-added extraction samples from Yupingfeng Granule was higher than the ammonia-washedsamples. The transfer rate measured by the two methods was significantly different. RSD of the optimized method for the determination of astragaloside IV was less than 4%.Conclusion With easy operation and high conversion rate, the astragaloside IV assay methodmodified from 2020 Chinese pharmacopoeia is applicable to Yupingfeng Granule, which is superior to ammonia-washed method and could be widely applied to quality control method for Yupingfeng Granule.
Key words:Yupingfeng Granule;Astragaloside Ⅳ;Determination;Ammonia-added Extraction Method; Ammonia-washed Method
2020年版中国药典于2020年12月实施,与2015版药典一部比较,中药修订了452个品种,其中包括了黄芪的黄芪甲苷含量测定方法的改变,由氨洗法改进为加氨提取法[1-2]。在按药典方法检测黄芪药材的日常药品检验工作中发现,2015版药典方法以甲醇浸泡过夜后索氏提取,再以水饱和正丁醇萃取,最后氨洗并过D101型大孔树脂柱纯化,2020版药典方法仅以含氨甲醇加热回流即可,操作简便,样品制备时间短,测得黄芪甲苷含量高,总体优于2015版药典方法。然而,以黄芪甲苷作含量测定指标的大多数成方制剂,如玉屏风颗粒,于2020版药典中方法未作变更,仍采用氨洗法,样品溶液制备耗时费力,方法有待优化[3-15]。同时,黄芪甲苷测定需加碱转化,具有一定特殊性,制剂方法与药材标准方法不一致,可能会影响制剂从投料生产、制备到成品检测的质量控制。作者对玉屏风颗粒采用加氨提取法检测黄芪甲苷的可行性进行研究,通过比较加氨提取法和氨洗法黄芪甲苷测定结果,探讨参考新版药典的黄芪甲苷测定法对玉屏风颗粒质量控制的影响,并在此基础上提出建立相关质量控制方法的建议。
1 仪器与试药
1.1 仪器 Agilent 1200,1260高效液相色谱仪- Alltech 3300蒸发光散射检测器。
1.2 试剂 提取样品用甲醇、氨水为分析纯(广州化学试剂厂),乙腈为色谱纯(Thermo Fisher),水为超纯水(Millipore Adavantage A10制备)。
1.3 对照品、对照药材及样品 黄芪甲苷对照品(批号:110781-201616;含量以93.0%计)购自中国食品药品检定研究院;玉屏风颗粒(批号:180203、180905、181001)购自广东环球制药有限公司;阴性对照为依玉屏风颗粒处方工艺制成的缺黄芪样品。
2 方法与结果
2.1 不同方法测定黄芪甲苷含量比较
2.1.1 玉屏风颗粒不同制备方法样品黄芪甲苷含量测定 2020版药典玉屏风颗粒黄芪甲苷含量测定方法即氨洗法,与加氨提取优化法对比见2.2。
2.2 玉屏风颗粒黄芪甲苷含量测定方法优化
[JP2]2.2.1 液相条件 色谱柱:Waters Xbridge C18(4.6 mm×250 mm,5 μm);柱温:30 ℃;流动相:乙腈-水(32∶68);进样量:10 μL;检测器:ELSD,漂移管温度45 ℃,载气流速1.5 L·min-1。[JP]2.2.2 样品溶液制备 取玉屏风颗粒样品,研细,取约2.5 g,精密称定,置具塞锥形瓶中,精密加入含4%浓氨试液的80%甲醇溶液100 mL,密塞,称定重量,加热回流2 h,放冷,再称定重量,用溶剂补足减失的重量,摇匀,滤过,精密量取续滤液50 mL,蒸干,残渣加水15 mL,微热使溶解,用水饱和的正丁醇振摇提取6次,每次15 mL,合并正丁醇液,蒸干,残渣用80%甲醇溶解,转移至5 mL量瓶中,加80%甲醇至刻度,摇匀,滤过,取续滤液,即得。
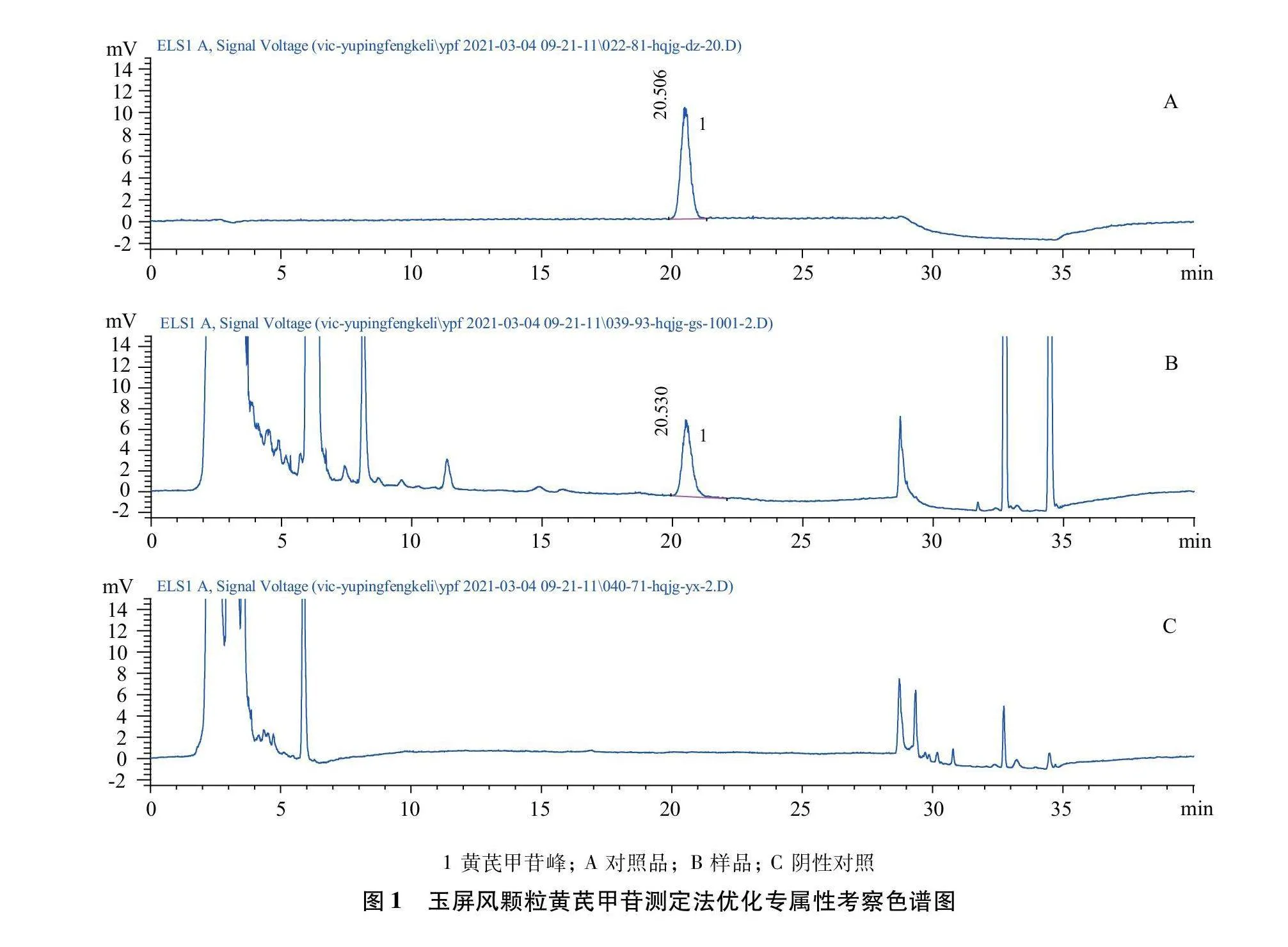
2.2.3 专属性考察 按玉屏风颗粒工艺制备缺黄芪的阴性对照,取黄芪阴性对照,制成阴性对照溶液。取对照品溶液、样品溶液、黄芪阴性对照溶液进行测定,结果样品黄芪甲苷色谱峰位置上无阴性干扰。如图1所示。
2.2.4 线性范围考察 取黄芪甲苷对照品加80%甲醇配制系列浓度的对照品溶液,以峰面积的对数(Y)对黄芪甲苷浓度的对数(X)进行回归,作标准曲线。结果在59.14~236.57 μg·mL-1范围内呈线性关系,标准曲线为Y=1.668 6X+7.947 4(r2=0.999 8)。
2.2.5 精密度试验 同一样品溶液(180905)重复进样6次, RSD为0.57%。
2.2.6 稳定性试验 同一样品溶液(180905)分别在0 h、2 h、4 h、6 h、8 h、12 h、16 h、20 h、24 h进行测定,RSD为0.79%。
2.2.7 重复性试验 取同一批样品(180905)制备6份样品溶液,测定含量,RSD为2.41%。
2.2.8 加样回收率试验 取已知含量的样品(180905),精密加入一定量黄芪甲苷对照品溶液,测定含量,计得平均回收率为101.03%,RSD为3.84%。见表1。
2.2.9 样品测定 分别以药典法和优化方法测定多批样品黄芪甲苷含量。见表2。
3 讨论
3.1 2020版药典黄芪甲苷含量测定法的特点和对成药质量检测的影响 加氨提取法具有以下优点:①无需提取后氨洗,减少操作步骤,误差降低;②样品制备时间短;③溶剂对黄芪甲苷的溶解度增加,提取的同时碱化,使得黄芪甲苷提取、转化效率更高。玉屏风颗粒益气固表止汗,由黄芪、白术、防风三味组成,依药典,每100 g本品含黄芪120 g,主要工艺为防风提取挥发油,药渣及余二味加水煎煮,煎液醇沉,回收乙醇后浓缩,制粒后喷挥发油。本研究选取的制剂为含黄芪处方加水提取的颗粒剂,是中药制剂中常用工艺和剂型,经试验,样品制剂直接套用2020版药典方法,会出现以下问题:①2020版药典方法因黄芪甲苷测得含量较高,方法中省去除杂、浓缩的步骤,故检测器测得响应较低,不利于成分复杂、黄芪甲苷含量低的样品测定,而且玉屏风颗粒在提取后直接测定所得峰面积仍较小,不便于建立方法,为满足检测要求须提高样品溶液浓度;②中成药的提取工艺多以水为溶媒,溶剂含水易使样品测定受其它成分和辅料的影响,玉屏风颗粒在加入溶剂超声提取后,多黏结,不易分散,影响目标成分溶出和测定结果的Rw6yj3NCliLQ2RlQQhVIfg==重复性,需以回流法,通过加热沸腾使样品分散、溶解。
3.2 含测法变更对成药源头、生产的影响 2020版药典除变更了黄芪甲苷测定方法外,还将限量标准从0.040%上调至0.080%,这将影响相关成药的原料药材准入,因此成品的质量标准亦应根据实际情况调整。不同测定方法含量不同,但不同方法之间的提取效率、含量未发现有无明显比例关系,不同方法计得的黄芪甲苷转移率存在明显差异,因此方法变更可能需调整生产过程中以黄芪甲苷含量为指标的质量控制参数。
3.3 黄芪甲苷含量测定方法优化考察 研究建立了玉屏风颗粒的黄芪甲苷加氨提取测定法,方法学考察结果良好。对玉屏风颗粒样品提取方法进行考察,分别以索氏回流、加热回流提取6 h,结果含量差异不大,考虑操作简便性,选择提取方法为加热回流;分别以加热回流提取1 h、1.5 h、2 h、2.5 h、6 h,结果分别为0.6239 mg·g-1、0.7603 mg·g-1、0.8242 mg·g-1、0.8071 mg·g-1、0.7995 mg·g-1,故选择提取时间为2 h;样品提取后直接浓缩,残渣较难溶解,样品溶液放置一段时间后有较多沉淀析出,通过正丁醇萃取后,浓缩残渣较易溶解,样品溶液澄清,无明显沉淀析出;比较水饱和正丁醇萃取对测定的影响,分别萃取4次、5次、6次,结果分别为0.6972 mg·g-1、0.6767 mg·g-1、0.8157 mg·g-1,故确定萃取次数为6次。本研究优化的玉屏风颗粒黄芪甲苷含量测定方法切实可行,比原方法操作简便快捷,可为提高相关质量标准提供参考。
本研究以玉屏风颗粒为例进行探讨,认为加氨提取法较氨洗法有优势,应用于成药制剂质量评价具一定可行性,但质量检测方法的方法变更将影响成药从源头、过程到成品的质量控制,建议完善、提高相关中成药的质量标准,使与原料药材测定方法一致。
参考文献
[1]国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2015:302.
[2]国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2020:315.
[3]刘蓬蓬,鞠成国,林桂梅,等.HPLC-CAD分析黄芪甲苷提取过程中黄芪皂苷类成分动态变化[J].中国中医药信息杂志,2022,29(11):92-96.
[4]范佳儿,刘银榕,晁志,等.当归补血丸指纹图谱及3种指标成分含量测定方法的建立[J].中国药房,2022,33(11):1343-1347,1354.
[5]梁曜华,李春,冯伟红,等.连续单因素法优化黄芪中黄芪甲苷的含量测定方法[J].中国中药杂志,2021,46(2):391-397.
[6]蒋湘,廖强,韦环.复方扶芳藤合剂中多种成分含量测定[J].中药材,2019,42(11):2611-2616.
[7]杨志城,张福明,孙彩虹,等.基于HPLC-DAD-ELSD及响应面设计优化黄芪浸润工艺研究[J].中草药,2020,51(24):6196-6204.
[8]黄诗莹,陈秋谷,王佛长,等.黄芪-丹参煎液HPLC指纹图谱及多指标定量测定研究[J].中草药,2019,50(20):4950-4956.
[9]董丹华,刘玉军,李亚男,等.HPLC法测定圣愈汤冻干粉中4个指标成分的含量[J].中国药房,2020,31(5):576-580.
[10]颜冬兰,叶惠煊,黄胜,等.HPLC-ELSD法同时测定补血生乳颗粒中8种成分[J].中草药,2019,50(20):4957-4961.
[11]江霞,陈秋谷,郭丽琴,等.健脾益肾丸指标成分的含量测定及其对CRF模型大鼠钙磷代谢和炎症因子的影响[J].中国药房,2019,30(16):2193-2199.
[12]任承涛,田莲超,李云,等.基于多成分测定的贞芪扶正颗粒质量控制[J].中国实验方剂学杂志,2019,25(9):150-158.
[13]陈伟韬,黄春瑶,刘璐.加减玉液颗粒的质量标准研究[J].今日药学,2020,30(7):482-484,488.
[14]卢向红,贺敏才,汪霞.扶正合剂质量标准提高研究[J].中国民族民间医药,2022,31(2):55-59.
[15]王法宇,吴迪,赵凤明,等.HPLC法测定消栓颗粒剂中黄芪甲苷的含量[J].中国民族民间医药,2021,30(1):31-33.
(收稿日期:2023-09-07 编辑:刘 斌)

