咸酥花生生产过程EDTA-2Na使用量的质量控制研究
林莉

摘要:新鲜带壳花生在生产加工工艺中使用EDTA-2Na作为络合剂,可有效防止因金属离子作用而导致产品变质。本实验通过电导率监测和返滴定试验,探究加工助剂EDTA-2Na残留量的控制方法,得出了黑土地和红土地分别在漂洗、蒸煮工序中络合反应完成时EDTA-2Na的使用量。为控制生产过程EDTA-2Na使用量,该方法可操作性强,便于指导实际生产。
关键词:EDTA-2Na;花生生产;质量控制
Research on Quality Control of EDTA-2Na Usage in the Production Process of Salted Peanuts
LIN Li
( Review Technology Centre of Longyan Industrial Products Production License, Longyan 364000, Fujian, China )
Abstract: In the production and processing of fresh shelled peanuts, EDTA-2Na serves as a complex agent to prevent product spoilage due to the action of metal ions effectively. In this experiment, the control method of residual amount of processing aid EDTA-2Na was explored through conductivity monitoring and back titration experiments, and the amount of EDTA-2Na used in rinsing or cooking processes of black soil and red soil respectively when the complex reaction was completed was obtained. The method is operable and convenient to guide the actual production environments..
Key Words: EDTA-2Na; Peanut production; Quality control
0引言
龙岩咸酥花生以其独特的香、脆、酥风味闻名遐迩,从明朝万历年间就有生产,已有400多年的历史,2008 年被列入国家地理标志产品保护名单,产品远销国内外市场[1]。带壳花生在加工过程中,外壳易受吸附于其表面的土壤中的金属离子作用而发黑,为防止其发黑,通常加入具有强配位能力的乙二胺四乙酸二钠(EDTA-2Na)。通过EDTA-2Na强配位能力的氨基和羧基,花生壳表面的金属离子络合为稳定的络合物,从而有效地防止产品品相因金属离子作用而变黑[2]。由于《食品安全国家标准 食品添加剂使用标准》(GB 2760-2014)中并未对“熟制坚果与籽类”食品类别/名称的EDTA-2Na的使用量或残留量进行规定[3]。大多数生产企业只是以测试成品中可食部分残留量是否检出,来推断生产过程EDTA-2Na的使用量。过量EDTA-2Na的摄入,会造成人体微量元素的流失,严重的还表现出腹泻、呕吐和血压下降等症状,还可能产生肾脏病变等疾病,因此,在相关国家标准未具体作出规定的情况下,生产者也应严格控制EDTA-2Na作为加工助剂的使用量。由于受种植地区、种植方式等差异影响,吸附于花生外壳表面土壤的金属离子量不同,生产过程可能出现EDTA-2Na使用量不足或者超标的问题。因此,开发EDTA-2Na生产过程监测方法,对咸酥花生的品质控制和成本降低具有重要的意义。
目前,食品中EDTA-2Na的检测方法主要有滴定法[4]、分光光度法、离子色谱法、薄层色谱法、液相色谱法、液相色谱质谱联用法[5]等,这些方法普遍存在前处理复杂[6]、检测时间漫长和使用设备昂贵等问题,在农产品加工等中小型企业中难以开展。随着食品工业的发展,传统咸酥花生不断向规模化、标准化方向发展。但在产业化发展进程中,食品工业用加工助剂的管理往往存在着重视不足或管理盲区等现象。作为监管人员,应当充分研究并开发相关应用技术,为制定和完善标准操作规范奠定基础,同时提高食品生产者使用加工助剂的风险防范意识。基于此,文中拟通过对黑土壤、红土壤带壳花生在漂洗、蒸煮等不同生产工序中,使用EDTA-2Na的用水进行电导率监测,通过电导率的突变,确定络合终点附近EDTA-2Na的使用量,并结合返滴定的方法,测试计算出络合终点EDTA-2Na的使用量,以期为实际生产中添加剂的减量使用提供可行的方法和依据。
1 材料与方法
1.1材料
选取荚果外观形态完整、无破损,网纹清晰的生花生果;
黑土地的生果:产自福建省龙岩市新罗区大池镇;
红土地的生果:产自广东省陆丰市南塘镇。
1.2 主要试剂与仪器
主要试剂:
乙二胺四乙酸二钠(EDTA-2Na,分析纯),甲基红(AR),乙醇(AR),西陇科学股份有限公司;锌标准溶液(0.05mol/L),深圳市博林达科技有限公司。
主要仪器:
SevenMulti S40数显电导率仪,梅特勒-托利多仪器(上海)有限公司;L-420离心机,湖南湘仪实验室仪器开发有限公司。
1.3 方法
1.3.1试剂制备
EDTA-2Na溶液的配置(1×10-3mol/L):精确称取18.6g(精确至0.0001g)EDTA-2Na加入到500mL的温水中溶解,过滤,冷却,转移至1000mL容量瓶中定容,摇匀后,取20mL定容至1000mL。
锌离子溶液的配置(1×10-6mol/L):取0.05mol/L锌滴定液2mL至100mL容量瓶中定容,摇匀后,取1mL定容至1000mL。
1.3.2 材料处理及测定
龙岩咸酥花生工艺流程:花生果→浸泡→清洗(去泥沙)→漂洗→蒸煮→一次烘烤→冷却→浸泡盐水→二次烘烤→筛选包装。
黑土地生果试验流程——漂洗阶段:称取一锅次120kg花生果清洗去泥后,移入盛200L清水漂洗池中搅拌,每3min加入配制的EDTA-2Na溶液4mL充分搅拌后记录EDTA-2Na溶液消耗量V1,取50mL清洗液加到离心管中,经离心5min后取上清液,重复测定电导率三次取平均值κ。
黑土地生果试验流程——蒸煮阶段:称取一锅次120kg花生果清洗去泥、漂洗后,移入盛200L清水蒸煮池中搅拌,每3min加入配制的EDTA-2Na溶液4mL充分搅拌后,EDTA-2Na溶液消耗量V2,取50mL清洗液加到离心管中,经离心 5min后取上清液,冷却至25℃,重复测定电导率三次取平均值κ。
红土地生果试验流程与黑土地生果试验流程一样,漂洗阶段消耗EDTA-2Na溶液记为V3,蒸煮阶段消耗EDTA-2Na溶液记为V4。
前期试验发现,随着EDTA-2Na不断加入,溶液的电导率与EDTA-2Na使用量先呈现一段曲线后再呈现出一段线性关系,这可能是由于溶液中的离子被络合后,使得溶液电导率主要受过量的EDTA-2Na影响[7]。
为准确计算出漂洗和蒸煮过程中EDTA-2Na准确使用量,当电导率K与VEDTA-2Na呈良好线性关系时,表明EDTA-2Na已过量,采用返滴定的方法,计算出过量的EDTA-2Na量:取其上清液50mL,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25mL、pH=10.0的氨-氯化铵缓冲液10mL与铬黑T指示剂少量,用1×10-6mol/L锌离子溶液滴定至溶液由紫色变为纯蓝色[8]427,1519。根据锌离子溶液CZn的消耗量VZn,分别得出黑、红土地在漂洗、蒸煮工序络合终点附近上清液EDTA-2Na使用量,V为一锅次EDTA-2Na溶液使用量。黑土地漂洗工序按下列公式计算V,其他工序以此类推:
(1)
为检验该方法在实际生产中的效果,咸酥花生终产品EDTA-2Na残留量按GB 5009.278-2016检测方法进行检验,对比不同生产工序中加入EDTA-2Na对终产品残留量的影响,进行质量安全风险分析。
1.4 数据统计与分析
实验结果运用Excel软件进行绘图并进行线性拟合。
2 结果与分析
2.1漂洗工序EDTA-2Na溶液用量与电
导率关系
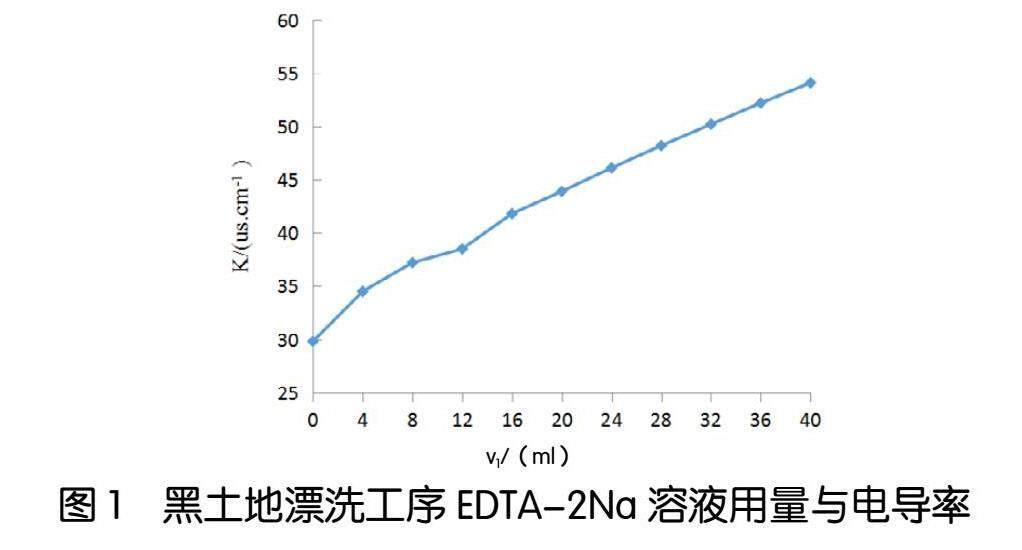
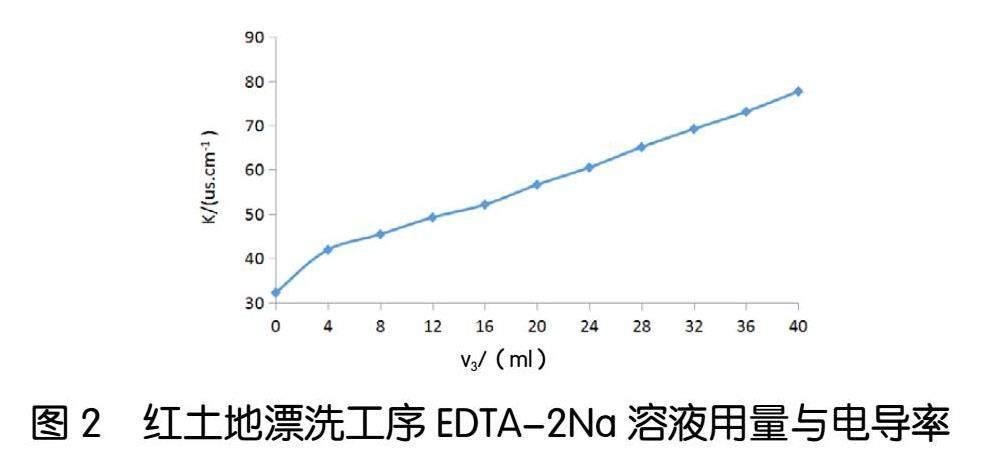
图1和图2分别为红、黑土地在漂洗阶段溶液EDTA-2Na用量与漂洗水电导率的关系图,从图中可以看出,对于红、黑土地,漂洗水的电导率与EDTA-2Na溶液用量先呈现曲线关系,之后再呈现出线性关系,黑土地在加入16~40mL范围内绘制标准曲线,回归方程为y=2.057x+39.84,相关系数R2为0.9994;红土地在加入20~40mL范围内,回归方程为y=1.052x+35.44,相关系数R2为0.9994,两种土质的线性关系均良好。试验结果表明,黑土地在加入EDTA-2Na16mL时,红土地在20mL时,漂洗水中的金属离子被络合完成。
2.2蒸煮工序EDTA-2Na溶液用量与电导率
与漂洗阶段类似,在蒸煮工序中,随着EDTA-2Na不断加入,黑土地在加入12~40mL范围内绘制标准曲线,回归方程为y=15.16x+906.8,相关系数R2为0.9970;红土地在加入16~40mL范围内,回归方程为y=14.90x+992.1,相关系数R2为0.9961。对于红、黑土地,蒸煮用水的电导率与EDTA-2Na溶液用量先呈现曲线关系,之后再呈现出线性关系。试验结果表明,黑土地在加入EDTA-2Na12mL时,红土地在16mL时络合完成。
2.3 返滴定
络合终点附近确定后,通过返滴定,计算得出:黑土地漂洗工序络合需消耗EDTA-2Na 9.4mL,蒸煮工序需消耗9.0mL;红土地漂洗工序络合需消耗EDTA-2Na 9.68mL,蒸煮工序需消耗9.20mL。
2.4 终产品EDTA-2Na残留量
为验证本论文方法的可行性,根据上述花生漂洗和蒸煮阶段试验计算的EDTA-2Na需要添加的量,取试验烘烤后的花生,检测其EDTA-2Na含量,结果如表1所示。
2.5 分析
花生受生长环境土壤的影响,重金属含量不同。而土壤中重金属含量的多少,除了受地区差异影响外,矿产资源、农药化肥、工业污染等也是重要影响因素[9]。由于高温多雨和风化作用影响,铁、铝等不活泼元素随水流渗透并沉淀于土壤中,红的色彩占优势,形成红色土壤。若土壤中有机质的腐殖化在土壤中积累,根据含量不同,形成褐色或黑色土壤。
试验通过确定花生清洗工序的水与花生果的比例、清洗时间和搅拌频率,以及清洗后花生果感官的清洁程度,以排除清洁程度对电导率的直接影响。图1、2、3、4结果均显示络合完成后,电导率对EDTA-2Na加入量呈线性关系。终产品残留量如表1所示,在络合完成时,残留量均为未检出;而随着EDTA-2Na持续加入,当超出一定量时,结果显示检出。因此可知,试验使用方法是可行而有效的。
对比漂洗、蒸煮工序加入EDTA-2Na电导率变化情况,蒸煮工序用水的电导率更高。由于电导率容易受温度的影响,随着温度的升高或降低,电导率会发生相应的变化。温度升高时,离子间的水化作用减弱,黏度降低,运动阻力减小,此时在电场的作用下,离子的定向运动加快,从而生产工序用水的电导率增大[10]。因此,试验中蒸煮工序用水的电导率,需经水浴冷却后再测量,排除了溶液温度的影响。但影响电导率的因素复杂。电解质增多,或溶液中离子活动能力增强,有利于溶液中离子配合物生成,使得络合反应加快或更充分。如图3、图4所示,结果表明,蒸煮工序电导率高,更快达到络合终点,并且在络合反应终点附近时,电导率形成突跃,且终产品中未检出残留。
3 结论
本实验重点研究在不同工序(漂洗、蒸煮)、不同土壤(黑土地、红土地)中加入EDTA-2Na,通过电导率监测发现,在蒸煮工序中络合终点附近电导率形成突跃,络合完成后成明显线性关系,再以返滴定测定过量的EDTA-2Na,即可求得络合完成时EDTA-2Na的用量。本方法简单,可操作性强,有利于指导实际生产,有效控制EDTA-2Na残留量。
参考文献
[1]乌吉木.高效液相色谱法测定番茄酱中乙二胺四乙
酸二钠[J].现代食品,2021,(24):208-212.
[2]孔红星,陈绮莹,蒙海森,等.表面增强拉曼散射
技术在快速检测预包装干米粉中乙二胺四乙酸二钠
的应用[J].食品科学,2023,44(18): 331-338.
[3]中华人民共和国国家卫生和计划生育委员会.食品
安全国家标准 食品添加剂使用标准:GB 2760-2014[S].
北京:中国标准出版社,2014.
[4]陈浩然.用氧化锌代替氯化锌测定乙二胺四乙酸和
乙二胺四乙酸二钠的含量[J].科技信息(科学教研),
2007,(12):260+390.
[5]中华人民共和国国家卫生和计划生育委员会、国家
食品药品监督管理总局.食品安全国家标准食品中
乙二胺四乙酸盐的测定:GB 5009.278-2016[S].北京:
中国标准出版社,2016.
[6]王磊,唐娟,于春娣,等.花生中重金属含量的影响
因素及其来源[J].中国食品学报,2022,22(1):8.
[7]董文峰,黄征青.电导率法测定EDTA二钠盐水溶液
的浓度[J].广州化工,2017,45(6):3.
[8]国家药典委员会.中国药典[M].北京:中国医药科
技出版社,2015:427,1519.
[9]史文娇,汪景宽, 边振兴,等.黑龙江北部土壤中
主要重金属和微量元素状况及其评价[J].土壤通报,
2005,36(6):4.
[10]姜丽,程兆辉.除盐水箱水质下降原因分析及解决
措施[J].电力建设,2008,29(9):97-100.

