DNA-有机分子杂化体的合成及应用研究


摘 要:随着DNA化学修饰技术的发展,疏水分子和DNA通过固相反应合成了两亲性DNA有机杂化物,两亲性有机杂化物可以被视为新的构建块,然后在溶液中自发组装成各种纳米结构,组装体在药物输送、靶向递送及生物传感等领域有着重要的应用。论述了DNA-有机分子杂化体的组装、合成方法以及在生物医药方面的研究进展。
关 键 词:DNA;有机分子;合成;组装体;应用
中图分类号:O641.3 文献标识码: A 文章编号: 1004-0935(2024)05-0768-04
随着脱氧核糖核酸(DNA)纳米技术的发展,人们已经构建了各种各样的DNA纳米结构和DNA器件,它们在材料科学和生物医学方面具有潜在的应用前景。利用DNA的可编程性和生物相容性,利用疏水有机分子对DNA进行化学功能化的新型构件越来越受到人们的关注。在两亲性的驱动下,DNA-有机分子两亲性被证明具有自组装或进一步诱导的层次组装,提供了新的特异性。
疏水小分子,由于其分子尺寸很小、共价修饰DNA后,由于两亲性不足以支持进一步组装,因此小分子共价DNA的组装发展比较迟缓[1][1]。近些年来,科研工作者们通过官能团衍生适当增加疏水分子的拓扑结构或通过拓展芳香环增强π-π堆积作用等方法提升疏水比例[2][2],实现了DNA-有机小分子在水溶液中组装出多种形貌、功能优异的纳米结构。胆固醇结合的DNA链(胆固醇-DNA)通常用作检测和动态运动过程中的锚[3-4][3,4]。据报道,具有可变修饰的胆固醇-DNA可以形成胶束结构。ZHANG[5]等指出人[5]具有特定序列的胆固醇DNA也可以在酸性条件下形成球形胶束和纳米棒。
核酸-聚合物两亲体(NAPAs)是一类生物偶联物,由共价连接到疏水聚合物上的核酸链组成。这些大分子在水溶液中进行自组装,产生形态和功能上有趣的纳米结构,具有高密度核酸冠和聚合物核。2015年,刘冬生课题组报道了带有亲水刚性段、两端带有疏水性软段的DNA三嵌段共聚物PPO- dsDNA-PPO,并研究了它们的自组装行为[6]。[6]制备的组件可以作为智能药物递送的绝佳平台,因为其具有高效的DNA、RNA和疏水性小分子药物装载能力。
一类具有独特结构、分散单一的树状大分子与DNA结合,将得到一类新的超分子构筑单元DNA-树状分子嵌段共聚物,其组装体在生物传感器[7]、药物递送[8]和其他相关领域具有潜在的应用。2023年,赵智勇课题组[9]设计并合成了G-quadruplex与树状大分子杂交(G20-Den)和单链DNA与树状大分子杂交(D20-Den)作为对照。G20-Den杂交可以形成紧凑的G-四倍体结构,这意味着二级结构不受有机分子的影响。由于强π-π堆叠和疏水相互作用,G20-Den和D20-Den在MES缓冲液中都自组装成长度为几微米的纳米纤维。G20-Den纳米纤维通过简单的超滤具有可回收性的优点,并且在3次循环后仍能保持其催化性能。这项研究为制备具有高催化效率的多酶提供了一种新的策略[10],也为 DNA催化剂用于绿色化学目的的再利用提供了潜在的应用。
1 DNA-有机分子杂化体的合成
合成DNA-有机分子杂化体常用的方法有液相合成和固相合成,溶液偶联适合用于亲水分子的偶联,对于一些疏水分子的偶联,反应溶剂一般为混合溶剂,但由于溶剂不相溶而导致合成效率并不高。固相合成是在有机溶剂中固体载体上表现出的反应。此外,还有最近开发的方法,包括聚合酶链式反应(PCR)[11]、后聚合[12]、有机相反应[13][13]。
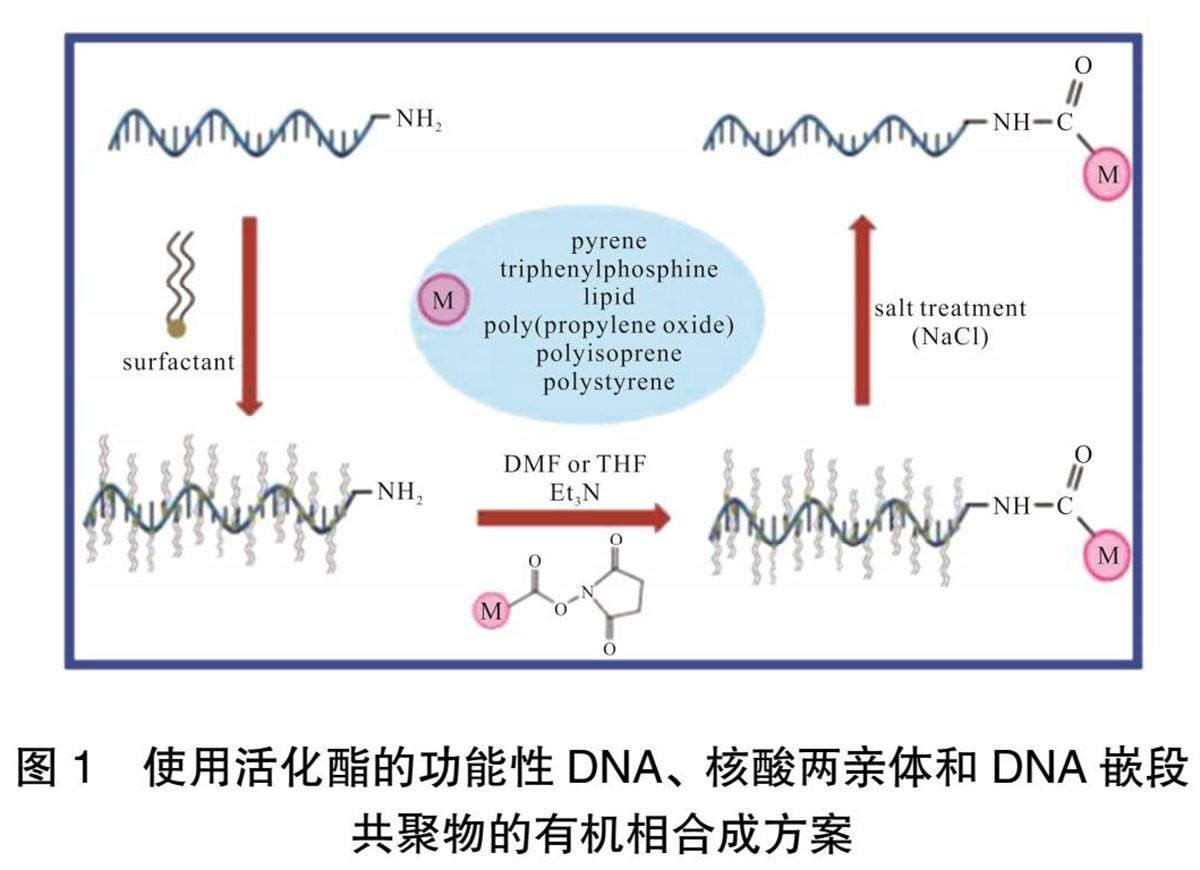
水性环境中的溶液相DNA修饰已被证明是在不同DNA位置上偶联亲水分子的高度通用和有效的方法。然而,含有疏水功能部分的两亲性DNA杂化材料的合成效率较低,这是因为很难找到既能容纳极端亲脂分子又能容纳亲水DNA链的溶 剂[14]。2014年刘凯等指出了一种通过引入疏水性DNA表面活性剂复合物作为反应性支架的核酸修饰和聚合的有机相偶联策略[15],高效生产了一系列显著的两亲DNA结构(DNA-芘[16]、DNA-三苯基膦、DNA-烃[17]和DNA嵌段共聚物)和一系列具有高DNA接枝密度的新型刷型DNA侧链均聚物,如图1所示。
固相功能化主要基于相同的磷酰胺化学[18],疏水基团可以容易地与2-氰基乙基-N,N-二异丙基磷酰胺基团偶联,然后将其修饰为固体载体CPG上的DNA。由于固相法中不同有机溶剂的相容性,它被认为是疏水功能化的通用方法。还应注意,pling反应对水和氧敏感,所以需要在无水和无氧条件下进行[19]。此外通过固相合成对DNA的化学修饰不限于磷酰胺化学。由氨基封端的DNA和羧基修饰的疏水分子形成酰胺,叠氮封端DNA和炔官能化的疏水分子之间的Huisgen环加成(铜催化的炔叠氮环加成),Sonogashira偶联和3′端DNA与亚磷酸酯酰胺化学的功能化也可以用疏水分子在末端功能化DNA,这也拓宽了固相合成的应用。
DNA-有机分子的合成的其他方法还包括基于PCR的修饰、后聚合、胶束模板化等方法[20]。
2 DNA-有机分子杂化体的应用研究
在过去的几十年中,许多DNA-有机分子两亲分子[6,21]通过偶联不同的疏水分子(包括合成聚合物、树枝状物和小有机分子)而被设计和合成。当这些组分分子具有内在功能,如氧化还原、光物理和生物特性时,它们将为最终组装提供合理设计的功能。虽然两亲性组装的驱动力疏水相互作用是非定向的,但DNA和疏水分子的结合将为两亲性组装过程带来更多的可寻址性和可编程性。组装体外围高密度的DNA序列,可有效增加组装体的靶向效果和功能负载,内核的疏水区可以负载药物分子或功能分子。
ALP是一种水解酶,可以从核酸或蛋白质中去除磷酸基团[22-23]。值得注意的是,ALP已被广泛用于将亲水性磷酸化小分子转化为疏水性去磷酸化产物,用于分子成像、疾病诊断和癌症治疗。邹建梅等合成了磷酸化脂质共轭寡核苷酸(DNA-lipid-P),以开发基于去磷酸化诱导的疏水性增加的DNA两亲分子的酶响应自组装[24],如图2所示。
用于酶触发药物递送的DNA纳米胶囊如图3所示[25]。纳米胶囊由有机核和DNA壳组成,可通过DNA连接酶与治疗信使RNA(mRNA)裂解DNA酶进一步偶联。DNA纳米胶囊可以在核心中包含小药物分子,并设计为响应酯酶降解,已知酯酶在内体中高浓度存在。内体逃逸是纳米级药物递送系统中的一个重要问题。在这种方法中,酯酶引发的纳米胶囊降解可以改善内体逃逸,从而提高药物效率。
最近,Schnichels和Herrmann研究了负载溴莫尼丁的DNA脂质胶束,以改善青光眼治疗[26]。这些DNA胶束有利于药物的保留释放,并在体外和体内表现出优异的生物相容性。2019年,LIU等开发了通过主客体相互作用的DNAPDI组装体的可逆形态调节[27]。由于PDI单元的强π-π相互作用,DNA-PDI首先组装成球形胶束。葫芦素尿苷的加入导致了从球体到2D DNA纳米的形态学转变,并在675 nm处明显增强了荧光。
2021年,SIONED 等结合实验和原子分子动力学(MD)模拟研究了疏水标记DNA与合成膜和细胞膜的相互作用[28]。DNA双链体通过与末端胆固醇锚结合或通过电荷中和的硫代磷酸烷基酯(PPT)带的化学合成而变得疏水。他们的MD模拟直接揭示了脂质膜内PPT-DNA的复杂结构和能量学,表明较长的烷基PPT链提供了最稳定的膜锚定,但可能破坏溶液中的DNA碱基配对。当在细胞上测试时,胆固醇DNA均匀分布在细胞表面,而烷基PPT-DNA在质膜上聚集成簇状结构。当他们将研究扩展到活HeLa细胞时,证明了合成膜和生物膜中DNA相互作用的差异。与简化的巨大单层囊泡和模拟双层相比,这突出了细胞膜的复杂性。因此,在合成和生物脂质环境中进行实验对于理解DNA纳米结构与膜的相互作用至关重要。
利用有机分子拓扑结构的合理设计,基于DNA嵌段共聚物、DNA-树状分子杂化体、DNA-脂质的两亲分子的自组装,也进行了讨论。此外,基于DNA纳米结构的两亲性组装的最新进展也因其独特的性质和新颖的组装行为而备受关注。已经证明,这些DNA有机两亲体聚集体不仅充当生物医学和材料科学中装载药物种类或功能分子的载体,而且可以模拟生物系统[29],以帮助理解生命系统[30-31]。随着两亲DNA杂交体的快速发展,有望将其引入更复杂的DNA支架中,以开发生物激发系统和生物医学智能纳米系统。此外,通过使用刺激疏水分子,它有可能扩展到动态DNA纳米结构[32]。结合反应性实体,也可以制备刺激反应性生物材料,这在生物医学领域(包括药物递送和治疗)中显示出巨大的潜在应用。
3 结束语
总结了DNA两亲分子的最新进展,包括它们的合成、自组装和应用。合成方法主要有固相合成法和液相合成法,但由于液相合成效率较低,因此固相合成是合成DNA-有机分子杂化体常用的合成方法。DNA-有机分子形成的组装体外围高密度的DNA序列,可有效增加组装体的靶向效果和功能负载,内核的疏水区可以负载药物分子或功能分子。可以预期,该领域将为自组装带来更多的基础研究,并在各个领域中得到更多的应用。
参考文献:
[1] TRINH T, SALIBA D, LIAO C, et al. “Printing” DNA strand patterns on small molecules with control of valency, directionality, and sequence[J]. Angew. Chem. Int. Ed., 2019, 58(10): 3042-3047.
[2] WANG X, SUN H, LIU J, et al. Ruthenium-promoted C–H activation reactions between DNA-conjugated acrylamide and aromatic acids[J]. Org. Lett., 2018, 20(16): 4764-4768.
[3] STENGEL G, SIMONSSON R A, CAMPBELL F, et al. Determinants for membrane fusion induced by cholesterol-modified DNA zippers[J]. J. Phys. Chem. B, 2008, 112(28): 8264-8274.
[4] KOCABEY S, KEMPTER S, LIST J, et al. Membrane-assisted growth of DNA origami nanostructure arrays[J]. ACS Nano, 2015, 9(4): 3530–3539.
[5] ZHANG Y, PENG R A, XU F, et al. Hierarchical self-assembly of cholesterol-DNA nanorods[J]. Bioconjugate Chem., 2019, 30(7): 1845–1849.
[6] WU F, SONG Y, ZHAO Z, et al. Preparation and self-assembly of supramolecular coil-rod-coil triblock copolymer PPO-dsDNA-PPO[J]. Macromolecules, 2015, 48(20): 7550-7556.
[7] ZHOU M, DONG S. Bioelectrochemical interface engineering: toward the fabrication of electrochemical biosensors, biofuel cells, and self-powered logic biosensors[J]. Acc. Chem. Res., 2011, 44(11): 1232-1243.
[8] TYRRELL Z L, SHEN Y, RADOSZ M. Fabrication of micellar nanoparticles for drug delivery through the self-assembly of block copolymers[J]. Prog. Polym. Sci., 2010, 35(9): 1128-1143.
[9] DENG C, YANG H, LIU S, et al. Self-assembly of dendrimer-DNA amphiphiles and their catalysis as G-quadruplex/hemin DNAzymes[J]. Polymer, 2023, 266: 125621.
[10] MALEKI H, KHOSHNEVISAN K, BAHARIFAR H. Random and positional immobilization of multi-enzyme systems[J].Methods in molecular biology, 2022,2487:133-150.
[11] FUJITA T, NAGATA S, FUJII H. Oligoribonucleotide-mediated blockade of DNA extension by Taq DNA polymerases increases specificity and sensitivity for detecting single-nucleotide differences[J]. Anal. Chem., 2023, 95(6): 3442-3451.
[12] KOPIASZ R J, KOZON D, PACHLA J, et al. Controlled post-polymerization modification through modulation of repeating unit reactivity: proof of concept discussed using linear polyethylenimine example[J]. Polymer, 2021, 217: 123452.
[13] ZHAO Z, DONG Y, DUAN Z, et al. DNA-organic molecular amphiphiles: synthesis, self-assembly, and hierarchical aggregates[J]. Aggregate, 2021, 2(4): e95.
[14] K?LMEL D K, RATNAYAKE A S, FLANAGAN M E. Photoredox cross-electrophile coupling in DNA-encoded chemistry[J]. Biochem. Biophys. Res. Commun., 2020, 533(2): 201-208.
[15] LIU K, ZHENG Q, LIU L, et al. Nucleic acid chemistry in the organic phase: from functionalized oligonucleotides to DNA side chain polymers[J]. J. Am. Chem. Soc., 2014, 136(40): 14255-14262.
[16] KASHIDA H, ITO Y, KAKUTA T, et al. Orientational control of circularly polarized luminescence from pyrene clusters by using a DNA scaffold[J]. Chemistry-A European Journal, 2023: e202300182.
[17] DU H, WANG P, WU J, et al. The roles of polymerases ν and θ in replicative bypass of O6- and N2-alkyl-2′-deoxyguanosine lesions in human cells[J]. J. Biol. Chem., 2020, 295(14): 4556-4562.
[18] WANG T, PFISTERER A, KUAN S L, et al. Cross-conjugation of DNA, proteins and peptides via a pH switch[J]. Chem. Sci., 2013, 4(4): 1889-1894.
[19] GRAJKOWSKI A, CAWRSE B M, TAKAHASHI M, et al. An improved process for the release of synthetic DNA sequences from a solid-phase capture support[J]. Tetrahedron Lett., 2022, 106: 154077.
[20] CHOWDHURY P, KIM S, LEE E S, et al. DNA micelle-templated copper nanoclusters for fluorescent imaging of MUC1-positive cancer cells[J]. Microchimica Acta, 2022, 189(11): 404.
[21] SCHNITZLER T, HERRMANN A. DNA block copolymers: functional materials for nanoscience and biomedicine[J]. Acc. Chem. Res., 2012, 45(9): 1419-1430.
[22] ALONSO A, SASIN J, BOTTINI N, et al. Protein tyrosine phosphatases in the human genome[J]. Cell, 2004, 117(6): 699-711.
[23] SHI Y. Serine/threonine phosphatases: mechanism through structure[J]. Cell, 2009, 139(3): 468-484.
[24] ZOU J, GAO Q, NIE J, et al. Enzymatic dephosphorylation-triggered self-assembly of DNA amphiphiles[J]. RSC Advances, 2021, 11(30): 18322-18325.
[25] AWINO J K, GUDIPATI S, HARTMANN A K, et al. Nucleic acid nanocapsules for enzyme-triggered drug release[J]. J. Am. Chem. Soc., 2017, 139(18): 6278-6281.
[26] SCHNICHELS S, HURST J, DE VRIES J W, et al. Improved treatment options for glaucoma with brimonidine-loaded lipid DNA nanoparticles[J]. ACS Appl. Mater. Interfaces, 2021, 13(8): 9445-9456.
[27] DU T, YUAN W, ZHAO Z, et al. Reversible morphological tuning of DNA-perylenebisdiimide assemblies through host-guest interaction[J]. Chem. Commun., 2019, 55(25): 3658-3661.
[28] JONES S F, JOSHI H, TERRY S J, et al. Hydrophobic interactions between DNA duplexes and synthetic and biological membranes[J]. J. Am. Chem. Soc., 2021, 143(22): 8305-8313.
[29] JI X, LI Q, SONG H, et al. Protein-mimicking nanoparticles in biosystems[J]. Adv. Mater., 2022, 34(37): 2201562.
[30] WU N, ZHAO Y. DNA Nanostructures as drug carriers for cellular delivery[J]. Chemical Research in Chinese Universities, 2020, 36(2): 177-184.
[31] DONG J, ZHOU C, WANG Q. Towards active self-assembly through DNA nanotechnology[J]. Top. Curr. Chem., 2020, 378(2): 33.
[32] YU L, MA Z, HE Q. Dynamic DNA nanostructures for cell manipulation[J]. ACS Biomaterials Science & Engineering, 2023, 9(2): 562-576.
Synthesis and Application of DNA-Organic hybrid
ZHAO Xiaohuan
(College of Chemistry and Material Engineering, Wenzhou University, Wenzhou Zhejiang 325035, China)
Abstract: With the development of DNA chemical modification technology, amphiphilic DNA organic compounds are synthesized by solid phase reaction between hydrophobic molecules and DNA. Amphiphilic organic compounds can be regarded as new building blocks and then spontaneously assembled into various nanostructures in solution. The assemblers have important applications in drug delivery, targeted delivery and biosensing. In this paper, the assembly and synthesis of DNA- organic molecules were discussed, as well as the research progress in biomedicine.
Key words: DNA; Organic molecules; Synthesis; Assembly; Application
收稿日期: 2023-03-18
作者简介: 赵晓换(1997-),女,河南省鹤壁市人,硕士,研究方向:超分子化学。

