氢化物发生-原子荧光光谱法(HG-AFS)测达里诺尔湖流域底泥样硒
薛舒文 苏丹 张嘉璇 张营 徐苏男

基金项目:国家自然科学基金项目面上项目(52170163);沈阳市中青年科技创新人才支持计划(RC220064);沈阳市科技计划项目(22-322-3-14)
第一作者简介:薛舒文(1999-),女,硕士研究生。研究方向为生态学。
*通信作者:苏丹(1980-),女,博士,教授,硕士研究生导师。研究方向为污染生态与环境工程。
DOI:10.19981/j.CN23-1581/G3.2024.15.018
摘 要:氢化物发生-原子荧光光谱法(HG-AFS)是测定硒(Selenium, Se)的理想方法,能精确测定水样和含水地球化学样品(底泥)中Se的含量。由于达里湖底泥中Se含量相对较低,有机质的还原状态较高,在测量Se含量时往往因为过于复杂且低于仪器检出限而不能被检测到有效值。该文应用HG-AFS测定达里诺尔湖底泥中Se的含量,使用微波消解石墨赶酸作为前处理方法,并使用HG-AFS进行Se含量的测试,采用此法测定底泥中Se元素具有快速、准确、重现性好,被确定为一种快速可靠的对底泥样品Se含量进行测定的方法。
关键词:硒;湖泊底泥;氢化物发生-原子荧光光谱法;微波消解;测定
中图分类号:X592 文献标志码:A 文章编号:2095-2945(2024)15-0083-04
Abstract: Hydride generation-atomic fluorescence spectrometry (HG-AFS) is an ideal method for the determination of selenium (Se). It can accurately determine the content of Se in water samples and water-bearing geochemical samples(sediment). Because the selenium content in the sediment of Dali Lake is relatively low and the reduction state of organic matter is high, the effective value can not be detected because the Se content is too tedious and lower than the detection limit of the instrument. In this paper, HG-AFS was used to determine the content of Se in the sediment of Dalinor Lake, microwave digestion of graphite acid was used as the pretreatment method, and HG-AFS was used to test the content of Se. The determination of Se in sediment by this method is rapid, accurate and reproducible, and has been determined as a rapid and reliable method for the determination of Se in sediment samples.
Keywords: selenium; lake sediment; hydride generation-atomic fluorescence spectrometry; microwave digestion; determination
硒(Selenium)是第34號非金属元素,对生物的作用有利、害双重性[1],其循环呈现出高度的时空不均匀性[2],故而对环境中Se的检测是至关重要的。氢化物发生-原子荧光光谱法(HG-AFS)是一种灵敏度高、气相干扰少的测量微量元素的方法[3-4],也是国标中的第一个方法。但由于湖泊底泥的Se含量较少,有机质含量较多,测定总Se时往往因为方法过于复杂、低于仪器检出限等问题,不能被检测到有效值。
达里诺尔湖(E116°26′~116°45′,N43°13′~43°23′)是典型高原内陆碱水湖,湖水的pH接近9[5],流域内主要的支流是贡格尔河。达里湖流域的入湖水量小于蒸发量,且近年来受到气候干旱的影响,湖泊的面积日益减小而盐度不断增加[6]。达里湖的水化学组成碳酸盐所占组分最大[7],这在高原半咸水湖泊中较为少见,沉积物受到水化学、地质构造、气候变化多重因素影响,可能表现出与典型咸水湖不同的沉积特征。因此,对达里湖这一特殊地区的底泥进行特异的测定Se条件确定,是有着实践价值的。
本文通过采用氢化物发生-原子荧光光谱法(HG-AFS)对达里湖底泥中Se的测定进行了探究,得到了一种方便可行的,适合于湖泊底泥的Se含量测定方法。
1 材料与方法
1.1 采样点
根据达里诺尔湖及贡格尔河的水化学性质选择采样点,于2023年4月末河水完全解冻后,使用抓泥斗采集表层沉积物,样品放入密封袋中4 ℃保存,在实验室条件下冷冻干燥。
1.2 方法原理
样品参考NY/T 1104—2006《土壤中全硒的测定》[8]及DZ/T 0279.14—2016《区域地球化学样品分析方法 第14部分:硒量测定 氢化物发生-原子荧光光谱法》[9]并进行改良,采用微波消解的前处理方式,将Se的形态全部转变为四价Se,并使用原子荧光进行测定。在酸溶液中,以硼氢化钠(NaBH4)作为还原剂产生H2,可在氢化物发生系统中与载流运载的四价Se反应生成气态H2Se。上述2种气体和氩气一起通入,以氧气(O2)为助燃气体,由炉丝点燃,形成氩氢(Ar-H)火焰,将氢化Se还原为原子Se,原子器中的Se原子被激发,被激发的Se原子回到较低的能量状态,并发出特征波长的光(即原子荧光)。原子荧光的强度与被测元素的含量应呈线性关系,由测定荧光强度通过标准曲线公式以得出Se元素在待测样品中的含量[10]。
1.3 仪器及试剂
1.3.1 仪器
MD8H微波消解仪,奥普乐仪器有限公司;GD25石墨赶酸仪,奥普乐仪器有限公司;AFS-9800双道原子荧光光度计,北京科创海光仪器有限公司;Se高性能空心阴极灯,北京龙天韬略科技有限公司;超纯水机,美国Millipore公司。
1.3.2 试剂
HNO3(p=1.42 g/mL),优级纯(沈阳市新化试剂厂);HF,优级纯大于等于40%(国药集团化学试剂有限公司);HCl(p=1.18 g/mL),优级纯(国药集团化学试剂有限公司);NaOH,优级纯;NaBH4,分析纯大于等于96.0%(国药集团化学试剂有限公司);Se标准液,1 000 mg/L(国药集团化学试剂有限公司);试验所用水均为超纯水(电阻大于等于18.2 MΩ·cm);载气为氩气(纯度99.99%)。
1.3.3 载流
5%HCl溶液(体积分数),量取25 mL HCl缓慢加入500 mL水中,搅拌均匀。
还原剂(临用时配制):10g/L NaBH4溶液,称取2.5g NaOH用一定量去离子水溶解防止后续试剂大量水解,再准确称10.0g NaBH4,搅拌均匀。
1.3.4 Se标准使用液(0.10 mg/L)
准确移取10.0 mL Se标准储备液(Se标准溶液1 000 ?滋g/mL)到100 mL的容量瓶中,用5%HCl溶液稀释至刻度。
1.4 Se标准曲线系列的配制
使用相应量程的移液管准确吸取0,2.0,4.0,6.0, 8.0和10.0 mL Se标准使用液(见1.3.4章节)置于100 mL容量瓶中,5%HCl溶液(见1.3.3章节)用来进行定容,定容方法为重量法。得到的标准系列浓度为0,2.0,4.0, 6.0,8.0和10.0 ?滋g/L。
1.5 样品的预处理
底泥样品冷冻干燥,挑出动植物残体、大石块等杂质,晾干磨碎,分别过50和80目的筛。取一定量的样品放入聚四氟乙烯消化管,加入一定比例的混酸,静置一夜进行预消化。
消解后冷却至室温,用石墨赶酸仪在120 ℃下赶酸50 min,赶酸过程中观察聚四氟乙烯管口红棕色烟的冒出情况,在赶酸进行至10~20 min,且红棕色气体不再冒出时加入5 mL(1∶1)HCl进行赶酸。赶酸完成后冷却至室温,对所剩液体定容采用重量法定容,具体步骤是使用分析天平称取余液体质量,并用去离子水准确定容至25.0 g。定容后的液体在4 ℃環境下保存待测。
1.6 仪器工作参数
消解仪的工作参数设置分为2个工步,工步1为升温时间5 min,恒温时间5 min,温度100 ℃,功率6 W;工步2在工步1基础上,升温时间5 min,恒温时间5 min,温度120或130 ℃,功率6 W。
赶酸仪工作条件为120 ℃下恒温赶酸50 min。
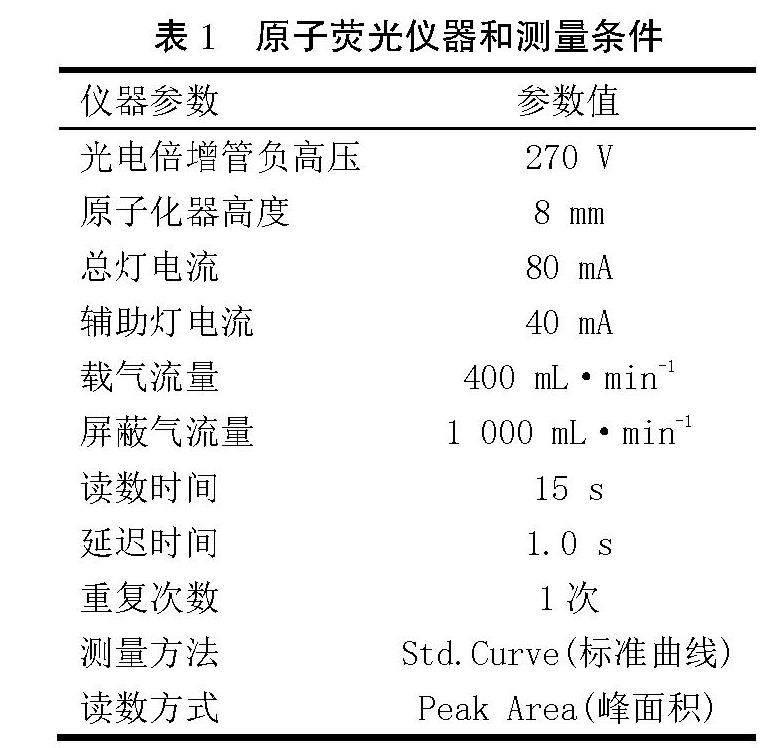
原子荧光AFS-9800的设置见表1。
表1 原子荧光仪器和测量条件
1.7 测定程序
根据测量仪的条件,使用5%的HCl溶液作为载流,打开气路和电路,按照表2中的参数设置,并将炉丝预热至少30 min,随后用载流进行测试。如果连续2次测量之间的荧光差小于5,则表示仪器稳定,可以继续测量。测量标准空白值后,测量标准曲线并检查线性相关系数是否大于0.999 0。最后,根据之前测量程序的设置,测量样品空白值和各个样品的浓度。
2 结果
2.1 标准曲线、检出限和精密度
将标准溶液及其对应的荧光值绘制标准曲线(图1),在0~10 μg/L范围内线性回归方程为If=60.8×C-33.8(R2=0.999 5)。
图1 Se标准曲线
对同一Se标准溶液连续测定10次,RSD为1.48%,对空白溶液连续测定10 次得到方法检出限为0.01 μg/L,检出限范围为0.01~20 μg/L。
2.2 前处理条件的选择
2.2.1 消解酸体系的选择
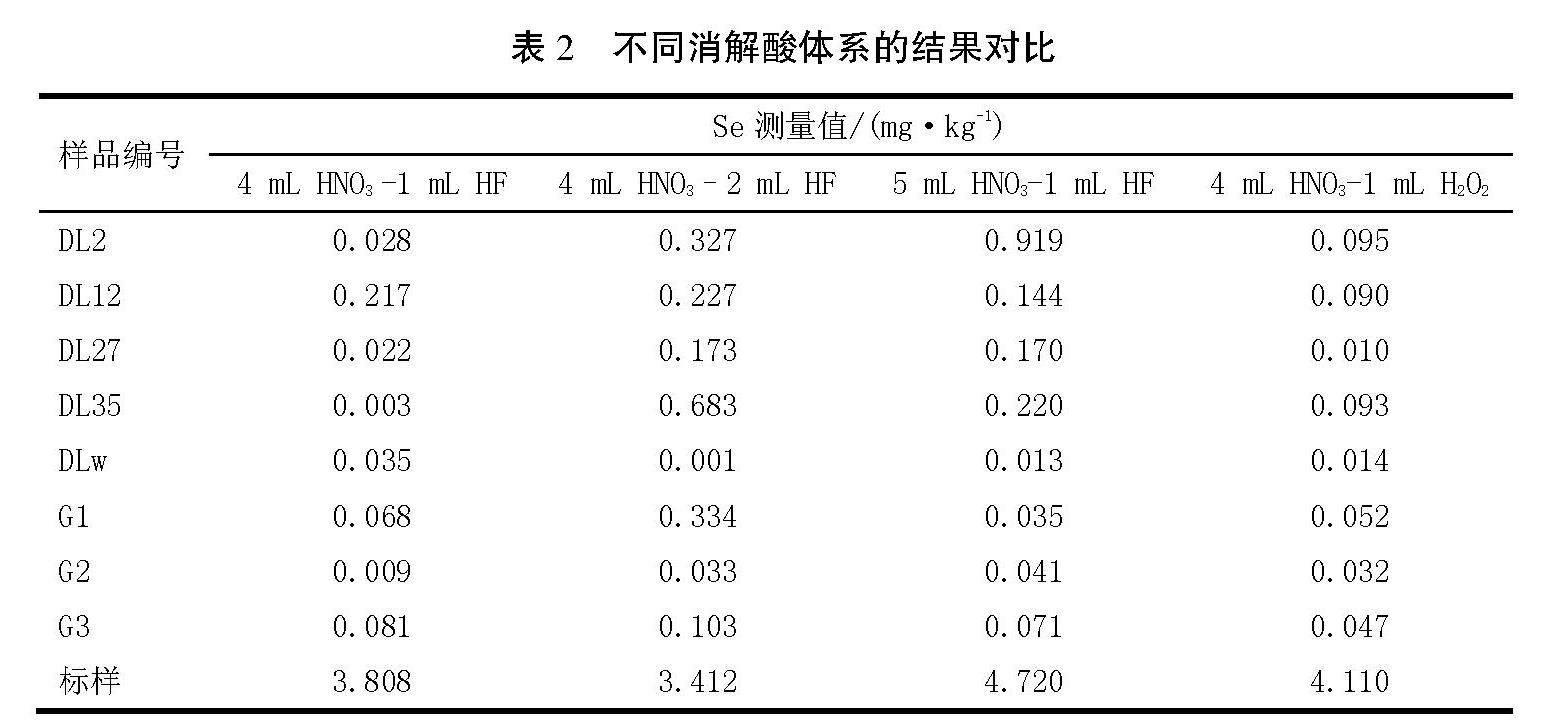
微波消解体系通常以硝酸HNO3为主的强酸进行消解。消解分别采用HNO3-H2O2、HNO3-HF两种方式进行消解,HNO3的使用量为4~5 mL,其余试剂使用量为1~2 mL,结果见表2,HNO3-H2O2消解的底泥仍有浑浊和褐色固体颗粒,并未消解完全,而HNO3-HF消解液均澄清,添加1 mL HF对比添加2 mL HF的测量结果更准确,因此采用添加5 mL HNO3和1 mL HF作为最终微波消解的条件。
2.2.2 定容HCl浓度的选择
消解完成后采用HCl定容,其作用为保持体系中的Se为四价Se,HCl的酸度在一定程度上会影响荧光强度和空白值。在保证优级纯HCl不被污染的条件下,应尽可能保持样液体的酸度和载流相一致。
本实验采用1 mL和2 mL浓HCl定容,定容后样液的酸度分别为5%和20%,以此对比HCl浓度对测定结果的影响,结果见表3。结果表明,5%HCl体系的样品数值重现率最好,用酸量少,故采用加入2 mL HCl的方式进行赶酸。
表3 不同HCl酸度结果对比
2.2.3 消解温度、时间的选择
微波消解的优势在于消解属于密闭的环境,样品中的Se不易蒸发流失,不足之处在于温度、时间均对消解是否完全产生影响。对底泥消解温度和时间的选择见表4,结果表明,在温度120 ℃,恒温5 min的条件下较为稳定,消解液完全澄清,测定数值准确可信。
表4 不同温度和时间条件结果对比
2.2.4 测定分析
使用选定方法测定达里湖底泥,所得结果见表5。标准样品的平均加标回收率为103%,在95%~110%之间,说明了数据的可信性和准确性。
表5 底泥样品中Se元素含量
3 讨论
3.1 消解优化条件筛选
Se的元素性质较为稳定,操作过程中不易受仪器本身条件和无机的环境影响。但湖泊底泥的Se含量较低,消解过程中容易受到污染。污染源主要有消解管污染、操作人员手动操作失误等。因此,测定底泥的消解管需要用1∶3的硝酸完全浸泡清洗,并且保证专管专用,避免有机质等高Se样品的污染。
实验证明,消解过程中使用5 mL HNO3和1 mL HF的混酸体系,消解后的样品澄清透明,符合测定条件,微波消解最佳温度为120 ℃消解5 min。赶酸时加入2 mL HCl,定容至20 mL。在样品优化条件下,底泥能够消解完全,测定的Se含量符合检验。
3.2 底泥中Se元素测定的常见影响因素分析
3.2.1 人为因素干扰分析
测定沉积物中Se元素的样品前处理消解方法主要有水浴法、电热板解法、微波消解法。湿解法是国标中推荐的方法之一[11],对操作人员的操作手法,加酸量消解时间等要求较高,且容易糊底。本實验选用微波消解后赶酸的前处理法消解底泥样品。
3.2.2 检测成本、操作步骤及时间分析
对前处理仪器而言,微波所需的仪器成本明显高于电热板湿法消解,实验耗材成本[12]。但微波消解操作过程简单,不容易出现糊底的问题,且由于不使用高氯酸,实验安全性更好。底泥样品微波消解时间约为40 min,赶酸大约需要2 h,微波消解最多可以设计16个孔位,赶酸仪30个孔位,均有孔位限制,故而时间长、单批处理样品数量受限。对于微波消解的这些不足,可通过多批次消解管,以组为单位进行预消解和消解,以保证提高消解效率,减少样品之间的交叉污染。
4 结论
1)从前处理优化的角度来看,本方法采用了微波消解联用原子荧光光谱法,此前处理能有效减少湖泊底泥中的Se流失,且使用HNO3-HF消解,操作过程较为安全。
2)从操作步骤的角度看,测定方法简单易行,操作员学习成本低,又能够最大程度保证数据准确,减少污染。
3)从方法优点的角度看,本测定方法适合湖泊底泥这类元素地球化学样品,测量结果准确,重现性好,对达里湖底泥样品Se含量测定有效。
参考文献:
[1] GABOS M B, ALLEONI L R F, ABREU C. Background levels of selenium in some selected Brazilian tropical soils [J]. Journal of Geochemical Exploration, 2014(145):35-9.
[2] 温汉捷.分散元素硒的有机成矿作用初析[J].地球学报,1999(2):78-82.
[3] 徐永新,雒昆利.氢化物发生-原子荧光光谱法对水中总硒含量测试方法改进研究[J].光谱学与光谱分析,2012,32(2):532-536.
[4] 彭太丁,莫通伟,蔡凌云.氢化物原子荧光光度法测定水中硒方法的改进[J].光谱实验室,2012,29(3):1491-1493.
[5] 杨富亿,文波龙,李晓宇,等.达里诺尔湿地水环境和鱼类多样性调查II.达里湖水体的碱度、pH和硬度[J].湿地科学,2020,18(6):646-652.
[6] 任丽敏,何江,吕昌伟,等.达里诺尔湖生物有效态重金属的形态分布及生态风险评价[J].农业环境科学学报,2013,32(2):338-346.
[7] 赵胜男,史小红,崔英,等.内蒙古达里诺尔湖湖泊水体与入湖河水水化学特征及控制因素[J].环境化学,2016,35(9):1865-1875.
[8] 中华人民共和国农业部.土壤中全硒的测定:NY/T 1104—2006[S].2006.
[9] 中华人民共和国国土资源部.区域地球化学样品分析方法 第14部分:硒量测定 氢化物发生—原子荧光光谱法:DZ/T 0279.14—2016[S].北京:地质出版社,2016.
[10] 任柯颖.原子荧光光度法测定水质中硒元素[J].科技创新与应用,2020(23):131-132.
[11] 段玲敏,施白妮,程常磊.微波消解——氢化物发生原子荧光法测定土壤中硒[J].世界有色金属,2019(24):270-271.
[12] 郭晶,杨卉竹,白晶,等.土壤样品前处理法对原子荧光检测硒的影响[J].中国地方病防治,2023,38(1):44-45,69.

