苦参碱通过Hippo信号通路促进大鼠皮肤创面愈合及血管生成
曾 华,郑 勇,周 林,冯上新,唐 俊,孙妍婧,罗 玮
0 引 言
肛肠疾病手术后的创面多为开放性创面,加之粪便的残留和刺激,极易受细菌感染,导致伤口愈合缓慢,甚至引发局部和全身感染[1]。如何加速创面愈合一直是困扰临床医师的难题。创面愈合是由多种类型细胞参与,经不同阶段后协调有序的生理过程,涉及细胞迁移、增殖、血管生成、胶原沉积和细胞外基质重塑等[1-2]。正常的创面愈合受到阻碍时,创面的病理变化主要表现为持续的炎症反应和血管生成的异常,从而导致创面迁延不愈。针对炎症反应和血管生成的调控,可以作为加速创面愈合的潜在基础。Hippo信号通路是组织发育和机体平衡的主要协调因子,在血管生成中发挥重要作用[3]。血管内皮生长因子(vascular endothelial growth factor,VEGF)是在胚胎发生过程中调节血管生成的分子,也是在伤口愈合、炎症以及肿瘤生长和转移过程中调节组织中血管生成的分子[4]。研究表明,Hippo信号通路是VEGF诱导的血管生成的关键介质,其激活可通过调节创面修复过程中VEGF、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)、转化生长因子β1(transforming growth factor-β1,TGF-β1)等介质的表达来促进皮肤创面愈合[5]。苦参是我国传统名贵中药之一。现代研究发现,苦参中提取的多种天然化合物具有广泛的药理学活性,其中苦参碱(Matrine,MT)因具有抗菌、抗肿瘤、抗氧化、抗炎和抗纤维化等多种药理作用而受到关注[6]。此外,研究发现MT在治疗皮炎和湿疹中表现出良好的化学活性[7]。然而,MT对皮肤创面愈合的作用机制仍未阐明。因此,本研究拟通过构建全层皮肤切除创伤大鼠模型,初步探讨MT促进皮肤创面愈合的可能机制。
1 材料与方法
1.1 实验动物SPF级SD大鼠,5~7周龄,雌雄各半,体重180~200 g,购自湖北省动物实验研究中心,生产许可证编号为SCXK(鄂)2020-0018,合格证编号为No.42000600044386。设置饲养温度为22 ℃,湿度为55%~60%,12 h光暗循环适应性喂养1周。
1.2主要药品与试剂苦参碱标准品(≥98%,货号CFN98835)购自武汉ChemFace公司。将苦参碱溶于纯水制备成浓度为3 μg/mL的混合液备用。Hippo-Yap通路特异性抑制剂Verteporfin(97%;货号S80258)购自上海源叶生物科技有限公司。京万红软膏购自天津达仁堂京万红药业有限公司(国药准字Z20023137)。蛋白提取试剂盒(货号YT8951)购自北京伊塔生物科技有限公司;苏木精伊红(HE)染色试剂盒(货号G1120-100)购自北京索莱宝科技有限公司;白细胞介素-6(IL-6;货号PI328)、肿瘤坏死因子-α(TNF-α;货号PT516)、白细胞介素-1β(IL-1β;货号PI303)酶联免疫吸附试剂盒购自上海碧云天科技公司;NE-PER核提取试剂和细胞质提取试剂购自美国Thermo Fisher Scientific公司;兔源VEGF单克隆抗体(货号ab32152)、兔源哺乳动物Ste20样激酶1(mammalian sterile20-like 1,MST1)单克隆抗体(货号ab245190)、兔源磷酸化MST1(p-MST1)单克隆抗体(货号ab51134)、兔源大肿瘤抑制因子1(large tumorsuppressor gene1,LATS1)单克隆抗体(货号ab243656)、兔源磷酸化LATS1(p-LATS1)单克隆抗体(货号ab111334)、兔源磷酸化YAP(p-YAP)单克隆抗体(货号ab76252)、兔源YAP单克隆抗体(货号ab81183)、兔源三磷酸甘油醛脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)多克隆抗体(货号ab9485)、兔源组蛋白H3(histone H3;H3)多克隆抗体(货号ab1791)均购自美国Abcam公司。
1.3主要仪器JJ-12J型脱水机和JB-P5型包埋机(武汉俊杰电子有限公司);RM2016型病理切片(上海莱卡仪器有限公司);NIKON ECLIPSE CI型正置光学显微镜(日本尼康公司)。
1.4动物建模、分组及给药从61只大鼠中随机数字表法选择6只作为对照组,其余55只大鼠用于构建全层皮肤切除创伤模型[8]。剃除大鼠背部毛发后,以2%戊巴比妥钠(40 mg/kg)腹腔注射法麻醉大鼠。于大鼠背部做一直径20 mm圆形标记,沿标记切除全层皮肤,深度约为2 mm,所有造模大鼠的取皮部位及形状保持一致。创伤后按压创面止血,使用碘伏对大鼠创伤部位进行消毒后,拍照记录创面情况。建模4 h后,肉眼可见皮肤创面损伤,无死亡、感染现象,即为建模成功。共55只大鼠参与建模,48只成功建模的大鼠参与后续实验。将48只模型大鼠随机为模型组、PD组、MT组、MT+VP组,每组12只。对照组麻醉后剃除背部相同部位毛发,不做皮肤创伤处理。
造模成功后即刻给药。对照组大鼠于剪毛区涂抹100 μL等渗盐水。模型组于创面涂抹100 μL等渗盐水。PD组于创面涂抹100 μL的京万红软膏[7]。MT组于创面涂抹浓度为200 ng/mL苦参碱混合液100 μL[9]。MT+VP组于创面涂抹浓度为300 μg/L苦参碱混合液100 μL后,腹腔注射100 mg/kg VP[10]。各组给药1次/d,持续7 d。
1.5大鼠创面愈合情况分别于造模后0、3、7和14 d对创面边缘进行测量并拍照,采用ImagePro Plush.6.0图像分析系统对创面面积进行测定,并计算创面愈合率,公式如下:
创面愈合率(%)=(原始创面面积-第n天未愈合创面面积)/原始创面面积×100%
1.6标本采集于造模后7 d,每组随机抽取6只大鼠,麻醉后取下创面局部组织样本。一部分创面皮肤组织用于组织病理学分析,一部分创面皮肤组织制备匀浆,用于ELISA和Western blot分析。其余大鼠继续分笼饲养至创面完全愈合,记录完全愈合时间和疤痕厚度。
1.7酶联免疫吸附实验将皮肤组织匀浆后,于4 ℃下以离心半径10 cm、3000 r/min离心10 min后获得上清液样品,置于-80 ℃保存。采用相关检测试剂盒检测血清TNF-α、IL-6和IL-1β的水平。
1.8HE染色石蜡切片经脱蜡、梯度水化后,苏木精染色5 min,盐酸酒精分化2 s,水洗后用饱和碳酸锂溶液返蓝30 s。水洗后,用0.5%伊红染色1 min。经梯度乙醇和二甲苯处理后,用中性树脂封片。于光学显微镜下进行观察。
1.9免疫组化染色石蜡切片经脱蜡后,经3%双氧水灭活内源性酶、抗原热修复后,于封闭液中室温下封闭10 min。随后,将切片与抗CD31一抗于4 ℃下孵育过夜。经PBS洗涤后,于切片上滴加辣根过氧化物酶(horseradish peroxidase,HRP)标记的兔抗IgG二抗,37 ℃下孵育30 min。采用二氨基联苯胺(DAB)显色试剂盒显色后,经苏木精复染、脱水、透明,用中性树脂封固。
1.10蛋白免疫印迹分析将部分皮肤组织在含PMSF和磷酸酶抑制剂的RIPA缓冲液中制备组织匀浆,冰浴后于4 ℃下以以离心半径12 cm、10 000 r/min离心20 min。按照产品说明书,使用NE-PER核提取试剂和细胞质提取试剂分离核蛋白质和细胞质蛋白质。蛋白质用双喹啉酸(BCA)法进行定量。蛋白质样品经12% 聚丙烯酰胺凝胶电泳(SDS-PAGE)分离后转移到聚偏二氟乙烯(PVDF)膜上。随后,将膜用 5%脱脂牛奶阻断2 h。随后,将膜用一抗于4 ℃下孵育过夜。洗涤后,再将膜用过氧化物酶结合的二抗于室温下孵育2 h。洗涤后,用增强化学发光(ECL)检测试剂盒(Applygen Technologies Inc.)对膜进行显影。使用GAPDH或H3作为内部参照。采用Image J对条带图像进行分析。

2 结 果
2.1 创面愈合率建模时,各组大鼠创伤面积基本一致。造模后7 d和14 d时,PD组和MT组创面均较模型组缩小。定量分析显示,造模后3、7、14 d时,与模型组相比,PD组和MT组创面愈合率均明显升高(P<0.05);与MT组相比,MT+VP组创面愈合率均明显降低(P<0.05)。见表1。

表1 大鼠创伤愈合面积的比较
2.2创面组织炎症因子水平造模后7 d,与模型组相比,PD组和MT组IL-1β、IL-6、TNF-α水平均明显降低(P<0.05);与MT组相比,MT+VP组IL-1β、IL-6、TNF-α水平均明显升高(P<0.05)。见图1。
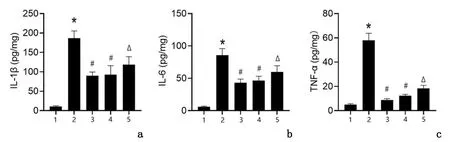
1:对照组;2:模型组;3:PD组;4:MT组;5:MT+VP组
2.3创面组织病理损伤HE染色显示,与对照组相比,造模后7 d,模型组可见明显炎性浸出层,肉芽组织水肿,成纤维细胞散在分布,少量新生毛细血管;而相较于模型组,PD组和MT组炎性细胞密度降低,炎性渗出层变薄或消失,肉芽组织水肿减轻,可见较明显成纤维细胞及新生毛细血管。相较于MT组,MT+VP组病理组织损伤加重。见图2。
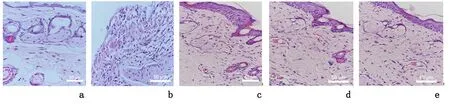
a:对照组;b:模型组;c:PD组;d:MT组;e:MT+VP组
2.4创面组织血管生成免疫组织化学分析显示,造模后7 d,与模型组CD31阳性染色细胞百分比[(5.44±0.65)%]相比,PD组[(53.62±5.39)%]和MT组[(50.58±6.26)%]明显升高(P<0.05);与MT组CD31阳性染色细胞百分比[(50.58±6.26)%]相比,MT+VP组[(42.73±5.32)%]明显降低(P<0.05)。见图3。

a:对照组;b:模型组;c:PD组;d:MT组;e:MT+VP组
Western blot分析显示,与模型组相比,PD组和MT组VEGF和TGF-β1蛋白表达明显升高(P<0.05);与MT组相比,MT+VP组VEGF和TGF-β1蛋白表达明显降低(P<0.05)。见图4。
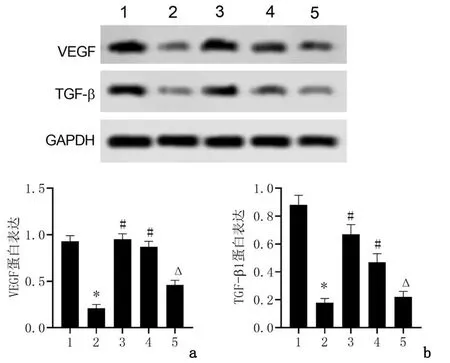
1:对照组;2:模型组;3:PD组;4:MT组;5:MT+VP组
2.5Hippo信号通路相关蛋白的表达量采用Western blot检测Hippo信号通路相关蛋白。结果显示,造模后7 d,与对照组相比,模型组MST1、LAST1和YAP蛋白磷酸化水平明显降低(P<0.05);与模型组相比,PD组和MT组MST1、LAST1和YAP蛋白磷酸化水平明显升高(P<0.05);与MT组相比,MT+VP组MST1、LAST1和YAP蛋白磷酸化水平明显降低(P<0.05)。见图5。
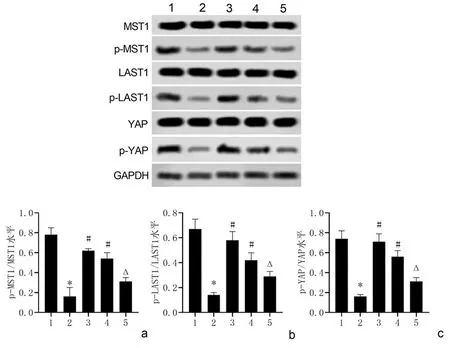
1:对照组;2:模型组;3:PD组;4:MT组;5:MT+VP组
2.6YAP核移位与对照组相比,模型组细胞质YAP蛋白表达明显降低,而核YAP蛋白表达明显增加(P<0.05);与模型组相比,PD组和MT组胞质YAP蛋白表达明显增加,而核YAP蛋白表达明显降低(P<0.05);与MT组相比,MT+VP组细胞质YAP蛋白表达明显降低,而核YAP蛋白表达明显增加(P<0.05)。见图6。

1:对照组;2:模型组;3:PD组;4:MT组;5:MT+VP组
2.7创面完全愈合时间及瘢痕厚度与模型组相比,PD组和MT组皮肤创面完全愈合时间明显减少,且瘢痕厚度明显降低(P<0.05);与MT组相比,MT+VP组创面完全愈合时间明显增加,且瘢痕厚度明显增加(P<0.05)。见表2。

表2 各组大鼠创面完全愈合时间及瘢痕厚度的比较
3 讨 论
皮肤是抵御外部侵略者的第一道防线。皮肤的完整性会因创伤、撕裂、割伤或挫伤而受损,从而导致皮肤伤口。皮肤伤口愈合过程涉及各种类型的细胞(例如白细胞、成纤维细胞和角质形成细胞)和多种因子,例如细胞因子、趋化因子、生长因子和酶。这些细胞和因子在每个伤口愈合阶段都有不同的特征。探寻多效应促进创面愈合的药物具有重要意义。近年来,大量天然药物来源的活性成分被证明具有促进创面愈合作用[11]。对天然产物的开发和利用对皮肤创伤的治疗具有积极意义。苦参是豆科植物苦参SophoraflavescensAit.的干燥根,具有清热利湿、解毒水肿、拔毒生肌之功效[12]。MT是从苦参根中提取的一种生物碱,被证实具有抗炎、抗氧化作用,并能够促进人皮肤角质形成细胞和成纤维细胞的增殖[13]。本研究发现,相较于模型组,MT组大鼠创面愈合率明显增加,且创面完全愈合时间缩短,瘢痕厚度降低。这些结果提示,MT能够加速全层皮肤切除创伤模型大鼠的皮肤创面愈合,且有利于抑制瘢痕过度增生。
炎症反应是创伤修复的重要阶段,对于清除病原微生物并为随后的组织修复和再生阶段创造合适的环境至关重要[14]。皮肤受损后,伤口区域募集多种炎性细胞,如中性粒细胞、单核细胞和巨噬细胞等,并释放各种生长因子、细胞因子和趋化因子[15]。在伤口环境中,中性粒细胞上调趋化因子的基因表达,如TNF-α,IL-1β,IL-6,VEGF和单核细胞化学引诱蛋白-1;招募巨噬细胞、T细胞和其他中性粒细胞;并促进成纤维细胞和角质形成细胞的血管生成和增殖[15]。单核细胞到达伤口并分化成巨噬细胞或树突状细胞。巨噬细胞负责吞噬凋亡中性粒细胞,清除伤口区域的细菌和死细胞,并在炎症期与中性粒细胞合作。巨噬细胞还分泌细胞因子,如TGF-β、TNF-α、IL-1和IL-6[16]。此外,巨噬细胞表型转运至修复状态,从炎症中消退并刺激角质形成细胞和成纤维细胞进行后续组织再生,促进向增殖期的过渡。然而,持续的炎症反应会损害创面周围正常组织,导致创面愈合困难,甚至引起感染。因此,在皮肤创面愈合中精确平衡促炎和抗炎反应十分重要。据报道,MT对中性粒细胞的浸润、巨噬细胞极化及单核细胞的迁移和粘附具有抑制作用[17-19]。MT的抗炎特性已经被广泛证实[20-21]。本研究发现相较于模型组,治疗6 d后,MT组创面炎性浸出层消退时间提前。同时,MT组IL-1β和IL-6水平均明显低于模型组。因此,MT可以通过减轻炎性细胞浸润、抑制促炎细胞因子分泌来减轻伤口的炎症过程,加速愈合过程。
除炎症反应外,创面血管生成障碍也是导致创面愈合延迟的主要因素[22]。血管生成是创面愈合过程中关键环节之一,对创面愈合起着十分重要的作用[23]。通过促进新生血管生成来促进创面愈合是目前开发相关药物的有效策略[23]。内皮细胞活化和增殖是综合各种调控因素后,最终促进血管生成的核心执行程序[24]。CD31在新生血管中表达阳性,是血管内皮细胞的标志物; VEGF和TGF-β1是血管生成、肉芽组织形成、胶原蛋白合成和细胞外基质沉积的效应因子,在血管内皮细胞的诱导、维持和生长中发挥着积极作用[25]。VEGF和TGF-β1表达的增加与伤口愈合的加速有关[26]。本研究中HE染色显示MT组大鼠创面新生血管数量明显增多。同时,免疫组织化学分析及蛋白质印迹法检测结果均显示,MT组大鼠创面中CD31、VEGF和TGF-β1的表达较模型组明显增多,可见MT能够促进创面血管生成。
目前尚不清楚MT促进皮肤损伤修复的机制。Hippo通路参与调节器官大小、组织再生和干细胞自我更新,是伤口修复过程中的关键信号通路之一[27]。在哺乳动物中,该通路的核心模块由MST1、LAST1/2激酶及其相互作用伙伴MOB激酶激活剂1组成。已证实,Hippo通路失调与糖尿病血管生成障碍和伤口愈合延迟有关[28]。Hippo信号的激活导致与转录因子相互作用并调控基因表达的YAP蛋白被排斥出细胞核。YAP作为一种新型转录因子,能有效增强促炎细胞因子的表达,同时提高TNF-α的表达水平。抑制YAP的表达或敲除YAP可以有效地下调促炎因子的表达,表明YAP能够发挥有效的促炎反应[29]。此外,Hippo信号通路还充当血管生成的各种信号通路的融合者,包括Wnt、VEGF和Notch等[30]。在皮肤伤口愈合过程中,Hippo-YAP介导的核信号传导对于VEGF和TGF-β1信号转导是必不可少的[31]。Pulkkinen等[32]观察到VEGF介导的内皮细胞增殖和血管生成主要通过Hippo信号通路传导来调节。Brewer等[33]在耳廓损伤小鼠模型中证实YAP活性在体内伤口愈合中至关重要。Yang等[34]发现,中性粒细胞细胞外陷阱通过抑制Hippo信号通路,使YAP与转录因子Smad2结合,并从细胞质转移到细胞核,促进内皮-间充质转化,最终阻碍糖尿病足小鼠血管生成并延迟伤口愈合。本研究中,我们试图确定MT在皮肤损伤大鼠皮肤伤口愈合中的促进作用是否涉及Hippo信号通路。结果发现,MT处理使MST1、LAST2和YAP的磷酸化水平明显增加,而YAP的核移位明显减少,提示MT能够激活Hippo途径,并抑制YAP的核移位。为进一步确定MT在皮肤损伤大鼠模型中的作用机制,本研究也使用了Hippo-YAP通路特异性抑制剂Verteporfin(VP)进行挽救实验。与预期一致,本研究发现,VP可在一定程度上消除MT对Hippo-YAP通路的激活作用。同时,MT对皮肤损伤大鼠组织损伤的改善、促炎细胞因子分泌的抑制、血管生成的促进作用均能够在一定程度上被VP所逆转。这些结果证实MT至少部分通过激活Hippo-YAP通路来发挥抗炎效应,并促进血管生成,从而加速创面愈合,在全层皮肤切除创伤大鼠模型中发挥保护作用。
综上所述,MT能够通过抑制炎症反应、促进血管生成加速全层皮肤切除创伤大鼠的皮肤创面愈合,这一过程可能涉及MT对Hippo-YAP通路的激活效应。

