浅析食品中农药残留前处理及检测技术研究进展
◎ 杨蜀军
(四川省阆中市食品药品和产品质量检验检测中心,四川 阆中 637400)
在我国农业生产中,农药使用的种类多、范围广、覆盖面大,部分从业者为了提高产量和质量,会违规使用高毒、高残留、禁用农药产品,不仅会造成环境污染问题,也会对周边居民的正常生产生活造成一些负面影响,甚至会引发一系列的恶性中毒事件,扰乱社会秩序。伴随农业与食品加工业携手迈向现代化阶段,相关部门有必要大力研发和应用农药残留检测手段,严格监管农产品的农药残留情况,从根本上消除食品安全风险。同时,相关部门要进一步提高对食品质量安全的重视程度,最大限度地保护人民群众的合法权益,营造良好的社会生活环境[1]。
1 农药残留前处理技术
1.1 固相萃取技术
固相萃取(SPE)是近年发展起来的一种样品预处理技术,具体方法如图1 所示。
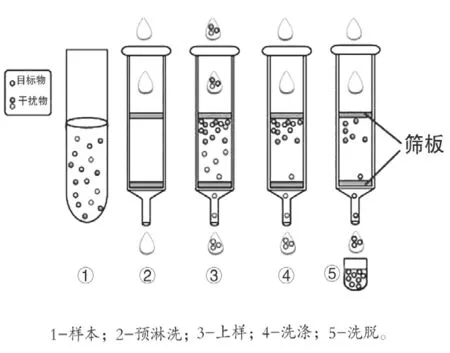
图1 固相萃取技术方法图
固相萃取技术主要起到分离与提纯化学制剂的作用,其应用范围相当广泛和多样,主要包括前处理痕量样品、分离工业化学制剂、充当吸附萃取工具等。固相萃取可以理解为涉及固液相的物理萃取手段,固相会向分离物施加远超分离物所处溶剂的吸附力量。一旦吸附剂床与样品溶液直接接触,前者就会任由溶液中的其他成分流过,而将分离物牢牢吸附下来。依靠这种对分离物的特异性吸附能力,可以实现对分离物的浓缩提纯。附剂和分离物分子会互相产生保留效应,正是在这种保留效应的作用下,样品溶液所含的分离物才无法脱离吸附剂的吸附力。
1.2 QuEChERS 法
在众多应用于蔬菜中农药残留检测分析的前处理技术中,QuEChERS 法占据了重要地位。这种检测手段是分散固相萃取技术的形式之一,其采用的吸附剂和样品所含的杂质会产生吸附力,从而起到吸附、清除杂质,提纯样品的效果[2]。
2 农药残留检测技术
2.1 化学分析检测技术
2.1.1 光谱分析法
农药分子结构自带的光谱特点是这种检测技术的基本原理,再辅以化学计量技术,便可精确检测农产品的农药含量。相较于以往常用的检测手段,光谱分析法无疑具备便捷性与难度低的优势,更适用于测定农药残留量。从当前检测技术的现状来审视,国内外普遍采取的食品农药残留光谱检测手段包括荧光光谱法、拉曼光谱法、可见/近红外光谱法。其中,荧光光谱法的基本原理是样品中的特定化学成分含量和样品本身的荧光强度存在正交关系,如此便可精确测定样品中的农药残留量[3]。
2.1.2 气相色谱法
气相色谱法(GC)作为一种分离分析技术,在我国工业、军事、建筑和农业等众多领域都有使用。GC的基本原理如下:当被置于固定液相以及气相中时,样品所含化学成分往往呈现差异化的分配系数,样品以气化状态进入色谱柱,其中包含的化学成分会不断被液相与气相分配,受化学成分本身在两相中的吸附能力或者溶解能力差异的作用,化学成分在色谱柱运行期间会呈现各种各样的速度,在历经足够长度之后,化学成分就逐渐分离,依次脱离色谱柱转移到检测器中,记录器会将放大处理过的离子流信号转化成对应的色谱峰,然后用色谱图表征和定量分析样品。
2.2 生化分析检测技术
2.2.1 酶抑制法
含有氨基甲酸酯或者有机磷的农药往往具备显著的酶活性抑制功能,酶抑制法正是基于上述特点测定食品残留农药的检测技术。这种检测技术通常表现为3 种形式:植物酯酶抑制法、有机磷水解酶法、胆碱酯酶抑制法。由于前处理难度和复杂性较低,酶抑制法的检测效率相当出色,可以用来一次性检测多个样品,且支持现场检测。酶抑制法不仅能以较快速度获得食品样品的农药含量结果,而且成本低、操作简单。然而,除了氨基甲酸酯或者有机磷的农药之外,该检测技术并不适用于其他农药[4]。
2.2.2 生物传感器法
HE 等开发了一款可以用来测定马拉硫磷的全新电化学生物传感器,其应用原理如下:将针状聚苯胺裹在空心碳球核-壳纳米结构之外,再将复合材料与乙酰胆碱酯酶牢牢对接,依靠纳米材料本身的比表面积优势,以有效提升生物传感器的表面活性物质固载量,这样一来,酶与传感器之间就会形成更加紧密的联系,最终的检测结果活性也将更加明显。相关研究通过检测发现,生物传感器的最低检出限是0.16 μg·L-1,在介于1.0~1.0×104 μg·L-1的情况下,检测电路和浓度之间,呈现显著的线性增长关系。
3 光谱法对农药克百威的残留检测
3.1 实验仪器
FS920 稳态荧光光谱仪(英国Edinburgh Instruments)、ME104 型电子天平(Mettler Toledo 公司)。
3.2 实验所用材料与试剂
(1)氨基甲酸酯类农药:克百威标准品及对应的储备液。克百威是一种结晶状的物质,整体无色,熔点大概在153.5 左右,如果在20 ℃的水环境下,其溶解度为320 mg·L-1。对于这种物质来说,除了在碱性环境下,其余时候都能够表现比较稳定的状态,整体稳定性较强。
(2)溶剂:甲醇(分析纯)、甲醇(色谱纯)、乙腈。甲醇的分子式为CH3OH,乙腈的分子式为C2H3N。
3.3 标准储备液的配制
3.3.1 以甲醇(分析纯)为溶剂
在实验之前,利用电子天平称取相应重量的克百威标准品,以此确保实验结果的准确性。本次实验选择的是浓度为98.6%的标准品,实验期间共称取0.008 g,在其中加入甲醇进行溶解,之后转移到容量为50 mL 的透明容量瓶中进行定容并摇匀,直至溶解。配置的标准储备液需要采取避光冷藏的方式存储[5]。
3.3.2 以甲醇(色谱纯)为溶剂
与上述步骤基本一致,要将称取的数量及定容的容量瓶分别改成0.026 g 及100 mL,以配置出浓度为260 μg·mL-1的溶剂。在配置完成之后,需要采取同样的方式存储,为之后的实验做准备。
3.3.3 以乙腈为溶剂
前期所有方式与前者一致,不同的是称重的标准品重量为0.018 g,最终配置出浓度为180 μg·m L-1的溶剂,同样采取避光冷藏的方式进行存储。
3.4 实验过程与方法
(1)称取3.3.3 中的标准储备液,稀释成浓度完全不同的13 组溶液,分别是4.500、3.000、2.250、1.500、1.000、0.750、0.500、0.250、0.100、0.075、0.050、0.030、0.025 μg·mL-1。
(2)称取3.3.1 中的标准储备液,稀释成浓度完全不同的13 组溶液,分别是4.000、3.200、2.000、1.600、1.000、0.800、0.500、0.320、0.200、0.100、0.080、0.050、0.032 μg·mL-1。
(3)称取3.3.2 中的标准储备液,稀释成浓度完全不同的13 组溶液,分别是3.250、2.160、1.730、1.300、1.080、0.860、0.540、0.260、0.130、0.086、0.065、0.054、0.032 μg·mL-1。
(4)将得到的实验结果导入MATLAB 软件中,绘制出相应的光谱立体图和等高线图,让实验结果更加直观、清晰。
3.5 实验结果与分析
用MATLAB 软件绘制克百威-乙腈溶液各浓度的三维荧光光谱图,包括立体图和等高线图,具体如图2 所示。
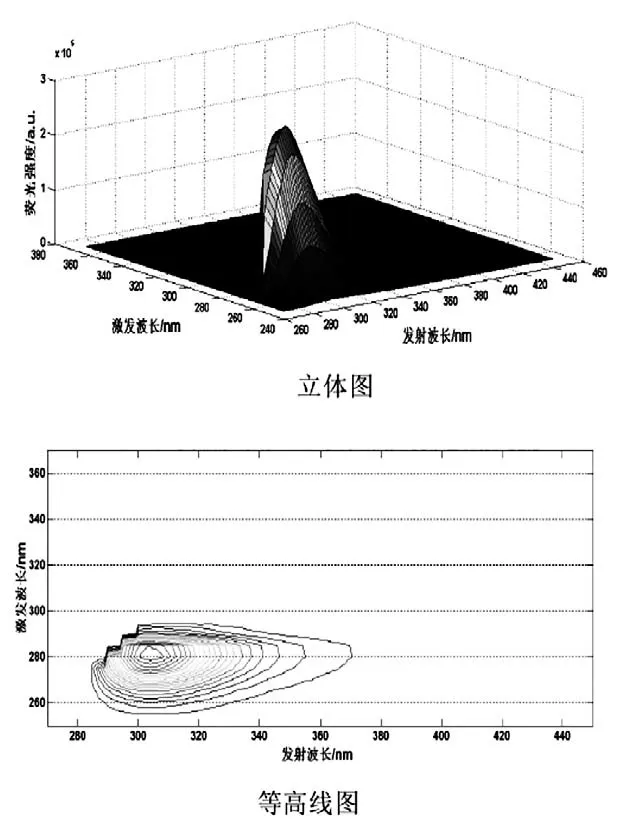
图2 4.500 μg·mL-1 克百威-乙腈溶液三维荧光光谱图
通过图2 可以看出,克百威-乙腈溶液表现的荧光强度与食品的农药浓度是正相关关系,也就是说,在后者越低的情况下,前者呈现的强度就会越低。与此同时,等高线图体现以下特点:无论农药含量多寡,溶液都会在激发波长280 nm 位置,呈现较大的荧光强度;溶液会在发射波长305 nm 位置产生特征峰,即相对显著的波峰。
4 结论
在现代化时代背景下,科学技术不断发展与进步,人们对于食品农药残留检测的重视程度逐渐提高,农药检测领域也出现了很多先进的检测技术。在不同的农药残留检测工作中,如果可以灵活使用不同的检测方式,并做好全过程监督与管理工作,那么最终的检测效果会更加理想。未来,进一步提升食品中农药残留前处理及检测技术水平,是必然的发展趋势。

