微波消解-原子荧光光谱法测定栀子中硒含量




摘 要:本文采用微波消解-原子荧光光谱法测定栀子中的硒元素含量。结果表明,使用8 mL硝酸和2 mL过氧化氢时,能够将0.300 0 g的栀子样品完全消解,并且荧光强度良好。方法在0~10 μg·L-1具有良好的线性关系,检出限为0.050 5 ng·mL-1,精密度为3.0%,加标回收率在96.80%~100.34%。该方法具有较高的准确性和灵敏度。
关键词:微波消解法;原子荧光光谱法;硒
Determination on Selenium in Gardenia by Microwave Digestion-Atomic Fluorescence Spectrometry Method
CHEN Si, WANG Jiao
(Xiangtan Medicine amp; Health Vocational College, Xiangtan 411102, China)
Abstract: The content of selenium in gardenia jasminoides was determined by microwave digestion and atomic fluorescence spectrometry. The results showed that 0.300 0 g of gardenia samples could be completely dissolved with 8 mL of nitric acid and 2 mL of hydrogen peroxide, and the fluorescence intensity was good. The detection limit was 0.050 5 ng·mL-1, the precision was 3.0%, and the recoveries were 96.80%~100.34%. The method has high accuracy and sensitivity.
Keywords: microwave digestion method; atomic fluorescence spectrometry; selenium
硒作为一种微量营养元素,对人类和动物的健康至关重要,同时也是植物生长的关键元素[1]。1988年,中国营养学会首次将硒纳入了我国居民每日所需的15种膳食营养素之中。成年人每天应摄取的硒含量为60~400 μg,但我国大部分地区的硒含量偏低,30%的地区严重缺乏硒元素,导致人们每日硒摄入量不足[2-3]。我国丰富的、具有药食同源的中草药提供了另一种有效的方式来弥补硒元素的缺乏,即通过使用富含硒的药食同源的中草药来补充硒元素,从而保障人们的身体健康[4]。栀子作为药食同源的中药材,具有泻火除烦、清热利湿和凉血解毒的作用,能治疗目热赤痛、胸心大小肠大热和胃中热气等。
目前,总硒的测定方法包括分光光度法[5]、原子吸收光谱法[6]、电感耦合等离子体质谱法[7]和原子荧光法[8]等。其中,氢化物-原子荧光光谱法因具有灵敏度高、干扰低特点而得到了广泛应用。硒含量检测中的样品前处理步骤至关重要[9]。该步骤的主要目的是预浓缩样品中的硒,同时打破样本的基质特性并提取硒元素,以确保样品符合仪器的检测标准。湿法消解、微波消解、高压罐消解和干法灰化等传统前处理方法均在此过程中发挥了重要作用。其中,湿法消解和微波消解因其高效性和可行性而成为首选前处理方法。本研究选择微波消解法对栀子样品进行前处理,利用原子荧光法测定栀子中的硒含量。
1 材料与方法
1.1 材料、试剂与仪器
栀子,采自湖南省湘潭县。硒粉(分析纯),上海沪试环保试剂科技有限公司;硝酸(分析纯),上海沪试环保试剂科技有限公司;30%过氧化氢(分析纯),西陇化工股份有限公司;盐酸(分析纯),江苏永丰化学试剂有限公司;铁氰化钾(分析纯),恒兴试剂;硼氢化钾(分析纯),国药集团化学试剂有限公司。
海光仪器HGF-V3,北京海光仪器有限公司;微波-消解仪,北京莱伯泰科仪器股份有限公司。
1.2 试样制备
将栀子样品去除杂质,用研磨机粉碎过20目筛,精密称定0.300 0 g粉末样品,按照表1参数条件进行前处理消解,同时做空白试验。
1.3 溶液配制及标准曲线制备
以硒粉为基础材料,配制成1 000 μg·L-1硒标准溶液,分别取0 mL、0.2 mL、0.4 mL、0.6 mL、0.8 mL和1.0 mL标准溶液于100 mL容量瓶中,加入2.5 mL铁氰化钾溶液为掩蔽剂,(5+95)盐酸溶液为稀释剂,定容,配制成硒浓度分别为0 μg·L-1、2 μg·L-1、4 μg·L-1、6 μg·L-1、8 μg·L-1和10 μg·L-1系列混合标准溶液,测定其荧光强度。以硒浓度为横坐标,荧光强度为纵坐标,绘制标准曲线。
1.4 微波消解法最佳条件的确定
1.4.1 不同硝酸用量对荧光强度的影响
精密称取0.300 0 g处理好的栀子样品,分别加入5 mL、6 mL、7 mL、8 mL、9 mL和10 mL硝酸和2 mL 30%过氧化氢,放入消解器中,常温预消解30 min。盖上消解器的内盖并来回振荡,以确保内部的物质混合均匀,然后置于微波消解仪中进行消解。消解完成,取出消解罐,置于通风橱,冷却到室温。打开消解器,放置在电热板上,60 ℃加热,赶酸直到产生白色烟雾。随后,冷却消解罐,将溶液转移至10 mL容量瓶中,加入5 mL盐酸(6 mol·L-1)和2.5 mL的铁氰化钾溶液(100 g·L-1),充分混合,用水定容至刻度线,置于原子荧光光度计上,测量其荧光值。每组试验平行3次。
1.4.2 不同过氧化氢用量对荧光强度的影响
精密称取0.300 0 g处理好的栀子样品置于消解罐中,分别加入0 mL、1 mL、2 mL、3 mL和4 mL"30%过氧化氢和8 mL硝酸,置于常温下预消解30 min,再置于微波消解仪中进行消解,冷却赶酸,溶液转移至10 mL容量瓶中,加入5 mL盐酸(6 mol·L-1)和2.5 mL铁氰化钾溶液(100 g·L-1),充分混合,用水定容至刻度线,于原子荧光光度计上测量其荧光值。每组试验平行3次。
1.5 栀子硒含量的测定
精密称取0.300 0 g处理好的栀子样品于消解罐中,加入8 mL硝酸和2 mL过氧化氢,于常温下预消解30 min,冷却赶酸,溶液转移至10 mL容量瓶中,加入5 mL盐酸(6 mol·L-1)和2.5 mL铁氰化钾溶液(100 g·L-1),充分混合,用水定容至刻度线,于原子荧光光度计上测量其荧光值。平行实验3次,并做空白对照实验。试样中硒含量的计算公式为
式中:X为样品硒含量,mg·kg-1;c为样液中硒浓度,μg·L-1;V为样液总体积,mL;m为样品质量,g。
1.6 加标回收率的测定
称取0.300 0 g处理好的栀子样品,按1.5的方法进行消解、赶酸,分别加入浓度为0.1 mg·kg-1、0.5 mg·kg-1和2.0 mg·kg-1的硒标准溶液进行加标回收试验,置于原子荧光光度计上测量其荧光值,通过荧光值计算硒含量。每个水平重复测定6次。
2 结果与分析
2.1 微波消解法最佳条件的确定
2.1.1 不同硝酸用量对荧光强度的影响
如图1所示,随着硝酸用量的增加,荧光强度出现先上升后下降的趋势。当硝酸用量为8 mL时,荧光强度达到最大值。硝酸用量过少会导致消解不完全,过量添加硝酸则可能会阻碍样品中硒元素转化为荧光物质,从而导致荧光强度降低。此外,在检测过程中,过量的硝酸还可能会释放出大量的酸性气体,这些气体会对实验设备造成潜在的损害。
2.1.2 不同过氧化氢用量对荧光强度的影响
由图2可知,随着过氧化氢用量的增加,荧光强度出现先上升后下降的趋势。当过氧化氢用量为2 mL时,荧光强度达到最大值。
2.2 硒标准曲线的建立
由图3可知,硒质量浓度在0~10 μg·L-1具有良好的线性关系,标准曲线方程为IF=161.724 4c+24.743 7,相关系数为0.999 93。
2.3 仪器的检出限和精密度
为了探究仪器及方法的重现性和检出限,进行了检出限和精密度测定。以2.5 mL铁氰化钾溶液为掩蔽剂,(5+95)盐酸溶液为稀释剂,容量瓶定容至100 mL,配制成空白溶液,连续测定11次空白溶液的荧光强度,计算测定结果的标准偏差s,检出限为3倍标准偏差除以标准斜率。结果表明,仪器的检出限为0.050 5 ng·mL-1。
选用质量浓度为1.0 μg·L-1的硒标准溶液,平行测定11次,得到精密度为3.0%,说明样品在消解和荧光值测定的过程中的精密度和平行性较好。
2.4 加标回收率试验
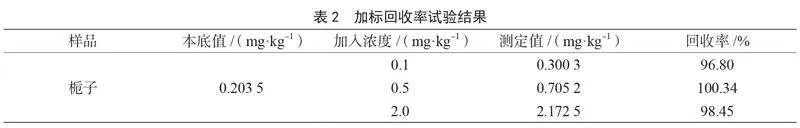
由表2可知,栀子样品的加标回收率在96.80%~100.34%。表明采用微波消解-原子荧光光谱法测量栀子中硒元素的精确度较高。
2.5 栀子中硒含量测定
取湘潭县5个不同批次栀子样品(每批次做3个平行),并将其充分磨碎、过20目筛。准确称取0.300 0 g样品,消解并测定其荧光强度,计算栀子样品中硒含量。结果表明,湘潭县的栀子中硒含量在0.198 9~0.235 6 mg·kg-1,平均值在0.213 3 mg·kg-1。
3 结论
试验采用微波消解法消解栀子,并对消解条件进行优化,以原子荧光光谱法测定栀子中硒含量。结果表明,栀子中含有一定浓度的硒元素,本研究为湖南省湘潭县地区栀子中硒元素含量提供了数据参考,对于人们的健康补硒需求具有重要的参考价值,同时为湘潭县栀子资源的深度开发和利用奠定了基础。
参考文献
[1]李志明,冯彩霞,刘家军,等.硒资源及其开发利用概况[J].地质与资源, 2002(3):11.
[2]徐巧林,吴文良,赵桂慎,等.我国富硒农产品及食品标准体系发展与展望[J]. 中国标准化,2019,44(1):136-144.
[3]张留圈,陆柏益.富硒农产品质量安全及其产业发展问题研究[J].农产品质量与安全,2020(2):3-9.
[4]郑伟.富硒农产品中硒含量检测方法研究[J].山西化工,2021,41(3):32-34.
[5]刘有芹,杨庆辉,黄函,等.紫外分光光度法测定枸杞子、陈皮、生姜中硒含量 [J].理化检验:化学分册,2010,46(30):329-330.
[6]SMRKOLJ P,STIBILJ V.Determination of selenium in vegetables by hydride generation atomic fluorescence spectrometry[J].Analytica Chimica Acta, 2004,512(1):、11-17.
[7]CAPELO J L,FERNANDEZ C,PEDRAS B,et al.Trends in selenium determination/speciation by hyphenated techniques based on AAS or AFS[J].Talanta,2006,68(5):1442-1447.
[8]KHAN N,JEONG I S,HWANG I M,et al.Method validation for simultaneous determination of chromium, molybdenum and selenium in infant formulas by ICP-OES and ICP-MS[J].Food Chemistry,2013,141(4):3566-3570.
[9]袁嫣昊,胡曙光,苏祖俭,等.食品中重金属检测快速前处理技术研究进展[J].食品安全质量检测学报,2019,10(14):4483-4491.
基金项目:湘潭市科技局计划指导项目“微波消解-原子荧光光谱法测定栀子中硒含量”(CG-ZDJH-202139)。
作者简介:陈思(1991—),女,湖南湘潭人,硕士,讲师。研究方向:分析化学。

