基于碳纤维强化的Fe0混养反硝化脱氮效能与机制
王铮,贾林春,史大林,何月玲,薛罡
(东华大学环境科学与工程学院,上海 201600)
含硝态氮(NO3--N)是污水处理厂二级生化出水的共性特征〔1〕,不仅会造成水体富营养化风险〔2〕,饮用后还会诱发肾癌、甲状腺癌和高铁血红蛋白症等疾病〔3〕。依靠有机碳源的异养反硝化是处理含NO3--N废水常用的脱氮方法〔4〕。但污水处理厂二级生化出水有机物含量低,外加碳源的成本较高且会发生二次污染〔5〕。
Fe0储量丰富,成本低廉且具有较强还原性,同时铁腐蚀产物无环境污染风险〔6〕。以Fe0作为电子供体替代外加有机碳源的自养反硝化脱氮,可大量减少外加有机碳源的投加量〔7-8〕。然而,Fe0自养反硝化菌生长周期较长〔9〕,且Fe0易于出现板结导致铁释放速率及脱氮效率降低〔10-11〕。为提升Fe0自养反硝化速率,将Fe0与外加有机碳源组合,形成自养与异养共存的混养反硝化,通过自养及异养反硝化的协同作用可实现稳定脱氮,避免单一Fe0自养反硝化反应速率慢、长期运行效率低的问题。已有研究表明,以乙酸钠作为外加有机碳源,Fe0介导的混养反硝化的TN去除效率高达90.7%,同时自养反硝化菌的丰度得到提高〔12〕。
然而,目前在Fe0与外加碳源协同实现混养反硝化脱氮的研究中,难以控制铁腐蚀程度。碳纤维(CF)具有化学、机械和导电性能稳定等优点〔13〕,其与Fe0形成的复合材料可以进一步促进Fe0腐蚀。碳纤维包裹在Fe0表面防止钝化,同时碳纤维表面产生大量铁氧化物,促进碳纤维对NO3--N的吸附作用,并强化功能微生物的附着〔14〕。此外,碳纤维与Fe0形成微观原电池〔15〕,促进Fe0缓慢持久地腐蚀。但碳纤维强化Fe0混养反硝化脱氮的具体过程、机理尚不清楚,有待进一步研究。
因此,本研究以含NO3--N合成废水为处理对象,分别构建两套Fe0生物反硝化近工程边界连续流反应器,即单独投加Fe0和投加Fe0耦合碳纤维的混养反硝化反应器。研究不同COD/NO3--N、水力停留时间(HRT)对脱氮效果的影响,分析了胞外聚合物(EPS)、电子传递活性(ETSA)变化规律及Fe0形态及组分变化规律。从微生物群落结构和反硝化功能基因角度,进一步探究碳纤维强化Fe0混养反硝化脱氮的效能与机制。
1 材料与方法
1.1 实验用水及接种污泥
实验进水采用含NO3--N模拟废水,控制进水NO3--N质量浓度为40~45 mg/L。配水中含有289 mg/L KNO3、25.5 mg/L K2HPO4、30 mg/L MgCl2·6H2O、20 mg/L CaCl2·2H2O、300 mg/L NaHCO3〔16〕。用1 mol/L HCl调节进水pH为6.5~7.0。
实验污泥取自上海市松江区某污水处理厂(含水率≥99%),新鲜污泥经含NO3--N模拟废水驯化后投入使用,使用时接种污泥质量浓度为3 500 mg/L。
1.2 实验装置及运行设计
实验装置为有机玻璃材质连续流反应器,长、宽、高分别为20.0、15.0、25.0 cm,有效容积为6.0 L。设置两组反应器,分别为装填无纺布包裹Fe0材料的对照组R0反应器,装填无纺布包裹碳纤维与Fe0混合材料的实验组R1反应器。用蠕动泵将配制的含NO3--N废水输送至反应器,实现连续流运行。装置如图1所示。
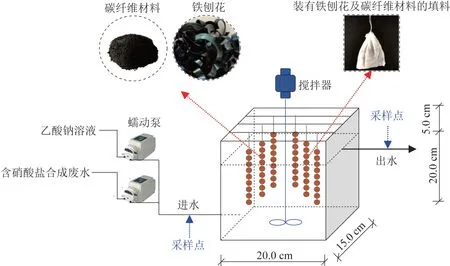
图1 实验装置Fig.1 Experimental equipment
碳纤维材料:将聚丙烯腈(PAN)高温碳化并研磨成100目的碳纤维粉末,投加量为10 g/L。
Fe0取自某钢铁厂,长度为1~4 cm,呈弯曲螺旋状。使用前去除表面污物与杂质,先用2.0 mol/L NaOH溶液碱洗30 min,再用2.0 mol/L HCl溶液酸洗1 h,然后用去离子水冲洗至中性备用。采用硝酸溶解法〔17〕测定其组分,在去离子水中浸泡24 h后测定其溶出情况(表1)。其中铁元素的质量分数>94%,虽有少量重金属Cr、Cu元素的存在,但没有重金属溶出,因此无二次污染风险。铁刨花投加量为30 g/L。按Fe0自养反硝化脱氮的理论消耗量〔18〕,见式(1),该投加量足以维持实验期间反应对Fe0的消耗。

表1 铁刨花重金属元素组成及占比Table 1 Metal element composition and proportion of iron scraps
反应器于室温运行,采用搅拌促进传质,进水溶解氧(DO)为6~8 mg/L。反应分6个阶段,具体运行设置见表2。通过调整乙酸钠的用量,在阶段Ⅰ~Ⅴ运行期设置不同的进水COD/NO3--N,以探究外加有机碳源投量对混养反硝化脱氮效能及机制的影响。在阶段 Ⅵ运行期,改变HRT明确其对脱氮效果的影响。

表2 反应器运行条件Table 2 Operation condition for reactor
1.3 实验分析方法及计算
废水样品通过0.45 µm滤纸过滤。TN、NO3--N、NH4+-N、NO2--N分别采用碱性过硫酸钾-紫外分光光度法、紫外分光光度法、纳氏试剂分光光度法、N-(1-萘基)-乙二胺分光光度法测定;COD采用重铬酸钾法测定;DO通过便携式溶解氧测定仪(HACH,美国)测定;pH采用便携式pH计(6010 m,JENCO)测定。通过电感耦合等离子体光发射光谱法(ICP-OES,PerkinElmer Optima 2100 DV)测定铁刨花的组分和溶出情况。EPS采用热提取法提取,用Lowry法〔19〕测定EPS中的蛋白质(PN)和腐殖酸(HA),用蒽酮-硫酸法〔20〕测定EPS中的多糖(PS)。采用INT-甲臜法测定微生物电子传递活性(ETSA)〔21〕。未使用和反应后Fe0的形态及组成变化通过扫描电镜-能量色散光谱仪(SEM-EDS,日立SU8100,日本)表征,以X射线衍射技术(Bruker D8 advance,德国)分析未使用和反应后Fe0铁化合物的变化。使用SPSS软件(25.0版,IBM)进行数据统计分析。
1.4 高通量测序
高通量测序委托上海派森诺生物科技股份有限公司。对筛选的菌株进行DNA提取和PCR扩增,采用正引物338F(5’-ACTCCTACGGGAGGCAGCA-3’)和反引物806R(5’-GGACTACHVGGGTWTCTAAT-3’)扩增16S rRNA基因V3~V4区。在Illumina Novaseq 6000平台进行建库和16S rRNA基因测序。将R0和R1中污泥的原始序列提交至美国国家生物技术信息中心(NCBI),登录号为PRJNA 946941。
2 结果与讨论
2.1 COD/NO3--N对Fe0混养反硝化脱氮效果的影响
两组反应器连续运行96 d,研究了不同进水COD/NO3--N对Fe0及碳纤维强化Fe0混养反硝化脱氮性能的影响,结果见图2。

图2 不同COD/NO3--N下TN、NO3--N、NO2--N、NH4+-N、COD、DO及pH变化Fig.2 Variations of TN,NO3--N,NO2--N,NH4+-N,COD,DO and pH versus different COD/NO3--N
由图2可以看出,在阶段Ⅰ(第1天至第15天)中无碳源投加,进水COD/NO3--N为0,R0的TN及NO3--N平均去除率为38.62%和43.75%,R1的TN及NO3--N平均去除率为59.72%和70.93%。此阶段体系发生Fe0自养反硝化,R0和R1均有一定的脱氮效果,且R1中TN及NO3--N平均去除率显著高于R0,表明在无外加有机碳源的条件下,碳纤维的投加有效促进了Fe0自养反硝化的脱氮效率。此阶段R0和R1中均有少量NO2--N积累,平均质量浓度为4.05 mg/L和5.00 mg/L〔图2(c)〕,且由于Fe0发生异化硝酸盐还原〔22〕,使少量NO3--N转化为NH4+-N〔图2(d)〕。在阶段Ⅱ(第16天至第31天)、阶段Ⅲ(第32天至第47天)将COD/NO3--N分别提升至0.5~0.6和0.8~1.0。R0和R1中TN及NO3--N的平均去除率较阶段Ⅰ均有所降低,较低的外加碳源投量无法获得稳定高效的混养反硝化脱氮效率。Fe0表面形成铁氧化物使得Fe0腐蚀供电子的能力下降,抑制了Fe0自养反硝化作用。值得注意的是,R1的TN及NO3--N去除率均明显高于R0,表明碳纤维可强化Fe0腐蚀。两阶段均未观察到NH4+-N、NO2--N的显著积累,表明体系未发生明显的异化硝酸盐还原。
在阶段Ⅳ(第48天至第63天)将COD/NO3--N提高至1.8~2.1。R0的TN及NO3--N平均去除率分别为57.12%和61.91%,R1的TN及NO3--N平均去除率提高至67.69%和73.96%。此阶段R0和R1再次出现少量NO2--N积累,NO2--N平均质量浓度分别为3.71 mg/L和3.74 mg/L,这表明大幅提高体系电子供给量可以激发微生物硝酸盐还原酶活性。在阶段Ⅴ(第64天至第79天)将COD/NO3--N提高至2.9~3.1,R0的TN及NO3--N平均去除率提升至80.99%和91.46%,R1的TN及NO3--N平均去除率进一步提升至89.04%和97.13%,此时已形成稳定的混养反硝化体系。此外,R1的NO2--N平均积累量为2.11 mg/L,低于R0的NO2--N平均积累量4.52 mg/L,这是由于碳纤维可进一步促进Fe0腐蚀,NO3--N几乎被完全还原,NO2--N还原过程中可利用电子相对较多。系统运行至第16天开始投加碳源,在阶段Ⅳ时COD/NO3--N提高到1.8~2.1,R0和R1中COD平均去除率分别为80.62%和85.59%,在阶段Ⅴ时COD/NO3--N提高到2.9~3.1,R0和R1中COD平均去除率分别为82.32%和86.65%。表明在缺氧环境下,反硝化过程对外加碳源利用较为充分,因此这两阶段脱氮效率较高。由此推断,碳源投加量增加及碳纤维材料的投加可消除铁氧化产物覆盖所导致的Fe0腐蚀速率及反硝化效率降低的问题,进而强化Fe0自养反硝化。
保持COD/NO3--N为2.9~3.1的条件下,在运行阶段Ⅵ(第80天至第95天)将HRT降低至12.0 h,与前一阶段相比,R0的TN及NO3--N平均去除率下降至69.48%和79.73%,R1的TN及NO3--N平均去除率下降至80.26%和90.25%。结果表明,HRT对自养反硝化效果影响较大,较低的HRT不利于生长速率慢的铁自养反硝化菌在反应器中持留。R1的TN及NO3--N平均去除率显著高于单独投加Fe0的R0,表明此阶段碳纤维对Fe0混养反硝化过程的强化作用依旧显著。
如图2(f)所示,COD/NO3--N的提升使得异养反硝化微生物大量消耗DO,并使反应器内长时间维持较低DO浓度水平。由图2(g)可以看出,随着COD/NO3--N的提高,两反应器pH出水不断提高,在阶段Ⅴ时R0、R1的出水维持在8.51、8.58左右,出水pH偏高可能是异养及铁自养反硝化产碱所致。因此,可将pH和DO的变化规律作为反硝化体系稳定性的监测参数。
2.2 污泥特性变化
2.2.1 EPS变化
为探究不同COD/NO3--N和碳纤维投加对Fe0混养反硝化体系内污泥EPS的影响,测定了脱氮效果差异显著的阶段Ⅲ~阶段Ⅴ各反应器中污泥EPS含量及组分。
由图3可知,随着COD/NO3--N的提高,R0和R1的LB-EPS和TB-EPS含量均显著上升。当进水COD/NO3--N达到2.9~3.1时,R0污泥中单位质量VSS的LB-EPS和TB-EPS分别升高至50.64 mg/g和107.71 mg/g,R1污泥中单位质量VSS的LB-EPS和TB-EPS分别升高至81.97 mg/g和145.00 mg/g。LB-EPS、TB-EPS中具有促进反硝化电子传递的蛋白及腐殖酸含量亦呈升高趋势〔23〕。由于Fe0释放的电子由胞外向胞内转移,因而EPS及其蛋白质、腐殖酸的提升可促进其胞外电子转移,进而提升Fe0自养反硝化。
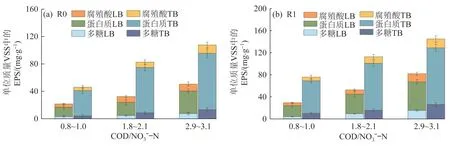
图3 不同COD/NO3--N条件下R0(a)及R1(b)内EPS组成和含量变化Fig.3 Variations of EPS composition and content in R0( a) and R1( b) under different COD/NO3--N
对比R0和R1,R1的污泥EPS含量显著高于R0。由于碳纤维具有络合Fe3+的能力,对带负电荷的微生物有较强的黏附及固定作用,从而促进EPS的产生〔24〕;同时碳纤维可强化Fe0腐蚀,促使R1产生更多的Fe3+,进一步刺激EPS的产生〔25〕。这与R1比R0具有更高的脱氮效率相一致(图2)。
2.2.2 电子传递活性变化
ETSA用于表征微生物胞内电子转移活性,从而间接反映反硝化电子传递活性〔26〕。为进一步研究COD/NO3--N及碳纤维对Fe0混养反硝化体系电子传递的影响,分析了阶段Ⅲ~阶段Ⅴ时R0和R1的ETSA水平(以单位时间单位质量VSS产生O2的质量计),结果见图4。

图4 不同COD/NO3--N条件下各反应器ETSA变化Fig.4 Variations of ETSA in each reactor under different COD/NO3--N
由图4可知,进水COD/NO3--N对Fe0混养反硝化系统中电子传递活性有显著影响。当进水COD/NO3--N由0.8~1.0增加至2.9~3.1时,R0中单位质量污泥的ETSA由4.34 µg(/g·h)增加至40.52 µg(/g·h),R1的ETSA由9.24 µg(/g·h)增加至46.84 µg (/g·h)。结合前述随进水COD/NO3--N增加混养反硝化效率提升的现象,表明提高COD/NO3--N可促进体系ETSA,有利于反硝化脱氮。对比R0与R1,R1体系内ETSA显著高于R0,表明碳纤维材料的投入可进一步提升ETSA水平,强化Fe0混养反硝化脱氮效率。
2.3 Fe0形态及组分变化
Fe0是自养反硝化电子供体,其表面形貌、组分的变化与体系反硝化脱氮效果直接相关。为此对比分析了未使用的铁刨花及R0、R1反应后铁刨花的外观形态及组分变化,结果见图5和表3。
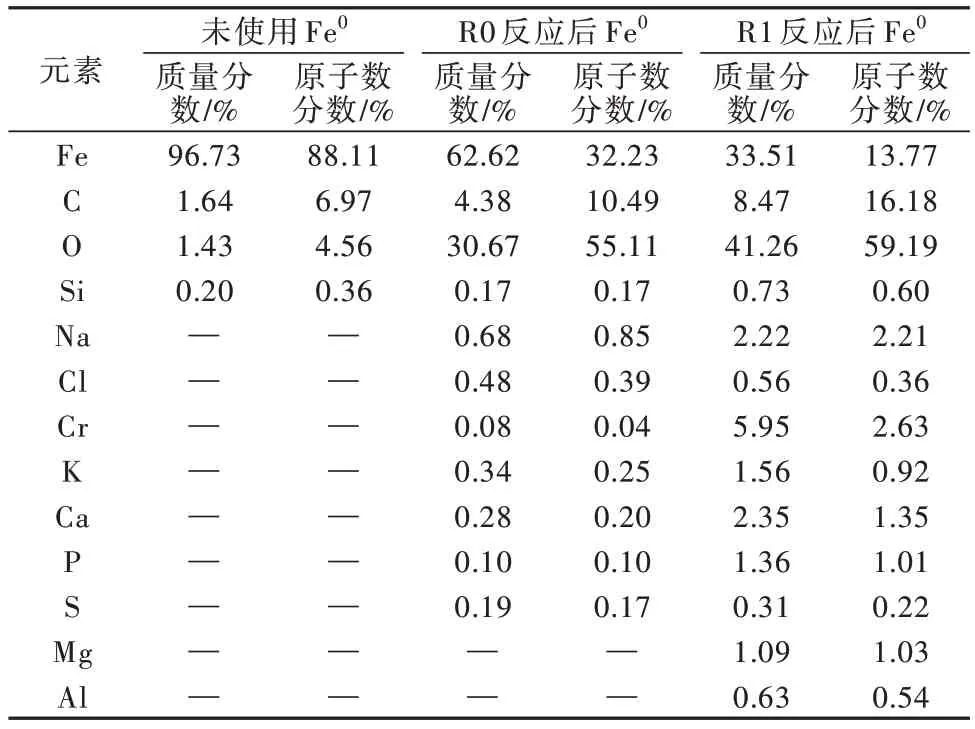
表3 未使用Fe0、R0及R1反应后Fe0的EDS分析Table 3 EDS analysis of Fe0 before and after used in R0 and R1

图5 未使用的铁刨花及R0、R1反应后铁刨花的外观形态Fig.5 Surface morphology images of Fe0 before and after used in R0 and R1
根据图5(a)~图5(c)可知,与未使用的Fe0材料相比,R0中Fe0表面形成突出的红锈,且与材料之间黏连紧密,发生明显板结现象,导致Fe0腐蚀供电子能力减弱,这也是R0在阶段Ⅱ~阶段Ⅲ脱氮能力降低的潜在原因(图2)。R1中Fe0表面呈黑色,未出现显著的黏连、板结现象。由于R1中Fe0表面被碳纤维包裹,削减了进水DO的氧化作用。同时,Fe0与碳纤维形成微观原电池加速电子介导活性,进一步抑制了Fe0的氧化腐蚀〔27〕。SEM表征结果发现〔图5(d)~图5(g)〕,未使用的铁刨花表面光滑平整,参与混养反硝化后,R0中Fe0表面被部分腐蚀。与R0不同,在R1中反应后的Fe0表面发生明显的腐蚀现象,呈皴裂状,表明碳纤维与Fe0的电化学腐蚀作用强于DO氧化腐蚀。通过比较R0和R1中Fe0的形态变化,可以得出,碳纤维显著强化了Fe0腐蚀,使得R1具有更高的反硝化脱氮率(图2)。
由表3可知,未使用的Fe0表面Fe元素质量分数和原子数分数分别为96.73%和88.11%,O元素质量分数和原子数分数分别为1.43%和4.56%。R0反应后Fe0表面Fe元素质量分数和原子数分数分别为62.62%和32.23%,O元素质量分数和原子数分数分别为30.67%和55.11%,表明R0反应后Fe0被铁氧化产物包埋,导致其Fe元素含量降低,O元素比例增加。R1反应后Fe0表面Fe元素质量分数和原子数分数分别为33.51%和13.77%,O元素质量分数和原子数分数分别为41.26%和59.19%,R1反应后Fe0表面Fe元素含量显著减少且远低于R0,同时O元素比例增加,表明碳纤维材料有效促进了Fe0的腐蚀,这与前述碳纤维强化Fe0混养反硝化脱氮效率更高相一致(图2)。此外,由于碳纤维附着于Fe0表面,导致R1中C元素含量较高。少量Na、Cl、Cr、K、Ca等元素可能来自配水成分或活性污泥。同时,R1中Fe0表面还包含Mg、Al元素,这可能是由于Fe0产物和碳纤维形成的复合材料的吸附作用〔28〕。
对比分析了未使用的铁刨花及R0、R1反应后铁刨花表面物质的XRD,结果见图6。
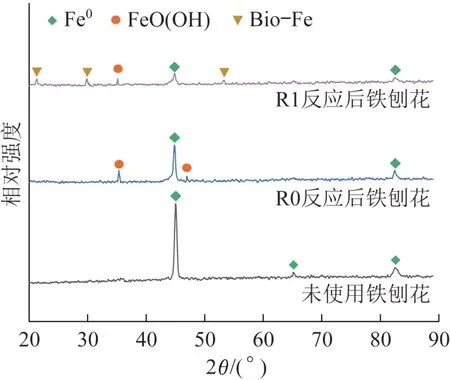
图6 未使用、R0和R1反应后Fe0的XRDFig.6 XRD patterns of Fe0 before and after used in R0 and R1
由图6可知,未使用的铁刨花表面主要存在单质Fe(2θ为44.8°、65.2°、82.5°)〔29〕。在参与混养反硝化后,由于Fe元素被氧化,从零价铁转化为Fe2+或Fe3+,R0和R1的铁刨花中单质Fe的峰强度显著下降。R0中反应后的Fe0表面Fe元素主要以FeO(OH)(2θ为35.3°、46.8°)的形式存在,可能由Fe2O3、Fe3O4等氧化物转化而来〔30〕。而R1中反应后的Fe0表面包括FeO(OH)(2θ为35.3°)和含铁有机复合物(Bioorganic-Fe complexes)(2θ为21.2°、29.9°、53.1°),且FeO(OH)峰强较弱。含铁有机复合物是指生物有机质与铁化合物的络合物,常在EPS中发现〔31〕。外加有机碳源与碳纤维促进R1中EPS增加,参与了Fe0自养反硝化的电子介导作用,从而生成了含铁有机复合物,其对微生物的生长有一定促进作用。结合前述SEMEDS结果可知,碳纤维的投加可显著促进Fe0的腐蚀,提高体系脱氮效率。
2.4 微生物群落结构及功能基因
通过微生物群落结构变化进一步分析不同COD/NO3--N和碳纤维强化Fe0对群落结构的影响。研究了阶段Ⅲ~阶段Ⅴ这3个阶段R0和R1中微生物群落结构,AR0、AR1为阶段Ⅲ的污泥样品,BR0、BR1为阶段Ⅳ的污泥样品,CR0、CR1为阶段Ⅴ的污泥样品。微生物多样性分析结果见表4。

表4 各反应器微生物群落丰富度和多样性分析Table 4 Microbial community richness and diversity analysis in each reactor
由表4可知,Goods-coverage的范围为0.962~0.982,表明测序结果可以有效反映微生物群落的真实情况。其中,Observed-species和Chao1表征丰富度,随着COD/NO3--N由0.8~1.0提高至2.9~3.1,R0体系污泥的Observed-species和Chao1分别从2 103.60和2 389.84降至1 441.80和1 920.16,R1体系污泥的Observed-species和Chao1分别从2 231.20和3 142.84降至1 270.90和1 709.30,各样品丰富度显著下降,表明提高COD/NO3--N有利于优势反硝化微生物的富集;提高进水COD/NO3--N至1.8~2.1和2.9~3.1,R1体系污泥的Observed-species和Chao1显著低于R0,表明碳纤维材料的投加强化了反硝化群落的稳定性。而Shannon表征多样性,CR1的Shannon降至最低为6.717 88,表明阶段Ⅴ时R1内反硝化微生物富集程度最高,与R1在阶段Ⅴ时优异的脱氮性能相一致(图2)。以上结果表明,碳纤维的投加与外加有机碳源投加量的提高对混养反硝化系统中优势菌种的富集具有促进作用。
图7为各反应器中阶段Ⅲ~阶段Ⅴ这3个阶段污泥在门水平、属水平和功能基因分布。
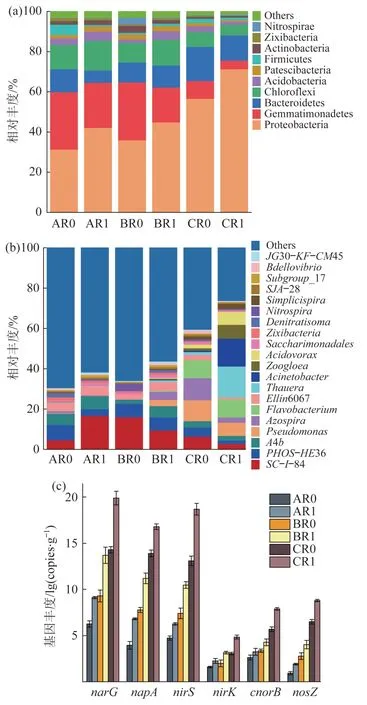
图7 各反应器门水平(a)、属水平(b)和功能基因(c)分布Fig.7 Distribution of bacteria presented in each reactor at phylum level (a),genuslevel (b) and functional genes (c)
从门水平分析〔图7(a)〕,变形菌门(Proteobacteria)是Fe0混养反硝化体系的优势菌门,是典型的异养反硝化细菌〔32〕。随着COD/NO3--N的提高,各反应器污泥中Proteobacteria的相对丰度均显著提升。当COD/NO3--N提高到2.9~3.1时,R0污泥中Proteobacteria相对丰度提高至56.64%,R1污泥中Proteobacteria相对丰度提高至71.33%,与TN及NO3--N去除规律基本一致(图2)。R1中污泥在3个阶段的Proteobacteria相对丰度显著高于R0,表明碳纤维的投加有效促进了异养反硝化微生物的富集。
从属水平分析〔图7(b)〕,前5种丰度较高的菌属为SC-I-84菌属、PHOS-HE36菌属、A4b菌属、假单胞菌属(Pseudomonas)及固氮螺菌属(Azospira)。其中SC-I-84菌属、PHOS-HE36菌属、A4b在R0中的相对丰度高于R1中污泥,表明投加碳纤维材料使得R1中污泥对混养反硝化体系中的优势菌种具有选择性。而Pseudomonas、Azospira相对丰度总体随进水COD/NO3--N的提高而增加。Pseudomonas是一种具有混合营养和异养反硝化能力的菌属〔33〕,并能利用Fe0发生自养反硝化,在COD/NO3--N为2.9~3.1时,Pseudomonas在R0和R1污泥中的相对丰度分别高达10.37%和6.53%。Azospira是一种具有氧化Fe0同时还原NO3--N功能的自养反硝化菌属〔34〕,当进水COD/NO3--N增至2.9~3.1时,在R0污泥中,其丰度增加至10.96%。此外,不动杆菌属(Acinetobacter)在各反应器运行至阶段Ⅴ时的污泥中相对丰度较高,分别为0.69%和13.80%,该菌属可通过Fe0自养反硝化作用去除NO3--N〔35〕,在R1污泥中的相对丰度显著高于R0,表明碳纤维材料的投加显著促进了Fe0自养反硝化微生物的富集。以上结果表明,碳源的投加不仅提高异养反硝化作用及其优势菌的相对丰度,同时促进了Fe0自养反硝化;碳纤维的投加强化了Fe0自养反硝化,使具有Fe0自养反硝化作用的优势菌丰度进一步增加。
反硝化功能基因的丰度可以反映反硝化细菌的脱氮能力,在阶段Ⅲ~阶段Ⅴ这3个阶段对R0和R1中的污泥样进行反硝化功能基因定量分析,相关结果如图7(c)所示。narG和napA编码硝酸盐还原酶,nirK和nirS编码亚硝酸盐还原酶,cnorB及 nosZ分别编码一氧化氮还原酶及一氧化二氮还原酶。随着进水COD/NO3--N的提高,两个反应器的反硝化功能基因丰度也不断提高,当COD/NO3--N为2.9~3.1时丰度达到最高,说明此时体系有更多的反硝化功能酶来提高混养反硝化脱氮率。在各COD/NO3--N条件下,R1各功能基因的丰度显著大于R0,碳纤维材料的投加显著提高了反硝化功能基因的丰度,这与前述微生物群落结构特征相一致〔图7(b)〕,再次阐明了碳纤维对Fe0混养反硝化脱氮的强化作用。
3 结论
1)碳纤维对Fe0混养反硝化脱氮具有显著强化作用,在COD/NO3--N为2.9~3.1、HRT为24 h的条件下,TN及NO3--N平均去除率分别高达89.04%和97.13%,显著高于单独投加Fe0的系统。
2)随着进水COD/NO3--N的提高,具有促进反硝化电子传递的蛋白质及腐殖酸含量呈升高趋势,促进ETSA提升,碳纤维的投加可进一步促进EPS的合成,碳纤维强化了Fe0混养反硝化体系内微生物对电子的利用率,提高体系反硝化脱氮效率。
3)Fe0形态及组分变化表明,单独投加Fe0反应器内Fe0反应后表面形成突出的红锈,有局部腐蚀的现象,表面铁氧化物较多,主要以FeO(OH)的形式存在;而投加碳纤维和Fe0反应器内Fe0反应后表面呈黑色皴裂状,发生明显腐蚀现象,表面腐蚀氧化物更多,除FeO(OH)外还有含铁有机复合物,说明碳纤维不仅促进Fe0的深度腐蚀,还可促进铁的生物反应。
4)据微生物群落及反硝化功能基因变化规律,COD/NO3--N的提高和碳纤维的投加有利于反硝化微生物富集,强化反硝化菌群的稳定性,显著促进了异养反硝化菌属及动杆菌属(Acinetobacter)等铁自养反硝化相关菌属丰度;并提高体系内反硝化功能基因的丰度,使体系具有更强的反硝化能力。

