三聚氰胺固化单宁微球的制备及其吸附性能研究
梁力丽,代玉兰,于婷婷,何花,刘琦
(1.四川幼儿师范高等专科学校,四川 绵阳621000)2.鄂尔多斯市农畜产品质量安全中心,内蒙古 鄂尔多斯 017000)
0 引言
随着石化资源的日益枯竭以及人们对环境保护的意识的提高,核能作为一种清洁的高效能源,逐渐成为双碳目标下能源转型的重要能源而得到了极大的发展。
铀是核能开发中最重要的一种基础原料。无论是铀矿的开采,含铀原料的使用以及核工业的发展均会产生大量的含铀废水。铀元素属于放射性重金属元素,一般以六价(UO2+2)[1]的形式存在,会对环境和生物造成很大的危害。因此含铀废水的有效处理对环境保护和人体健康至关重要。
目前,从含铀废水中浓缩和分离铀的工艺方法主要有离子交换法[2]、吸附法[3]和电化学方法[4]等。其中吸附法具有价格低廉、原料来源广、操作简单、吸附效率高和应用范围广等优点被广泛用于含铀废水处理。
1 材料与方法
1.1 材料与设备
1.1.1 药品/试剂
三聚氰胺(AR,成都科龙化工试剂有限公司),杨梅单宁(77%,广西百色林化提供),戊二醛(50%,核工业北京化工冶金研究院),硝酸铀酰(99%,湖北楚盛威化工有限公司),偶氮胂III(AR,上海梯希爱化成工业发展有限公司),盐酸(37%,成都科龙有限公司),冰乙酸(AR,成都科龙化工试剂有限公司),乙酸钠(AR,成都科龙化工试剂有限公司)。
1.1.2 仪器设备
U-3900型紫外-可见分光光度计(日立高技术有限公司),激光粒度分析仪(美国Brookhaven仪器公司),UItra55高分辨冷场发射扫描电镜系统(德国Carl Zeiss公司),Nicolet-6700傅里叶红外光谱仪(赛默飞世尔科技(中国)有限公司)。
1.2 实验方法
1.2.1 三聚氰胺固化单宁微球的制备
用量筒量取200 mL超纯水于500 mL三口烧瓶中,用机械搅拌器搅拌,并将水浴锅加热至80℃;准确称取2.5 g三聚氰胺加入三口烧瓶中,加热搅拌使三聚氰胺溶解;同时,准确称取2.5 g杨梅单宁溶于50 mL超纯水形成单宁溶液,待三聚氰胺充分溶解后缓慢加入杨梅单宁溶液,控制pH=7~8;80℃水浴搅拌20 min,溶液保持澄清透明,然后滴加5 mL 37%戊二醛,保持温度80℃反应40 min,利用曼尼希反应,实现杨梅单宁与三聚氰胺的交联,形成MA-T微球,得到棕色悬浊液。随后,将交联过后的微球悬浮液离心,用乙醇和纯热水交替洗涤后,在55℃下干燥24 h即得三聚氰胺固化单宁微球(MA-T)吸附剂。
1.2.2 批量吸附实验
称取一定量的硝酸铀酰,加入适量水溶解定容后,配制成一定浓度的铀吸附液,并调pH至测试条件(pH为1~6)。
取50 mL铀原液于锥形瓶中,准确称取一定量的MA-T微球吸附剂,置于锥形瓶中,每个条件设置三个平行样,密封后于恒温振荡培养箱中,一定温度下振荡吸附24 h。吸附结束,将试液过滤后,用紫外-可见分光光度计测量吸附前后铀的吸光度。
在NX软件平台,利用Menu Script工具编辑满足用户的菜单样式。设计人员用记事本创建和编辑扩展名为*.men的文件,即可得到相应的菜单形式。
以材料吸附量为吸附性能评价指标,研究pH、投料量、吸附时间、初始浓度和温度五个因素对于MA-T吸附剂吸附性能的影响,并对吸附热力学和吸附动力学模型进行拟合,推测吸附机理。
2 结果分析
2.1 三聚氰胺固化单宁微球的结构分析
三聚氰胺(MA),杨梅单宁(T)和三聚氰胺固化单宁微球(MA-T)红外吸收光谱如图1所示。纯三聚氰胺在3 469 cm-1和3 419 cm-1附近有较强的-NH2特征吸收峰,而在和杨梅单宁固化成微球后,-NH2特征峰消失,并出现了3 377 cm-1处羟基的伸缩振动,说明在微球制备过程中-NH2已被戊二醛充分交联。在2 935 cm-1附近,MA-T出现了新峰,此特征峰为-CH2不对称伸缩振动,说明在MA-T微球成型过程中戊二醛和三聚氰胺羟甲基化后与杨梅单宁交联反应成球,此特征峰为交联成球后,戊二醛中的亚甲基所引起的。纯三聚氰胺在814 cm-1附近存在较强的三嗪环的特征吸收峰,而MA-T微球在813 cm-1附近也存在较强的三嗪环的特征吸收峰,并且纯杨梅单宁中并不存在三嗪环吸收峰,说明三聚氰胺中的三嗪环被有效保留,MA-T微球在制备过程中保持了三嗪环的稳定。

图1 MA-T微球红外光谱对比图
2.2 三聚氰胺固化单宁微球的形貌分析
通过粒径分布、比表面积及扫描电镜分析MA-T的微观形貌及其物理性能。MA-T微球粒径分布结果如图2(a)所示。由图可知,制备的MA-T微球有效直径为212.0 nm,多分散系数为0.005。说明所制备的MA-T微球为平均直径212.0 nm左右的纳米微球,且多分散系数较小,粒径相对比较均一。如图2(b)所示,为三聚氰胺固化杨梅单宁微球扫描电镜图,同样证明了MA-T为几百纳米的微球,且容易团聚。

图2 MA-T微球(a)粒径分布图和(b)SEM图
通过BET比表面积测试的到MA-T微球BET比表面积为146.13 m2/g,具有较高的比表面积,赋予MA-T微球上更多的活性基团能更好的与目标铀酰离子结合。
2.3 三聚氰胺固化单宁微球的铀吸附性能
2.3.1 pH的影响
pH值所引起的酸效应对金属离子的配位作用影响较大,影响吸附剂对金属离子的配位结合,进而影响吸附剂的吸附效果。因此,在pH值为2~6的范围内,探讨MA-T微球吸附剂对铀酰离子的吸附性能。实验结果如图3(a)所示。MA-T微球的吸附效果随着pH值的增大呈上升趋势,在低pH条件下,MA-T结构中的活性基团如-NH2进一步质子化形成-NH+3,酚羟基极性减弱,而铀在pH<3的水溶液中以UO2+2形式存在,带正电荷的铀酰离子与质子化的-NH+3由于静电斥力而导致吸附几乎为零。在pH增加到4以上时,MA-T中-NH2质子化减弱,更有利于-OH等活性基团与铀的配位作用。在pH=5.8时达到测试范围内最大值,随后吸附效果下降。说明在这个范围内pH=5.8时MA-T微球吸附效果最好,此时吸附容量为83 mg/g。因此,在后续的吸附实验中,我们均选取pH值为5.8作为实验条件。

图3 (a)pH值对MA-T微球吸附铀酰离子的影响(C0=20 mg/L,pH=2.0~6.0,投料量:0.01 g,T=298.15 K,t=24 h);(b)吸附剂用量对MA-T微球吸附铀酰离子的影响(C0=20 mg/L,pH=5.8,投料量:0.002~0.3 g,T=298.15 K,t=24 h);(c)铀初始浓度对MA-T微球吸附铀酰离子的影响(C0=20-200 mg/L,pH=5.8,投料量为0.01 g,T=288.15-328.15 K,t=24 h);(d)吸附时间对MA-T微球吸附铀酰离子的影响
2.3.2 投料量的影响
在吸附剂的实际使用中,不仅对吸附剂的吸附效果有一定要求,而且要考虑到吸附剂的利用率。为了探究在不同投料量下的MA-T微球的吸附特性,用醋酸和醋酸钠准确调节浓度为20 mg/L的铀溶液pH到5.8,且每个投料量条件下取50 mL铀原液,分别加入0.002、0.005、0.01、0.05、0.1、0.2、0.3g MA-T微球,每个条件设置三个平行样,在25℃,摇速160 rpm条件下振荡吸附24 h。实验结果如图3(b)所示。
从图3(b)中可以看出,随着投料量由0.002 g增加到0.05 g,吸附容量从238 mg/g迅速下降到18 mg/g。这是因为随着吸附剂用量增大,在一定的铀初始浓度下,平均分配给每个吸附剂分子的铀含量减少,即分配给吸附剂分子用于结合铀酰离子的有效活性位点减少,并且吸附剂之间互相碰撞聚结,最终导致单位质量的吸附剂吸附U(VI)的量减少。同时去除率随着投料量的增加而增大,在投料量为0.05 g时,去除率达到最大为99.86%;之后随着投料量的增加,去除率保持恒定不变。这是因为随着吸附剂量的增加,总的吸附剂活性位点增多,以至于基本能达到对U(VI)的完全去除。综合考虑吸附容量和去除率,选取投料量为0.01 g作为后续吸附实验的实验条件。
2.3.3 铀初始浓度的影响
为了探究不同浓度铀原液对MA-T微球对铀酰离子吸附性能的影响,同时探究温度对吸附的影响,分别配制了浓度为20、70、130、190、240 mg/L的铀溶液,并调节其pH为5.8,各取50 mL置于锥形瓶中,分别加入0.01 g MA-T微球,分别放入温度为15、25、35、45、55℃的恒温振荡培养室,设置摇速为160 rpm,吸附24 h。实验结果如图3(c)所示。MA-T微球对铀酰离子的吸附量随铀溶液初始浓度的增加而增大,在测试条件下,当铀浓度为240 mg/L时吸附容量达到最大为426 mg/g。这可能是因为铀溶液的浓度增大时,会增大铀酰离子向材料表面及内部扩散的驱动力,使铀酰离子迅速向材料表面及内部迁移,最终导致与MA-T微球上的活性基团结合的数量增大,即MA-T微球活性基团利用率增大。这与Fick第一定律的规律相吻合。
2.3.4 吸附时间的影响
为了探究不同吸附时长下MA-T微球的吸附特性。准确配制浓度为20 mg/L的铀溶液,调节pH值到5.8,MA-T微球投料量为0.01 g,按照前述吸附测试方法在25℃的恒温振荡培养箱,摇速160 rpm振荡进行吸附实验。分别在吸附0.25、0.5、1、2、3、4.5、6、8、10、12、14、16 h时测试吸附液的吸光度值,并计算吸附容量。实验结果如图3(d)所示。随着吸附时间的增加,MA-T微球吸附量逐渐增大,在8 h达到平衡,此时吸附容量为89 mg/g。在吸附的前3 h内,MA-T微球对铀酰离子的吸附十分迅速,这是因为吸附开始时,MA-T微球表面存在大量活性位点,铀酰离子被活性基团捕获的几率较大;在3~8 h内,MA-T微球的吸附速率明显变缓,这是因为随着铀酰离子与微球表面活性位点的结合,剩余活性位点表少,同时空间位阻增大,铀酰离子与微球活性位点结合就变得困难,吸附速率下降;8 h后,MA-T微球对铀酰离子的吸附达到平衡,吸附容量不再增加,这是因为微球表面活性位点已全部被铀酰离子占用,因此吸附达到平衡。
2.3.5 等温吸附拟合
表1为MA-T微球对铀酰离子的吸附等温模型拟合参数。可以发现,Langmuir模型的线性拟合相关系数要大于Freundlish模型的线性拟合相关系数,说明该吸附过程更符合Langmuir等温吸附模型,说明此吸附过程为吸附剂表面均匀的单层吸附,吸附剂表面局部空位有限、各空位活性相同。

表1 Langmuir和Freundlich模型的线性拟合参数
2.3.6 吸附动力学
MA-T微球吸附剂吸附U(VI)后的准一级动力学和准二级动力学模型拟合结果如表2所示。准一级动力学模型线性拟合后的相关性系数(R2)小于准二级动力学模型的线性拟合。其中,准二级动力学模型线性拟合的相关性系数(R2)为0.999,这表明MA-T微球吸附剂吸附U(VI)的过程更符合线性准二级动力学模型,吸附过程的速控步骤为化学反应,且吸附受到至少2种以上因素影响。据此推测杨梅单宁中-OH和三聚氰胺中的少量-NH2与铀发生了配位作用[7]。

表2 准一级动力学模型和准二级动力学模型的线性拟合参数
2.3.7 吸附机理
由图4可以看出,吸附后在902.4 cm-1处出现了新的吸收峰,是由O=U=O基团的伸缩振动引起的。同时吸附铀酰离子后,单宁上-OH的吸收峰由3 377cm-1移动到3 417cm-1,并且峰形变窄,表明铀酰离子通过酚羟基结合到MA-T微球上。
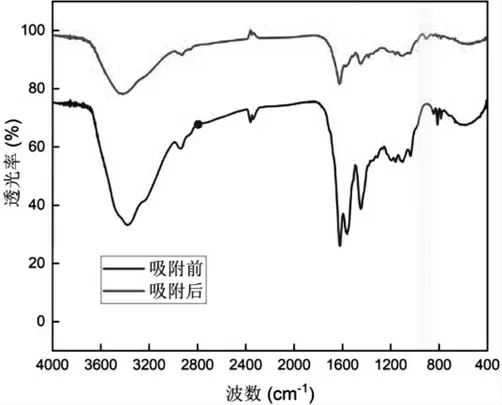
图4 MA-T微球吸附铀酰离子前后红外光谱对比图
3 结论
通过曼尼希反应成功将杨梅单宁交联固化在了三聚氰胺上制成了三聚氰胺固化单宁微球,为粒径约200 nm的纳米微粒,主要通过其表面活性位点-OH等对含铀废水中的铀酰离子进行配位反应达到富集铀的目的,其吸附方式属于单分子层化学吸附。MA-T微球在pH值为5.8条件下对铀酰离子的吸附效果最好。在pH值为5.8、铀初始浓度为240 mg/L、328K下MA-T微球对铀的吸附容量可达426 mg/g。
——“单宁”

