经皮椎间孔镜技术与传统后入路减压植骨融合内固定术治疗老年退行性腰椎管狭窄症的近期疗效比较
杜壮文 欧阳帆 王恩梁 曾繁宽
腰椎管狭窄症属于脊柱外科常见疾病,主要症状包括间歇性跛行、乏力、双下肢逐渐加重的酸痛感,主要发病人群为老年人[1]。目前,临床多采取手术治疗,后入路减压植骨融合内固定术是既往常见手术方式,术后可使病人临床症状得到有效缓解。但该方式需切开病人皮肤、皮下组织及腰背筋膜,对病人后续恢复具有一定影响,且存在并发症。经皮椎间孔镜技术可在椎间孔镜直视下直接切除突出的髓核组织及增生的黄韧带,扩大椎间孔,在不破坏脊柱稳定性的前提下解除神经根的压迫[2]。本研究探讨经皮椎间孔镜技术与传统后入路减压植骨融合内固定术治疗老年退行性腰椎管狭窄症的近期疗效及对骨代谢指标的影响。
对象与方法
一、对象
我院2018年1月~2021年1月收治的老年退行性腰椎管狭窄症病人100例。纳入标准:(1)确诊为退行性腰椎管狭窄症[3];(2)初次确诊并行手术治疗;(3)年龄55~70岁,病例资料齐整;(4)符合对应相关手术指征。排除标准:合并腰椎骨折及全身感染性疾病;具有手术禁忌证;全身恶性肿瘤或重要脏器功能严重不全;精神疾病、认知障碍或治疗依从性较差;因各种原因退出本研究者。依照不同手术方法将其分为观察组和对照组,每组各50例,观察组采用经皮椎间孔镜治疗,对照组采用后入路减压植骨融合内固定治疗。两组基本资料比较,差异无统计学意义(P>0.05)。见表1。
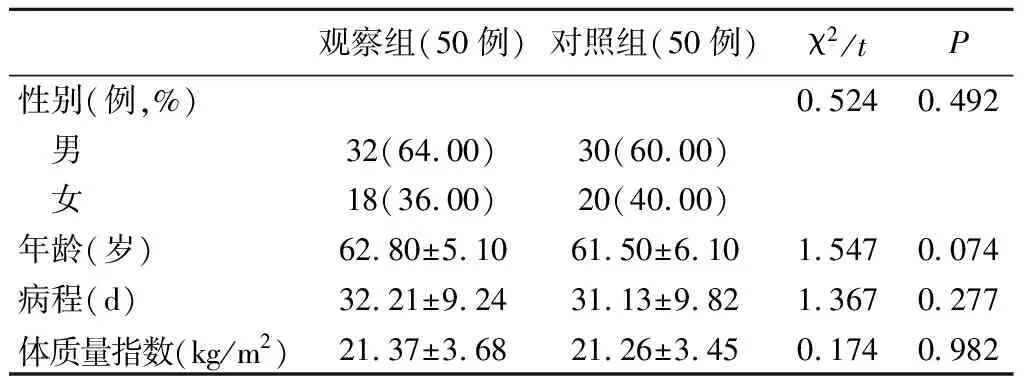
表1 两组病人一般资料比较
二、方法
1.经皮椎间孔镜技术:术前30分钟,通过静脉注射抗生素,侧卧位,采用经皮椎间孔脊柱内镜系统(transforaminal endoscopic spine system,TESSYS)技术标准入路方式,采用C臂机透视,确定穿刺位置,局部麻醉并进行穿刺。穿刺成功后,于关节处注射3 ml利多卡因,通过穿刺针将导丝置入硬膜外间隙,以导丝为中心,将皮肤切开约1 cm,逐级置入扩张管;透视下明确位置,采用环锯逐步打磨扩大椎间孔,同时置入保护套管,放置椎间孔镜,注入造影剂探查椎管责任间隙实际状况,利用椎间孔镜,根据需要使用蓝钳清除盘黄间隙处后纵韧带及黄韧带,使神经根显露,然后逐步摘除突出髓核,并切除上关节突和增生的黄韧带行神经根全程减压,当镜下可见神经根减压明显,硬膜囊恢复自然搏动,无活动性出血,撤出内镜系统,缝合切口。
2.传统后入路减压植骨融合内固定术:病人取侧卧位,C臂机透视,确定穿刺位置,切开皮肤约10 cm,根据病人不同情况,进行半椎切除减压或全椎减压,对神经根管进行扩大,邻近节段后韧带复合体彻底切除,纤维环切开后把病变椎间盘切除并进行植骨融合,连接横杆,并进行加压固定。最后冲洗干净,留置引流管,缝合伤口。
3.观察指标与评价标准:比较两组临床疗效,手术、术后卧床及住院时间和术中失血量;比较两组术前、术后1周及术后3个月腰、腿视觉模拟评分(visual analogue scale,VAS) 评估疼痛等级、Oswestry功能障碍指数(Oswestry disability index,ODI)、日本骨科学会腰痛疾患评定表(Japanese Orthopaedic Association,JOA)评分。参照改良Macnab法评估临床疗效[4]:优:腰腿疼痛症状完全消失,具备正常生活、工作能力;良:腰腿疼痛症状减轻,日常活动轻微受限,不影响正常工作;可:腰腿疼痛症状减轻有所缓解,但活动受限,日常生活、工作受限;差:腰腿疼痛症状加剧或无改善;总有效率=(优+良)/总例数×100%。JOA评分:分值为0~15,分值越高,病人疼痛越轻。ODI评分:范围为0~100%,百分率约低,病人功能障碍越改善。VAS评分:分值0~10分,分数越高表示疼痛程度越严重。于术前、术后1周及术后3个月,采集病人空腹静脉血5 ml,使用酶联免疫法测得病人血清骨特异性碱性磷酸酶(bone-specific alkaline phosphatase,BALP)、骨钙素(Bone γ-Carboxyglutamic Acid-Containing Protein,BGP)、骨形态发生蛋白-2(bovine bone morphogenetic protein,BMP-2)水平。两组病人均随访6个月,记录术后并发症发生情况。
三、统计学方法
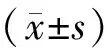
结果
1.两组围手术期临床指标比较见表2。观察组手术、术后卧床、住院时间均短于对照组,术中失血量少于对照组,差异有统计学意义(P<0.05)。

表2 两组围手术期指标比较
2.两组骨代谢指标比较见表3。结果表明,术后1周及术后3个月,两组BGP、BMP-2、BALP水平均高于术前,差异有统计学意义(P<0.05),且观察组均较对照组高,差异有统计学意义(P<0.05)。
表3 两组骨代谢指标比较
3.两组并发症比较见表4。观察组并发症发生率低于对照组,差异有统计学意义(P<0.05)。
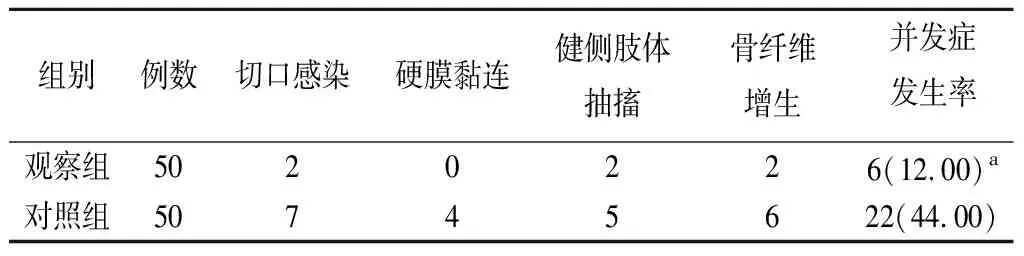
表4 两组并发症比较(例,%)
4.两组临床效果比较:观察组临床总有效率高于对照组(P<0.05)。见表5。
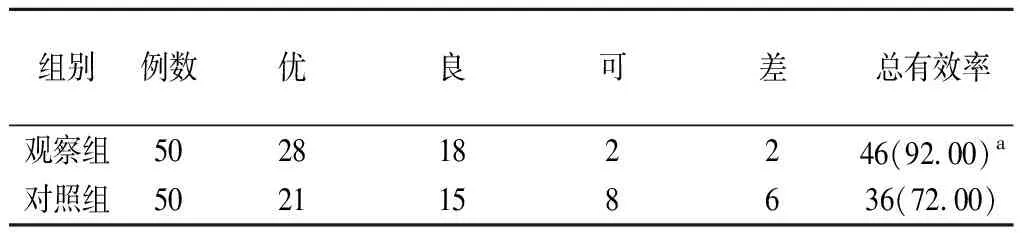
表5 两组临床效果比较(例,%)
5.两组腰、腿VAS、JOA及ODI评分比较见表6。结果表明,观察组术后1周及术后3个月JOA评分高于对照组,ODI及腰、腿VAS评分低于对照组,差异有统计学意义(P<0.05)。

表6 两组JOA及ODI评分比较(分)
讨论
腰椎管狭窄症在老年人中的发病率为1.7%~10%,侧隐窝、椎间孔、中央椎管都有可能发生,以侧隐窝狭窄发病率最高,可引发腰腿疼痛及无力感,可压迫神经,造成神经功能障碍[5]。目前,针对保守治疗一段时间后无明显效果及临床症状较为严重的病人,通过减压术及加固稳定术对症处理均具有一定效果。但传统手术方式治疗易引起如脊神经背支损伤等多种并发症,对病人预后造成不良影响[6]。
椎间孔镜技术是一种内镜脊柱系统技术,其由椎间孔安全三角进入椎间盘,对椎管内进行间接减压,既往主要用于腰椎间盘突出症、椎间孔外侧的极外侧型突出,在中央椎管狭窄、椎间孔狭窄中具有较大局限性。随着内窥镜技术及光学设备的不断发展,经皮内镜的手术适应证也随之发生改变。TESSYS技术可直接通过椎间孔进入椎管内膜外腔,有效松解神经根及硬膜囊压迫部位,其技术特点决定了TESSYS技术可应用于不同类型腰椎管狭窄症的治疗[7]。Huang等[8]采用经皮椎间孔成形术治疗神经根管狭窄症病人,其临床总有效率为86.23%,且VAS评分、ODI指数明显改善。本研究中,观察组临床总有效率较对照组高;观察组手术时间、术后卧床时间、住院时间均短于对照组,术中失血量少于对照组;术后1周及术后3个月,观察组JOA评分高于对照组,VAS、ODI评分低于对照组;观察组并发症发生率为低于对照组。提示在老年退行性腰椎管狭窄症病人中采用经皮椎间孔镜技术进行治疗,可有效降低病人疼痛,改善其腰椎功能,减轻术后并发症发生率,近期疗效较佳。经皮椎间孔镜技术可在微创的前提下,无须分离、牵拉神经根和硬脊膜,有效摘除突出的髓核组织,且可保留黄韧带,避免损伤腰椎,术后腰椎不稳情况及并发症发生率明显降低,利于病人术后腰椎功能恢复[9-10];经皮椎间孔镜技术在手术中可达棘突连线,增加正位深度的同时,使侧位保持在椎体后缘连线前,有效减轻了对脊柱后方结构的影响,且其手术切口明显较传统后入路减压植骨融合内固定术切口小,因而其对病人造成的损伤较小,从而有效改善病人围术期相关指标,利于病人术后恢复[11-12]。
老年退行性腰椎管狭窄症的发生与病人腰椎管部位退变、骨质增生、韧带钙化等密切相关,良好的骨代谢功能可改善病人骨功能。BGP是调节机体骨钙代谢的一种重要蛋白,对判断成骨细胞功能状况具有重要价值。BMP-2是一种高度保守的功能蛋白,在骨骼胚胎发育及再生修复中起重要作用。BALP是一种成骨细胞的代谢活性物质,临床可根据其值的变化来评估成骨功能状况。在本研究中,观察组术后1周及术后3个月BGP、BMP-2、BALP水平高于同期对照组,提示采用经皮椎间孔镜技术对老年退行性腰椎管狭窄症病人进行手术治疗,可促进其骨代谢指标的恢复。与传统后入路减压植骨融合内固定术相比,经皮椎间孔镜技术可有效减少对椎管内结构的干扰,最大限度使脊柱后方结构保持完整,明显减轻了对病人造成的创伤;同时在经皮椎间孔镜技术下,可有效切除突出的椎间盘组织,对神经根进行充分减压,从而利于病人术后快速恢复,促进骨代谢指标恢复正常[13]。
综上所述,经皮椎间孔镜治疗退变性腰椎管狭窄症对病人创伤更小,利于恢复,安全性更高,治疗疗效良好。但该手术方式对手术医生操作技术要求较高,需具备扎实的解剖基础,熟练的操作技术,同时术前需严格掌握病人手术适应证。

