第三届跨区域命题征集活动成果展示(下)
本刊编辑部
1.一种皂化废渣含有CaCO3、Ca(OH)2、Mg(OH)2和SiO2,对其进行综合利用可得到碳酸镁和轻质碳酸钙,实现“变废为宝”。其工艺流程如下,下列说法错误的是
( )
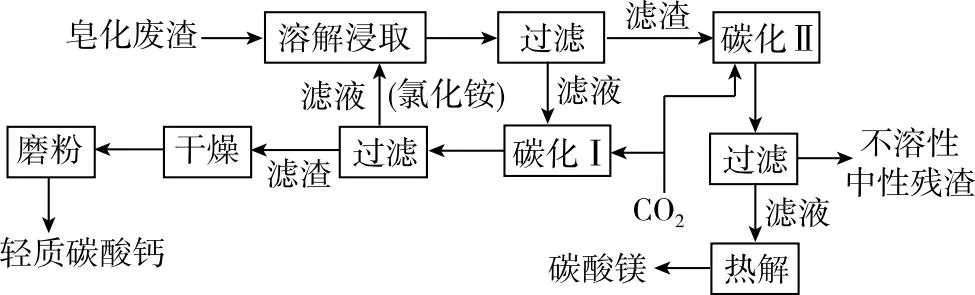
A.“溶解浸取”时可用稀盐酸代替氯化铵,且后续流程不变
C.此工艺不产生有毒有害物质,且有利于实现“碳达峰、碳中和”
D.此工艺中可循环利用的物质有NH4Cl和CO2
【参考答案】A
【命题意图】本题情境选自科技论文成果,属于学术探索情境,以皂化废渣的综合利用为试题情境,实现了“变废为宝”,体现了化学的社会价值。本题考查了物质选择、反应原理、环境保护、循环利用等必备知识。试题解答过程中,需要运用到理解与辨析、分析与推测的关键能力。题目题干和设问都以化学学科核心素养为导向,很好地考查了证据推理与模型认知、宏观辨识与微观探析、科学态度与社会责任的核心素养,引导学生关注化学价值,树立可持续发展意识和绿色化学观念。
【流程分析】
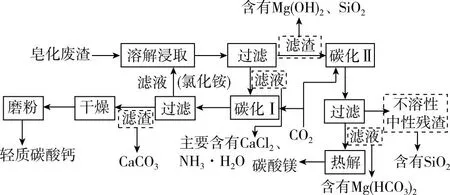
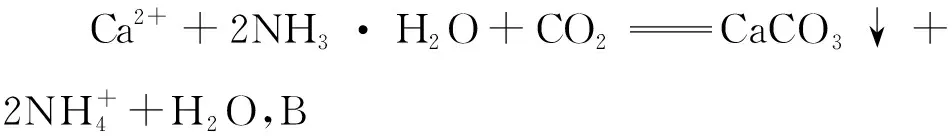
【创新点分析】题干情境选自科技论文,具有一定的新颖性。设问考查角度和形式创新,例如:考查浸取液的类型,浸取液不同(稀盐酸或氯化铵),反应不同,导致后续流程不同,从而体会选用氯化铵浸取的优点;“碳化Ⅰ”反应的书写考查学生前后联系、透过现象看本质的能力;吸收CO2,助力实现“碳达峰、碳中和”,考查环境保护;物质循环利用考查对流程物质转换过程的理解、物质成分的判断,树立绿色化学理念。
河北省石家庄市行唐县职业教育中心 牛聪哲
【试题评语】本题作者命题情境选自科技论文成果,作者以皂化废渣的综合利用为试题情境。试题设问综合,考查了学生理解与辨析、分析与推测等关键能力。题干和设问都以化学学科核心素养为导向,很好地考查了证据推理与模型认知、宏观辨识与微观探析、科学态度与社会责任的学科核心素养。本题选材设计较好,有一定新颖性和价值。
北京教育学院 王春
2.银锌渣中含有Bi、Pb、Ag、Zn、Au等金属,某有色设计研究院利用湿法—火法联合工艺回收银锌渣中Bi、Ag、Au,工艺流程如图。已知:分离混合物中Au单质与从含金的化合物中提取Au单质相比,前者回收率高,回收成本低。流程中加入的物质均过量。
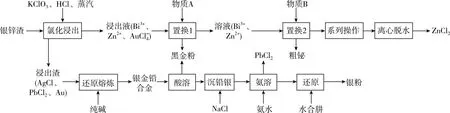
回答下列问题:
(1)通入蒸汽的目的为_______
;
(2)“氯化浸出”中KClO3的作用:_______
________;在实际生产中选择KClO3起始浓度为25 g/L较为适合,请简述理由:_______
;
(3)物质A、B分别是________;
(4)已知“还原熔炼”中碳酸钠与氯化银反应产生两种无色气体,写出该过程的化学反应方程式:________________________;
(5)“酸溶”时,可选择的酸是________;
(6)已知加入水合肼(N2H4·H2O)后微热,写出“还原”过程的离子反应方程式:_______
;
(7)已知ZnCl2的溶解度如表,“系列操作”为_______
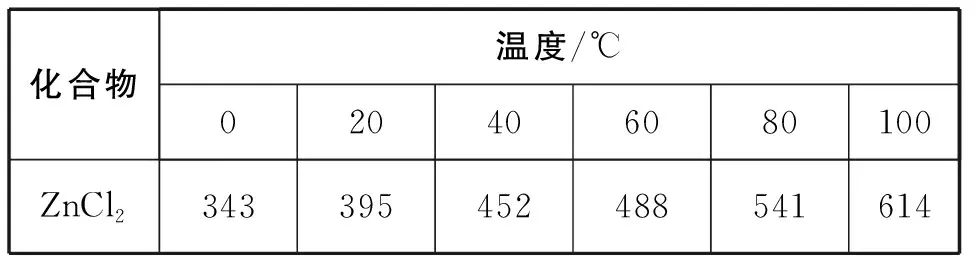
;溶解度/(g/100 g水)
(8)已知:室温下PbCl2的Ksp为1×10-4,AgCl的Ksp为1.8×10-10。若酸溶、过滤后的溶液中含Ag+0.1 mol、Pb2+0.2 mol,加入NaCl溶液充分沉铅银后的溶液体积为100 mL,则需加入含________mol NaCl的溶液。(当溶液中离子浓度≤10-6mol/L时,认为离子完全沉淀去除)。
【参考答案】(1)给氯化浸出过程加热,加快反应速率,使银锌渣充分浸出
(2)做氧化剂,氧化金属单质(提供沉淀所需的Cl-,此作用可以写,也可以不写) 浓度过低,Zn、Bi的浸出率低,不能充分回收;浓度过高,浸出液中溶解的Au增多,不便于Au的回收
(3)Bi、Zn
(5)硝酸(HNO3)

(7)蒸发浓缩、降温结晶
(8)1.5
【命题意图】本题的情境来自真实的文献资料。银锌渣中含有Bi、Ag、Zn、Au、Pb等金属,通过合理科学的方法可以充分回收利用,特别是金、银等贵金属,对于工业有重要的意义。本题重点考查了氧化还原反应、金属元素及其化合物性质等必备知识。本题考查了获取信息、结合氧化还原反应原理基本知识书写陌生方程式的分析与推测能力,流程图理解与辨析能力等,考查了证据推理与模型认知、科学态度与社会责任的学科核心素养。
【流程分析】
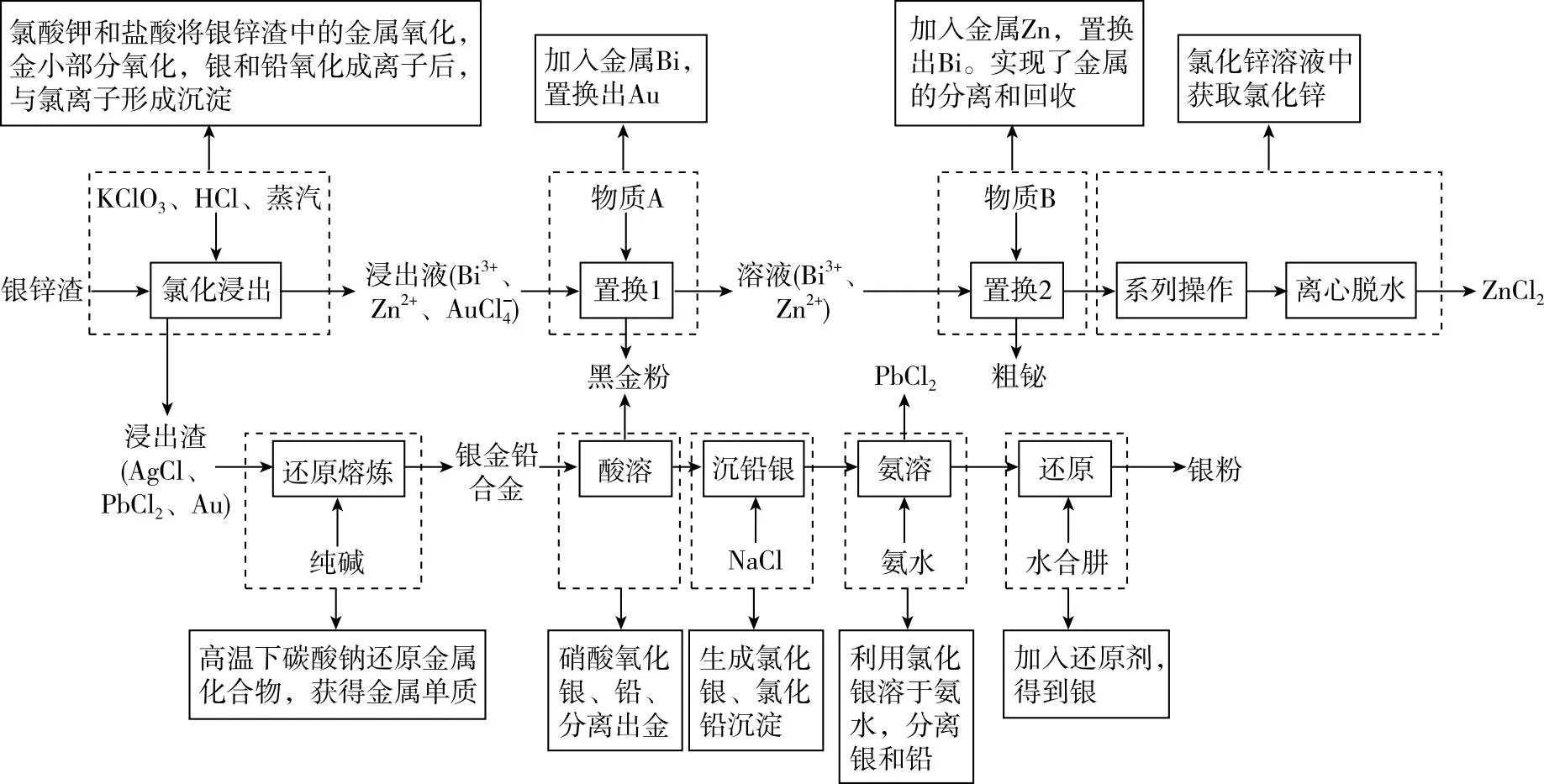
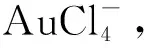
反应需要的Cl-Ag+~Cl-Pb2+~2Cl-
0.1 mol 0.1 mol 0.2 mol 0.4 mol
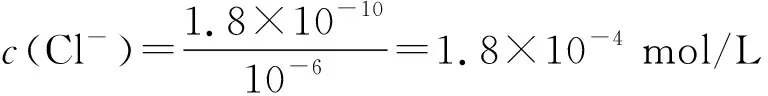
【创新点分析】题干材料真实新颖,集多种金属单质于一体,主要考查了较不活泼的金属回收,有一定的创新性。设问角度有第(1)“蒸汽”的作用,既真实又新颖。第(2)问中“在实际生产中选择KClO3起始浓度为25 g/L”的理由,要从两个方面阐述说明,设问角度新颖。A、B两种金属的分析也是亮点。需要通过流程图中分离金属的顺序分析出金属活动性的强弱顺序,最终确定金属的成分。结合溶解平衡的设问和考查,有一定的创新性和区分度。考查维度多,包括陌生方程式书写、金属还原性比较、金属配合物、溶解平衡、混合物分离提纯等等核心考点。
湖南省长沙市第一中学 熊娟
【试题评语】本题作者命题的情境来自真实的文献资料,对于工业实际生产有着重要的意义。本题作者所设问题重点考查了氧化还原反应、金属元素及其化合物性质等学科必备知识,考查了学生根据试题信息结合氧化还原基本知识书写陌生方程式的分析与推测能力,流程图理解与辨析能力等。同时,试题很好地考查了学生证据推理与模型认知、科学态度与社会责任等学科核心素养。另外,本试题选材新颖,原创性好,考查维度多且试题分析到位。
北京教育学院 王春
3.酸洗可除去不锈钢表面的氧化层,提高不锈钢表面的光亮度且延长不锈钢使用寿命。不锈钢酸洗废水中酸和金属的回收利用,有利于环境保护和不锈钢产业的可持续发展。
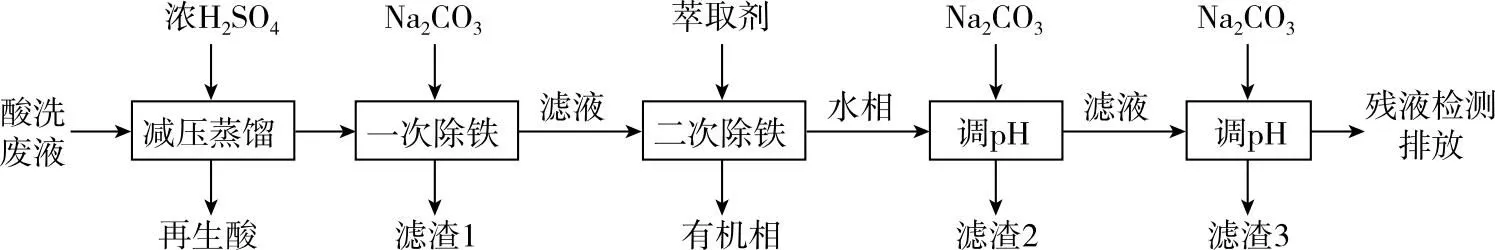
已知:①不锈钢酸洗废水成分如下表所示:
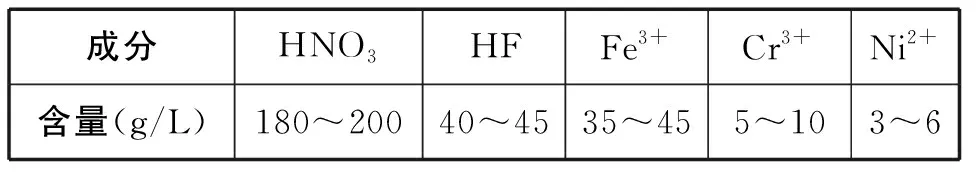
成分HNO3HFFe3+Cr3+Ni2+含量(g/L)180~20040~4535~455~103~6
②相关金属离子生成氢氧化物沉淀时的溶液pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算):

金属离子Fe3+Cr3+Ni2+开始沉淀的pH1.614.226.22沉淀完全的pH2.785.177.54
回答下列问题:
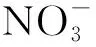
(2)若向除酸后的溶液中加入氢氧化钠溶液,当pH调节为2.78时,铁的沉淀率为98.82%,镍和铬的沉淀率接近100%,与理论上Cr3+、Ni2+在此pH下还没开始沉淀不符,分析原因是_______
_________。
(3)分两次除铁,有利于减少萃取剂的使用量。第一次沉铁采用黄钠铁矾法,加入碳酸钠调节溶液的pH至2,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的离子方程式:_______
;
若pH太小,则黄钠铁矾的产率________(填“偏大” “偏小”或“不变”)。
(4)二次除铁时用正三辛胺(R3N)作萃取剂,磺化煤油作稀释剂,通过有机萃取可以将酸液中残留的铁和镍、铬分离。其主要反应如下:

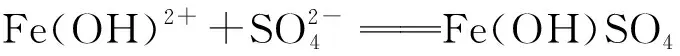


Fe(OH)SO4·(R3NH)2SO4④
pH过大不利于萃取的主要原因是________________。
(5)制得滤渣2时,需要调节溶液的pH范围是________。
(6)已知NiO的晶体结构与NaCl相似,其摩尔质量为M,晶体密度为ρ( g/cm3),则晶胞中Ni和O最近距离为________nm(列出计算式,NA为阿伏加德罗常数)。
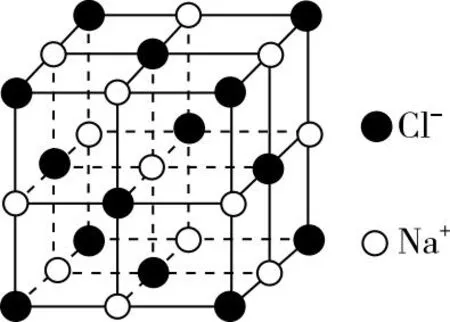
NaCl晶胞
【参考答案】(1)2∶5 平面三角形
(2)三价铁离子水解生成氢氧化铁胶体,有很强的吸附作用,会吸附大量的镍、铬共沉淀

(4)pH过大Fe3+会水解,生成Fe(OH)3难以被萃取
(5)5.17≤pH<6.22
【命题意图】不锈钢酸洗废水中酸和金属的回收利用,有利于环境保护和不锈钢产业的可持续发展。通过真实情境中的物质的分离、提纯,考查学生分析、解决问题的能力。
【流程分析】
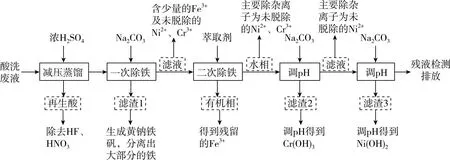
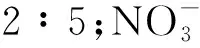
【创新点分析】一、题干材料的设置:选自硕士毕业论文,不锈钢酸洗废水中金属离子的资源化分离回收工艺研究,展示现实生活中存在的资源回收利用问题,创造真实情境,有效检测学生处理问题的能力。
二、设问考查角度:融合了物质结构与性质,考查工艺流程中涉及的基态离子的单电子数之比,阴离子的空间构型,调pH的原因分析,陌生方程式的书写,改变pH对产率的影响分析,晶胞的计算。
三、考查维度:
知识层面:工艺流程、物质的分离与提纯。
能力层面:考查学生接收、整合化学信息的能力。能从提供的新信息中准确地提取实质性的内容。
核心素养层面:考查宏观辨识与微观探析、变化观念与平衡思想、科学探究与创新意识的学科核心素养。1.考查基态Ni2+、Fe3+的单电子数之比,既需要学生熟悉价电子排布式,又要熟悉轨道表示式。2.当pH调节为2.78时,铁、镍和铬均沉淀,与理论上Cr3+、Ni2+在此pH下还没开始沉淀不符,增加学生思考维度。3.分两次除铁,有利于减少萃取剂的使用量,也是给学生一种思路,分离提纯不止一种方法,工业上往往是多种方法综合使用。4.二次除铁时用正三辛胺(R3N)作萃取剂,磺化煤油作稀释剂,通过有机萃取可以将酸液中残留的铁和镍、铬分离。pH过大不利于萃取,打破有机溶剂中不需要调pH的想法。5.制得滤渣2时,需要学生综合分析流程,考虑除去的物质,从表格中提取合适的信息进行填空。
四、设问形式为填空、计算、原因分析。
云南民族大学附属高级中学 罗玉玲
【试题评语】本试题作者题干材料的设置选自硕士毕业论文中有关不锈钢酸洗废水中金属离子的资源化分离回收工艺研究,很好地展示了现实生活中资源的回收利用问题,通过创造真实试题情境,有效检测学生对于实际问题的解决能力。另外,试题的设问很好地融合了物质结构与性质,考查化学工艺流程中涉及的基态离子的单电子数之比,阴离子的空间构型,调pH的原因分析,陌生方程式的书写,改变pH对产率的影响分析和晶体结构中晶胞的计算等核心知识。另外,本道题选材较为新颖,原创性好,作者对试题分析到位。
北京教育学院 王春
4.呋喃甲酸是抗菌素的一种,在食品工业中用作防腐剂,也用作涂料添加剂、医药、香料等的中间体,可用呋喃甲醛在碱性环境下发生交叉的Cannizzaro 反应制备(该反应大量放热)。
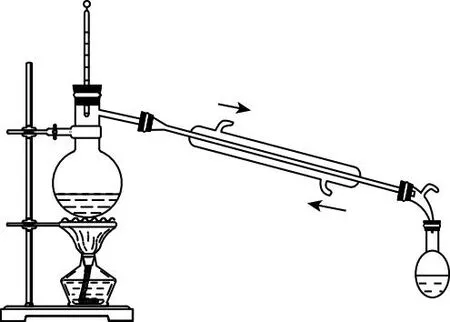
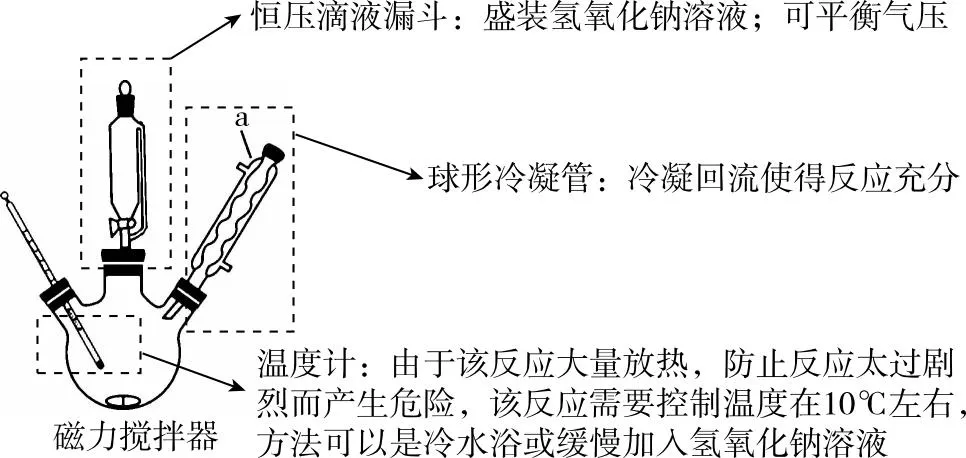
Ⅱ.实验装置:
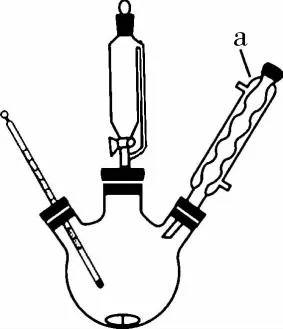
磁力搅拌器
Ⅲ.实验步骤:
Ⅳ.相关信息:
a.几种有机物的性质

名称性状相对分子质量溶解度冷水热水乙醇乙醚呋喃甲醛无色液体96微溶易溶易溶互溶呋喃甲醇无色液体98互溶互溶易溶易溶呋喃甲酸无色晶体112微溶易溶可溶易溶
b.呋喃甲酸在水中的溶解度:

温度T/℃0515100溶解度S/g2.73.63.825.0
回答下列问题:
(1)仪器a的名称为________。实验中需控制温度为10℃左右,可采取的措施是_______
(任写一种)。
(2)实验中需要使用新制的呋喃甲醛,原因是___________________;操作①的名称为________。
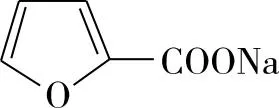
(3)产品Y是________;请写出向水溶液中加HCl调pH为3时发生反应的化学方程式:_______
____________________。
(4)若要对呋喃甲酸的粗产品进行纯化,正确的操作步骤为:________→活性炭脱色→蒸发浓缩→________→________→抽滤→洗涤→干燥。
(5)乙醚易挥发,遇明火易燃,其蒸气可使人失去知觉;在进行操作②时用装置B更好的理由是:
_________。
A
(6)取1.120 g纯化后的样品Y,配成100 mL溶液。准确量取20.00 mL于锥形瓶中,滴加指示剂,用0.080 0 mol/L氢氧化钾(经邻苯二甲酸氢钾标定)溶液滴定。平行滴定三次,平均消耗氢氧化钾溶液24.80 mL。则样品Y的纯度为________(保留三位有效数字)。
【参考答案】(1)球形冷凝管 冷水浴或缓慢加入氢氧化钠溶液
(2)呋喃甲醛会被空气中的氧气氧化 萃取分液
(4)加热溶解 趁热过滤 冷却结晶
(5)及时排出乙醚,以免对人体造成危害或使用电磁加热无明火,防止引燃乙醚蒸气
(6)99.2%
【命题意图】本题以有机物的制备为素材,要求学生从题干和表格中提取有用信息,综合考查学生的基本实验操作、仪器的识别、对装置的理解与改进、信息方程式的书写、物质的分离与提纯、滴定及相关计算。通过学科情境落实学生的信息获取与加工能力、证据识别与推理能力、实验操作与探究能力。
【实验分析】
【解题思路】由题意可知,控制温度约10℃,呋喃甲醛与氢氧化钠溶液反应生成呋喃甲醇和呋喃甲酸钠;向反应混合物中加水使呋喃甲醇和呋喃甲酸钠恰好溶解,向溶液中加入乙醚萃取分液得到溶有呋喃甲醇的乙醚溶液和溶有呋喃甲酸钠的水溶液,向呋喃甲醇的乙醚溶液中加入无机盐干燥除水,然后蒸馏分离得到乙醚和呋喃甲醇;向溶有呋喃甲酸钠的水溶液中慢慢滴加盐酸,结晶、过滤、洗涤、干燥得到呋喃甲酸。
【创新点分析】1.将文献中文字较多的实验步骤改为流程图的形式,言简意赅,减少学生的阅读量。2.信息给予的形式较多,有装置图、流程图和表格,要求学生能从中提取出关键信息,例如几种有机物的状态、在不同溶剂中的溶解性、呋喃甲酸在水中的溶解度随温度变化较大等信息,从而在物质的分离提纯时能选取适当的方法;对于学生信息提取和信息处理的关键能力要求较高。3.第(5)问需要学生结合题干信息分析装置的改进,以及对改进后的优点进行分析,锻炼学生的实验探究能力。
云南省昆明市第三中学 严涵钰
【试题评语】本题作者以有机物的制备为命题素材,综合考查了学生的化学实验基本操作、典型化学仪器的识别、装置的作用与改进、陌生反应方程式的书写、物质的分离与提纯、滴定及相关计算。试题注重通过学科情境考查学生的信息获取与加工能力、证据识别与推理能力、化学实验操作与探究能力。另外,本道题选材较为新颖,原创性好,试题设问层次较好,试题分析到位。
北京教育学院 王春
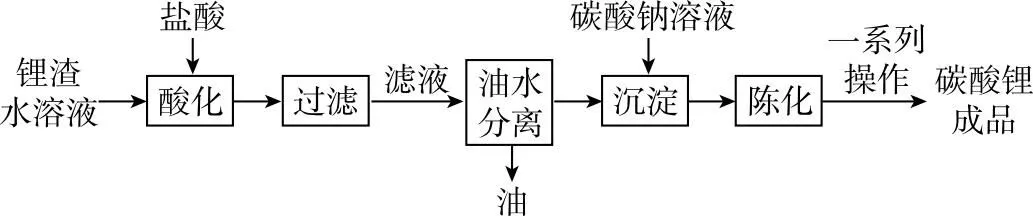
5.某实验小组利用废锂渣制备碳酸锂,实验过程如下:
已知:
①废锂渣含有大量的LiCl、少量LiOH、Li2O、Li3N、白油等;
②陈化是指沉淀完全后,使溶液在一定条件下静置存放一段时间;
③溴甲酚绿-甲基红的变色范围为pH<5.0时呈暗红色,5.0
回答下列问题:
(1)实验过程中用到的实验装置有________。
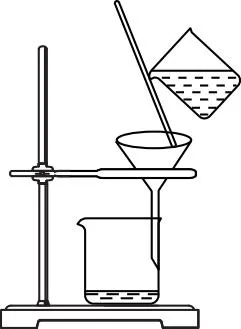
A
(2)废锂渣溶解时,Li3N发生反应的化学反应方程式为_________。
(3)沉淀时加入过量碳酸钠的原因是_______
_________。
(4)陈化可使微小晶体转化为较大颗粒晶体,减小晶体的比表面积,减少对________(填离子符号)的吸附,晶体生长过程体现了晶体的________性。
(5)原子吸收光谱法能检验Li2CO3产品中是否残留其他金属阳离子,原因是_________。
(6)滴定法测定产品中碳酸锂的含量时,常用溴甲酚绿-甲基红作指示剂,标准盐酸溶液进行滴定,到达滴定终点时溶液变为暗红色。在滴定终点前需________除去溶解的CO2,原因是_______
_________。
【参考答案】(1)AC

(3)使反应向生成Li2CO3的方向进行,提高碳酸锂的产率
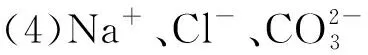
(5)金属离子中的电子由低能级向高能级跃迁,吸收一定频率的光,形成特征谱线
(6)加热煮沸 滴定终点pH=5.0,若不煮沸,则CO2溶于水形成H2CO3,增大了H+浓度,使滴定终点提前,造成测定结果偏小
【命题意图】本题利用废锂渣制备碳酸锂作为试题素材,属于实验探究情境。考查了实验仪器的使用、物质的鉴别、物质的分离和提纯、实验误差的分析、碳酸锂的溶解度和反应原理的应用。试题选择废物回收的实验,融入了绿色化学的理念,面对复杂、陌生的研究对象及问题情境,在“证据推理”“科学探究与创新意识”核心素养的统领下,综合实验仪器的分析、无机物性质、实验操作的选择、离子的检验、反应规律的应用等知识内容,实现了对学生的信息获取与加工能力、综合分析能力、解释能力、推理判断能力和简单设计能力的考查。
【实验分析】


【创新点分析】试题的设计需要学生利用结构、反应原理知识对实验中的方法和原理进行理解,从多角度认识实验设计的原理,体现结构决定性质、性质体现应用的观念,考查了学生对知识的结构化理解和迁移联想能力。
湖北省安陆市第一高级中学 杨世全 张小惠 陈玉莲 李巍
【试题评语】本题作者利用文献中废锂渣制备碳酸锂作为试题命题素材,综合考查了学生化学实验仪器的使用、物质的分离和提纯、实验误差的分析、碳酸锂的溶解度和反应原理的应用等必备知识。试题选择废物回收的实验,融入了绿色化学的理念,面对复杂、陌生的研究对象及问题情境,很好地考查了学生“证据推理”“科学探究与创新意识”等核心素养,实现了对学生信息获取与加工能力、综合分析推理能力、简单实验方案设计能力的考查。另外,本题综合考查能力较好,有一定新颖性。
北京教育学院 王春

