基于不确定度评估研究ID-LC-MS/MS法检测鸡蛋中氟虫腈砜残留量的关键控制点
张巧艳,方维焕,郑蔚然,王夏君,刘超纲, 王 强,
(1.浙江省农业科学院 农产品质量安全与营养研究所,浙江 杭州 310021; 2.浙江大学 动物科学学院,浙江 杭州 310058; 3.浙江省农业科学院 作物与核技术利用研究所,浙江 杭州 310021)
2017年,瑞士等15个欧盟国家和中国香港相继在鸡蛋中检测出氟虫腈,“毒鸡蛋”事件发酵成为全世界范围内的重大食品安全事件[1]。氟虫腈曾是一种使用广泛的苯基吡唑类杀虫剂,因对蜜蜂、水生生物等造成严重毒害作用而被禁用于农业生产和畜禽养殖[2]。鸡蛋中氟虫腈的来源可能是养鸡场非法使用氟虫腈杀灭跳蚤、虱子而导致养殖环境污染;或者农田长期残留氟虫腈引起农作物污染,通过饲料进入蛋鸡体内,然后转移至鸡蛋中。研究发现,氟虫腈在鸡蛋中的残留标示物主要是其代谢物氟虫腈砜,在残留消除过程中氟虫腈砜的含量常常远高于氟虫腈[3]。而且,氟虫腈砜对肝细胞的毒性也强于原药氟虫腈。在降低细胞活力上,氟虫腈砜比氟虫腈强54倍;用乳酸脱氢酶(LDH)漏出率评估细胞损伤程度,氟虫腈砜毒性是氟虫腈的37倍[4]。鸡蛋中氟虫腈砜的精准检测结果一定程度上可以反映氟虫腈的污染水平和潜在风险。
方法验证、不确定度评估和质量控制是确保可靠测量的关键,是检测实验室质控体系的重要组成部分[5]。检测结果的不确定度来源于测量过程,体现测量值与标准值之间的统计学差异。一般认为,不确定度越小,所述结果与被测量的真值愈接近[6]。评估测量不确定度最常见的方法是“自上而下”法(Top-down)和“自下而上”法(Bottom-up)。前者主要使用实验室现有的检测数据和信息评定不确定度;后者需要对测量过程所有可能影响结果的因素进行系统的分析和不确定度评估[7]。国家有证标准物质具有准确、可靠的量值和计量溯源性,可用于测量不确定度评估、检测质控和方法优化[8]。浙江省农业科学院通过药代动力学实验获得天然的含氟虫腈砜的鸡蛋液,经冷冻干燥、磨粉过筛、辐照灭菌等步骤将其加工成鸡蛋粉,经均匀性检验、稳定性检验、多家实验室联合定值,以及不确定度分析,研制了鸡蛋粉中氟虫腈砜残留分析标准物质。该产品已获批为国家二级标准物质,编号为GBW(E)100779。
鉴于高通量净化设备设计需求,浙江省农业科学院开发了一种多功能净化柱(PAC柱),可实现鸡蛋提取液的一步直通式净化,并基于同位素稀释液相色谱串联质谱法(ID-LC-MS/MS)建立了氟虫腈、氟虫腈砜、氟虫腈亚砜和氟甲腈同步快速检测方法,方法的准确度、灵敏度和精密度能够满足鸡蛋样品氟虫腈及其代谢物残留检测需求[9]。同位素稀释质谱法是国际计量组织公认的基准测量方法之一,可用于提供较高准确度和精密度,以及较小不确定度的检测结果。它测量的不是单纯的浓度,而是样液中目标物与内标的摩尔数量的比值[10]。本研究以GBW(E)100779为测试样,先加水复原成鸡蛋液,再用乙腈提取,用PAC柱净化,结合ID-LC-MS/MS法进行氟虫腈砜的残留检测,基于“自下而上”法开展测量不确定度评估,详细探讨影响检测结果准确性的主要因素,为鸡蛋精准检测的质量控制提供新思路。
1 材料与方法
1.1 试剂、材料和仪器
鸡蛋粉中氟虫腈砜残留分析标准物质[GBW(E)100779]来自浙江省农业科学院/浙江大学;乙腈中氟虫腈砜溶液标准物质[GBW(E)084271]来自浙江省农业科学院;将氟虫腈砜-13C6标准品(纯度99.8%,上海安谱实验科技股份有限公司)用乙腈稀释成质量浓度为2 μg·mL-1的稳定同位素稀释剂(内标溶液);甲醇、乙腈(色谱纯,德国默克集团);氯化钠、无水硫酸钠(分析纯,上海凌峰化学试剂有限公司);PAC多功能净化柱(200 mg,3 mL,自制)[9];万分之一天平(美国康州HZ电子有限公司);UltiMate 3000液相色谱-TSQ Quantum Discovery三重四极杆质谱联用仪(赛默飞世尔科技)。
1.2 标准工作溶液制备
用1 mL移液枪准确吸取1.00 mL氟虫腈砜溶液标准物质置于100 mL容量瓶中,用乙腈定容,摇匀,从中准确吸取0.50 mL置于另一100 mL容量瓶中,用乙腈定容,摇匀,获得氟虫腈砜质量浓度为5.00 μg·L-1的标准工作溶液。接着,用10 mL移液管分2次准确吸取20 mL标准工作溶液置于棕色样品瓶中,用100 μL移液枪准确吸取50 μL内标溶液加入标准工作溶液中,摇匀,配制成同位素稀释的氟虫腈砜单点校准标准工作溶液。
1.3 样品前处理
将鸡蛋粉从冰箱中取出,恢复至室温。用万分之一天平称取1.25 g鸡蛋粉(精确到0.000 1 g)置于50 mL塑料离心管中,加入3.75 g纯净水,涡旋振荡1 min,超声10 min,30 ℃避光水浴1 h,复原成5 g鸡蛋液。
用10 mL移液管分2次准确吸取20 mL乙腈加入鸡蛋液中,涡旋振荡1 min,超声30 min。用100 μL移液枪准确吸取50 μL内标溶液加入提取液中,涡旋振荡30 s。加入2 g 氯化钠和6 g无水硫酸钠,涡旋振荡1 min,6 200×g离心5 min,获得上清液。用移液枪吸取2 mL上清液,利用重力作用通过PAC柱,加压挤干填料,完全收集流出液,过0.22 μm微孔滤膜,待上机测定[9]。
1.4 色谱质谱条件
色谱柱:ACE Excel 2 C18柱(2.1 mm×100 mm,2 μm);柱温:35 ℃;流动相:A相为水,B相为甲醇,梯度洗脱,0~4.0 min(40% A~ 10% A),4~5.5 min(10% A),5.5~7.0 min(10% A~40% A),7.0~10.0 min(40% A);流速0.25 mL·min-1,进样量5 μL。
质谱系统使用电喷雾离子源,负离子模式扫描(ESI-),氩气为碰撞气,氮气为鞘气和辅助气。毛细管电压3 800 V,鞘气25 arb,辅助气4 arb,碰撞气2 mTorr,离子源温度320 ℃。采用选择反应监测(SRM),氟虫腈砜:m/z450.9>281.8(10 eV)、m/z450.9>243.8(66 eV);氟虫腈砜-13C6:m/z456.9>287.8(10 eV)、m/z456.9>249.8(66 eV)。
2 结果与分析
2.1 测量不确定度评估
鸡蛋液加工成鸡蛋粉,实测脱水率为75%,即1.25 g鸡蛋粉[GBW(E)100779]加入3.75 g水可复原成5 g鸡蛋液。在前处理过程中,鸡蛋液中的水分经氯化钠盐析后与乙腈相分离,被无水硫酸钠吸附,将氟虫腈砜及其内标物转移至乙腈相中。在优化条件下,鸡蛋粉中的氟虫腈砜被乙腈充分提取,通过单点比较法可以获得提取液中氟虫腈砜的浓度,从而计算出鸡蛋粉中氟虫腈砜的残留量。计算公式推导如下:
(1)
(2)
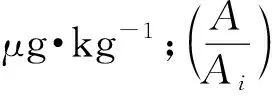
检测结果以鸡蛋粉计,鸡蛋液中的水分对量值无影响。由公式(2)可知,在定值过程中,同位素内标浓度c和样品提取溶剂体积V没有参与结果的计算。峰面积的测量重复性是由仪器的随机误差造成的。针对某次测量,当检测仪器固定时,检测质量主要依赖于前处理过程。在仪器条件满足检测要求且氟虫腈砜完全提取的前提下,测量不确定度主要由以下4部分引入,按JJF 1059.1—2012《测量不确定度评定与表示》[11]进行各部分的不确定度评定。
2.1.1 标准工作溶液浓度引入的不确定度
氟虫腈砜溶液标准物质GBW(E)084271具有相对较小的不确定度,其量值可溯源至澳大利亚国家计量研究院的氟虫腈砜纯度标准物质NMIA P1731。检测过程以GBW(E)084271[相对扩展不确定度为2%(k=2)]为参考物质,由此引入的相对不确定度为:
稀释过程带来的不确定度主要来自各种移液器具的承载体积。本研究所用的容量瓶和移液管均为A级器具,其他移液器具均检定合格。按JJG 646—2006《移液器检定规程》[12]和JJG 196—2006《常用玻璃量器检定规程》[13]确定容量允差,重复测定10次获得重复性标准偏差,由各种体积引入的不确定度分量汇总于表1中。容量瓶体积带来的不确定度主要来源于温度变化对溶剂乙腈的影响。制备标准工作溶液或者溶液标准物质时,选择室温变化较小的实验环境,有利于缩小不确定度。通过两步稀释将参考物质(100 μg·mL-1)制备成标准工作溶液(5 μg·L-1),稀释过程引入的相对不确定度计算如下:
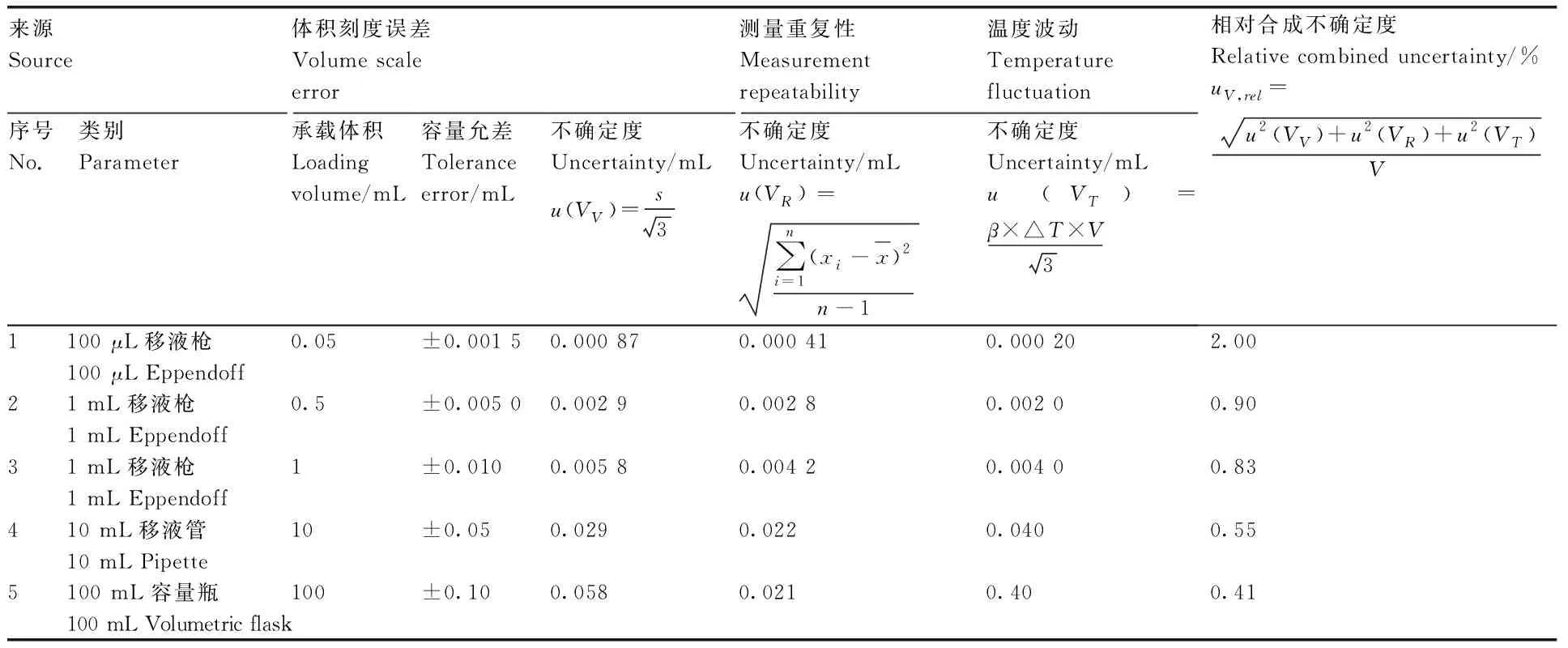
表1 各种体积引入的不确定度及其来源汇总Table 1 Uncertainties caused by volumes and their sources
氟虫腈砜标准工作溶液浓度引入的相对不确定度来自参考物质及其稀释过程,合成如下:

2.1.2 标准工作溶液移取体积引入的不确定度
单点校准标准工作溶液由20 mL标准工作溶液和50 μL内标溶液混合制备而成,两者的体积比是400∶1。标准工作溶液移取体积的少量偏差(±0.5 mL)对单点校准标准工作溶液中氟虫腈砜的浓度几乎无影响,但会通过影响内标的浓度影响最终检测结果。制备时,选择实验室常用的10 mL分度移液管,分2次吸取标准工作溶液,合成的相对不确定度为:
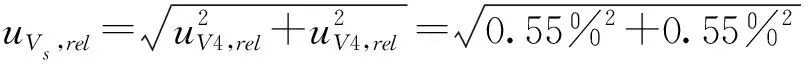
2.1.3 内标溶液添加体积引入的不确定度
同位素稀释质谱法是在试样中加入已知量的、与被测元素相同但同位素丰度不同的物质(简称“稀释剂”),混合均匀达到平衡后,用质谱测量混合试样中被测元素的同位素丰度比值,由此计算出被测元素的含量。鸡蛋粉中氟虫腈砜残留分析标准物质用ID-LC-MS/MS法检测时,在20 mL的标准工作溶液和样品乙腈提取液中分别加入50 μL稳定同位素稀释剂,由此引入的相对不确定度为:
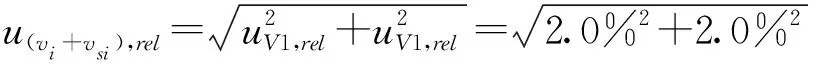
2.1.4 鸡蛋粉样品称样量引入的不确定度
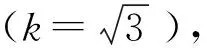
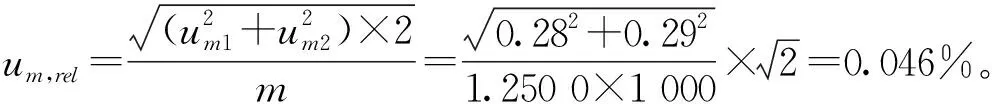
2.1.5 关键控制点分析
在测量不确定度评估中,通常使用石川图(Ishikawa diagram),又名鱼骨图(Fish-bone diagram),详尽展示测量不确定度分量的来源,反映可能影响整个检测过程的潜在参数[14]。由图1可见,鸡蛋粉中氟虫腈砜残留检测的不确定度主要有4个分量,定值结果的测量不确定度计算模型及其结果如下:
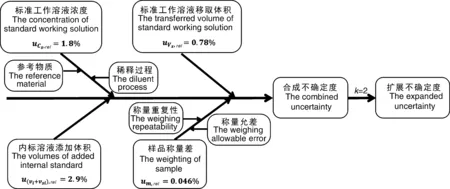
图1 ID-LC-MS/MS法检测鸡蛋粉中氟虫腈砜的不确定度评估鱼骨图Fig.1 Fish-bone diagram of uncertainty evaluation on determination of fipronil-sulfone in egg powder by ID-LC-MS/MS
k为包含因子,对应置信概率95%,一般取k=2。则检测结果的相对扩展不确定度为:
U定值,rel=k×u定值,rel=2×3.6%=7.2%。
以每个分量的平方占所有分量平方和的百分比计算各不确定度分量的贡献率。由图2可见,检测结果的主要不确定度来源于内标溶液添加体积,贡献率为68.59%。因此,添加内标过程是鸡蛋粉中氟虫腈砜ID-LC-MS/MS法测定的关键控制点。从表1可知,刻度误差、测量重复性、温度波动都可能引起体积偏差,最终影响检测结果。内标溶液的添加体积相对较小,且溶剂乙腈容易挥发,常规检测时一般使用移液枪快速移取、直接添加。100 μL移液枪检定合格的容量允差范围相对较大,是导致50 μL体积引入的不确定度偏大的主要原因。移液枪使用前进行移取体积的准确性校正,可以确保检测结果更接近真值。20 ℃时,水的体积膨胀系数为2.1×10-4℃-1,约为乙腈的六分之一。当内标的溶剂更换为水后,移取体积因受温度波动而对不确定度的贡献会明显减小。若用不易挥发的溶剂(例如水)稀释内标,降低不确定度的方法还可以考虑用质量代替体积[15]。
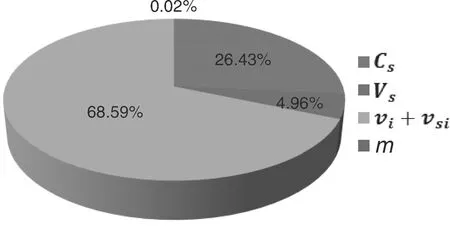
Cs,标准工作溶液浓度对合成不确定度的贡献率;Vs,标准工作溶液移取体积对合成不确定度的贡献率;vi+vsi,内标溶液添加体积对合成不确定度的贡献率;m,样品称样量对合成不确定度的贡献率。Cs, Vs, vi+vsi and m were the contribution ratio of the concentration of standard working solution, the transferred volume of standard working solution, the added volumes of internal standard solution and the weighting of sample, respectively.图2 ID-LC-MS/MS法检测鸡蛋粉中氟虫腈砜的不确定度分量贡献图Fig.2 Contribution of each component in the combined uncertainty for determination of fipronil-sulfone in egg powder by ID-LC-MS/MS
用万分之一天平(特种准确度级)称量鸡蛋粉(1.25 g左右)带来的不确定度几乎可以忽略不计(图2)。当样品为均质的鸡蛋液(5 g左右)时,用万分之一天平称量,检测结果以鸡蛋液计,称量带来的不确定度小于鸡蛋粉,其他测量不确定度分量的贡献率与鸡蛋粉一致。
2.2 参考基准材料评估
氟虫腈砜单点校准标准工作溶液由参考物质、稀释剂和内标溶液混合制备而成。制备前用LC-MS/MS对上述材料进行分析。由图3可知,稀释剂乙腈(也是样品提取溶剂)中不存在氟虫腈砜和氟虫腈砜-13C6;参考物质[GBW(E)084271]中存在氟虫腈砜,无氟虫腈砜-13C6;内标溶液中存在氟虫腈砜-13C6,无氟虫腈砜。这些材料在使用时互不干扰,不会给氟虫腈砜及其内标的浓度准确性带来风险,也不会给样品提取及其内标添加过程增加额外的不确定性因素。鸡蛋粉[GBW(E)100779]经乙腈提取、PAC柱净化后,用LC-MS/MS分析,获得的色谱与质谱特征与图3-B一致;用ID-LC-MS/MS法检测,提取液经同位素稀释、PAC柱净化后进行分析,能够获得与图3-B、图3-C特征一致的色谱图和质谱图。
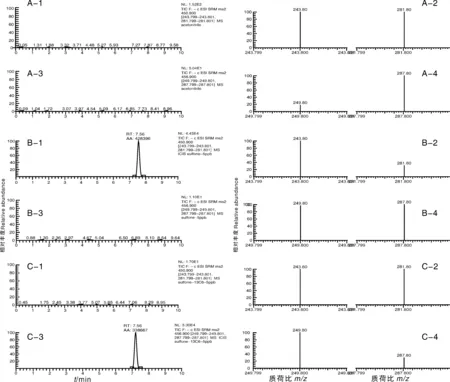
A,稀释剂(乙腈);B,参考物质[GBW(E)084271];C,内标溶液(氟虫腈砜-13C6)。1和2分别为针对氟虫腈砜的提取离子色谱图和质谱棒状图,3和4分别为针对氟虫腈砜-13C6的提取离子色谱图和质谱棒状图。A, Diluent solvent (acetonitrile); B, Reference material [GBW(E)084271]; C, Internal standard solution (fipronil-sulfone-13C6). 1 and 2, The extracted ion chromatogram and mass spectra centroid for fipronil-sulfone; 3 and 4, The extracted ion chromatogram and mass spectra centroid for fipronil-sulfone-13C6.图3 用于氟虫腈砜检测的参考物质、稀释剂和内标溶液LC-MS/MS图Fig.3 LC-MS/MS profiles of reference material, diluent solvent and internal standard solution for the fipronil-sulfone detection
2.3 前处理方法评估
氟虫腈砜的完全提取是准确反映鸡蛋粉中氟虫腈砜残留量的首要条件,也是有效地测量不确定度评估的前提。乙腈对氟虫腈及其代谢物具有极好的溶解能力,还可以沉淀大部分蛋白质,有利于释放目标物,减少提取过程中的乳化现象[9]。本研究以GBW(E)100779为测试样,以乙腈为提取溶剂,辅助超声提取。由表2可见,超声提取5 min,鸡蛋粉中氟虫腈砜的含量平均值略偏小,相对标准偏差(RSD)较大。延长超声时间至10 min,提取得率明显增加。超声30 min时检测结果最高,6次测量的平均值与GBW(E)100779的标准值(77 μg·kg-1)最接近,而且RSD相对较小,可视为鸡蛋粉中的氟虫腈砜已被提取完全。当用空白鸡蛋粉加标制备质控样用于提取效果比较时,不同超声时间对检测结果无显著性差异。
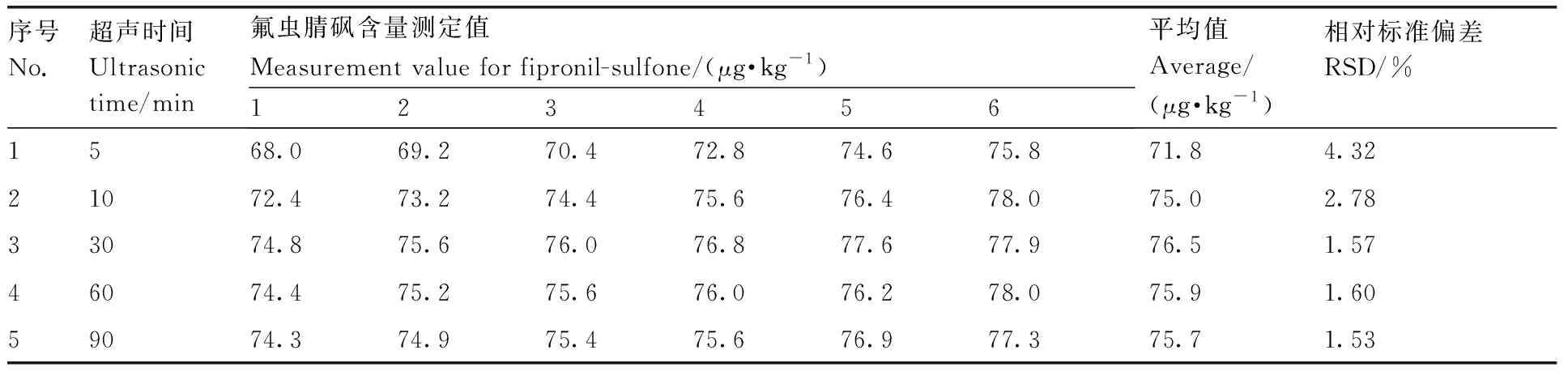
表2 不同超声时间下提取的鸡蛋粉(GBW(E)100779)的ID-LC-MS/MS检测结果Table 2 Test results of egg powder (GBW(E)100779) by ID-LC-MS/MS after extraction for different ultrasonic times
鸡蛋粉乙腈提取液中含有除目标物之外的蛋白质、脂肪、色素等杂质,需经净化处理,以减少它们对仪器的污染和对检测灵敏度的影响。PAC柱是一种多功能净化柱,可用于鸡蛋提取液的快速直通式净化,以去除主要的杂质,使进样液中氟虫腈砜和内标的基质效应均能同步满足检测要求[9]。同位素稀释质谱法可以恰当地消除净化过程的损失,以及伴随复杂基质的基质效应对准确测量的影响[15]。基于PAC柱的净化程序不会影响检测结果的准确性。
3 结论
本研究基于国家有证标准物质[GBW(E)100779]建立了ID-LC-MS/MS法检测鸡蛋粉中氟虫腈砜残留量的测量不确定度评估模型,系统分析了影响检测结果准确性的主要因素,得出以下结论:参考基准的合理选择和目标物的完全提取是准确测量的前提,同位素内标的精准添加是获得可靠结果的关键。针对动物源性食品中的污染物,通过代谢试验和加工处理,研制与天然阳性样品基本一致的标准物质,可逐步替代传统外加标的质控样,有效用于检测方法的优化和检测质量的评估。

