奥希替尼治疗EGFR基因突变型NSCLC患者对其血管新生及外周血Hcy水平的影响
夏莉,娄志霞,陈茉莉,黄祥,周德伟,胡宗涛
(中国科学院合肥肿瘤医院,1.内科;2.肺部肿瘤中心;3.肿瘤综合治疗中心,安徽 合肥 230031)
非小细胞肺癌(non-small cell lung cancer,NSCLC)是危害人类健康的主要恶性肿瘤之一,约占肺癌的85%[1-2]。NSCLC的治疗方法包括手术、放射疗法、化学药物治疗,晚期NSCLC患者往往无法满足手术指征,通常采用以铂类药物为基础的化疗方案来延长生命。但调查[3]显示,患者治疗后5年生存率未超过30%。随着驱动基因突变的发现,NSCLC个性化靶向治疗取得了一定成果。对于表皮生长因子受体(epidermal growth factor receptor,EGFR)基因突变型NSCLC患者,EGFR酪氨酸激酶抑制剂(EGFR-tyrosine kinase inhibitor,EGFR-TKI)已成为其重要的治疗方法。奥希替尼是EGFR-TKIs类第三代药物,其可阻断EGFR活化突变,有利于延长患者生命周期[4]。有资料[5]显示,对于可以抗肿瘤血管生成的靶向治疗,其存在脱靶反应,能够引起血管内皮生长因子(vascular endothelial growth factor,VEGF)抑制,继而影响心血管功能。目前已有研究探讨奥希替尼对EGFR基因突变型NSCLC患者的治疗效果,但关于其对肿瘤血管新生和患者心功能的影响尚不明确。同型半胱氨酸(homocysteine,Hcy)为心血管疾病高危因素,是反映心血管功能的重要指标[6-7]。本研究欲探讨奥希替尼治疗对EGFR基因突变型NSCLC患者血管新生及外周血Hcy水平的影响。
1 资料与方法
1.1 一般资料
选取2021年1月至2023年3月中国科学院合肥肿瘤医院收治的104例EGFR基因突变型NSCLC患者为研究对象。纳入标准:(1)病理检查诊断为NSCLC,二代测序(next-generation sequencing,NGS)方法行基因检测证实为EGFR基因经典突变如19 delete突变或21 L858R突变,并且不合并其他基因突变;(2)TNM分期为Ⅲb期~Ⅳ期;(3)无靶向治疗史;(4)预计生存周期>3个月。排除标准:(1)继发性肺癌;(2)血液循环系统存在功能失调;(3)严重内科疾病;(4)在研究开始前1个月内接受过放疗或化疗;(5)对化疗产生不良反应或不能耐受;(6)合并其他恶性肿瘤;(7)处于孕期或哺乳期的妇女;(8)患有影响身体代谢或自身免疫系统的疾病。按照不同的治疗方案将研究对象分为对照组和观察组,每组各52例。对照组中,男性29例,女性23例;年龄(61.73±7.41)岁;病理类型:鳞状上皮细胞癌35例,腺癌12例,大细胞癌3例,腺鳞癌2例;TNM分期:Ⅲb期18例,Ⅳ期34例;KPS评分(75.53±4.88)分;EGFR基因突变类型:19外显子26例,21外显子26例。观察组中,男性32例,女性20例;年龄(61.28±7.05)岁;病理类型:鳞状上皮细胞癌31例,腺癌15例,大细胞癌3例,腺鳞癌3例;TNM分期:Ⅲb期15例,Ⅳ期37例;KPS评分(76.12±5.04)分;EGFR基因突变类型:19外显子23例,21外显子29例。两组患者一般资料比较,均无统计学差异(P>0.05)。见表1。本研究符合赫尔辛基宣言要求。
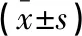
表1 两组患者一般资料比较
1.2 方法
对照组:予以培美曲塞和顺铂治疗,两种药物的使用剂量分别为500、75 mg/m2,执行方式为从第1天开始以静脉滴注形式进行,每21 d为1个治疗周期,并确保疗程总计不超过6个周期。观察组:在对照组化疗基础上辅以奥希替尼治疗,80 mg,口服,1次/d,治疗21 d。
1.3 观察指标
分别于治疗前及治疗后抽取患者清晨空腹静脉血5 mL,制备血清样本待测。(1)血管新生指标:采用酶联免疫吸附法,检测血清VEGF、血管生成素2(angiopoietin-2,Ang-2)水平。(2)外周血Hcy和脑钠肽(brain-natriuretic peptide,BNP):采用酶循环法检测外周血Hcy水平,酶联免疫法检测BNP水平。(3)心血管相关不良反应:记录两组治疗过程中发生的心血管相关不良反应,包括心律失常、房颤、心力衰竭、高血压等。
1.4 临床疗效评估
两组患者均在治疗结束后1个月进行临床疗效评估。完全缓解(CR):肿瘤病灶完全消失,维持时间超过1个月;部分缓解(PR):肿瘤病灶较治疗前缩小>30%,维持时间超过1个月;疾病稳定(SD):肿瘤病灶较治疗前缩小<30%或增大<20%,维持时间超过1个月;疾病进展(PD):肿瘤病灶增大>20%或有新病灶[8]。客观有效率(ORR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。
1.5 统计学分析
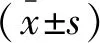
2 结果
2.1 两组患者临床疗效比较
观察组ORR与对照组比较,差异无统计学意义(P>0.05),DCR高于对照组(P<0.05)。见表2。
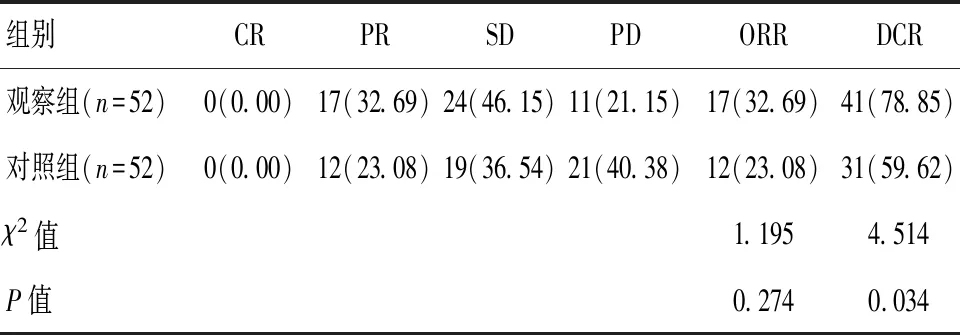
表2 两组患者临床疗效比较[n(%)]
2.2 两组患者血管新生指标比较
治疗后,两组血清VEGF、Ang-2水平均降低(P<0.05),且观察组低于对照组(P<0.05)。见表3。
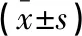
表3 两组患者血管新生指标比较
2.3 两组患者血清Hcy、BNP水平比较
治疗后,两组患者血清Hcy、BNP水平均升高(P<0.05),且观察组高于对照组(P<0.05)。见表4。
表4 两组患者外周血Hcy、BNP水平比较
2.4 两组患者心血管相关不良反应比较
观察组患者心血管相关不良反应总发生率高于对照组(P<0.05)。见表5。
表5 两组心血管相关不良反应比较[n(%)]
3 讨论
靶向药物在临床的推广应用使得NSCLC治疗模式逐渐转向以基因为导向的个性化靶向治疗,EGFR基因突变型NSCLC在亚裔人群中相对常见,采用EGFR-TKIs类药物治疗在很大程度上可以使此类患者获得更好的生存期[9]。奥希替尼属于EGFR-TKIs类第三代药物,已被用于多种恶性肿瘤的临床治疗[10]。本研究主要探讨奥希替尼治疗EGFR基因突变型NSCLC患者对其血管新生及外周血Hcy水平的影响。
血管新生是多数恶性肿瘤发展的重要过程,对癌细胞转移具有促进作用[11]。VEGF是血管生成重要因子,能够刺激细胞增殖和血管分化。研究[12]显示,VEGF表达水平与NSCLC预后存在密切关系,VEGF高表达的NSCLC患者预后相对较差。Ang-2为促血管生成因子,在促进血管生成的同时还可以抑制抗肿瘤免疫反应[13]。资料[14]指出,Ang-2在NSCLC中可能作为致癌基因发挥重要作用。本研究显示,两组患者治疗后血清VEGF、Ang-2水平均降低(P<0.05),且观察组低于对照组(P<0.05),观察组DCR高于对照组(P<0.05),提示奥希替尼治疗可以更好地抑制EGFR基因突变型NSCLC患者血管新生,改善EGFR基因突变型NSCLC患者近期临床疗效。这可能是奥希替尼能够作用于EGFR信号通路,抑制EGFR自身磷酸化过程,继而干扰肿瘤血管生成信号相关通路,抑制血管新生,从而改善临床效果。
尽管奥希替尼具有抗肿瘤血管新生作用,但其也可能会造成VEGF轴抑制,介导内皮损伤和血管收缩及重塑等,增加心脏和血管不良反应发生风险。目前虽然关于奥希替尼在心血管系统方面的研究报道较少,但奥希替尼也存在一定心脏毒性,其对患者心血管系统的影响也需引起重视。Hcy是一种含巯基氨基酸,其在自身氧化过程中能够产生一系列氧自由基,促使脂质过氧化而引起细胞内钙离子超载,同时还会诱导白介素6(interleukin-6,IL-6)等炎性因子表达,激发炎症反应[15]。研究[16]表明,高水平Hcy可造成心肌细胞损伤和促使心肌细胞凋亡,对心血管疾病发生具有重要影响。BNP为临床常用心功能指标,其水平变化可反映患者心功能受损情况[17]。本研究显示,两组治疗后外周血Hcy、BNP水平均升高(P<0.05),且观察组外周血Hcy、BNP水平高于对照组(P<0.05)。提示奥希替尼治疗会影响EGFR基因突变型NSCLC患者心血管功能。此外,观察组心血管相关不良反应总发生率高于对照组(P<0.05),表明在化疗基础上辅以奥希替尼治疗会增加心血管相关不良反应发生风险。分析其原因可能是,具有抗肿瘤血管生成的TKIs类药物参与了Notch途径,能够限制血管生成和细胞自我更新,继而诱导心肌细胞凋亡及心脏纤维化;并且其抑制血小板衍生生长因子及其受体能够诱使间皮细胞损伤,从而使血管通透性增强,影响冠状微血管功能[18]。另一方面,TKIs类药物可作用于AMP活化蛋白激酶,促使能量代谢减弱及线粒体功能损伤,继而造成心肌受损[19]。
综上,在化疗基础上予以奥希替尼治疗,可以更好地抑制EGFR基因突变型NSCLC患者血管新生,提高临床疗效,但也会引起外周血Hcy水平升高,影响心血管功能,因此在治疗时,需密切关注患者心血管系统情况,对于存在心血管系统异常的患者,警惕使用奥希替尼。

