微动敏感床垫式睡眠监测系统诊断阻塞性睡眠呼吸暂停及睡眠参数一致性评价
梁锡丽, 许婷, 陈莉雅, 江茵, 谢晴娥, 廖生武, 冯媛△
1南方医科大学第一临床学院(广东广州 510515); 南方医科大学南方医院 2精神心理科(睡眠医学中心), 3医疗质量管理科, 4健康管理科(广东广州 510515)
目前,多导睡眠监测(polysomnography,PSG)是诊断阻塞性睡眠呼吸暂停(obstructive sleep apnea,OSA)等睡眠疾病的金标准,需要在受试者头面部、胸腹部和肢体、手指等处同步连接多个导联收集相应的生理信号。因为设备昂贵、操作复杂、技术门槛高等问题很难大规模开展。此外,由于监测过程中连接导联线多,对受检者的睡眠造成干扰,出现“首夜效应”,导致患者体验差,在一定程度上限制了其接受检查的意愿。因此,采用“无干扰”或低干扰技术监测睡眠成为一种刚性需求,并将在睡眠疾病诊疗向基层渗透、睡眠健康管理向家庭延伸中起到桥梁作用[1]。微动敏感式床垫式监测系统(micro-movement sensitive mattress sleep monitoring system,MSMSMS)由特制床垫内的微动敏感压力传感器感受受检者心搏、呼吸和其他身体运动所产生的压力变化,整个检测过程使患者在更接近自然状态下进行睡眠监测。为“无干扰”监测睡眠状况提供了一种新的选择。已有研究表明,MSMSMS在诊断中、重度OSA上与PSG相比具有相当的敏感度和特异度[2],但它是否对不同程度的OSA具有分层筛查效应、能否准确反映睡眠的其他重要信息,尤其是睡眠结构的具体信息尚存争议。本研究拟在睡眠呼吸患者人群中,同步采集、比较MSMSMS与PSG所得的睡眠呼吸、睡眠结构等多参数,研究MSMSMS诊断不同程度OSA的敏感度与特异度,观察其在诊断、分度和睡眠多指标的检测上是否与金标准PSG可靠或一致,为普及无干扰方式监测和评价睡眠提供依据。
1 资料与方法
1.1 一般资料 2018年1—4月期间在南方医科大学南方医院睡眠中心以“打鼾”为主诉就诊且排除有心律失常的受试者,签署知情同意书,接受PSG和床垫同步监测。嘱咐患者检查前24 h禁用对睡眠有干扰的药物如安眠药、组胺类药物,检查当天禁酒、禁茶,避免咖啡及兴奋性饮料等。监测整晚睡眠时长6 h以上。共纳入完成同步检查的受试者71例,具体纳入流程见图1。其中4例因软件闪退或记录意外中断导致数据部分丢失,予以剔除,共有67例患者的数据纳入分析,采用各自的规则分别判定和分析数据,并由具有资质的同一睡眠技师独立完成数据的整理和审核。
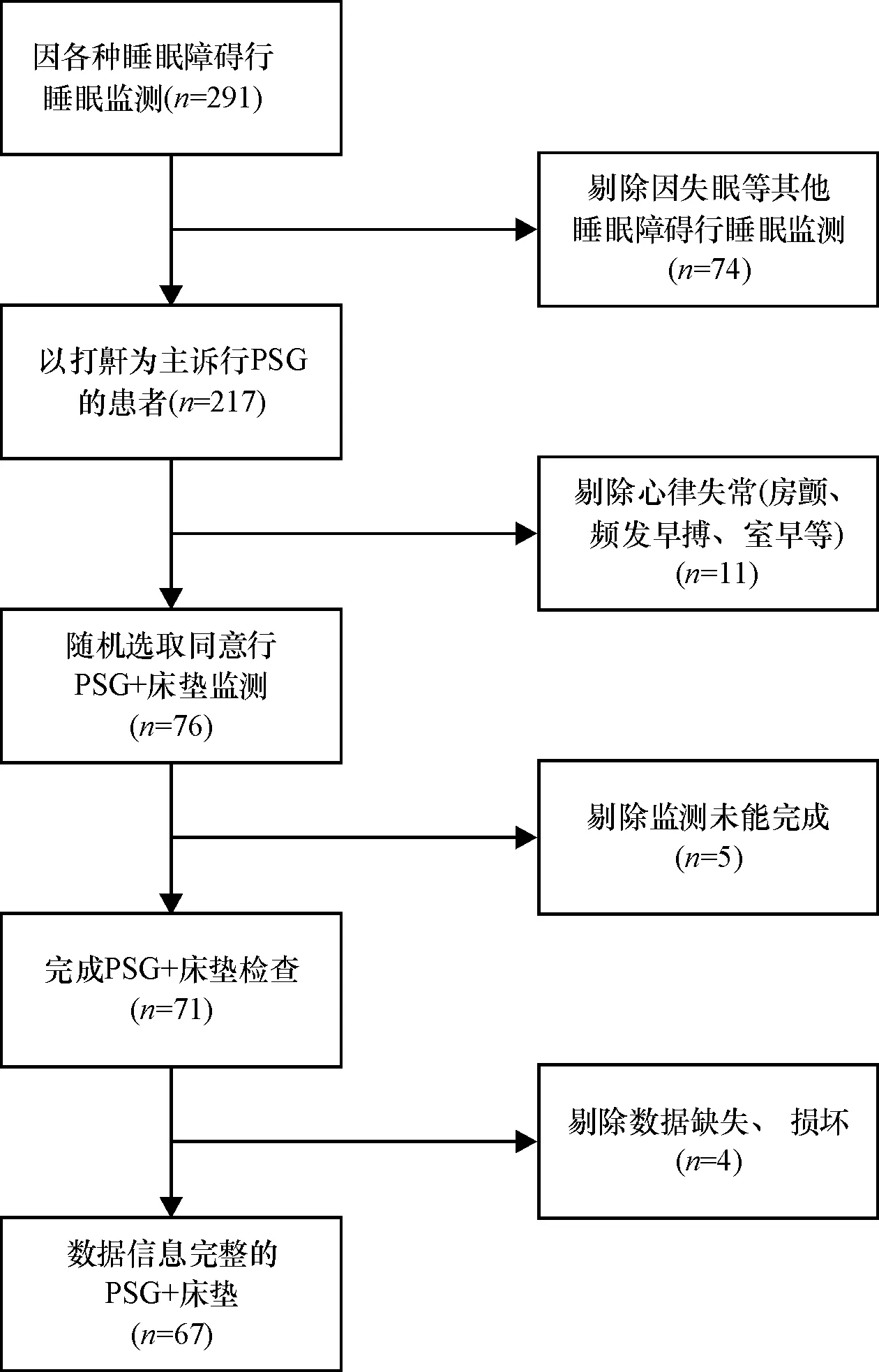
图1 受试者筛选流程图
1.2 多导睡眠监测实施和分图方法 采用Sandman(美国)64导睡眠监测系统,按照美国睡眠医学会《睡眠及其相关时间判读手册规则、术语和技术规范 2.3版》进行采集数据及分图判读。其中,低通气事件定义为鼻气流幅度较基线下降30%且伴有SaO2≥3%或伴有觉醒,持续时间≥10 s。各项纳入分析睡眠参数指标包括:总记录时间、总睡眠时间(total sleep time,TST)、睡眠潜伏期(sleep latency,SL)、睡眠效率、入睡后觉醒(WASO)时间和次数;非快速眼动期睡眠时间(NREMT)及所占的比例,包括浅睡眠(shadow sleep)(PSG中定义为N1+N2期时间和比例)、深睡眠(deep sleep)(PSG中定义为N3期时间和比例);快速眼动期睡眠(REM)时间及所占比例;呼吸暂停低通气指数(apnea hypopnea index,AHI)包括呼吸暂停指数(apnea index,AI)、低通气指数(hypopnea index,HI);最低血氧饱和度(lowest oxygen saturation,LSaO2)、平均血氧饱和度(mean oxygen saturation,MSaO2)、呼吸紊乱指数(respiratory disturbance index,RDI)等。
1.3 微动敏感床垫式睡眠监测和事件判定 采用空军航空医学研究所研发、北京阳升公司生产的MSMSMS睡眠床垫监测系统,采集呼吸波、心冲击图、心率、体动、指氧饱和度等数据经仪器自带软件分析,事件判读标准同前[2],除用RDI表示呼吸紊乱指数对应PSG中的AHI外,其余纳入分析指标同PSG。其中,床垫监测系统未对NREM睡眠分期进行详细划分,仅提供浅睡眠、深睡眠的信息,相应指标在PSG中的定义见上描述。
1.4 诊断和分度标准 根据《阻塞性睡眠呼吸暂停低通气综合征诊治指南(2011修订版)》[3]进行OSA诊断,并依据AHI/RDI值进行分度,其中轻度(5~14.9次/h)、中度(15~29.9次/h)、重度(≥30次/h)。
1.5 统计学方法 采用SPSS 23.0统计软件进行分析。计量资料以均数±标准差描述。两组之间计量资料采取配对t检验比较其实际值差异,用Bland-Altman分析中Two-way random models Agreement type或组内相关系数来评价一致性,有序分类变量的计数资料采取了weighted kappa分析来评价可靠性。其中ICC值及weighted Kappa值分级如下:差(<0.00)、较差(0.00~0.20)、一般(0.21~0.40)、中等(0.41~0.60)、较强(0.61~0.80)以及强(0.81~1.00)[4]。取P<0.05为差异有统计学意义。
2 结果
2.1 研究人群一般特征 受试者的基本信息见表1。在67例受试者中,男55例(82.1%),女12例(17.9%);平均年龄(44.00±15.69)岁;体重(75.02±16.12)kg;体质指数(BMI)(26.42±4.91)kg/m2;监测前收缩压(131.39±15.26)mmHg;舒张压(82.75±11.94)mmHg。受试者MSMSMS总记录时间(570.40±40.21)min;PSG总记录时间(497.37±57.54)min。
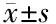
表1 两种睡眠监测设备对OSA的诊断及分度的频数交叉表
2.2 MSMSMS与PSG在基于AHI值的OSA诊断及分度的比较
2.2.1 PSG-AHI值与MSMSMS-RDI的相关性 经PSG测得AHI与MSMSMS测得RDI组内相关系数为0.967(0.943,0.980),RDI与AHI的线性回归方程中,R2=0.953,见图2A。PSG与MSMSMS两种方法在判定AHI(RDI)值上具有很强的一致性,见图2B。

注:A:相关性线形图;B:一致性界线Bland-Altman图
2.2.2 两种诊断方法对OSA严重程度判断的一致性 两者同时诊断为轻度OSA 13例,中度OSA 9例,重度OSA 27例,这两种诊断方法对55例受试者的诊断意见一致,对12例受试者不一致。Weighted kappa系数为0.841(95%CI:0.766~0.928),提示两者在OSA分度上具有强的一致性(P<0.001)。见表1。
2.2.3 诊断不同程度OSA分析 诊断试验受试者工作特征(ROC)曲线分析表明,分别以PSG中AHI≥5、15、30为诊断截断值,床垫监测所得的RDI对OSA、中重度OSA及重度OSA的诊断均具有较高的敏感度和特异度,曲线下面积(AUC)分别为1(95%CI:1~1)、0.999(95%CI:0.996~1)和0.967(95%CI:0.932~1)(P<0.001)。其中当RDI=5.35时,诊断OSA的敏感度和特异度为100%;RDI=16.8时,诊断中度及以上OSA的敏感度和特异度分别为97.7%和100%;RDI=29.5时诊断重度以上OSA的敏感度和特异度分别为87.5%和94.3%。见图3、表2。
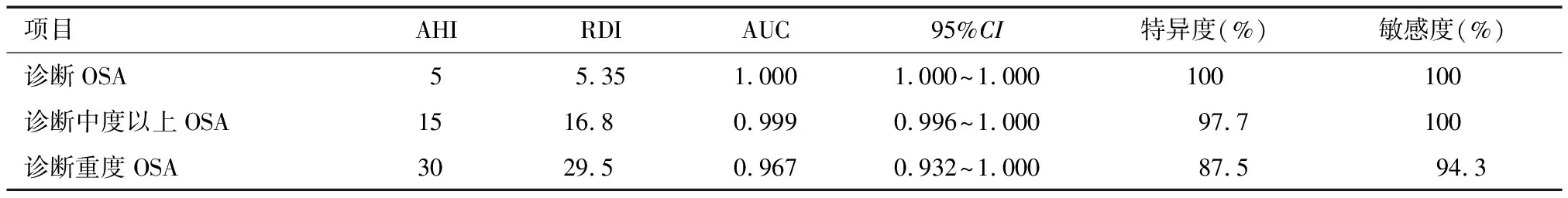
表2 不同程度OSA的诊断特异度及敏感度

注:A:诊断OSA;B:诊断中度以上OSA;C:诊断重度OSA
2.3 MSMSMS与PSG各参数间的比较 床垫系统的平均记录时间和记录睡眠时间较PSG增多,睡眠效率稍有增高,分别为93.14%和87.7%;在睡眠潜伏期判定上,床垫监测具有更短的睡眠潜伏期,平均约4.69 min,两者在REM睡眠潜伏期的判定上差异无统计学意义(P>0.05)。见表3。
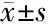
表3 两种睡眠监测设备各参数间的比较配对t检验 (n=67)
在入睡后觉醒时间和次数上,床垫系统较PSG更少检出觉醒相关信息,更多判出浅睡眠和REM睡眠的时间,较少判出深睡眠比例和时间,差异有统计学意义(P<0.001)。而两者在NREM及REM睡眠比例判别上差异无统计学意义(P=0.654,P=0.657)。
在呼吸和血氧参数的直接比较中,对呼吸暂停指数的判定差异无统计学意义(P=0.162),配对差值和95%CI为1.7(-0.7~4.1);而在HI上差异有统计学意义(P<0.001)。两者在平均血氧饱和度和最低血氧饱和度的比较上差异虽然有统计学意义,但差值较小,分别为-0.44和-1.51 cmH2O,不具有临床意义。
2.4 MSMSMS与PSG各参数间的一致性分析 两种设备测得呼吸和血氧参数的一致性均有统计学意义(P<0.05)。其中AI、LSO2、MSO2的有较强的一致性;而HI虽有统计学意义(P=0.038),但一致性较弱。
MSMSMS在睡眠总时间、睡眠效率、入睡后清醒时间等睡眠信息中与PSG检测相比,一致性具有统计学意义(P<0.05),ICC在0.2~0.4之间,提示一致性一般。在SL、入睡后清醒时间次数、快速动眼潜伏期等指标检测中,两者的检测的一致性较差。
两者在浅睡眠时间、浅睡眠所占的比例以及深睡眠时间,具有中度一致性,且差异有统计学意义(P<0.05)。而在非快速眼动睡眠时间及比例、快速眼动睡眠时间及比例,两者检测的一致性较差。见表4。
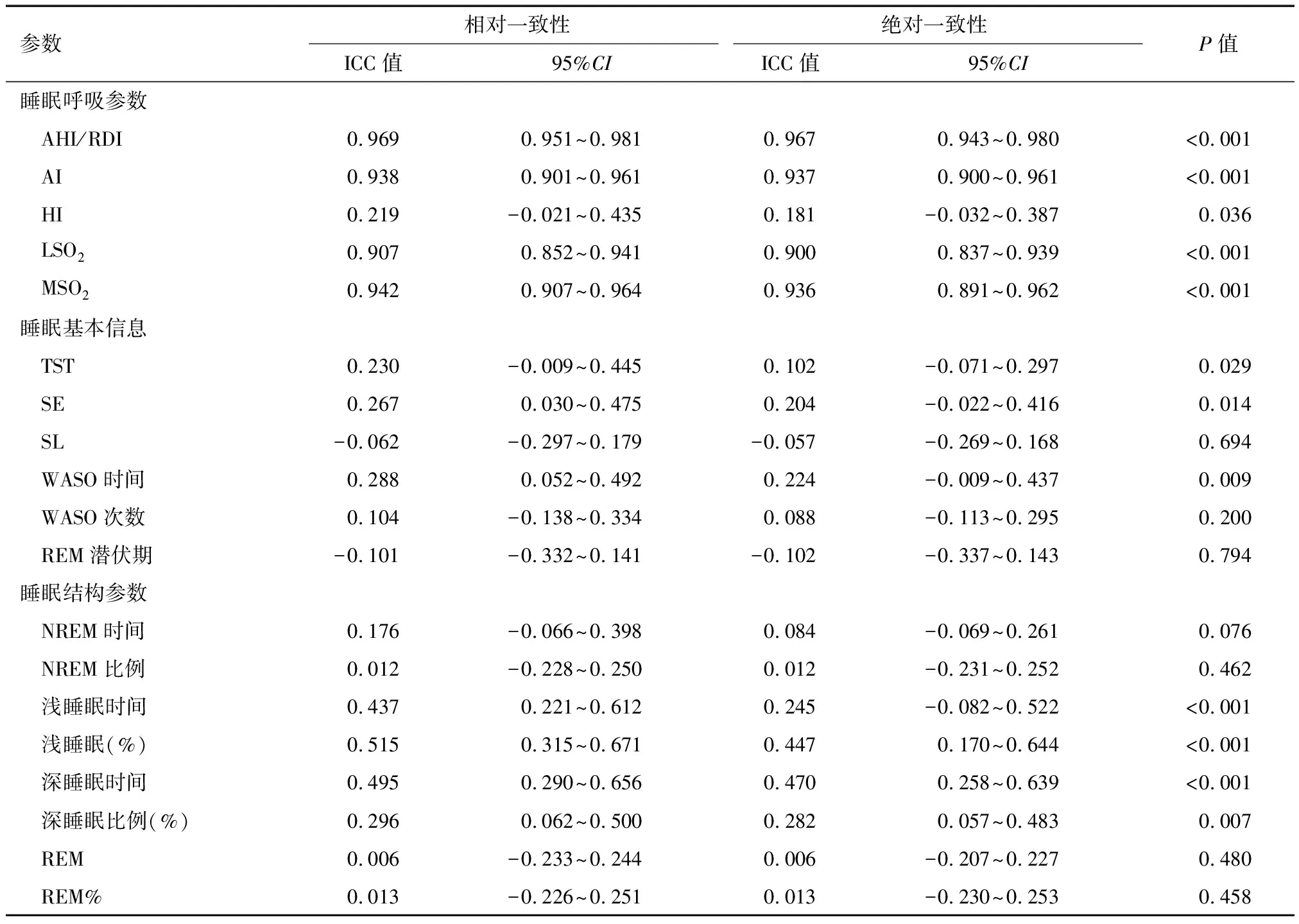
表4 两种睡眠监测设备睡眠相关多参数一致性比较(n=67)
3 讨论
OSA是一类常见的、多发的、容易受忽视的睡眠疾患,人群患病率超过4%[5],其中我国OSA患病人数居全球首位,达1.76亿[6]。已经证实,OSA与心脑血管疾病、代谢性疾病、心脏病等多种慢性疾病的发生、发展密切相关[7-9],对慢性病管理至关重要。我国有世界上最庞大的OSA患者群,若得不到及时的筛查及诊治,将严重损害人群健康,增加国家和社会慢病管理的负担。因此采用准确且可及的手段来监测睡眠、诊治包括OSA在内的睡眠疾病已经成为社会健康发展的需求。
在此项研究中,我们同步比较了多导睡眠监测和微动敏感式床垫在OSA人群中多个睡眠监测参数的一致性,研究证实:微动敏感床垫式睡眠监测系统在诊断OSA和分度上与多导睡眠监测有高度的一致性;进一步发现微动敏感床垫式睡眠监测系统对于OSA患者除低通气外呼吸和血氧参数与PSG一致性较强;对睡眠结构的监测,在浅睡眠、深睡眠时间和比例上与多导睡眠监测相比有中度一致性,而在REM期和睡醒相关参数的判断上一致性欠缺。
尽管有技术人员值守的PSG仍然是睡眠监测的核心技术和OSA诊断的金标准,但是越来越多的非脑电监测系统被用于诊断OSA。在这类设备中,按照采集方式分为接触式采集和感应式采集两类。微动敏感床垫系统主要通过感应式采集多项生理信号,优点在于尽可能减少检测设备对受试者睡眠情况的干扰。
已有的研究对比了初筛设备诊断OSA(通常以AHI值作为诊断标准)的敏感度和特异度,提出初筛设备是中重度OSA筛查的很有力的工具[10-11]。在本研究中,证实了微动敏感床垫式睡眠监测与PSG在诊断OSA及分度上具有较好的一致性,不仅局限于中重度OSA,对于轻度OSA同样具有较好的诊断价值和区分度。传统初筛设备通常对轻度OSA诊断的假阴性率偏高,而我们发现床垫系统对于轻度以上OSA的诊断甚至优于重度OSA。一方面可能由于床垫系统本身提供了睡眠相关信息,能够较准确的计算RDI值。RDI和AHI的计算是基于呼吸事件的数量和整夜睡眠时间的,传统的初筛设备由于缺乏睡眠时间信息往往用佩戴设备信息作为睡眠时间估算值,从而导致RDI或AHI值偏低。另一方面,重度OSA患者由于呼吸不畅更倾向于翻身多动,床垫系统分辨睡醒状态并非基于脑电判断,部分依赖于体动信息,可能影响其睡眠状态的判断,从而影响RDI值计算。
虽然MSMSMS与PSG采用不同的技术原理,二者对呼吸事件的判断规则也有所不同,但它们对呼吸事件的检测效果却有良好的一致性,尤其是呼吸暂停事件。但我们发现,两者对于低通气事件检测的一致性不佳,这与亢丹等[2]的结论一致。推测低通气状态下由于呼吸努力度与正常呼吸相比变化不大,不会对床垫系统产生异常的压力变化,而且低通气通常较少引起皮质下微觉醒,导致通过MSMSMS检出率较传统PSG减少。另外,PSG分析不同的低通气定义方式也可能是产生差异的原因之一[11]。
PSG优于低干扰的初筛设备主要在于它能够准确提供丰富的睡眠信息,判断受试者的睡醒状态和睡眠结构,从而能够更加精确计算睡眠呼吸紊乱指数,并提供受试者睡眠深度的客观状态。与低干扰的初筛设备不同,MSMSMS并未牺牲采集参数的可及性,它能提供睡眠结构信息[12],但这些睡眠信息在以往的临床应用中尚未充分利用,原因在于少有资料比较两者睡眠信息的一致性和差异。我们在OSA受试者上比较了床垫式低干扰监测设备与PSG相比睡眠结构的差异,发现它们在浅睡眠时间和比例、深睡眠时间上有中度一致性。这与张庆丰等[13]在失眠患者以及亢丹等[2]在OSA患者中发现不同。张庆丰等[13]在失眠患者中发现,床垫与PSG相比,在睡眠总时间、睡眠效率和REM睡眠比例差异无统计学意义,但深睡眠、浅睡眠比例有不同。不同的研究人群可能是造成这种区别的原因之一,失眠患者清醒时间中体动增多,基于体动信息判断的睡醒判断与PSG脑电信息一致性尚可[14]。亢丹等[2]在OSA患者中发现床垫与PSG相比睡眠结构显著不同,是通过t检验直接比较实际值而得出的。床垫系统以体动信息来判定患者的睡醒状态,在清醒而静止的状下,受试者容易被误判为睡眠状态,因而能够解释本研究中对于入睡潜伏期、入睡后觉醒时间和次数的判定上,床垫系统均显著少于PSG。这也说明相较于直接比较数据而言,校正了睡醒状态后的比例指标,如NREM和REM睡眠比例在设备间比较中更具有评价睡眠状态的稳定性。而且,我们使用了更新的PSG分图规则;并且在未刻意限制两种方法监测时长无差异的前提下,用一致性判定的方法更加合理,且结果更宜推广到一般检测状态。
另外,我们发现,床垫系统在睡眠潜伏期相关指标和REM分期判断上一致性较差。同样的结果也出现在采取非脑电技术进行睡眠分期的其他技术[15-16],如心肺耦合CPC检测中[17]。这类非脑电睡眠分期技术通常基于自主神经活动信号反映睡眠,认为睡眠与交感/副交感中枢位置临近;皮层脑电与心率、呼吸等可能同时反映了深部脑活动的变化[18]。这种变化尽管在传统的REM和NREM睡眠中有区别,但不足以完美区分两种睡眠;而且REM期睡眠和清醒状态下交感活动可能有相似性,难以准确判断。目前看来,仍需发掘更加合适的指标或算法来匹配基于自主神经活动的非干扰式睡眠监测方法与基于脑电的经典睡眠分期间的联系。
本研究存在以下缺陷:首先,研究对象平均体重为75 kg,研究结果可能无法外推至儿童或低体重人群中。有人认为,儿童因为体重较轻,对MSMSMS的感应敏感度是一项挑战;另外,儿童夜间睡眠中多动,可能会影响到觉醒和睡眠分期的判别。徐晖等[19]利用MSMSMS对儿童鼾症者进行OSA筛查,认为它由于高敏感性,可用于儿童监测;但该项研究并未同时与PSG监测进行比较。其次,并未对床垫和PSG的监测时间进行严格统一和限制,也未对两者的睡眠监测信息进行逐帧对比。由于两者在睡醒判断上的原理和标准不一,基于脑电以30 s为一帧判断睡眠的方式未必适合床垫的逻辑,另外,通过校正监测时间的数据也可提供相当的信息。再次,本研究仅进行了一晚的监测,未能对多晚的情况进行连续性监测和比较,以考察其稳定性。实际上,微动敏感床垫相对于PSG而言,由于操作简便、容易实施、干扰性小,更方便进行长时间连续监测。有理由相信,连续进行数晚的监测,相比经典的PSG,患者对床垫式监测的耐受度和接受程度会更高。
总之,本研究通过一晚同步的监测证实了MSMSMS与PSG在OSA诊断以及病情分度上均具有相似的敏感性和特异性及很强的一致性,不仅能用于中重度OSA的诊断,对轻度的诊断和筛查也有很好的应用价值。除此之外,MSMSMS在评判受试者的睡眠结构上也有一定的意义,可以较准确反映浅睡眠和深睡眠比例情况。MSMSMS作为无干扰、长时间动态监测的一类设备,与智能分析软件结合,能够实时监测和回顾数据;如进一步与人工智能、信息技术相结合,可能为今后居家人群,尤其是老年人监测睡眠,以及远程获取睡眠多种信息提供可行的技术选择。
利益相关声明:所有作者声明在本研究中无利益冲突。
作者贡献说明:梁锡丽负责查阅文献、数据解释、撰写论文;许婷负责入组患者筛查、PSG报告分析和数据整理;陈莉雅负责数据统计分析;江茵负责床垫数据采集;谢晴娥负责核对数据;廖生武负责指导立意、修改论文;冯媛负责课题设计、修改论文并最终定稿。

