阴离子树脂分离橄榄苦苷的过程及性能研究
徐 锋,曾小成,吴学文,张有发,熊 艳*
1湘潭大学化工学院,湘潭 411105;2湖南杰萃生物技术有限公司,湘潭 412007
油橄榄(OleaeuropaeaL.)属木犀科木犀榄属常绿乔木,在我国和地中海国家广泛种植,是这些国家和地区的主要农业经济作物之一[1-4]。目前橄榄资源的开发利用主要集中在果实的利用上,橄榄叶则作为废料被遗弃在种植园内,造成了极大的资源浪费,现代研究发现在橄榄叶中含有丰富的裂环烯醚萜苷类、酚类、五环三萜类以及黄酮类化合物[1,5-7]。其中橄榄苦苷(oleuropein,OL)是最主要的活性物质,具有抗氧化、抗病毒、杀菌消炎、降血糖、抗高血压、抗癌等作用,广泛应用于食品、医药、化妆品等领域[6-13]。OL属裂环烯醚萜苷类,易溶于水,乙醇,甲醇等溶剂,在酸、碱、高温、光照等条件下易分解成羟基酪醇[5]。
目前,分离OL的方法主要有大孔树脂吸附、高速逆流萃取及超临界萃取等[14-18]。其中,高速逆流萃取和超临界萃取分离效果较好,可以得到纯度很高的OL,但这两种方法对于设备、人员操作等方面要求很高,不适合于大规模工业生产。大孔树脂具多孔结构,吸附性能优良,广泛应用于植物活性成分的富集、分离和纯化[19-23]。大孔树脂富集、分离OL主要的机理是二者在一定条件下可通过氢键、范德华力发生可逆的相互作用,从而将其从提取液中选择性富集、分离[22,23]。近年来,众多学者聚焦于非极性、弱极性树脂富集、分离橄榄叶提取物中的OL。Tian等[5]利用大孔树脂D101富集分离OL,经乙酸乙酯萃取得到纯度为63.43%的OL产品。Wang等[8]利用AB-8树脂富集分离OL,纯度从9.16%提升到了20.38%。Sahin等[21]研究发现XAD 7HP树脂吸附OL的机理符合准二级动力学。Liu等[24]研究发现大孔吸附树脂BMKX-4富集OL的机理符合准二级动力学、Freundlich模型,并将OL的纯度提升到47.59%。理论上来说,OL属于多酚类化合物,阴离子树脂吸附机理可实现其富集、分离。然而,目前尚未见到有关阴离子树脂分离OL研究的报道,因此,我们采用阴离子树脂(LX-68M),研究其静态、动态吸附和解吸附OL的性能,进一步研究了OL的泄露曲线、洗脱曲线及阴离子树脂再生的稳定性,以期为阴离子树脂富集、分离、纯化OL及相似天然产物提供理论参考依据。
1 材料与方法
1.1 材料与设备
橄榄叶由湖南杰萃生物技术有限公司赠予,湖南中医药大学童巧珍教授鉴定为油橄榄(OleaeuropaeaL.)的干燥叶,标本(2022001)存于湖南杰萃生物技术有限公司;OL标准品(纯度98%,MUST-21052502,成都曼思特生物科技有限公司);色谱纯乙腈(天津市科密欧化学试剂有限公司);无水乙醇(湖南汇虹试剂有限公司)。
色谱柱(BDS HYPERSIL C18,5 μm,4.6 mm ×250 mm);阴离子交换树脂(LX-68M,粒径为0.12 mm,西安蓝晓科技新材料股份有限公司);双功能数显恒温振荡器(SHA-B,上海梅香仪器有限公司);高效液相色谱仪(LC-10Tvp,赛智科技(杭州)有限公司);自动液相色谱分离层析仪(MB99-1,上海沪西分析仪器厂有限公司)。
1.2 实验方法
1.2.1 液相条件
流动相为0.1%磷酸溶液∶乙腈=77∶23等度洗脱;流速1.00 mL/min;检测波长231 nm;柱温30 ℃。
1.2.2 标准曲线测定
准确称取OL标准品,配制成1.0 mg/mL的标准溶液,再依次配制成0.025、0.05、0.10、0.15、0.20、0.30 mg/mL的标准溶液,并用HPLC测定不同浓度标准溶液峰面积,取其峰面积平均值(n=3)。以峰面积为纵坐标Y,OL浓度为横坐标X,绘制标准曲线。回归方程为Y=1.01×107X-2.03×105,R2=0.999 2。相对标准偏差(RSD)为1.74%(n=6),说明分析结果的精密度符合测量要求。
1.2.3 橄榄苦苷的提取
取干燥好的橄榄叶粉末加适量70%乙醇,浸泡过夜;将70%乙醇以2 BV/h的流速进行渗漉提取5 h,提取液回收乙醇至无醇味后静置8 h,过滤,将所得滤液浓缩至0.50 g/mL(生药浓度,以下同),备用。
1.2.4 静态吸附和解吸实验
树脂预处理:将树脂(LX-68M)浸泡在体积分数为95%的乙醇溶液中溶胀24 h,超纯水洗至无醇味,再浸泡于质量分数为4% HCl溶液中12 h,洗至中性,最后在质量分数为4% NaOH溶液中浸泡12 h,洗至中性备用。
静态吸附实验:称取预处理好的树脂0.40 g(干重)于具塞锥形瓶中,加入40.0 mL浓度为0.20 g/mL的提取液;置于恒温振荡器每隔1 h取样,用HPLC测定吸附残液中OL的含量,按公式(1)计算树脂平衡吸附量。
(1)
其中,Qe(mg/g)为树脂平衡吸附量,C0、Ce(g/mL)分别表示提取液初始浓度及吸附平衡浓度,m(g)为树脂质量,V(mL)为提取液体积。
解吸附实验:将达到吸附平衡的LX-68M树脂用超纯水洗涤3次(3×40.0 mL)后,加入40.0 mL 70%的乙醇,置于恒温振荡器,每隔1.0 h取样,测定解吸液中OL的含量,共解吸8.0 h。按公式(2)计算解吸量。
Qd=Cd×Vd
(2)
其中,Qd(mg/g)为OL解吸量,Cd(g/mL)为解吸液OL浓度,Vd(mL)为解吸液体积。
1.2.5 提取液浓度对吸附性能的影响
称取树脂0.20 g于50 mL离心管中,加入20.0 mL不同浓度(0.05、0.10、0.15、0.20、0.25、0.30 g/mL)的提取液,置于恒温振荡器吸附8.0 h以上,测定残液中OL的含量。
1.2.6 不同浓度乙醇对解吸性能的影响
将达到吸附平衡的LX-68M树脂用超纯水洗涤三次,加入20.0 mL不同浓度(0%、15%、30%、45%、60%、75%、90%)的乙醇;置于恒温振荡器解吸8.0 h以上,测定解吸液中OL的含量。
1.2.7 LX-68M树脂动态吸附-解吸研究
称取LX-68M树脂5.0 g采用湿法装柱,层析柱规格为1.0 cm × 40 cm。取浓度为0.25 g/mL的橄榄叶提取液,在不同上样流速(1.0、2.0、3.0、4.0、5.0 BV/h)下上样。流出液中OL浓度超过提取液OL浓度的10%可视为树脂达到吸附饱和,并绘制泄露曲线,此时对应的体积为泄露体积。上样结束后,先用超纯水进行洗涤,待流出液检测基本无OL时;再用45%乙醇溶液进行洗脱,在不同流速(1.0、2.0、3.0、4.0、5.0 BV/h)下进行解吸,每1.0 BV接一次解吸液,测定洗脱液中OL的含量。
2 结果与讨论
2.1 树脂静态吸附、解吸性能
为获得LX-68M树脂的吸附、解吸性能参数,对树脂进行静态吸附、解吸实验研究。静态吸附结果如图1a所示,LX-68M树脂在起始2.0 h内快速吸附,吸附量达到27 mg/g以上,此后吸附速率增长变缓,且在7.0 h后达到吸附平衡。因此,选择7.0 h为树脂的吸附平衡时间。解吸实验结果如图1b所示,70%乙醇为解吸液时,树脂解吸OL较快,在3.0 h左右达到解吸附平衡;为确保OL的回收率,我们选择解吸时间为4.0 h。图1表明树脂对于OL的吸附量大,解吸速度较快,LX-68M树脂可作为富集、分离、纯化OL的材料。
2.2 LX-68M树脂分离橄榄苦苷的影响因素
我们进一步研究了上样浓度、乙醇浓度对LX-68M树脂吸附OL、解吸的影响规律。结果如图2所示,上样浓度在0.05~0.20 g/mL范围内,随着上样浓度的增加,OL的平衡吸附量也在相应增加;当上样浓度超过0.25 g/mL时,树脂的吸附量达到平衡。这可能是因为浓度的增大,上样液中其他成分的浓度也随之增大,与OL形成吸附竞争,使得树脂中的结合位点数减少,导致树脂对于OL吸附能力的下降[25]。因此,LX-68M树脂对于OL的最佳上样浓度在0.20~0.25 g/mL之间。
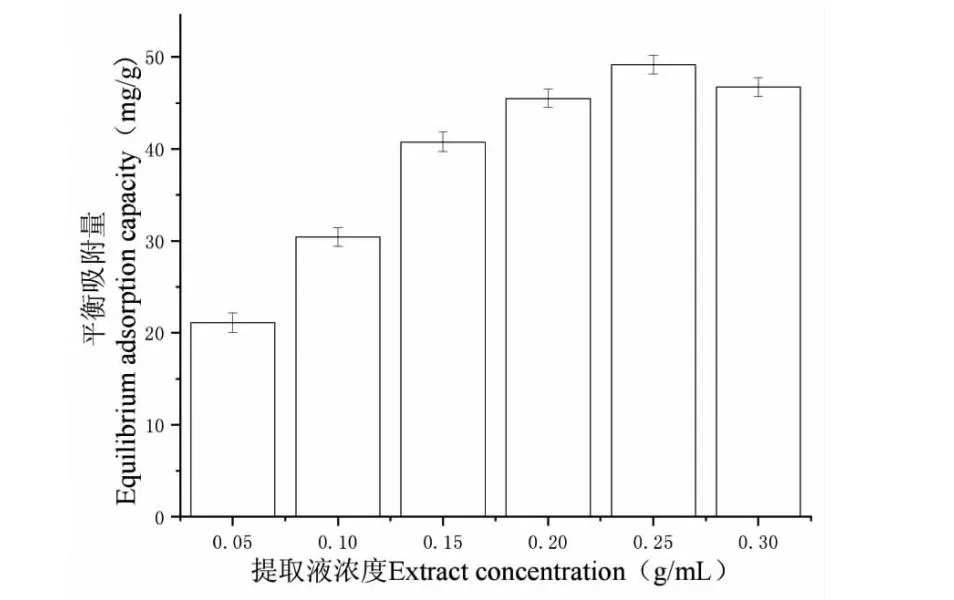
图2 不同上样浓度橄榄苦苷吸附量Fig.2 OL adsorption capacity of ifferent concentrations solution
为探索乙醇浓度对LX-68M树脂解吸性能及OL纯度的影响,选择7个不同浓度乙醇进行解吸实验。结果如图3a所示,解吸液乙醇浓度≤ 60%时,OL的纯度随着乙醇浓度的升高而升高;解吸液乙醇浓度超过60%后,OL的纯度开始下降。OL属于弱极性物质,随着乙醇浓度的增加,解吸液极性下降,解吸率也在增加,但这也使得了其他弱极性物质被洗脱出来,最终导致OL纯度的下降。解吸率由如图3b所示,解吸液乙醇浓度≤ 45%时,OL解吸率随着乙醇浓度的升高而增加,当解吸液乙醇浓度达到45%时,OL解吸率达到最大。因此,综合考虑试剂消耗和对OL收率、纯度的影响,选择45%乙醇作为洗脱剂。提取原液、吸附残液和解吸液高效液相色谱图如图4所示,说明LX-68M树脂实现了橄榄苦苷的分离纯化。
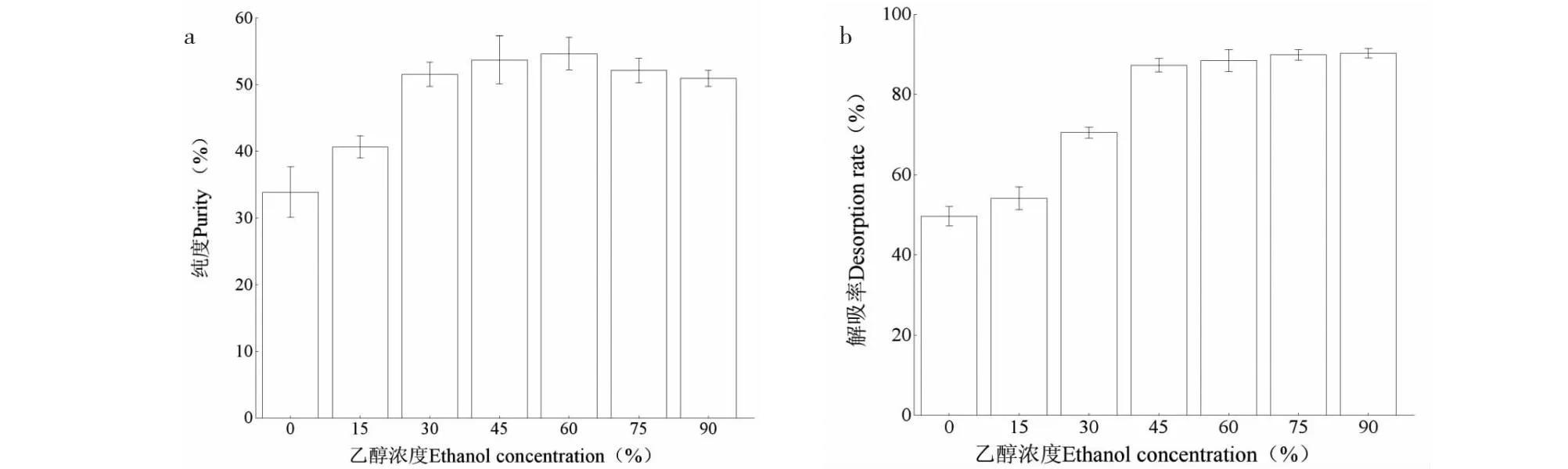
图3 不同浓度乙醇解吸橄榄苦苷纯度(a)、解吸率(b)Fig.3 Purity (a) and desorption rate (b) of oleuropein by ethanol at different concentrations
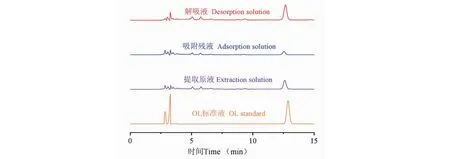
图4 OL标准品、提取原液、吸附残液、解吸液高效液相色谱图Fig.4 HPLC chromatogram of OL standard,extraction solution,adsorption solution,desorption solution
2.3 LX-68M树脂吸附动力学
为研究LX-68M树脂对OL的吸附动力学机理和吸附速率的影响参数,采用准一级,准二级和Elovich等动力学模型对相关动力学数据进行分析(表1)。其中实验数据和模型预测值之间的一致性由相关系数(R2)表示。R2值越高(接近或等于1)表示树脂的吸附动力学机理与动力学模型越吻合[26]。

表1 静态吸附动力学模型
吸附动力学参数如表2所示。以R2值为参考指标,可以看出LX-68M树脂吸附OL的行为更符合准二级动力学模型(R2=0.993 4)。此外,准二级动力学模型的理论吸附量Qe1=39.46 mg/g,与实验所得的平衡吸附量Qe=36.79 mg/g最接近。结果表明LX-68M树脂吸附OL可能符合化学吸附原理,从而达到富集、分离、纯化OL的目标[21,22,27,28]。进一步发现准二级动力学模型中初始吸附速率H(45.51mg/(g·h))较大,半吸附时间t1/2小于1 h,表明LX-68M树脂是吸附OL的良好材料。

表2 LX-68M树脂静态吸附动力学模型参数
2.4 LX-68M树脂静态等温吸附
等温吸附模型通常用来描述一定温度下吸附剂和被吸附物、平衡浓度与平衡吸附量以及各参数对吸附状态之间的相互作用关系。为确定OL的等温吸附行为,采用Langmuir、Freundlich等模型(表3)对相关动力学数据进行拟合、分析。其中实验数据和模型预测值之间的一致性由相关系数(R2)表示。R2值越高(接近或等于1)表示树脂的等温吸附与该等温静态吸附模型越符合。

表3 Langmuir和Freundlich等温静态吸附模型
由表4数据可知,Langmuir模型拟合曲线中,LX-68M树脂的R1值在0.96和0.99之间,说明在生药浓度范围为0.05~ 0.30 g/mL有利于OL的选择性吸附。然而,Qm值(83.10 mg/g)与实验值Qe(36.79 mg/g)差距较大。因此,Langmuir模型不能完全解释LX-68M树脂吸附OL的行为。Freundlich模型拟合曲线的R2=0.964 2,大于Langmuir模型拟合曲线的R2=0.850 6,表明Freundlich模型能更好地描述OL在树脂上的吸附行为。且Freundlich模型中1/n小于1,说明在该实验条件下有利于OL的吸附[22,25,29,30]。树脂的Kf=4.37 mg1-n/(g·mLn),这进一步表明LX-68M树脂对OL具有合适的吸附位点和吸附能力[22]。因此,LX-68M树脂吸附OL的过程更符合Freundlich等温吸附模型。

表4 LX-68M树脂的Langmuir和Freundlich等温静态吸附参数
2.5 LX-68M树脂动态吸附、解吸研究
采用动态吸附、解吸实验研究了上样速率、上样体积、洗脱速率、洗脱液体积对LX-68M树脂吸附、解吸性能的影响,结果如图5所示。图5a显示上样浓度为0.25 g/mL时,上样速率在1.0-5.0 BV/h范围内,4.0 BV流出液中OL的含量均小于1%,可看作吸附饱和。而上样速率在1.0 BV/h和2.0 BV/h下,上样体积分别为7.0 BV、6.0 BV时流出液中OL浓度开始上升,超过原液中OL浓度的10%,此时所对应的体积即为泄漏体积,3.0~5.0 BV/h上样速率下泄漏体积均为5.0 BV。由图5b可知,1.0~5.0 BV/h洗脱速率下均在2.0 BV时OL解吸量最大,并在洗脱液体积达到10.0 BV时,OL的总解吸率分别为87.85%、87.08%、81.14%、78.45%、75.12%。
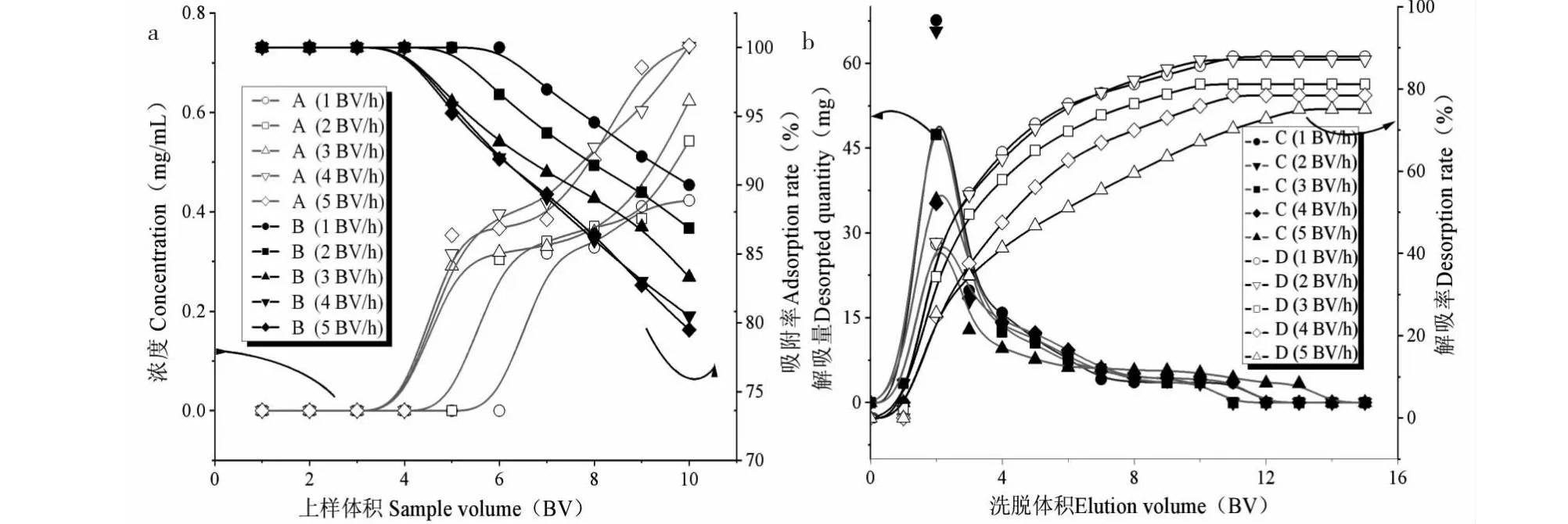
图5 LX-68M树脂不同流速下泄露曲线(a)、解吸曲线(b)Fig.5 Leakage curve (a),desorption curve (b) of LX-68M resin at different flow rates
总吸附量、解吸量如表5、表6所示,上样或解吸流速越快,总吸附率、总解吸率越低,原因可能是速率越快,提取液、洗脱液与树脂接触的时间越短,导致吸附、解吸率下降。且上样和洗脱速率超过2.0 BV/h后,总吸附率和总解吸率均大幅度下降,为保证较大的吸附、解吸率,同时综合考虑吸附、解吸时间及溶剂消耗,最终选择上样速率、洗脱速率均为2.0 BV/h,上样体积为6 BV,解吸液体积为10.0 BV。

表5 LX-68M树脂动态吸附性能参数

表6 LX-68M树脂动态解吸性能参数
在选择的最佳条件下取LX-68M树脂5.0 g采用湿法装柱,层析柱为1.0 cm ×40 cm,在上样浓度为0.25 g/mL,解吸液为45%乙醇,吸附、解吸速率均为2.0 BV/h时,所得到的OL纯度达到52.33%,吸附率、解吸率分别为86.86%、87.08%。进一步说明LX-68M树脂是富集、分离、纯化OL的良好材料。
2.6 LX-68M树脂再生
称取树脂0.20 g于50 mL离心管中,加入20.0 mL 0.25 g/mL提取液,置于恒温振荡器吸附6.0 h,用45%乙醇溶液解吸4.0 h,结果如图6所示。重复性实验表明,经4次吸附-解吸后树脂的吸附量为初始吸附量的54.9%。进一步,将经4次吸附-解吸后的树脂进行再生处理:先用2%NaOH溶液浸泡振荡12 h,用超纯水洗至中性,再用95%乙醇浸泡振荡12 h,用超纯水洗至无醇味。对再生后的树脂进行吸附实验,吸附率达到初始吸附率的93.51%,说明LX-68M经过再生后仍具有良好的吸附效率,具有一定工业化前景。
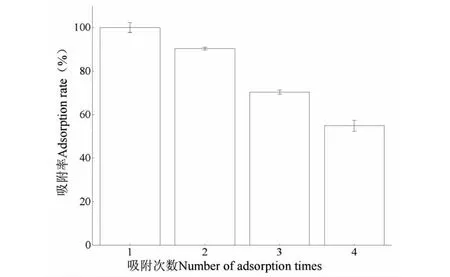
图6 LX-68M树脂重复利用实验Fig.6 Recycling experiments of LX-68M resin
3 结论
等温吸附实验结果显示,Freundlich等温吸附模型能很好地描述实验温度下LX-68M树脂吸附OL的过程,相关系数R2=0.964 2,即吸附利于进行。LX-68M树脂对OL的吸附更符合准二级动力学,R2=0.993 4,表明LX-68M树脂对于OL的吸附为物理吸附和化学吸附同时发生,且以化学吸附为主[31],其机理可能是树脂的基团与OL的官能团通过形成化学键。经静态、动态吸附与解吸附实验的优化得出最佳的分离条件为:提取液浓度0.25 g/mL,洗脱液为45%乙醇,上液速率为2.0 BV/h,上样体积为6.0 BV,解吸速率2.0 BV/h,解吸液体积为10.0 BV;此时的吸附率、解吸率分别为86.86%、87.08%,所得OL的纯度为52.33%。当树脂吸附-解吸4次后吸附效率为54.9%,经再生后,吸附率达到初始吸附率的93.51%,表明树脂再生后仍具有较好的吸附性能。上述结果说明,LX-68M树脂对于OL具有良好富集、分离、纯化效率,且与现有工艺相比,本工艺为常温常压操作,安全简便,所用均为绿色无毒的溶剂,可以为阴离子树脂在OL及相似天然产物分离纯化工业上的应用提供理论研究基础和技术支持。虽然本研究探讨了LX-68M树脂对OL的吸附过程,但杂质与OL产生的吸附竞争行为,也会对分离效率产生一定的影响。因此,仍需进行相关研究以确定相应的吸附机理,为LX-68M树脂的进一步开发利用提供理论依据。