DAG和LML型结构脂质的热力学及煎炸应用特性研究
连伟帅,孙晓洋,高雪琴
河南牧业经济学院 食品与生物工程学院,河南 郑州 450046
0 引言
油脂是我们日常饮食中必不可少的一种食品原料,具有独特的风味。但过量摄入油脂会引起脂肪累积,导致肥胖及由肥胖引起的多种慢性疾病[1]。研究[2]证实,甘油二酯(Diacylglycerol,DAG)具有与天然动植物油脂相同的脂肪酸组成,是一种既具有油脂风味,又不会使脂肪在体内累积的健康油脂,但目前针对其理化性质及应用的研究仍较少。目前市场上流通的“Enova”食用油脂产品,是将混合油脂水解后,分离提取游离脂肪酸,并对液体脂肪酸进行酯化而获得的DAG产品,该产品的脂肪酸组成已与天然动植物油脂大不相同。
Y.Cao等[3]在DAG的基础上开发了长-中-长(Long-Medium-Long,LML)型结构脂质,并初步证实该结构脂质具有与DAG相似的可降低餐后血脂水平、减少实验动物体内脂肪累积等生理功能,具有替代日常食用油脂的潜力。作为一种新型结构脂质,目前LML型结构脂质的制备还处于起步阶段,但因其结构与常规油脂中的甘油三酯(Triacylglycerol,TAG)相似性较高,故具有良好的应用前景[4]。
在日常食品加工中,食用油脂的应用非常广泛,其中,煎炸工艺对其品质的要求最高[5]。在煎炸工艺中,食用油脂需长时间处于较高温度,而高温对其理化性质及稳定性的要求均较其他加工工艺更为苛刻[6]。
基于此,本研究拟以近年来热门的功能性健康油脂DAG(50%DAG、90%DAG)和LML型结构脂质为研究对象,针对目前三者理化性质的分析不全面且缺乏应用特性研究的现状,以大豆油为对照,研究其理化性质、热力学特性及煎炸应用特性,以期为功能性油脂在日常膳食中的应用提供科学依据和参考。
1 材料与方法
1.1 主要材料与试剂
一级大豆油、新鲜荷兰土豆,广州市售;p-茴香胺试剂、卡尔费休试剂,百灵威科技有限公司;淀粉指示剂,国药集团化学试剂有限公司;乙醚、异丙醇、三氯甲烷、冰乙酸、硫代硫酸钠、异辛烷,上海润捷化学试剂有限公司;37种脂肪酸甲酯标准品,上海Sigma-Aldrich有限公司。以上试剂均为分析纯。
1.2 主要仪器与设备
Agilent 7890A型气相色谱仪,安捷伦科技有限公司;Warters 2695型高效液相色谱仪,美国Waters公司;PB-10标准型pH计,德国Sartorius公司;V20 S型卡尔·费休水分测定仪,瑞士Mettler Toledo公司;NDJ-1型旋转式黏度仪,上海精科有限公司;VERTEX 70型傅里叶变换红外光谱(FTIR)仪,德国Spectro公司;TG 209 F1 Libra型热重分析仪、DSC 214型差示扫描量热仪,德国Netzsch公司;TA. XT. plus型质构仪,英国SMS公司;AF229型全自动分光色度仪,德国罗威邦公司;AVANCEⅢHD600型脉冲核磁共振仪,德国Bruker公司。
1.3 实验方法
1.3.1DAG和LML型结构脂质制备参照D.M.Li等[7]的方法制备DAG,所得DAG的含量为90%,根据实验需要,使用大豆油进行稀释。参照W.S.Lian等[8]的方法,以大豆油乙酯与三辛酸甘油酯进行酯交换制得LML型结构脂质,其中TAG的含量在99.2%以上,中链脂肪酸含量不低于30%。
1.3.2 油脂样品理化指标测定1)酸价(AV)测定。参照《食品安全国家标准 食品中酸价的测定》(GB 5009.229—2016)[9],称取约2 g油脂样品(m)于250 mL锥形瓶中,加入50 mL乙醚-异丙醇混合液(V(乙醚)∶V(异丙醇)=1∶1)和3滴酚酞指示剂,振摇混匀;用0.05 mol/L的KOH溶液对样品进行滴定,当试样初现微红色且15 s内无明显褪色时,为滴定终点。记录所消耗的KOH溶液体积(V/mL);同时进行空白实验,并记录所消耗的KOH溶液体积(V0/mL)。按照下式计算AV/(mg KOH·g-1):
AV=(V-V0)×c×56.1/m
式中,c为KOH溶液浓度。
2)过氧化值(POV)测定。参照《食品安全国家标准 食品中过氧化值的测定》(GB 5009.227—2016)[10],称取2~3 g油脂样品(m1)于250 mL碘量瓶中,加入30 mL三氯甲烷-冰乙酸混合液,轻轻振摇混匀;加入1 mL饱和KI溶液,塞紧瓶盖,振摇0.5 min,静置3 min;加人100 mL蒸馏水,摇匀后,立即用0.002 mol/L的硫代硫酸钠标准溶液滴定至淡黄色;加入1 mL淀粉指示剂,继续滴定并摇晃,溶液蓝色消失为终点,记录所消耗的硫代硫酸钠标准溶液体积(V1/mL);同时进行空白实验,并记录所消耗的硫代硫酸钠标准溶液体积V′0(≤0.1 mL)。按照下式计算POV/(g·(100 g)-1):
POV=(V1-V′0)×c′×0.126 9×100/m1
式中,c′为硫代硫酸钠标准溶液浓度。
3)茴香胺值(AnV)测定。参照《动植物油脂 茴香胺值的测定》(GB/T 24304—2009)[11],称取1 g油脂样品(m2),用异辛烷定容至50 mL(V2);在具塞试管中加入5 mL样品溶液和1 mL冰醋酸,盖上盖子后摇匀,暗处静置8 min后,在2 min内将样品溶液转移至比色皿中,用异辛烷在350 nm处校正零点,以异辛烷为对照,测定吸光度(A0);在具塞试管中加入5 mL样品溶液和1 mL茴香胺试剂,按照上述方法测定吸光度(A1);在具塞试管中加入5 mL异辛烷和1 mL茴香胺试剂,按照上述方法测定吸光度(A2)。按照下式计算AnV/(mmol·kg-1):
AnV=V2×1.2×(A1-A2-A0)/m2
4)水分含量测定。参照马跃龙等[12]的方法,将一定体积的卡尔·费休试剂A液加入反应瓶中,浸没铂金电极,边搅拌边用卡尔·费休试剂B液预滴定至终点;准确加入100 mg油脂样品(减差法),用卡尔·费休试剂B液预滴定至终点,记录检测到的水分含量。
5)色度测定。参照王海霞[13]的方法,采用全自动分光色度仪进行测定。使用基色板对仪器进行校准后,称取约25 g油脂样品于槽型比色皿中,置于仪器上进行测定,读取L*(亮度值)、a*(红度值)和b*(黄度值);将比色皿用乙醇冲洗并吹干后,再测定下一个油脂样品。
6)黏度测定。将一定体积的油脂样品放入旋转式黏度仪容器中,使转子在液体中匀速旋转,待数值趋于稳定后读取数值,即为油脂样品的黏度。
1.3.3 油脂样品性质测定1)甘油酯组成测定。参照D.M.Li等[14]的方法,将经无水硫酸钠脱水后的20 μL油脂样品加入1 mL流动相(V(正己烷)∶V(异丙醇)∶V(甲酸)=18∶1∶0.003)中,采用高效液相色谱仪测定油脂样品中的甘油酯组成。具体分析条件为:Phenomenex Luna 5um Silica 100A色谱柱(250 mm×4.60 mm),柱温箱温度30 ℃,流动相流速1 mL/min,柱压2.76 MPa,进样量10 μL。
2)脂肪酸组成测定。参照X.M.Wang等[15]的方法,采用气相色谱仪(色谱柱为CP-SIL88毛细管柱)测定油脂样品中的脂肪酸。具体分析条件为:柱前压137 kPa,分流比25∶1,N2流量25 mL/min,空气流量400 mL/min,H2流量40 mL/min;升温程序为在140 ℃保留5 min,以4 ℃/min速率升温至200 ℃并保留2 min,再以4 ℃/min速率升温至220 ℃并保留17 min。
3)FTIR谱图测定。参照P.N.G.Siou等[16]的方法,将除水后的油脂样品均匀涂抹至模型压片上,再置于FTIR仪上进行检测,检测波数为4000~400 cm-1。
4)热重分析(TG)方法。参照顾敏芬等[17]的方法,采用热重分析仪对油脂样品进行TG分析。检测温度为室温至600 ℃,升温速率为10 ℃/min,记录油脂样品在加热过程中的失重起始温度、失重峰值温度及失重速率曲线。
5)差示扫描量热分析(DSC)方法。参照L.Zhao等[18]的方法,采用差示扫描量热仪对油脂样品进行DSC分析。检测温度为-70~80 ℃,升温速率为10 ℃/min,对检测得到的油脂结晶曲线进行分析,记录结晶起始温度、结束温度、峰值温度等指标。
6)固体脂肪含量(SFC)测定。参照《动植物油脂 脉冲核磁共振法测定固体脂肪含量 间接法》(GB/T 37517—2019)[19],称取3~4 mg油脂样品于脉冲核磁共振仪的核磁管中,置于60 ℃水浴中恒温加热1 h,使油脂样品完全呈液态后,在0 ℃条件下冷却30 min,将预冷后的油脂样品在5~30 ℃条件下进行检测。每个温度检测时均应预热30 min。
1.3.4 油脂样品高温煎炸实验1)实验设计及取样。取大豆油、DAG和LML型结构脂质各3 L,分别置于4.5 L油炸锅中,将油炸锅温度设置为180 ℃,加热稳定1 h以上,待温度稳定在(180±5)℃后,待用。将新鲜荷兰土豆洗净去皮,切成1 cm×1 cm×8 cm土豆条,开水漂烫2 min后,置于冷水中,备用。每次煎炸土豆条200 g,煎炸持续5 min,间隔15 min后再进行下一次煎炸实验,每小时煎炸3个批次土豆条。取煎炸第0 h、2 h、4 h、6 h、8 h和10 h的油脂样品各50 mL,冷却后保存于-20 ℃冰箱中,并取1批次、7批次、13批次、19批次、25批次和30批次的煎炸土豆,备用。
2)煎炸后油脂分析方法。煎炸后油脂样品的理化指标按照1.3.2方法进行测定。
3)被煎炸土豆条质构特性测定。参照R.Xiong等[20]的方法,采用质构仪分析被煎炸土豆条的质构特性[21]。采用P/50探头进行全质构(TPA)分析:测前和测中速度均为1 mm/s,测后速度为5 mm/s,压缩比为75%,两次压缩之间停顿5 s,出发力值为0.2 N。采用A/WEG探头进行剪切力分析:测前和测中速度均为1 mm/s,测后速度为5 mm/s,压缩比为95%,出发力值为0.2 N。
1.4 数据统计与分析
每组实验均重复3次,数据通过SPSS分析软件进行处理,结果使用(平均值±标准差)表示,同因素不同水平进行单因素方差分析(ANOVE),采用软件Origin 9.0绘图。
2 结果与分析
2.1 DAG和LML型结构脂质的甘油酯和脂肪酸组成分析
DAG和LML型结构脂质的甘油酯和脂肪酸组成见表1。由表1可知,大豆油和LML型结构脂质的主要组分为TAG,只有少量DAG存在;50%DAG和90%DAG的脂肪酸组成与大豆油的脂肪酸组成基本一致;LML型结构脂质中C8∶0含量为30.28%,且含有少量C10∶0(0.13%),其余脂肪酸的组成与大豆油的脂肪酸组成也基本保持一致。
2.2 DAG和LML型结构脂质的理化性质分析
DAG和LML型结构脂质的理化指标见表2。由表2可知,4种油脂的色度中,L*和a*基本相同,b*随着油脂中DAG含量的增加而增加,而LML型结构脂质的a*、b*与大豆油相比均略有增加,但低于50%DAG和90%DAG,这可能是因为DAG和LML型结构脂质在经分子蒸馏分离时,180 ℃的高温导致油脂色度有一定程度的加深。在新版《大豆油》(GB/T 1535—2017)[22]中,对一级大豆油的色泽要求为淡黄色或浅黄色,而在旧版《大豆油》(GB/T 1535—2003)[23]中,要求一级大豆油的b*应低于20,a*应低于2,而4种油脂的色度均符合上述标准。与大豆油相比,50%DAG和90%DAG的黏度均增加了0.2 Pa·s,而密度基本一致,这表明油脂的密度受甘油酯分子结构和脂肪酸组成改变的影响较小。50%DAG、90%DAG和LML型结构脂质的AV和POV均低于国家一级大豆油要求的0.5 mg KOH/g和0.13 g/100 g。相较于大豆油,50%DAG、90%DAG和LML型结构脂质的AnV均有所升高,这可能是因为精炼过程中温度较低,实验室自制设备不能达到优异的脱臭条件,但该数值仍处于较低水平,与胡桃油的AnV(6.35 mmol/kg)较接近[22]。
2.3 DAG和LML型结构脂质的FTIR分析


表1 DAG和LML型结构脂质的甘油酯和脂肪酸组成Table 1 Glyceride and fatty acid composition of DAG and LML structured lipids %

表2 DAG和LML型结构脂质的理化指标Table 2 The physical and chemical indicators of DAG and LML structured lipids
2.4 DAG和LML型结构脂质的TG分析
DAG和LML型结构脂质的TG分析如图2所示。由图2可知,大豆油的失重峰值为409.3 ℃,50%DAG的失重峰值为412.2 ℃,但50%DAG的失重起始温度为280 ℃,略早于大豆油(290 ℃)。随着DAG含量增加到90%,失重起始温度提前至250 ℃,失重峰值也降至366.7 ℃,与LML型结构脂质较接近。这表明甘油骨架上—OH的暴露及长链脂肪酸被中链脂肪酸取代均会导致油脂失重起始温度等降低[24]。

图1 DAG和LML型结构脂质的FTIR谱图Fig.1 The FTIR chromatograms of DAG and LML structured lipids

图2 DAG和LML型结构脂质的TG分析Fig.2 TG analysis of DAG and LML structured lipids
2.5 DAG和LML型结构脂质的DSC分析
DSC是油脂检测中常用的一种热力学分析方法,通过监测油脂从低温到高温的融化过程,获得油脂熔融曲线[25]。DAG和LML型结构脂质的DSC熔融曲线如图3所示。由图3可知,大豆油的熔融过程在30 ℃下快速完成了相态变化,这可能是由其成分中99%以上都为TAG所致。50%DAG的整个结晶区间为-35.7~13.2 ℃,横跨39.4 ℃,这一结果与I.F.Oliveira等[26]和P.N.G.Siou等[16]的研究结果较一致。90%DAG的熔融区间跨度仅为14.3 ℃,较50%DAG减少了63.7%,略低于LML型结构脂质(15.6 ℃)。
另外,大豆油、50%DAG、90%DAG和LML型结构脂质的相变峰值依次为-27.3 ℃、-27.5 ℃、-2.7 ℃和-10.4 ℃,且在50%DAG中出现了-3.7 ℃峰值,与90%DAG中出现的-2.7 ℃峰值非常接近。由此推断,50%DAG的熔融曲线是由TAG以-27.5 ℃为峰值的相态变化与DAG以-2.7 ℃为吸收峰的相态变化的结合。TAG与DAG的熔点有25 ℃左右的温差,故导致含DAG的油脂在结晶时会出现温度跨度较大的熔融曲线。LML型结构脂质中因存在熔点较低的中链脂肪酸,其结晶曲线的起点会相应提前,且基本不含DAG,而其熔融曲线起始温度为-10.4 ℃,远高于大豆油(-30 ℃)。
2.6 DAG和LML型结构脂质的SFC分析
DAG和LML型结构质脂质的SFC随温度的变化如图4所示。由图4可知,在5 ℃时,SFC随着4种油脂中DAG含量的增加而升高,90%DAG中的SFC达到11.36%,LML型结构脂质中因存在中链脂肪酸,其SFC高于50%DAG。陈琼等[27]的研究也发现,DAG的结晶温度比TAG低10 ℃左右,这会导致在低温时SFC增加。在20 ℃时,4种油脂中的SFC均处于较低水平,而在25 ℃时,基本均无固体脂肪存在。而大豆油的结晶温度远低于检测温度,故在整个检测过程中,大豆油中的SFC均在2%以下。
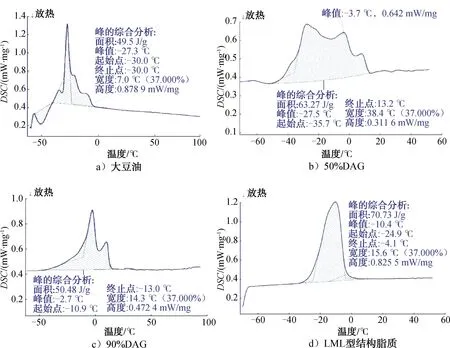
图3 DAG和LML型结构脂质的DSC熔融曲线图Fig.3 DSC melting curve chart of DAG and LML structured lipids
2.7 DAG和LML型结构脂质煎炸应用特性分析

图4 DAG和LML型结构脂质的SFC随温度的变化Fig.4 The change of SFC of DAG and LML structured lipids with temperature

图5 煎炸油脂样品AV随煎炸时间的变化Fig.5 The change of AV of fried oil samples with frying time
2.7.1 煎炸对DAG和LML型结构脂质AV的影响由于被煎炸土豆中含有大量的水分,油脂在高温、有水的环境下会发生甘油酯水解等一系列反应,而水解出的游离脂肪酸非常不稳定且易被氧化,因此煎炸后油脂的品质、使用周期等受油脂煎炸后AV的影响较大。煎炸油脂样品AV随煎炸时间的变化如图5所示。由图5可知,随着煎炸时间的延长,煎炸油脂样品的AV均呈上升趋势,其中90%DAG在煎炸2 h后的AV明显高于其他油脂样品,且在煎炸10 h时达到1.18 mg KOH/g,其次是50%DAG,而LML型结构脂质和大豆油在煎炸10 h后的AV均处于较低水平。这可能是由于DAG中含有一个亲水性空位—OH,使水分子更易接近甘油酯分子而加速其水解,这与Y.Watanabe等[28]的研究结果较一致。在日本、德国等国家的煎炸油脂卫生标准中,要求煎炸油脂的AV应低于2 mg KOH/g[29],本研究中90%DAG在煎炸10 h后的AV是最高的,仍低于此标准要求。
2.7.2 煎炸对DAG和LML型结构脂质POV的影响煎炸油脂样品POV随煎炸时间的变化如图6所示。由图6可知,随着煎炸时间的延长,油脂样品的POV均呈上升趋势,但50%DAG和90%DAG的POV上升程度较缓慢,特别是50%DAG,在煎炸10 h时的POV基本与0 h时相同。这可能是因为DAG在煎炸过程中发生了较多水解反应,避免了脂肪酸的氧化反应。M.Shimizu等[30]的研究也发现,DAG在煎炸过程中的氧化脂肪酸含量低于TAG,但具体原因尚未得到证实。
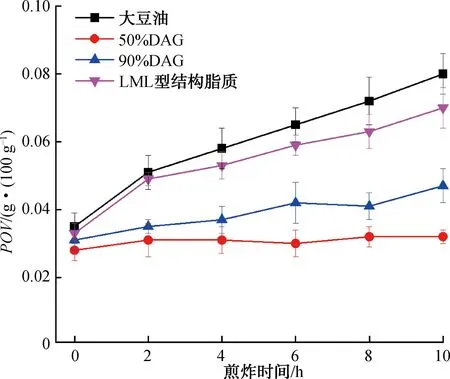
图6 煎炸油脂样品POV随煎炸时间的变化Fig.6 The change of POV of fried oil samples with frying time
2.7.3 煎炸对DAG和LML型结构脂质色度的影响煎炸油脂样品色度随煎炸时间的变化见表3。由表3可知,煎炸油脂样品的L*整体上均随着煎炸时间的延长而降低,90%DAG降低的程度较其他油脂样品明显,在煎炸10 h时降低了3.21,而大豆油仅降低了1.23,这可能是因为90%DAG在煎炸过程中发生了较多水解反应,其水分含量较高,导致澄清度降低。煎炸油脂样品的b*均呈上升趋势,在煎炸10 h时,大豆油增加最明显,增加了9.60,而90%DAG增加最少,仅增加了2.85。这可能是因为90%DAG的初始b*较高。大豆油和LML型结构脂质的a*整体上均呈降低趋势,而90%DAG则呈升高趋势,50%DAG呈先降低后升高趋势。煎炸10 h后,50%DAG和LML型结构脂质的色度仍满足《大豆油》(GB/T 1535—2003)[23]中一级大豆油的色度标准(a*<2,b*<20)。
2.7.4 煎炸对DAG和LML型结构脂质水分含量的影响煎炸油脂样品水分含量随煎炸时间的变化如图7所示。由图7可知,煎炸油脂样品在煎炸过程中的水分含量均呈先上升后下降的趋势,其中,在相同煎炸时间下,90%DAG的水分含量均高于其他油脂样品,且煎炸4 h时水分含量最大,为0.108%。这与前文90%DAG中AV偏高、L*偏低的结果相符。

图7 煎炸油脂样品水分含量随煎炸时间的变化Fig.7 The change of moisture content of fried oil samples with frying time
2.7.5 煎炸对DAG和LML型结构脂质AnV的影响煎炸油脂样品AnV随煎炸时间的变化如图8所示。由图8可知,随着煎炸时间的延长,煎炸油脂样品的AnV均明显上升,在煎炸10 h时,大豆油和LML型结构脂质的AnV均达到100以上,分别为162.81和141.26,而此时50%DAG和90%DAG的AnV均较低,特别是50%DAG,其AnV仅为53.71,具体原因仍需进一步研究。
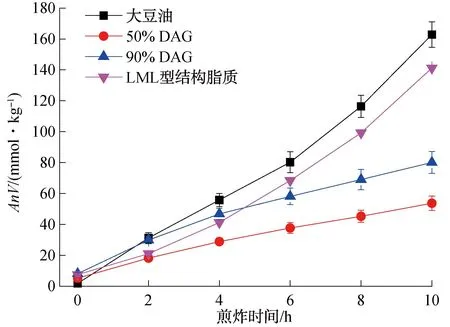
图8 煎炸油脂样品AnV随煎炸时间的变化Fig.8 The change of AnV of fried oil samples with frying time
2.7.6 煎炸对DAG和LML型结构脂质甘油酯组成的影响煎炸油脂样品的甘油酯组成如图9所示。由图9可知,经10 h煎炸后,大豆油中出现了1.31%的DAG;50% DAG中出现了少量MAG(0.82%)和FFA(0.38%);90%DAG中的DAG含量减少了2.78%,这些减少的DAG经水解反应转化成了MAG和FFA;而LML型结构脂质的DAG含量(2.46%)略高于大豆油,这可能是因为在高温煎炸过程中,中链脂肪酸相较于长链脂肪酸具有更好的稳定性,但其最终含量仍处于较低水平。
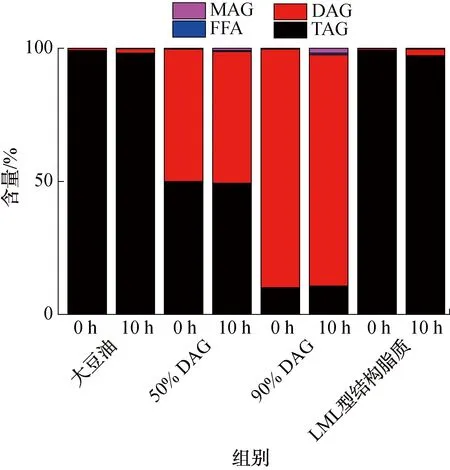
图9 煎炸油脂样品的甘油酯组成Fig.9 The glyceride composition of fried oil samples
2.8 被煎炸土豆条的质构特性分析
在煎炸过程中,油脂对煎炸物的影响主要体现在被煎炸物的脱水率及被煎炸物吸收煎炸油后的质构特性变化[26]。随着煎炸时间的延长,各批次被煎炸土豆条的水分含量均稍有降低,硬度逐渐升高。在煎炸10 h时,大豆油、50%DAG、90%DAG和LML型结构脂质所煎炸土豆条的水分含量分别为28.53%、28.69%、29.04%和28.57%,硬度分别为865 N、874 N、882 N和868 N。综上可知,煎炸油脂样品对被煎炸土豆条的水分含量和硬度的影响差异较小。
3 结论
本文以大豆油为对照,研究了50%DAG、90%DAG和LML结构脂质的理化性质、热力学特性及在高温煎炸中的应用特性,得到以下结论:50%DAG、90%DAG和LML结构脂质与大豆油的黏度、密度和POV基本一致,且LML型结构脂质与大豆油的甘油酯组成也基本一致,50%DAG、90%DAG的AnV较高,但仍低于一级大豆油标准。与大豆油相比,50%DAG、90%DAG和LML型结构脂质的失重起始温度均有20~30 ℃的降低,这是由其结构和脂肪酸的改变所致。油脂中的DAG会导致熔融曲线的区间变宽,相变速率下降,而90%DAG的相变过程则出现一定程度的缩短;与大豆油相比,LML型结构脂质在FTIR谱图中呈现一致的吸收峰,而50%DAG和90%DAG在3470 cm-1处出现明显差异。经10 h煎炸后,50%DAG、90%DAG和LML型结构脂质的AV、POV、色度、水分含量、AnV、甘油酯组成均表现出良好的稳定性,仅50%DAG和90%DAG中出现了由水解反应产生的MAG与FFA,但整体含量较低。后续将就结构和脂肪酸变化所引起的油脂性质变化进行深入研究,以探寻优质的日常食用油替代品,为功能性健康油脂的开发与应用提供参考。

