心房颤动相关急性缺血性脑卒中早期抗凝治疗有效性和安全性的Meta分析
王运香,齐旭慧,蔡焕焕,鲁志兵
1. 武汉大学中南医院心血管内科(武汉 430071)
2. 武汉大学心肌损伤与修复研究所(武汉 430071)
3. 武汉大学中南医院消化内科(武汉 430071)
心房颤动(atrial fibrillation,AF)是缺血性脑卒中(ischemic stroke,IS)的常见病因[1-3],在各种心源性卒中病因中,AF 相关性IS 在90 d 时发生不良功能结局的风险更高[4],并且AF 与IS 复发密切相关[5]。抗凝治疗是AF 相关IS 二级预防重要的一部分,且新型口服抗凝药物(new oral anticoagulants,NOAC),如利伐沙班、阿哌沙班、艾多沙班、达比加群酯,在有效性和安全性方面效果更优[1,6-10]。研究表明IS 复发风险在患病后最初几天内最高[11]。另一方面,AF 相关IS 出血转化风险较高[12],早期抗凝又具有相当大的出血风险。因此,抗凝治疗开始时间在临床上一直没有定论。美国心脏协会/美国卒中协会和欧洲卒中组织指南对此都缺乏具体建议[7-8]。有研究表明最佳抗凝治疗窗口为4~14 d[11],基于此研究,有指南推荐在卒中发作后4~14 d 开始口服抗凝治疗[13]。然而,近期研究表明4 d 内或者更早开始应用NOAC 抗凝并不劣于延迟抗凝[14-16]。因此,本文尝试收集目前已发表的临床研究,以评估在AF 相关急性缺血性脑卒中(acute ischemic stroke,AIS)发作后3 d 内应用NOAC 的有效性和安全性,为临床决策提供参考。
1 资料与方法
1.1 纳入与排除标准
纳入标准:(1)研究对象为AF 相关AIS 患者;(2)研究类型为随机对照试验(RCT)或非随机临床试验;(3)干预措施:试验组服用NOAC早期抗凝(≤3 d)治疗,对照组服用NOAC 延迟抗凝(>3 d);(4)结局指标:①安全性终点:大出血、症状性脑出血(symptomatic intracerebral haemorrhage,sICH)、全部脑出血;②有效性终点:IS 复发或短暂性脑缺血发作(transient ischemic attack, TIA)、总缺血事件(包括IS 复发、TIA及其他部位栓塞性事件的综合)。
排除标准:(1)研究对象为动物;(2)对同一组研究对象,在不同随访时间段内,只纳入数据最完整或随访时间最长的研究;(3)数据不全、无法提取结局指标或无法获取全文的研究;(4)个案报道、会议报告、综述性文献等。
1.2 文献检索策略
计算机检索PubMed、The Cochrane Library、Embase、中国知网、万方及维普等数据库。英文检索词包括:atrial fibrillation、ischemic stroke、anticoagulants、new oral anticoagulant、direct oral anticoagulant、NOAC、DOAC、rivaroxaban、apixaban、edoxaban、dabigatran、early;中文检索词包括:心房颤动、缺血性脑卒中、新型口服抗凝药、抗凝、利伐沙班、阿哌沙班、艾多沙班、达比加群酯、早期、时机。采取主题词加自由词的方法检索文献。检索范围均从建库至2022 年11 月4 日,文献语言限制为中英文。另外,还手动检索了已发表文章的参考文献列表,以确保检索文献的全面性。以PubMed 为例,本研究检索策略如下(框1)。
1.3 文献筛选和数据提取
由两位研究者独立进行文献筛选与数据提取,出现分歧时通过协商或与第三位研究者讨论解决。根据前文所述纳入、排除标准进行文献筛选。首先通过软件自动去重以及阅读文献题目和摘要进行初筛,排除重复与无关文献,然后阅读全文进行复筛,最终确定纳入Meta 分析的文献。本数据提取内容包括作者姓名、发表时间、研究地区、研究类型、样本量、抗凝剂类型、抗凝开始时间、随访时间、结局指标及患者特征。患者特征包括:(1)女性比例;(2)患者平均年龄;(3)美国国立卫生研究院卒中量表(NIHSS)、CHA2DS2-VASc 和HAS-BLED 评分;(4)伴随疾病。
1.4 纳入文献偏倚风险评估
本文采用Cochrane 风险偏倚评估工具对纳入文献中的RCT 研究进行质量评价,使用MINORS评价条目对非随机临床试验进行质量评价[17-18]。每项研究均由两名研究者独立进行质量评价和数据提取,意见不同时通过协商解决。
1.5 统计学分析
应用RevMan 5.4 软件进行数据分析及评价。二分类变量以相对危险度(relative risk,RR)及95%CI 表示。连续性变量以加权均数差及95%CI表示,所提取的数据为中位数及四分位数间距时使用数据转换工具[19]转换为±s。卡方检验及Q检验用于异质性检验,当I2<50%且P≥0.1时,认为各研究间异质性较小,采用固定效应模型分析,否则认为各研究间异质性较大,采用随机效应模型分析结果。双侧P值<0.05 被认为具有统计学意义。每项结局指标纳入文献较少,故未行发表偏倚评估。
2 结果
2.1 文献检索和筛选
共检索出1 016 篇文献,根据纳入排除标准,经层层筛选最终纳入7 篇临床研究,其中包括RCT 研究2 篇[20-21]和非随机对照试验5 篇[22-26](图1)。
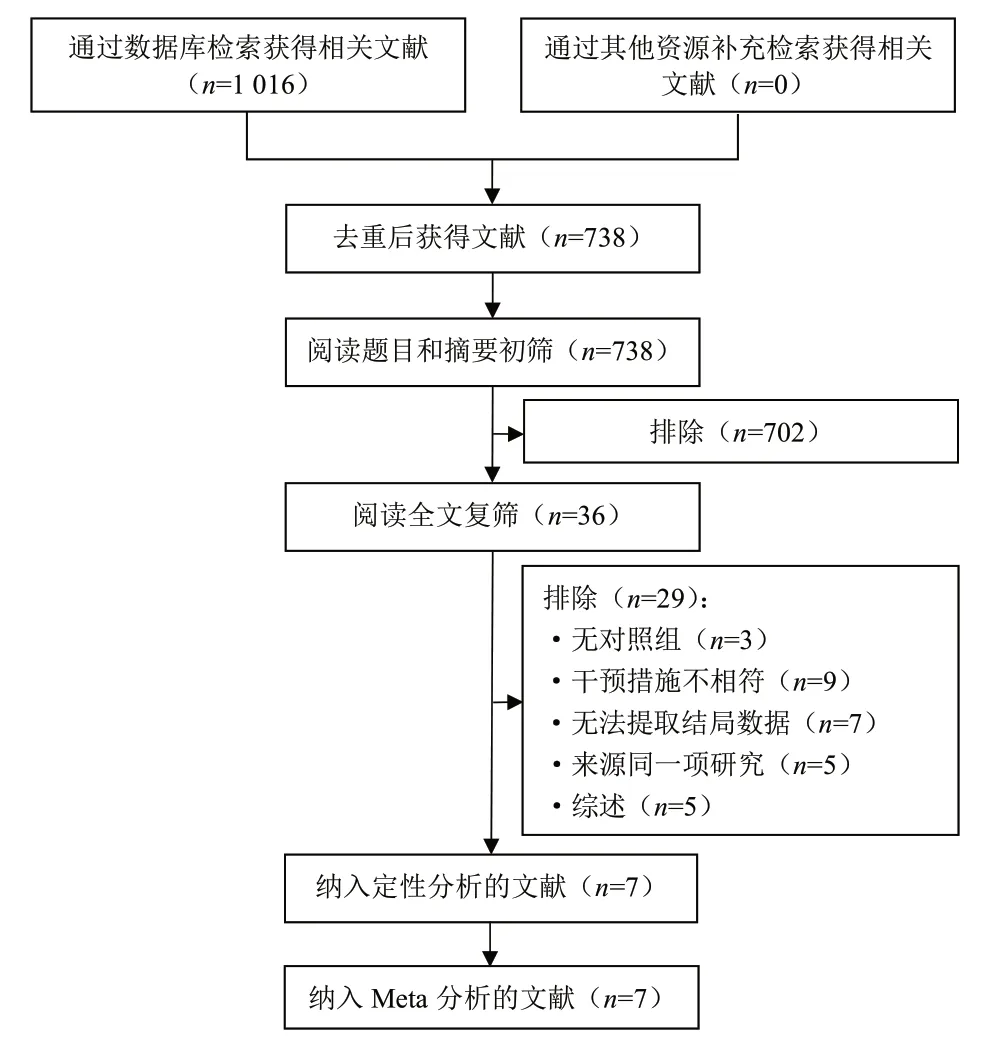
图1 文献筛选流程及结果Figure 1. Flow chart of literature screening and results
2.2 纳入文献基本信息和偏倚风险评估结果
纳入文献包括2 226 例AF 相关AIS 患者,早期抗凝组1 120例,对照组1 106例,来自4个国家,随访时间7 d 至2 年不等。各项研究基本特征见表1。本研究纳入的2 篇RCT 研究采用Cochrane风险偏倚评估工具进行质量评价(图2),2 篇研究均未明确说明实施了分配隐藏及盲法,且样本量偏少,可能存在混杂偏倚。5 篇非随机对照试验采用MINORS 评价条目进行质量评价(表1)。该评价条目共12 条,总分24 分,评分越高,研究质量越高。每项研究得分均在17 分以上,认为是高质量研究。
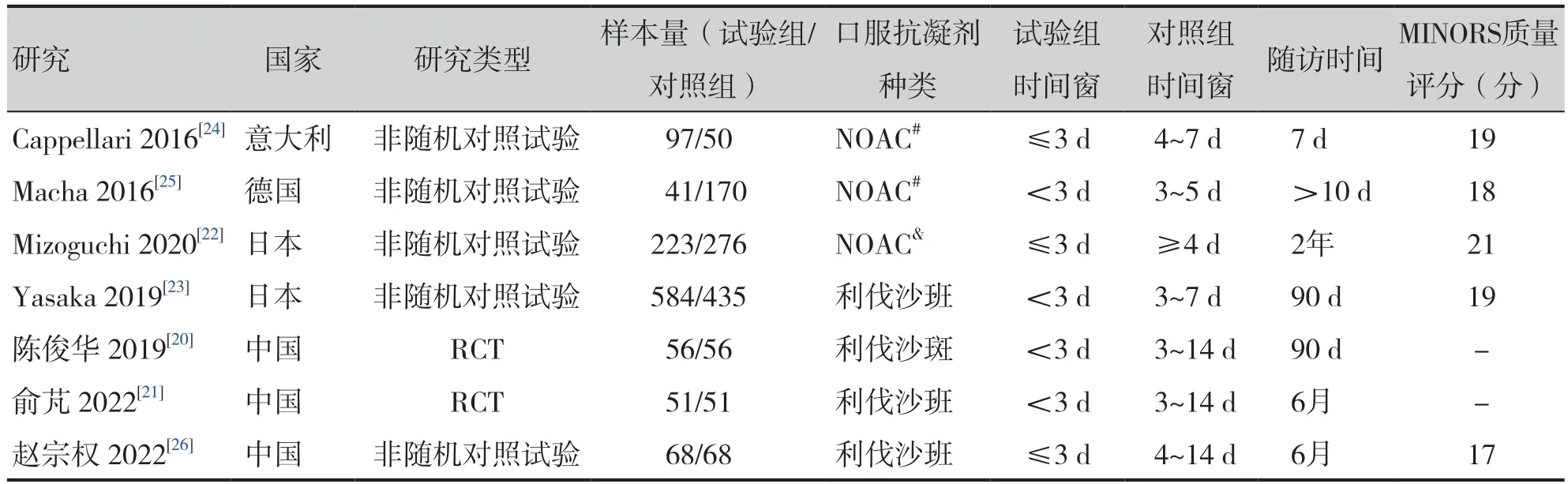
表1 纳入研究的基本特征及非随机对照试验研究质量评价Table 1. Basic characteristics of included literatureand non-randomized controlled trial research quality assessment
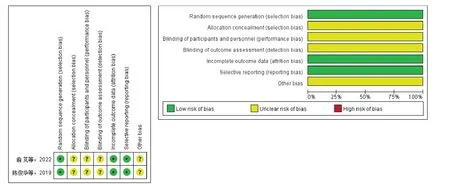
图2 随机对照试验质量评价Figure 2. Quality evaluation of randomized controlled trials
2.3 Meta分析结果
2.3.1 基线数据
本文比较了早期抗凝组和对照组的基线数据,早期抗凝组患者NIHSS 水平及合并糖尿病比例偏低(表2),进行敏感性分析,发现Macha等研究[25]对基线水平影响较大,且该研究中仅报道了1 例sICH 及2 例无症状性脑出血,剔除后发现各项基线水平差异无统计学意义(表3),且对主要结局指标无影响。

表2 7项研究早期抗凝组与对照组基线数据对比Table 2. Comparison of baseline data between early anticoagulation group and control group
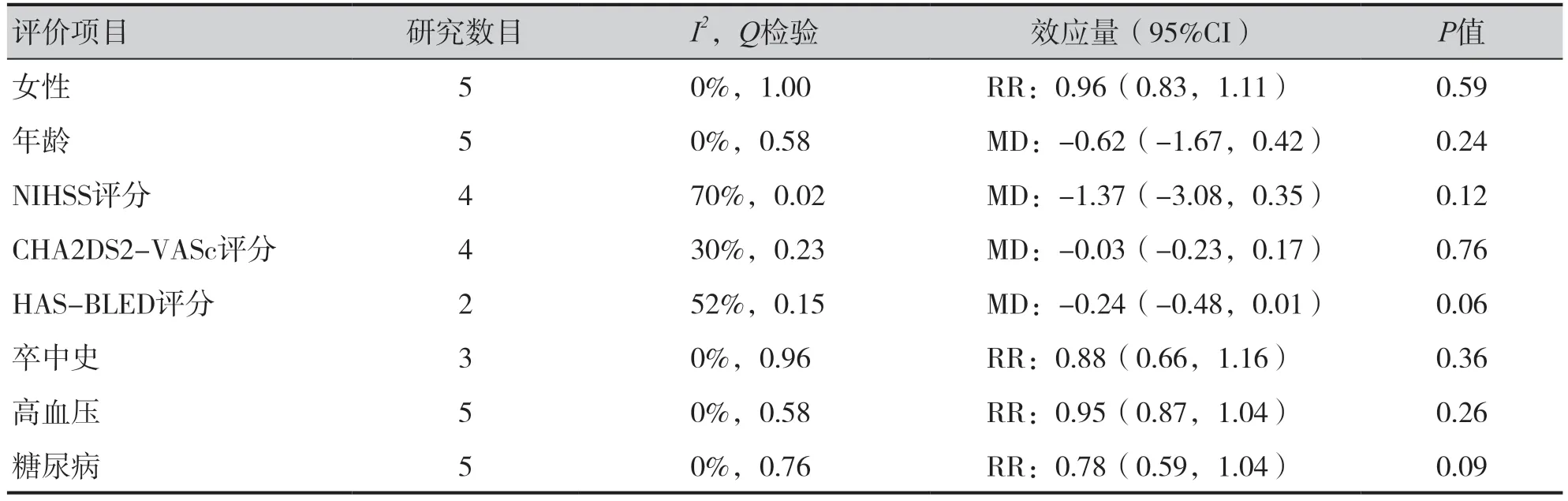
表3 6项研究早期抗凝组与对照组基线数据对比Table 3. Comparison of baseline data between early anticoagulation group and control group
2.3.2 总缺血事件
总缺血事件是IS 复发、TIA 及其他栓塞事件的综合指标。3 项研究[20,22,26]报道了缺血事件的结局,共747 例患者,包括早期抗凝组347 例,对照组400 例,各研究间无明显异质性(I2=46%,P=0.16),选择固定效应模型分析。结果显示,早期抗凝组和对照组相比,总缺血事件方面差异无统计学意义[RR=1.04,95%CI(0.67,1.61),P=0.88](图3)。
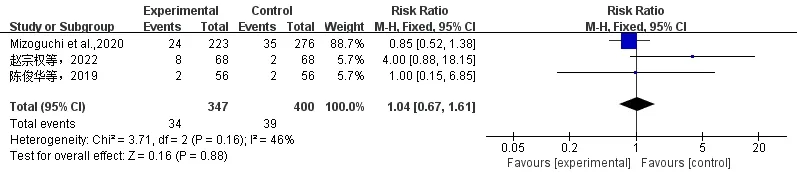
图3 总缺血事件森林图Figure 3. Forest plot for total ischemic events
2.3.3 IS复发或TIA
4 项研究[21-24]报道了IS 复发或TIA 的结局,共1 767 例患者,包括早期抗凝组955 例,对照组812 例,各研究间无明显异质性(I2=38%,P=0.20),选择固定效应模型分析。结果显示,早期抗凝组和对照组相比,IS 复发或TIA 方面差异无统计学意义[RR=0.88,95%CI(0.58,1.34),P=0.56](图4)。
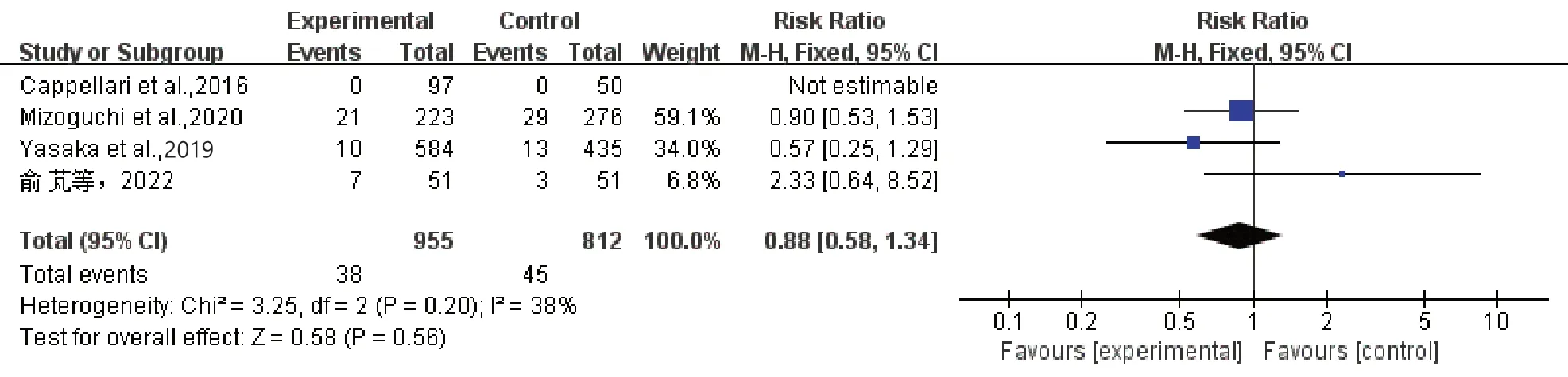
图4 IS复发或TIA森林图Figure 4. Forest plot for ischemic stroke recurrence or transient ischemic attack
2.3.4 大出血
大出血的定义依据国际血栓形成和止血协会的声明[27]。2 项研究[21,26]因未明确出血定义而被排除在外,3 项研究[20,22-23]报道了大出血的结局,共1 630 例患者,包括早期抗凝组863 例,对照组767例,各研究间无明显异质性(I2=30%,P=0.24),选择固定效应模型分析。结果显示,早期抗凝组和对照组相比,大出血方面差异无统计学意义[RR=1.24,95%CI(0.59,2.62),P=0.56](图5)。
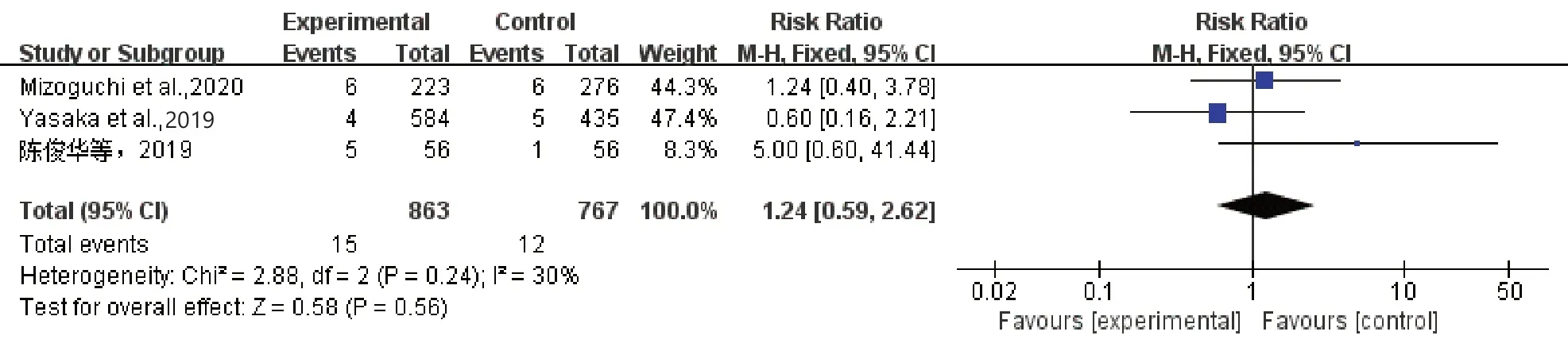
图5 大出血森林图Figure 5. Forest plot for major bleeding
2.3.5 sICH
1 项研究[24]报道了一例sICH 患者,但因未说明该病例发生在哪组而被排除在外。除此以外,4 项研究报道了sICH 的结局,共1 831 例患者,包括早期抗凝组899 例,对照组932 例,各研究间无明显异质性(I2=11%,P=0.34),选择固定效应模型分析[21-23,25]。结果显示,早期抗凝组和对照组相比,sICH 方面差异无统计学意义[RR=0.98,95%CI(0.44,2.17),P=0.96](图6)。
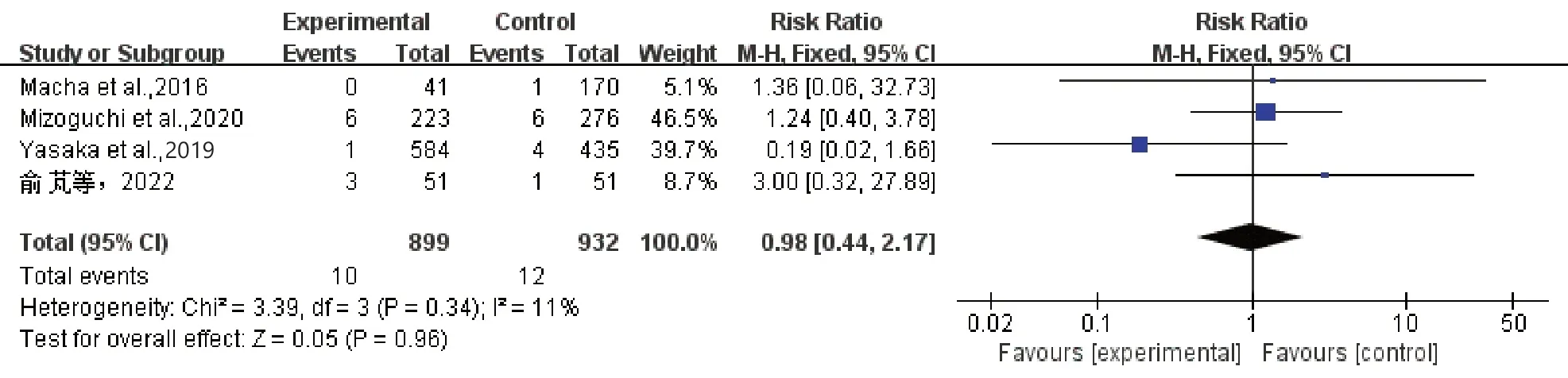
图6 sICH森林图Figure 6. Forest plot for symptomatic intracerebral haemorrhage
2.3.6 全部脑出血
全部脑出血包括sICH 和无症状性脑出血,原有脑出血患者复查发现范围较前扩大亦被包含在内。3 项研究报道了全部脑出血的结局,共1 377 例患者,包括早期抗凝组722 例,对照组655 例,各研究间无明显异质性(I2=0%,P=0.46),选择固定效应模型分析[23-25]。结果显示,早期抗凝组全部脑出血比例更低,结果具有统计学意义[RR=0.59,95%CI(0.44,0.77),P=0.000 5](图7)。

图7 全部脑出血森林图Figure 7. Forest plot for total cerebral hemorrhage
3 讨论
AF 是成人最常见的心律失常之一,给患者健康和社会经济带来了重大负担。研究表明,目前成人AF 患病率约2%~4%[28],随着人群寿命延长和对未确诊AF 患者的筛查,预计AF 患病率会增加2.3 倍[29-31]。IS 发生与AF 关系密切,总体而言,AF 使IS 的发生风险增加了五倍[1]。目前指南关于AF 相关IS 患者抗凝时机并没有统一推荐。由于大梗死比小梗死更容易发生出血转化,欧洲心脏节律协会于2013 年引入了“1-3-6-12 日规则”[32]。尽管IS 严重程度定义和时间点仅基于专家共识,但欧洲心脏节律协会以及加拿大、澳大利亚、中东、北非等一些国家已采用了此指南。另外,欧洲卒中组织指南[8]基于专家共识和间接观察数据,推荐使用“4-7-14 日规则”指导抗凝治疗,即轻度IS 和小梗死量(<1.5 cm3)患者在症状发作后第3 日或第4 日、中度IS 患者7 d 后、重度IS 和大梗死量患者14 d 后开始抗凝。然而,指南并未给出轻度、中度或重度IS 的确切定义。上述规则都源于维生素K 拮抗剂时代,目前已有大量证据证明NOAC 优于维生素K 拮抗剂,在应用NOAC 抗凝时可能并不适用。2018 年,美国心脏协会、美国卒中协会关于IS 患者早期管理的指南[33]建议在出现神经症状后4~14 d 开始口服药物抗凝,该项推荐主要依据为意大利的RAF 研究[11],但是该研究只有93 名(12%)患者接受了NOAC治疗。英国指南[34]建议,失能性IS 患者的口服抗凝药应推迟至发病后至少14 d,但对于非失能性IS,可根据临床医生的判断提前开始。抗凝治疗作为AF 相关IS 二级预防重要的一部分,明确此类患者何时启动抗凝治疗相当重要。
本研究发现,与3 d 后启动抗凝治疗相比,IS 发生后3 d 内开始抗凝在有效性方面相似,且不增加患者出血风险。需要注意的是,本研究纳入的大多数早期抗凝组患者NIHSS 评分较低,缺血程度更轻,结果解读需谨慎。Paciaroni 等[35]研究认为早期开始抗凝可能会导致或加剧脑实质出血,具有潜在的严重临床后果。尽管这一怀疑并没有确切的证据支持,并且梗死后出血转化对临床恶化的独立贡献仍不确定[36],但是这仍然导致临床医生推迟抗凝治疗。英国一项在线调查显示95%的临床医生不确定此类患者的抗凝时机[37]。一篇Meta 分析纳入6 项观察性研究和2项RCT 研究,共5 616 例患者,结果显示,相较于两周内开始抗凝,第一周内开始抗凝治疗具有相似的疗效和安全性[38]。更早的一篇汇总分析纳入8 项前瞻性队列研究,共2 550 名患者,结果表明IS 发生5 d 内开始应用NOAC 抗凝治疗并未增加安全性问题[39]。上述两项研究的基线水平并不完全匹配,早期抗凝组的NIHSS 评分偏低,因此普遍性可能仅限于IS 程度较轻和梗死量较小的患者。一项研究的亚组分析结果显示,在中度IS(NIHSS 评分8~15 分)的370 例患者中,3 d 内应用NOAC 抗凝患者有169 例,延迟抗凝组患者201 例,在有效性方面,早期组无IS 复发,而延迟组有3 例IS 复发;在安全性方面,早期组有3例患者出现大出血,其中包括1 例颅内出血,延迟组有1 例非颅内大出血,表明早期应用NOAC抗凝治疗并不劣于延迟抗凝[14]。
上述研究多为非随机对照研究,早期组和晚期组的患者特征之间存在一些差异,具有一定的混杂偏倚,因此需要高水平的RCT 研究明确此类患者的抗凝时机。TIMING 研究是第一项评估AF 相关IS 患者使用NOAC 早期抗凝(4 d 内)和延迟抗凝(5~10 d)有效性和安全性的RCT 研究,结果显示,在IS 复发、sICH 或死亡的综合结局方面,早期抗凝并不劣于延迟抗凝,在早期开始NOAC 的患者中,IS 复发和死亡的患者数更低,在90 d 的随访期间,两组患者都没有出现sICH[16]。此外,还有几项正在进行的RCT研究以明确IS 后开始NOAC 的适当时机,包括OPTIMAS 研究(NCT03759938)、ELAN 研究(NCT03148457)和START 研究(NCT03021928),OPTIMAS 研究无论卒中严重程度如何,将早期开始应用NOAC抗凝治疗的时间设置为4 d或更短,后2 个研究中早期抗凝组则按严重程度设置不同的NOAC 起始治疗时间,这些研究将提供AF 相关IS 患者抗凝策略的可靠数据。
本研究具有一定的局限性。第一,本研究纳入文献较少,且大多为非随机对照试验,此类研究的局限性可能带来了严重的选择偏倚,纳入的2 篇RCT 研究均没有明确说明实施了盲法。第二,本文一共纳入2 226 例患者,且两篇RCT 研究仅纳入214 例患者,样本量较少。第三,早期抗凝组NIHSS 评分偏低,尤其是全部脑出血指标的数据主要来源于Yasaka 等研究,该研究中早期抗凝组大梗死(≥22.5 cm3)占比19.7%,而对照组大梗死占比34.9%,对照组缺血性脑卒中程度更重,且脑出血主要为梗死后出血转化,因此本研究结果可能限于卒中程度较轻和梗死量较小的患者[23]。第四,对照组抗凝开始时间并不统一,且并未与目前指南推荐保持一致。第五,每项研究随访时间长短不同,这对结局指标的发生可能产生一定的影响。本研究预计,随着上述RCT 研究结果的发现,这些局限性将得到解决,从而为AF 相关IS 患者制定个体化早期抗凝指南提供数据支撑。应当强调的是,由于其他血栓形成、促动脉粥样硬化和促炎因素可能会增加NOAC 治疗患者的AIS 风险[40-41],因此在个体化抗凝策略中,定期重新评估可能对NOAC 反应不足的伴随因素也至关重要。
总之,本研究结果表明,对于IS 严重程度较轻且梗死面积较小的AF 相关AIS 患者,在症状发作后3 d 内开始应用NOAC 抗凝治疗具有与延迟抗凝(3 d 后)相似的有效性和安全性。

