电化学技术在食品检测中的应用研究进展
王 艳,包士雷,孙立瑞,窦博鑫,辛嘉英,张 娜
(哈尔滨商业大学食品工程学院,黑龙江 哈尔滨 150028)
食品检测分析技术是保障食品质量和安全、助力食品工业发展的关键之一。目前,常用的方法如气相及液相色谱法、分光光度法、固相萃取法、质谱法等多是基于大型仪器,虽然具有灵敏度高、应用广泛等优点,但仍然存在一些现实问题,如专用仪器设备价格昂贵、操作技术要求较高、检测耗时长、检测成本高和分析过程繁复[1],这使得其无法实现便捷式的快速检测。开发精确便捷的检测技术,在食品行业有着广泛的需求。相较之下,电化学技术由于其操作要求较低、精密度及灵敏度较高且设备便宜等优点,受到广泛关注和研究。本文从电化学检测分析技术方法、基本原理和在食品领域中的应用现状等方面进行全面的综述和分析,为电化学技术在食品检测中的应用与发展提供参考。
1 电化学检测技术类型及原理
近年来,随着电化学检测技术不断探究创新,其类型已发展出众多检测形式用以满足多种环境下物质的检测需求,根据待测物质的理化性质及检测机理的不同,将电化学检测技术分为两种,一种为直接电化学检测技术,另一种为间接电化学检测技术。
1.1 直接电化学检测技术
原理:基于检测物自身结构的易氧化还原特性,比如一些含有电活性基团的物质如酚[2-3]、醇[4]、醛[5]及化合物,以及金属离子[6]等具有优良电活性的物质,在一定的电位条件下容易在电极上得失电子,并发生氧化或还原反应从而产生电化学信号,实现电化学相关检测。
由于检测条件、物质性状的不同,使用裸电极进行检测产生的电信号可能较弱,对其痕量检测需要进行电信号的有效放大,通过研究发现,在裸电极上修饰不同类型的材料如纳米材料[7]、金属-有机框架材料[8],以及一些生物材料[9]等,利用不同材料结构特征可提高电极比表面积[10],增加电子传递速率并提供更多活性位点以提升催化效率[11],优化检测限、灵敏度及选择性等,从而提高对物质的直接电化学检测性能。
1.2 间接电化学检测技术
由于某些食品组分不具备明显的电化学活性,导致电化学响应较弱,研究发现在检测系统中添加如二茂铁、铁氰化钾及亚甲基蓝等电活性物质(即氧化还原介质),将酶、抗体、适配体或DNA等特异性识别元件固定在电极表面,利用待测物质与识别元件的特异性结合,其相互作用使电活性物质产生的电信号发生变化,从而达到间接检测的目的。此类技术目前主要通过构建电化学传感器实现应用,根据识别元件的不同,可分为电化学酶传感器[12]、电化学适配体传感器[13]、电化学免疫传感器[14]、分子印迹传感器[15]等。各种传感器在食品组分检测中的应用情况如表1所示。

表1 不同传感器在食品电化学检测中的应用Table 1 Application of different sensors in food electrochemical detection
2 电化学技术在食品检测中的应用
2.1 直接电化学检测技术在食品检测中的应用
直接电化学检测技术是基于物质结构中含有的电活性物质发生氧化还原反应产生电信号的原理进行检测,对于检测过程而言,由于电活性物质的直接信号表达,省去了繁琐的识别信号原件修饰、信号转换及复杂的反应过程,使整个检测过程更加快速高效。但同时也存在因不同电极或物质结构等因素,导致在电极上反应的电子转移动力学缓慢、电化学响应较弱以及过电位高等问题。针对这些问题,近年来的研究拟通过使用各种类型材料,将裸电极进行改性修饰以实现信号放大,可有效增强电活性物质在电极反应过程中的信号响应。根据修饰材料以及增强机制的不同,直接电化学检测技术可分为基于酶促反应机制及非酶促反应机制两类。
2.1.1 基于酶促反应机制的直接电化学检测技术应用
酶促反应又称酶催化或酵素催化作用,是以酶作为催化剂进行催化的化学反应。在直接电化学检测技术中通过将酶修饰在电极上,催化待测物质进行氧化从而产生电信号实现检测。近年来,基于酶促反应的直接电化学检测技术已实现于第三代生物传感器的开发应用当中。三代生物传感器的检测机制如图1所示。相较于前两代生物传感器[32-33],可以看出第三代传感器在电子传递过程中,无需通过间接检测O2的消耗或酶反应产物H2O2的生成,亦不需要使用电子媒介体进行传递。反应的信号全部来源于酶分子与被检测物质之间的氧化还原反应[34],因其电流密度大,使灵敏度升高确保电化学生物传感器的高选择性,提高检测的精准度,可应用于食品中物质的检测。

图1 三代生物传感器电子转移机制图Fig.1 Schematic diagrams of electron transfer mechanism in three generations of biosensors
基于酶促反应机制的直接电化学检测技术应用如表2所示,通过酶促反应对食品进行直接电化学检测的应用相对较少,现开发用于营养相关成分的检测如葡萄糖[35-37]、果糖[38]、乳糖[39]、胆固醇[40]等,在真菌毒素[41]方面也有相关检测。由于酶的活性中心普遍深埋于分子结构内部,电子转移距离过远使得酶与电极间电子转移的效率下降,经研究发现金属纳米材料[37,39]的高导电性、高催化性可起到增大酶与电极间电子传递速率的作用。通过制备如金、银等贵金属纳米颗粒修饰电极,可有效增加电活性表面积和电子转移速率,结合天然酶类物质进行共同修饰,可用于对营养物质如糖类、胆固醇等进行基于酶促反应的直接电化学检测[37,39],研究表明贵金属纳米材料的修饰能有效促进电子传递,并协同催化酶促反应使信号增强。酶生物传感器的另一大问题在于将酶直接吸附在电极表面容易造成变性失活。有研究发现碳基材料[42]具有稳定性高、比表面积大等优点,将酶固定在上面可增加酶的稳定性并保持原有催化活性,常用材料有碳纳米管、石墨烯及其复合材料等[35,40,42],研究表明,通过碳基材料复合制备生物传感器可以有效提高组装酶与电极表面之间的电子转移能力[40]。此外,Wu Shuyao等[40]发现使用层层自组装技术进行电极制备,可以在温和条件下固定更多的酶,有利于保持酶的生物活性,可提升其对胆固醇的亲和力,进一步增强传感器检测的稳定性、抗干扰性。

表2 基于酶促反应的直接电化学检测技术在食品相关组分检测中的应用Table 2 Application of direct electrochemical detection technology based on enzymatic reaction in the detection of food components
2.1.2 基于非酶促反应机制的直接电化学检测技术应用
基于酶促反应的直接电化学检测技术通过天然酶对待测物进行催化反应,实现有效的信号放大效果。其拥有良好的选择性及高灵敏度、抗干扰能力强等优点。但天然酶存在易失活、固定化过程复杂费时等问题。近年来,研究发现通过引入碳基纳米材料如石墨烯[43]、碳纳米管[44]等,以及纳米金属[45]、金属氧化物纳米材料[46]、复合纳米材料[47]等修饰电极,利用纳米材料比表面积高、导电性好、携带活性基团多等特点,可实现检测性能的有效提升。纳米材料的修饰及催化过程如图2所示,修饰后能有效加快电流传递、增加电极表面积及反应活性位点,对待测物起到良好的电催化作用[48],催化过程产生电信号用于待测物的相关检测。

图2 纳米材料修饰电极过程(A)和纳米材料催化反应机制(B)Fig.2 Electrode modification by nanomaterials (A) and catalytic mechanism of nanomaterials (B)
针对某些电活性物质信号响应差、氧化过电位较高等所导致的检测灵敏度偏低、检测结果不理想等问题,非酶促反应机制的直接电化学检测技术利用各种纳米材料的高导电性、高催化性[11]实行有效的信号放大策略,对食品组分中电活性物质的催化及检测有着广泛的应用(表3)。检测性能取决于修饰材料的响应能力、催化活性以及稳定性等,近年来,研究者致力于将多种纳米材料复合制备,以弥补单一修饰材料在检测性能方面的不足。

表3 不同修饰材料在食品电化学检测中的应用Table 3 Application of different modifying materials in food electrochemical detection
碳基材料的成本较低且具有良好的稳定性,作为修饰材料广泛应用于电化学设备的制作及检测过程中[49-51],但由于其选择性和催化活性较差,部分研究通过将碳基材料进行表面改性和功能化以提升碳基材料的电活性[52],也有研究选择将碳基材料与其他活性材料进行复合[53-56],利用不同材料结构的优良性质,形成协同作用以提升传感器的检测性能。碳基材料也可用于解决电极的生物污染问题[57]。研究人员利用快速泡沫印章辅助聚二甲基硅氧烷图案,控制过滤过程中单壁碳纳米管在聚偏二氟乙烯膜上的区域选择性沉积,基于碳纳米管的结构特性制备了一次性防污传感器。该传感器可有效提高防污能力,并提升了检测的重现性,可用于直接检测咖啡、牛奶等复杂基质中的吗啡[57]。
金属纳米粒子的比表面积高,结合其自身结构的小尺寸效应使其具有良好的电催化活性[58],可用于食品中亚硝酸盐[59]、重金属等痕量污染物检测时的信号提升,增强检测的精密度。但此结构效应也造成了颗粒聚集、反应性差等缺点。金属纳米颗粒一般被分散或负载在载体上,因为金属和载体之间的相互作用会影响电荷转移、纳米颗粒形貌等因素,通过选择适当的载体如石墨烯、碳纳米管等进行复合制备[60-61],利用碳基材料[62]的性质可增强设备的稳定性及活性表面积。研究人员通过复合制备使材料间形成协同催化效应,有效地提高了电子传递速率,可进一步提升检测灵敏度,并将其成功应用于多种酱料中偶氮染料的检测[54]。
金属氧化物因其成本低、易于制备且电活性高等优点,广泛应用于食品相关组分中化学物质的检测[63-66]。有研究表明,使用如TiO2、Fe2O3、CuO等金属氧化物材料修饰电极可在较宽线性范围表现出优良的催化活性[64,66],有团队发现过渡金属氧化物不仅资源丰富,且具有多种氧化形态,能够活化所吸附的物质,具有良好的催化性能。通过其丰富的活性位点和尺寸可设计性,与金属有机框架(metal organic frameworks,MOFs)材料共同制备修饰传感器可显著提高催化性能,可用于牛乳中双氧水等物质的检测[65]。
与天然酶相比,MOFs具有结构稳定、成本低、活性可调等优点,合成方法众多,如机械法、水热法、电化学法等,经研究证明电化学原位合成法可在电极表面原位生成目标物质,可方便传感器的构建[67]。此法构建的传感器具有反应速度快、条件温和、化学试剂消耗少等优势,已成功用于食品中亚硝酸盐的检测,结果显示可有效催化待测物质氧化并增大电流响应[67]。研究发现单一的MOFs催化活性相对不易显现,可将MOF与其他纳米材料制备成复合MOFs提高其催化活性[67-71],如将MOF与贵金属纳米粒子进行复合,并与羧基化的碳纳米管共同修饰到电极表面,利用复合纳米材料的高催化性能对物质含量进行检测,相比于裸电极,复合材料可以扩大电活性表面积并加速电子转移,对待测物质的氧化还原过程表现出良好的催化性能[71]。
2.2 间接电化学技术在食品检测中的应用
在食品相关组分检测中,存在一些物质由于自身性质特点,无法使用直接电化学检测技术进行定性定量检测,于是间接电化学检测技术开始广泛应用。即通过检测系统中其他电活性物质的信号变化,与待测物质建立联系。一般表现为待测物质与修饰物特异性结合后,其反应可影响电活性物质产生电信号的形式进而实现检测。基于特异性反应及影响信号的方式不同,可将间接技术分为基于信号放大机制检测技术和基于抑制信号机制检测技术。
2.2.1 基于信号放大机制检测技术
利用信号放大机制的食品间接电化学检测技术在适配体传感器中应用相对较多。通过在电极上修饰适配体或适配体-介质复合物,构建适配体电化学传感器实现检测,构建及检测过程如图3所示。以适配体与待测物质的特异性结合反应为基础,检测结果通常表现为使介质的电氧化还原信号增大,并建立与待测物质含量的线性关系,从而实现快速检测。

图3 适配体传感器的构建及信号放大机制检测原理Fig.3 Construction of aptamer-based sensors and their detection principle based on signal up-regulation
适配体通常是由指数富集进化技术筛选出的寡核苷酸序列,可以是DNA或RNA,具有特异性强、识别标靶范围广等特点,可轻易识别标志物的结构差异,可与蛋白、核酸及许多有机无机分子、标靶复合物等结合并发生反应,使基于信号上调机制的适配体传感器拥有着高特异性和灵敏度。近年来,适配体传感器在食品安全检测中应用广泛,基于信号上调机制的适配体传感器在食源性有害物质检测中的应用如表4所示,主要集中于如抗生素[72-77]、真菌毒素[20,22,78-83]、重金属残留[84-88]以及食源性致病菌[89-92]等天然或人工制造的食源性有害物质检测,目前,根据检测机制以及是否采用标记物进行标记等不同,可将电化学适配体传感器分为标记型和非标记型。
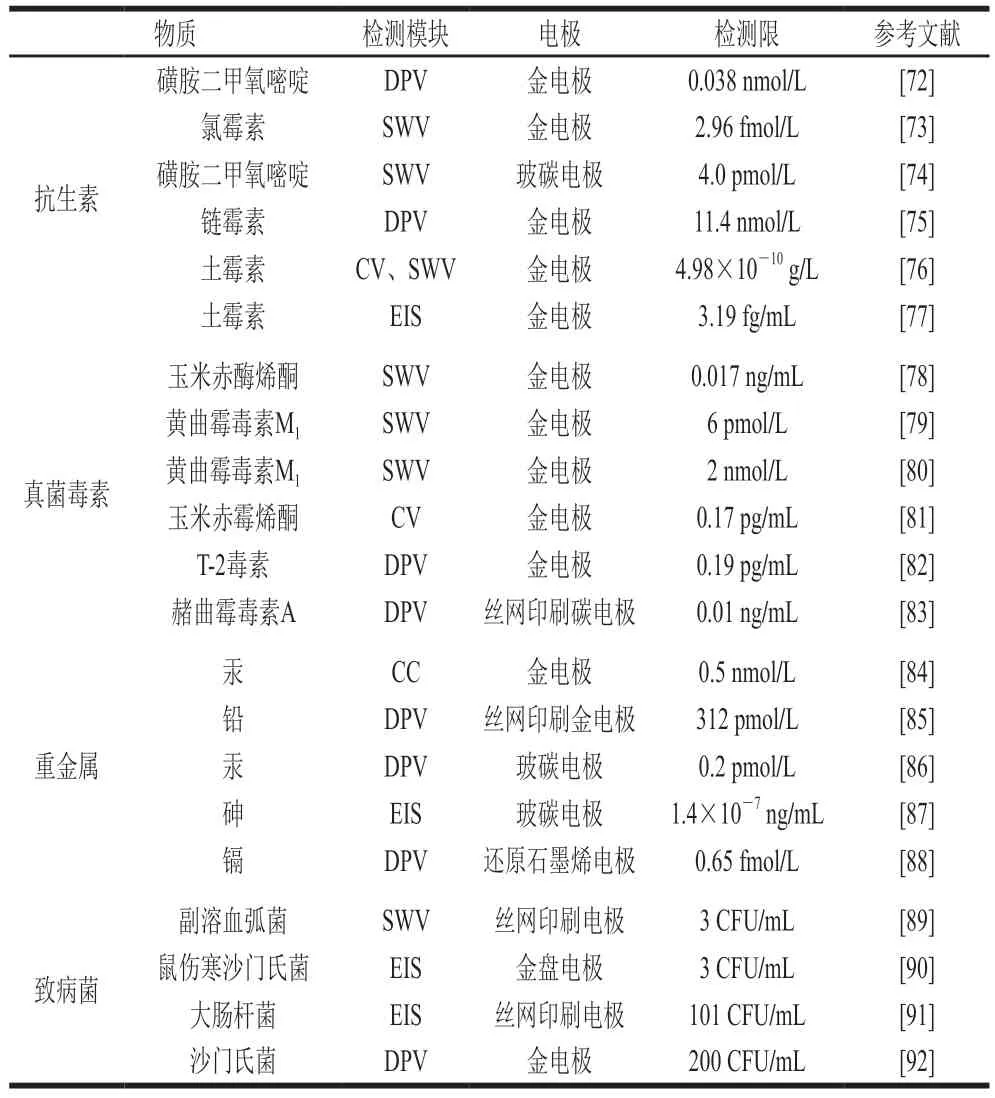
表4 基于信号放大机制的适配体传感器在食源性有害物质检测中的应用Table 4 Application of aptamer-based sensors based on signal upregulation in the detection of harmful foodborne substances
标记型适配体传感器通过将电活性物质如氧化还原活性分子、酶类物质以及纳米材料与适配体结合,在检测过程中引起适体数量或空间构型改变,或利用自身结构、催化性等引起的电信号变化进行定量检测。根据此性质有研究发现,在金电极表面修饰含有电活性物质的单链DNA,待测物存在时会与适配体形成稳定的复合物,从而导致适配体无法与单链DNA形成互补双链DNA,使电极表面的单链DNA被体系中的核酸酶P1消化水解,抗双链DNA抗体无法修饰到电极上,使空间位阻减小,电活性物质的电信号增大。结果证明,该方法可在0.1~500.0 nmol/L浓度范围检测抗生素,具有较低的检测限[72]。重金属的痕量检测对于食品安全具有重要意义,研究发现利用亚甲基蓝(methylene blue,MB)标记的适配体及其部分互补DNA共同修饰电化学适配体传感器,电极表面的cDNA-适配体通过cDNA的释放,能够发生较大构象变化并促进MB的电子传递效率,从而显著提高电化学信号,检测限低至0.65 fmol/L[88],相较于同类型传感器[85,87],检测性能更为优异。
对于非标记型适体传感器,其检测机制是通过目标物质与适体进行识别反应,导致构象或空间位阻变化,电子传输过程的改变使电信号变化进而实施检测。基于此类机制的适体传感器已成功应用于食品中抗生素[74,77]、真菌毒素[79]及致病菌[90-91]的检测中。有研究发现利用重金属与胸腺嘧啶的特异性识别反应,通过修饰含有T-T碱基错配的双链互补DNA可实现对汞的特异性检测[84,86],T-T错配会阻断DNA双链内部电荷转移,而Hg2+通过与双链DNA特异性结合会形成T-Hg2+-T配位物,能够恢复DNA完全互补双链的碱基堆积状态,引起电极表面计时电量的变化,成功应用于鱼类样品的检测。
电化学适配体传感器由于兼具电化学的简便性、适配体的准确性而得到广泛应用,但同时也存在着以下问题:首先由于食品成分的复杂性,过多的干扰物质会导致预处理过程更加繁琐,影响检测的选择性和灵敏度;在食品样品中,许多待测物质往往以痕量形式存在,过多其他成分也会干扰检测的准确性。近年来多数研究利用DNA[93]、酶[94]的特异性,或引入功能化纳米材料[89,95]修饰电极进行信号增强,尽管生物识别原件可能存在如体系繁杂、反应条件苛刻等缺点,纳米材料也相对缺乏特异性,但为解决上述问题提供了不错的方向。对于适配体传感器未来的发展,应更多集中于解决如检测过程中,样品前处理的简化、适配体等识别原件的开发筛选、运输保存等问题,以及深入对多种物质实现快速、同时检测等,对传感器的小型化、集成化也应是重点研究的方向之一。
2.2.2 基于抑制信号机制检测技术
2.2.2.1 基于酶抑制作用的抑制信号机制
此类机制以酶作为识别原件修饰在电极上,通过对待测物进行特异性识别为基础。如图4所示,通过与待测物或耦合其他修饰物发生反应抑制酶的活性,降低酶对底物的催化能力,进而使酶催化反应产物的电信号降低,以达到对待测物的间接定量检测。
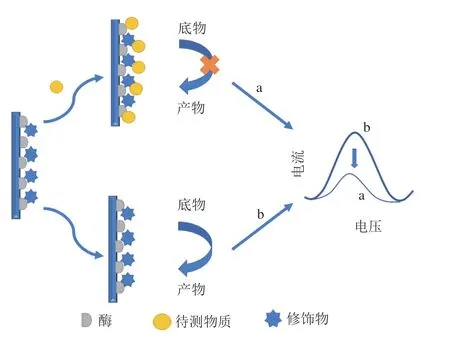
图4 酶抑制机制检测原理Fig.4 Detection principle of sensors based on enzyme inhibition
近年来基于此类机制开发的传感器如表5所示,主要在检测食品中农药残留、重金属污染方面有所应用。测定农药残留方面,在传感元件的选择上以乙酰胆碱脂酶和丁酰胆碱酯酶等应用居多。以乙酰胆碱作为底物,当有机磷农药存在时,农药中的磷酸基团会将酶的活性基团磷脂化,从而抑制酶的活性,使电信号降低。利用有机磷农药对酶催化活性的抑制作用,实现对各类农作物中有机磷农药残留高灵敏度、高特异性的检测[96-102]。有研究称乙酰胆碱酯酶对农药残留检测的灵敏度较高,但易受到重金属影响[93]。通过对酶传感器进行设计修饰可相应提升检测性能,如通过修饰纳米金属氧化物[95]、碳纳米管和导电聚合物等[96],利用自身的结构特性增大电机的比表面积,使酶的固定化更加稳定并提升催化性能及导电性,进而增加传感器的检测性能。
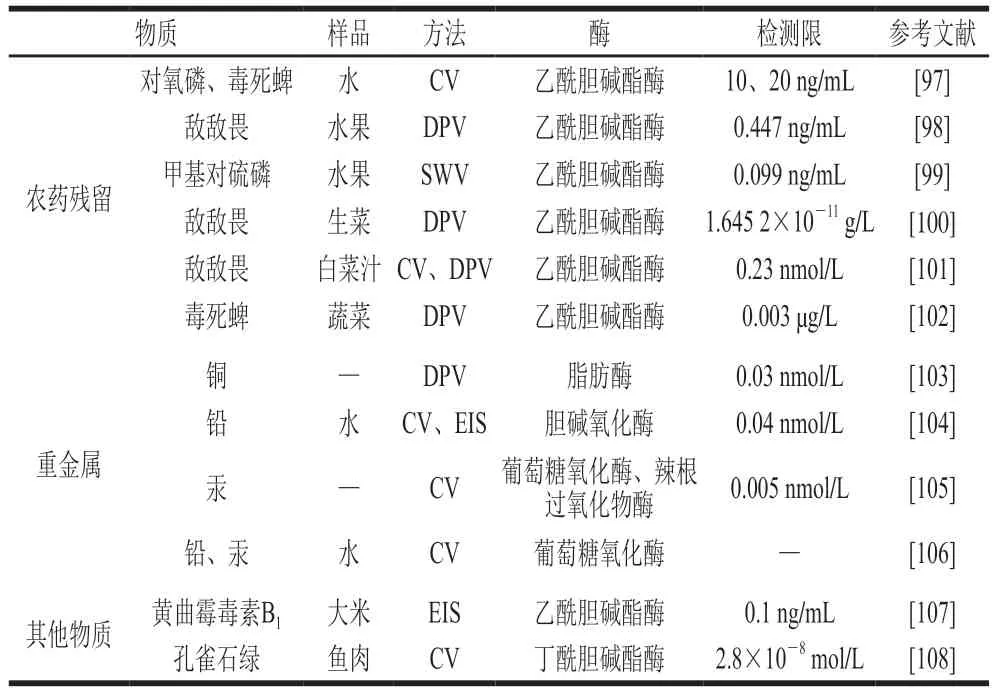
表5 基于酶抑制机制的传感器在食品电化学检测中的应用Table 5 Application of sensors based on enzyme inhibition in food electrochemical detection
基于酶抑制机制的电化学技术在食品中重金属检测相对较少,主要应用于水中的有毒金属残留如铅、汞等[103-106],本课题组也基于此类机制开发了一种甲烷氧化菌素(methanobactin,Mb)耦合脂肪酶生物传感器用于Cu2+的痕量检测,利用Mb可特异性捕获Cu2+的特点,在电极上固定化脂肪酶,检测脂肪酶水解底物三油酸甘油酯时电信号的响应情况。Cu2+与Mb特异性结合并在脂肪酶周围产生富集现象,抑制脂肪酶的催化活性使反应产物电信号降低,实现对Cu2+的快速定性检测,获得了较低的检测限,为食品中重金属的痕量检测提供了研究基础[103]。酶抑制型传感器尽管优点颇多,但其不足之处也显而易见。除了作为酶传感器的通病如稳定性较差、活性易受环境干扰等之外,其独特的传感机制也在一定程度上限制了传感器的构建及检测应用[96,105]。探究有效酶抑制剂以拓宽检测范围,研制新型材料以实现酶的高负载、高活性固定也逐渐成为此类机制技术的研究方向[102]。
2.2.2.2 基于门控制效应的抑制信号机制
通过利用待测物与电极修饰物的特异性结合反应,控制探针分子到达电极表面的数量,进而间接测定待测物浓度称作门控制效应[109]。如图5所示,该效应常用于利用分子印迹聚合物作为识别单元开发的电化学信号转导[110]、制备分子印迹电化学传感器,以及利用特异性反应如抗原抗体间的识别反应,控制电活性物质电信号大小的免疫传感器[111]的开发制备等。其检测过程如图5所示,待测物与电极表面修饰物质特异性结合,使得体系中的氧化还原探针与电极接触受阻,抑制其发生反应导致电信号下降,信号的下降与待测物含量呈线性关系,目前基于门控制技术开发的传感器由于其识别元件具有特异性、高选择性等,在食品安全相关检测方面也得到了广泛的应用。

图5 门控制效应检测原理Fig.5 Detection principle of sensors based on gate control effect
基于门控制效应的传感器在食品组分中的检测应用如表6所示。电化学免疫传感器通过将抗原/抗体修饰在电极上作为识别原件,通过抗原抗体与待测物质的特异性结合反应,使电信号发生相应变化实现检测。由于识别原件的免疫反应具有特异性,使其在检测过程中具有较高的专一性和灵敏度。与适体传感器类似,免疫传感器可以根据分析时标记物质的有无分为标记型和非标记型,其中标记型[112-115]通过将酶、纳米材料、电活性物质等修饰在二抗上,将标记物作为传感器的检测信号,标记物能影响检测灵敏度及检测限的高低。而非标记型[116-121]则在电极上修饰抗原或抗体,并通过免疫识别前后的信号变化达到检测的目的。相较之下,非标记型由于避免了复杂的标记过程,操作更为简便,使得检测性能相对更优。由于免疫传感器的抗体一般为活体制备,且需要与载体蛋白进行结合以解决免疫原性低等问题,这使得检测元件的活性易受环境影响,制作成本提高且降低检测的准确性。且由于待测物质如真菌毒素[118]、抗生素残留等的痕量存在,导致产生的信号微弱难以有效检测。为优化检测性能,近年来研究者致力于开发功能化的复合材料,如将金属纳米材料与石墨烯进行结合制备,这是由于石墨烯具有较大的比表面积,可更好地固定金属纳米材料及免疫识别元件。复合材料在增大检测设备反应面积的同时,其协同作用使信号高效传递,在肉类痕量抗生素残留检测中应用广泛[117,120]。目前,通过高效的制备方式及开发新型的基质电极,可实现免疫反应的放大[122],使传感器的性能得到进一步提升。

表6 基于门控制效应的传感器在食品电化学检测中的应用Table 6 Application of sensors based on gate control effect in food electrochemical detection
分子印迹聚合物是以待测物质作为模板材料,通过交联剂与功能单体完成聚合,再经过处理洗脱模板分子后,形成与待测物质互补的聚合物,其内部孔穴在形状、大小等空间构型以及官能团上都与待测物质互补,对待测物质具有极高的特异性识别能力。分子印迹传感器通过利用分子印迹聚合物与待测物质的特异性结合反应,将其转化为电化学信号,实现对食品中组分的检测。分子印迹传感器的适用对象往往是小分子物质,凭借其极高的特异性,对食品中的色素[123-124]、农药残留[125-127]、抗生素[128-129]及其他食源性有害物质[130-131]的痕量检测有着深入应用。目前提升检测灵敏度、制备更多合适的功能单体以及对大分子[132]组分进行研究检测等是分子印迹聚合物的研究重点。
2.3 电化学-光学联用在食品检测中的应用
随着电化学检测技术的不断发展,研究发现光化学检测具有较高的特异性、灵敏度[133],且制备方便。与现有的电化学技术结合应用,可有效提升检测性能,并扩大电化学传感器的应用范围。目前在食品检测领域,利用电化学-光学联用技术进行检测,可根据信号及传感原理的不同,分为光电化学传感器[134]和电化学发光法[135]两类。
光电化学传感器通过将光敏材料和识别原件共同修饰制备而成[134],通过电极信号的变化实现检测。在光照条件下,光敏材料表面会产生电子空穴对,通过待测物与识别原件的结合使材料本身发生变化,从而改变信号值达到检测目的。其产生的电流根据传递位置及发生反应的不同,还可分为阴极、阳极两种光电流。近年来在食品检测领域,光电化学传感器已被开发用于抗生素[136]、生物毒素[137-138]、小分子物质[139]等,并在农药检测方面得到了广泛应用[134,140]。由于传感器的特殊传感机制及构建材料的生物亲和性,使检测具有更高灵敏度及更低的背景干扰[131,134]。检测过程中,构建传感器的光敏材料会改变光电效应,进而影响检测效果。研究发现,利用无机半导体材料如金属氧化物、量子点等进行修饰,并结合生物识别原件共同制备传感器,在重金属、真菌毒素[141]及农药检测[142]中,可使传感器具有较高光催化活性及稳定性,改善因材料氧化性过高导致的选择性差等问题。
电化学发光法基于化学发光和电化学传感器相结合,通过待测物质在电致发光体系中所发生的电化学反应,并检测其生成产物的发光强度进行检验分析。在食品检测领域,相较于光电化学传感器,电化学发光法拥有更广泛的检测品类。在食品营养物质[143-145]、食品污染物[146-148]等食品相关组分的检测中发挥着重要作用。电化学发光技术由于发展时间较短,自身也存在如所使用的金属电极可吸附其他物质导致检测的准确性下降,以及光活性材料固定化不足等问题。近年来研究人员通过结合新型纳米材料、开发组装新方式等以解决传感器的不足[149-150],结果表明,功能化纳米材料的表面催化活性高,在晶体中的扩散通道短,利用修饰材料的结构增加固定化效率的同时,可提升生物识别能力,实现高效的信号传输,使检测效率大幅提升[150-151]。
3 结语
目前,相较于传统检测方法而言,电化学检测方法由于操作简单、分析速度快、较为经济环保等优点在食品相关成分检测方面越来越受到关注。但由于食品成分的复杂性、所含外源物质的未知性以及检测设备的材质适用性等,电化学技术在食品检测中的应用仍存在以下问题:一是由于食品中所含组分复杂,对待测组分的电化学反应造成干扰。特别是有的组分具有与待测物相似的氧化还原性能,会直接产生与待测物重叠的信号;二是现今的电化学检测方法多是针对单一物质的检测,对多组分同时检测研究相对较少;三是电极反应对环境条件敏感,电极表面易受检测液中杂质的污染,以及其他一些不确定因素的干扰,这使得要保证检测信号的重现性,对测试操作的要求很高;四是对于电化学传感器的构建,仍需寻找低成本、环境友好且能有效提高灵敏度的修饰材料,以及开发传感器活性组分的新型固定化、提高活性的新技术。
鉴于上述多种因素,电化学检测技术迄今仍多数局限于实验室研究,能够商品化应用的实例尚少。采取以下措施可以促进电化学检测技术走向实际应用:1)对食品进行复杂和高效的预处理,减少多组分间的干扰;2)将色谱分离方法与电化学检测技术相结合;3)开发一次性使用的检测电极。此外,电化学检测设备和方式的系统化、便携化、智能化,也是一个重要的发展方向。

