富锂锰基正极材料的聚苯胺包覆及其电化学性能
赵红伟,吴宇鹏,魏文添,施志聪
(1.广东工业大学材料与能源学院,广东 广州 510006;2.广州天赐高新材料股份有限公司,广东 广州 510275)
0 引言
清洁能源的推广应用在一定程度上缓解了环境污染和能源危机等问题[1]。高效、清洁的锂离子电池作为重要的储能材料之一,在一定程度上摆脱了对传统石化能源的依赖[2,3]。近年来,新能源交通工具的广泛推广,对锂离子电池的需求变得更加迫切。作为电池的重要组件之一,正极材料对电池的性能表现有着重要影响。在正极材料中,富锂锰基正极材料Li1.2Ni0.13Co0.13Mn0.54O2(LNCM)具有比容量大、输出电压高等优势[4],能够满足高能量密度电池的需求。然而,LNCM也存在循环性能差、电压下降显著等诸多问题[5,6],这些因素阻碍了其实际应用。因此,如何克服材料的缺陷,提升材料的性能成为关键问题。
LNCM是由LiTMO2(TM=Ni,Co,Mn)和Li2MnO3两相组成的固溶体[7],其电化学窗口为2.0~4.8 V。在充电电压为2.0~4.5 V时,LiTMO2具有电化学活性,伴随着Li+的迁移和过渡金属离子的氧化。当电压在4.5 V以上时,Li2MnO3相被激活,此阶段中Li+和“晶格氧”将会以“Li2O”的形式析出,同时部分晶格氧会形成类过氧根离子[8],该过程部分可逆,为材料提供了额外的比容量,但也导致了材料的初始库仑效率较低。LNCM作为一种p型半导体,其导电性较差,在高倍率下的放电比容量会大幅缩减,这些问题限制了其在实际领域中的应用。学者针对LNCM材料的缺陷,提出了不同的应对方案,对材料的改性方案主要包括离子掺杂改性[9]、晶体结构调控[10]、包覆改性[11]等。离子掺杂改性是一种简单有效的方案,通过提高化学键的强度来稳定材料的晶体结构,抑制材料在服役过程中的相变,并提高材料的热稳定性;晶体结构调控可制备具有特定取向的材料,将特定晶面暴露出来,降低离子迁移能垒,加快电化学动力学;包覆改性是在材料表面形成具有保护性的膜体,改善材料的性能。若材料本身的导电性较差,包覆层通常采用离子导体或电子导体。
本文先利用溶胶凝胶法制备LNCM,再通过低温氧化聚合结合质子酸掺杂的方式在正极材料表面形成聚苯胺包覆层,并提高包覆层导电率。与未改性的试样相比,包覆后的材料在循环稳定性、倍率性能等方面均有提升。
1 实验部分
1.1 主要药品和仪器
实验药品:醋酸锂(99%,Aladdin)、醋酸镍(99.5%,Aladdin)、醋酸钴(99%,Aladdin)、醋酸锰(99%,Aladdin)、醋酸锂(99%,Aladdin)、柠檬酸(99%,Aladdin)、苯胺(99%,Aladdin)、过硫酸铵(98%,Aladdin)、盐酸(37%,Aladdin)。
实验仪器:采用日本Rigaku XRD衍射仪,扫描角度10°~90°,扫描速度10°/min,扫描步长0.02°/s;采用德国ZEISS生产的Sigma 300扫描电子显微镜观察试样形貌;利用德国Bruker红外光谱仪进行红外光谱测试,测试范围为4 000~500 cm-1;利用Mettler Toledo生产的TGA2热重测试仪进行热重测试,测试温度在30~800 ℃,升温速率为10 ℃/min,气氛为空气。
1.2 原始试样以及改性试样的制备
将醋酸锂、醋酸镍、醋酸钴、醋酸锰按照1.2∶0.13∶0.13∶0.54的化学计量比溶于去离子水中,并搅拌1 h,得到溶液A。将摩尔量为过渡金属离子总量2.2倍的柠檬酸溶于去离子水中,并搅拌1 h,得到溶液B。在搅拌状态下,将溶液B缓慢滴入溶液A中,滴加完毕后继续搅拌2 h,得到溶胶。将溶胶在90 ℃的水浴锅中搅拌蒸发,经过4 h后得到干溶胶。将干溶胶转移至鼓风干燥箱中,在120 ℃下干燥36 h,得到凝胶。对凝胶进一步研磨后得到相应的粉末。将粉末在管式炉中进行500 ℃、5 h的低温烧结,待烧结料冷却后研磨10 min,随后进行900 ℃、12 h的高温烧结。两次烧结的气氛均为空气,最终得到黑色粉末状正极材料原始试样。
将2.0 g正极材料加入150 mL去离子水中,磁力搅拌40 min后超声处理20 min,并继续搅拌1 h,得到溶液C。在搅拌状态下,向溶液C中缓慢滴加1 mol/L的盐酸溶液,将溶液的pH值调到2.5。随后加入一定量的苯胺单体,并继续搅拌0.5 h。将一定量的过硫酸铵溶解在10 mL去离子水中,并缓慢滴加1 mol/L的盐酸,直至溶液的pH值为2.5,得到溶液D。将溶液C和溶液D转移至冰水浴中,在搅拌状态下缓慢滴加溶液D到溶液C中,滴加完毕后继续反应3 h,使苯胺单体在低温下发生氧化聚合反应生成聚苯胺。在实验中合成具有不同包覆量的改性材料,其中聚苯胺的理论包覆值分别为5%、10%、15%。将原始试样以及不同包覆量的试样分别记为PANI-0、PANI-1、PANI-2、PANI-3。
将正极材料、导电炭、PVDF按照8∶1∶1的质量比混合后研磨2 min,随后转移至烧杯中。加入适量的N-甲基吡咯烷酮(NMP)溶液并搅拌均匀,然后用刮刀将混合物涂覆在铝箔上,经过120 ℃真空干燥12 h后,将其裁切为直径12 mm的极片,活性物质载量为0.021 9 mg/mm2,并转移到手套箱中。电池壳的型号为CR2032,LNCM为正极,金属锂片为对电极,隔膜为Celgard-2400,电解液为5 V高电压电解液。电池的充放电测试选择新威电池测试柜,型号为CT-4008T,其中电压范围为2.0~4.8 V,温度为25 ℃。
2 结果与讨论
2.1 材料的晶体结构分析
图1为不同试样的X射线衍射(X-ray diffraction,XRD)图。可以看到,原始试样与改性试样均具有典型的α-NaFeO2结构,其中18°~22°的衍射峰对应于“LiMn6”超晶格[12],说明材料中存在Li2MnO3相。与原始试样相比,包覆后的材料没有出现新的衍射峰,各衍射峰也没有明显变化,说明材料的晶体结构未发生变化。各材料的006/102双峰分裂明显[13],表明材料的层状结构良好。(003)和(104)晶面的衍射峰强比R用来判断材料中锂/镍混排程度,当R>1.2时,说明材料的阳离子混排度较低[14],有利于电化学反应中Li+的脱嵌。原始试样和改性试样的晶体结构参数如表1所示。对比不同试样的R值可知,所有试样的R值均大于1.2,其中PAN-2的R值最大,说明此材料的性能可能优于其他材料。

表1 原始试样和改性试样的晶体结构参数Table 1 The lattice parameters of pristine and modified samples
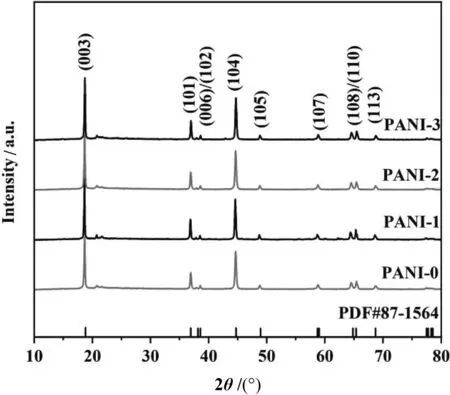
图1 原始试样和改性试样的XRD图谱Fig.1 XRD patterns of pristine LNCM and modified samples
2.2 材料的形貌分析
图2为不同试样的SEM图像。可以看到,在包覆前后,材料的粒度没有明显变化,但材料表面出现了点状颗粒,表明聚苯胺成功地包覆在正极材料表面;

图2 原始试样和改性试样的SEM图像 (a、b) PANI-0,(c、d) PANI-1,(e、f) PANI-2,(g、h) PANI-3Fig.2 SEM images of original and modified samples (a,b) PANI-0,(c,d) PANI-1,(e,f) PANI-2,(g,h) PANI-3
随着聚苯胺含量的增加,材料的表面粗糙度增加,轮廓变得模糊。
2.3 红外光谱分析
在有机物的合成过程中,产物的产率受苯胺单体的浓度、合成时间和氧化剂用量的影响,实际包覆量低于理论值。由于XRD测试未检测到聚苯胺,需要借助红外光谱对材料的有机成分进行分析。原始试样和改性试样的傅里叶红外光谱(Fourier-infrared spectrum,FTIR)如图3所示。其中,605 cm-1处为Mn-O振动吸收峰,包覆后的材料有较多新的吸收峰出现,1 587 cm-1和1 506 cm-1处为醌式单元(N=Q=N)和苯式单元(N-B-N)的特征吸收峰[15],1 300 cm-1处是芳香胺Ar-N的吸收峰,这表明材料中存在聚苯胺的有机化合物。
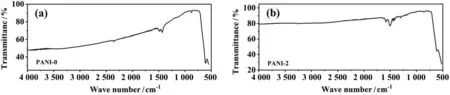
图3 原始试样和改性试样的FTIR图 (a) PANI-0,(b) PANI-2Fig.3 Fourier infrared spectrum of original and modified sample (a) PANI-0,(b) PANI-2
2.4 热重分析
为了确定聚苯胺的实际包覆量,对所有试样进行热重测试,测试结果如图4所示。可以看到,在升温过程中,原始试样没有出现明显的吸热或放热峰,这表明材料没有发生明显的氧化还原反应。然而,包覆样在185 ℃和360 ℃左右出现了两个吸热峰,这是因为在30~330 ℃,聚苯胺发生氧化反应导致失重;在330 ℃以上的高温,聚苯胺分子链断裂分解导致失重。聚苯胺的理论包覆值与实际包覆值如表2所示。

表2 改性试样的热重数据Table 2 Thermogravimetric data of modified samples

图4 原始试样和改性试样的热重曲线Fig.4 TG curves of pristine and modified samples
2.5 材料的电化学性能分析
不同试样的循环数据以及倍率数据如图5所示。循环测试条件为:25 ℃、0.2 C下充放电100圈。可以看到,PANI-0的初始放电比容量为239.4 mAh/g,循环100圈后,其放电比容量为保持率为98.2%。与原始试样相比,改性后的材料的放电比容量均有所提高,PANI-1、PANI-2、PANI-3的初始放电容量分别为265.3 mAh/g、276.1 mAh/g和253.8 mAh/g,且改性试样的放电容量更加稳定,其中PANI-2的循环稳定性最好,在0.2 C下,循环100圈后的容量保持率为99.5%,这得益于聚苯胺对主体材料的保护。作为导电聚合物,聚苯胺具有电化学活性,可以在充放电过程中提供一定的容量,表层的聚苯胺能够避免电解液与电极材料的直接接触,抑制前者对后者的侵蚀,从而提高材料的结构稳定性。对比不同试样的倍率测试结果可以发现,改性后的材料在不同倍率下的放电比容量均有提升。在0.1 C下,PANI-0、PANI-1、PANI-2、PANI-3的初始放电容量分别达到270.5 mAh/g、295.1 mAh/g、300.8 mAh/g、283.62 mAh/g;5 C下,PANI-2的放电比容量为137.1 mAh/g,高于原始试样的122.6 mAh/g。这是因为聚苯胺的加入能够增加活性物质与导电剂的导电接触位点[16]。通过质子酸的掺杂,聚苯胺的共轭结构提高,其电导率进一步提高,可以有效提高活性物质的导电性,减少材料在高负荷下的极化现象,从而优化了材料的性能表现。235.1 mAh/g,容量在循环和倍率性能测试中,PANI-2的表现优于原始试样和另外两个改性试样,因此选择PANI-0和PANI-2进行循环伏安测试并对比分析,如图6所示。观察原始试样的循环伏安曲线可知,其首次充电过程中,在4.23 V和4.76 V出现两个氧化峰[14],对应LiTMO2相的Ni2+和Co2+的氧化、Li2MnO3相中的Li+脱出和晶格氧的析出;在3.73 V和3.09 V处的两个还原峰分别对应Ni4+、Co4+的还原以及Mn4+的还原。PANI-2的测试结果与原始试样类似,但其Ni2+/Ni4+氧化还原电位差ΔV=0.4 V,小于PANI-0的0.5 V,说明改性试样的可逆性更好,随着循环的进行,峰电流提高,说明材料经过活化后反应活性提高。同时注意到,在高电压下,包覆材料中的不可逆反应得到抑制,材料的相变减少,其电压和比容量稳定。
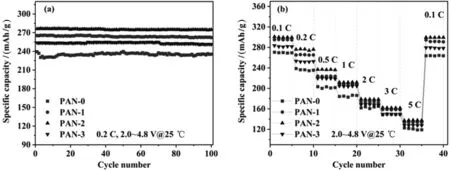
图5 原始试样品和改性样品放电数据图(a)不同样品循环数据图;(b)不同样品倍率数据图Fig.5 The discharge capacity of original and modified samples (a) Cycle performance;(b) Rate performance
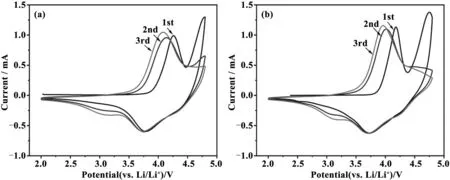
图6 不同试样的循环伏安曲线(a)原始试样;(b)PANI-2Fig.6 The CV curves of original sample (a) and modified sample (b)
为探究聚苯胺对材料阻抗的影响,对原始试样和改性试样进行了充放电前后的电化学阻抗测试,并进行了数据拟合,测试结果如图7所示。Nyquist图由高频区的圆弧和低频区的一条近似直线构成,其中圆弧与实轴的交点代表溶液阻抗Rs,圆弧的直径表示电荷转移阻抗Rct值,低频的斜线表示Werburg阻抗,Rsf为膜阻抗。可以看到,在循环前,原始试样与包覆试样的Rs值接近,但包覆试样的Rct值要小于原始试样。通过对各电池的阻抗数据进行拟合,发现PANI-0的Rct值为111.1 Ω,而PANI-2的Rct值仅为81.5 Ω,这与材料的倍率、循环测试结果相吻合。经过100圈循环后,由于结构演变、SEI膜增厚等原因,材料的阻抗增加,但包覆试样的阻抗值明显小于原始试样,其中PANI-2和PANI-0的Rsf、Rct值分别为8.54 Ω、133.8 Ω和25.73 Ω、215.4 Ω,这表明聚苯胺的加入能够有效降低材料的阻抗。循环前后不同试样的阻抗拟和数据如表3所示。
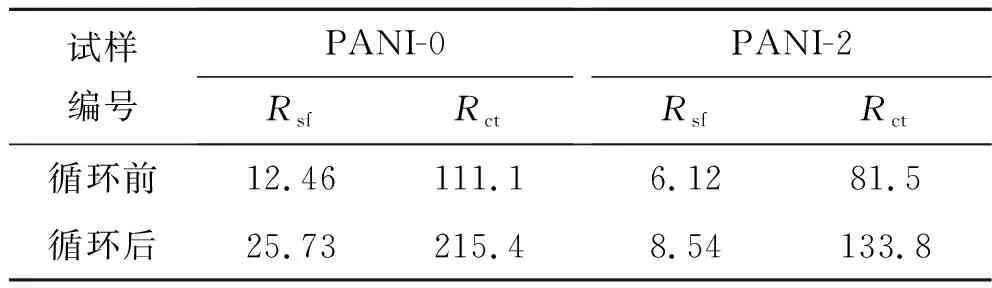
表3 循环前后不同试样的阻抗拟合数据 ΩTable 3 The impedance fitting data of different samples before and after cycles
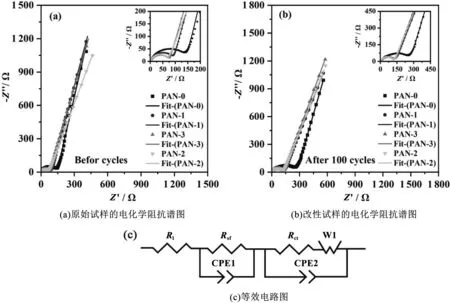
图7 原始试样和改性试样的电化学阻抗谱图及等效电路图,测试频率范围0.01 Hz~100 kHz Fig.7 Electrochemical impedance spectrum with testing frequency from 0.01 Hz to 100 kHz and equivalent circuit models
3 结论
本文通过溶胶凝胶法合成了富锂锰基正极材料Li1.2Ni0.13Co0.13Mn0.54O2,利用低温化学氧化聚合的方式,在正极材料表面形成有机包覆层——聚苯胺,聚合过程中通过质子酸掺杂的方式,降低聚苯胺分子内及分子间作用力,促进电子云的重排以及共轭结构的形成,进一步提高聚苯胺的导电性。与原始试样相比,包覆层有效提高了正极材料的导电性和电化学反应动力学,降低了材料的阻抗,同时减少了电解液与活性物质的接触,削弱了电解液对正极材料的侵蚀,稳定了材料结构。包覆层能够抑制材料在高电压下的不可逆反应,提高了循环稳定性和倍率效果。与原始试样相比,聚苯胺包覆量为4%(质量分数)时,材料在0.2 C下充放电循环100圈,其放电比容量为274.8 mAh/g,容量保持率达到99.5%,多种效果的协同作用有效改善了材料的性能。

