局部枸橼酸钠抗凝在血浆置换治疗中初始泵入速度研究*
高 超,吴 亿,杨 雯,郑红莲,赵笑兰
(陆军军医大学第一附属医院肾脏内科,重庆 400038)
血浆置换(plasma exchange,PE)是将血液引出至体外循环,通过血浆分离器,将血浆与血液中的其他成分相分离,再补充等量新鲜冰冻血浆或白蛋白溶液,非选择性或选择性地清除血液中的致病因子,是一种清除血液中大分子物质的血液净化疗法[1-2]。单重血浆置换是将分离出来的血浆全部弃除,同时补充等量的新鲜冰冻血浆或一定比例的新鲜冰冻血浆和白蛋白溶液[3]。为保障PE的顺利进行,合理选择抗凝剂尤为重要[4-5]。普通肝素与低分子肝素是目前PE治疗时较多采用的抗凝方式,但由于此抗凝方式可能诱发出血及血小板减少,存在出血或出血风险及肝衰竭患者在应用时有较大的安全性风险[6-7]。局部枸橼酸钠抗凝(regional citrate anticoagulation,RCA)在体外循环抗凝,不影响患者体内凝血机制,同时可以延长滤器寿命,减少补体和炎症细胞激活[8],被推荐为连续性肾脏替代治疗的首选抗凝方式[9-11]。近年来,RCA逐渐在血浆置换治疗中被应用,但枸橼酸钠泵入速度尚无推荐方案,本研究旨在探讨RCA血浆置换治疗时枸橼酸钠泵入的初始速度,以供临床参考。
1 资料与方法
1.1 一般资料
选取2021年1-12月在本院行RCA单重血浆置换的15例患者(67例次)纳入研究;根据枸橼酸钠初始泵入速度,将67例次治疗分为低速组(n=33)和高速组(n=34)。患者入选标准:(1)年龄≥18岁;(2)有活动性出血或高危出血风险;(3)行PE治疗,病历资料完整。排除标准:(1)严重肝功能障碍;(2)低氧血症(动脉氧分压<60 mmHg)和/或组织灌注不足;(3)代谢性碱中毒、高钠血症[3]。所有患者均被告知治疗的必要性,均签署知情同意书。本研究已通过陆军军医大学第一附属医院伦理委员会审批[审批号:(B)KY2023104]。
1.2 方法
1.2.1血浆置换方法
连续性血液净化设备购自德国贝朗公司;OP-08W血浆分离器购自日本旭化成公司;置换液选用新鲜冰冻血浆;血管通路选用无隧道无涤纶套中心静脉导管,采用正接方式建立体外循环,禁止反接以避免再循环[12]。血浆置换治疗开始时,先全血自循环5~10 min,密切观察,无异常后进入血浆置换程序。所有患者均采用单重血浆置换,血流量设定为150 mL/min,治疗时间2 h,血浆置换剂量为患者血浆容量,血浆容量=0.065×体重(kg)×(1-红细胞比容)[13]。
1.2.2枸橼酸钠抗凝方法
低速组采用4%枸橼酸钠,初始泵入速度与血流速度相同,应用微量泵补充葡萄糖酸钙(10%),泵速10 mL/h;高速组采用4%枸橼酸钠,初始泵入速度为血流速度的1.5倍,应用微量泵补充葡萄糖酸钙(10%),泵速15 mL/h[14-15]。葡萄糖酸钙于无隧道无涤纶套中心静脉导管处连接三通接头泵入患者体内。治疗过程中根据患者体内游离钙情况调整钙泵流量[16]。
1.2.3抗凝有效性观察
治疗15 min、1 h时,监测血浆分离器后游离钙浓度,目标值为0.25~0.40 mmol/L[17]。在治疗过程中,密切观察并详细记录静脉压及跨膜压,跨膜压>100 mmHg或体外循环出现凝血导致治疗非计划终止则为抗凝治疗失败。治疗结束用生理盐水回血后,目测评估血浆分离器和体外循环管路的凝血情况:0级为血浆分离器及管路无凝血或数条纤维凝血;Ⅰ级为血浆分离器及管路部分凝血或成束纤维凝血;Ⅱ级为血浆分离器及管路严重凝血或半数以上纤维凝血;Ⅲ级为需换血浆分离器[13]。
1.2.4抗凝安全性观察
观察患者治疗过程中是否出现口唇、指尖麻木及手足抽搐;治疗结束后有无并发出血。在治疗前、治疗1 h、治疗结束时,取患者外周血或在体外循环动脉端起始处采血,监测患者血气分析及体内游离钙浓度,体内游离钙维持在1.0~1.2 mmol/L[17]。游离钙<1.0 mmol/L且至少有1个低钙血症的症状或体征为低钙血症[18]。
1.3 统计学处理
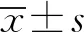
2 结 果
2.1 两组游离钙及压力指标比较
67例次血浆置换治疗均顺利完成,治疗过程中未出现因跨膜压、静脉压、滤器压降高限报警导致的非计划性结束治疗事件。两组治疗15 min时血浆分离器后游离钙浓度无明显差异(P>0.05);但治疗1 h时,高速组血浆分离器后游离钙浓度更低,差异有统计学意义(P<0.05),两组不同时间点,血浆分离器后游离钙浓度均在指南推荐的抗凝有效范围,见表1。
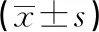
表1 两组游离钙及压力指标比较
2.2 两组不同时间点外周血气分析电解质比较
治疗结束时,两组pH、二氧化碳分压(PCO2)、碱剩余(BE)值、碳酸氢根(HCO3-)较治疗前均有所上升,游离钙浓度较治疗前均有所下降,但差异无统计学意义(P>0.05);与低速组相比,高速组在治疗结束时BE值更高,游离钙更低,差异有统计学意义(P<0.05)。治疗结束时,两组血钠较治疗前均有所上升;与低速组相比,高速组在治疗1 h、治疗结束时血钠更高,差异有统计学意义(P<0.05),见表2。

表2 两组不同时间点外周血气分析电解质比较
2.3 两组患者治疗后体外循环管路凝血情况及并发症情况比较
两组患者在治疗过程中未出现口唇、指尖麻木及手足抽搐,治疗结束时也未并发出血。低速组发生低钙血症4例次、碱中毒2例次,高速组发生低钙血症13例次、碱中毒8例次,两组比较差异有统计学意义(P<0.05);低速组发生血浆分离器、管路Ⅰ级凝血15例次,Ⅱ级凝血5例次,而高速组发生血浆分离器、管路Ⅰ级凝血14例次,Ⅱ级凝血发生4例次,两组比较差异无统计学意义(P>0.05),见表3。

表3 两组患者治疗后体外循环管路凝血情况及并发症情况比较[n(%)]
3 讨 论
血浆置换治疗时由于膜接触反应和生物相容性激活了凝血系统,诱发体外循环凝血,导致失血、置换液浪费和成本增加[19]。因此,体外循环中的血液抗凝在血浆置换过程中至关重要。有效的抗凝可以防止体外循环凝血,其中,全身肝素给药是最常用的方法,但对高出血风险患者不适用。RCA是在体外循环引血端输注枸橼酸钠,通过络合作用螯合血清中的钙离子,从而阻断体外循环中的凝血过程,然后经体外循环回血端适当补充钙离子,达到体外循环的局部抗凝且不影响患者体内凝血平衡[20-21]。因此,血浆分离器后游离钙浓度对枸橼酸钠抗凝血浆置换治疗十分关键。有研究表明,当血浆分离器后的游离钙浓度降至0.25~0.45 mmol/L时[22],可以获得良好的局部抗凝效果;专家共识中指出,体外循环游离钙浓度维持在0.25~0.40 mmol/L可有效局部抗凝[23]。本研究中,两组血浆分离器后游离钙浓度均在0.25~0.40 mmol/L,未出现因跨膜压、静脉压、滤器压降高限报警导致的非计划性结束治疗事件,提示不同速度的RCA在血浆置换治疗的有效性无明显差异。
枸橼酸钠本身无毒,它在体外循环中与血液中钙离子结合,进入体内后分解代谢为碳酸氢钠、水和二氧化氮,可以安全应用于血浆置换抗凝治疗[24-26]。枸橼酸钠输注不足会增加体外循环凝血风险,但使用过量会提高枸橼酸钠相关不良事件(如低钙血症、代谢性酸中毒或碱中毒)发生率,因此需要在保证有效抗凝的同时,避免枸橼酸使用过量,从而提高治疗效果[27]。有研究显示,导致枸橼酸钠蓄积中毒事件发生的主要原因是枸橼酸钠泵入速度过高[28]。临床常用的4%枸橼酸钠初始速度为血流速度的1.2~1.5倍,但这一常用的枸橼酸钠速度范围跨度较大,在临床应用时难以抉择。为了在有效抗凝的同时避免枸橼酸使用过量蓄积中毒,设定合适的枸橼酸钠泵入速度十分重要[29]。本研究中根据血流速度设定低速、高速两种枸橼酸钠抗凝方案,其中低速组设定枸橼酸钠泵入速度为血流速度的1.0倍,这是因为本研究采用的置换液为新鲜冰冻血浆(新鲜冰冻血浆每升溶液含有17~21 mmol柠檬酸盐)[28]。本研究结果显示,低速组患者低钙血症、碱中毒并发症例数少于高速组。
综上所述,在血浆置换时,枸橼酸钠的初始泵入速度设定为血流速度的1.0倍可以较好地控制血浆置换治疗时的相关压力参数,保障体外循环抗凝效果;同时又不会提高低钙血症及代谢性碱中毒等并发症的发生率,对患者全身凝血机制也无明显影响。

