替雷利珠单抗联合安罗替尼治疗晚期非小细胞肺癌的临床研究
林淑君,蓝佳琦,沈惠群,郭孟贤
福建医科大学附属漳州市医院,漳州 363000
非小细胞肺癌(non-small cell carcinoma,NSCLC)是临床上广泛存在的一种发病和病死概率高的恶性肿瘤,主要有腺癌以及鳞癌等类型,患者通常会出现胸闷、咳血、乏力等临床症状,相关研究表明,该疾病的产生通常与遗传、患者是否长期吸烟等因素有较大关联[1]。目前临床针对NSCLC 患者所开展的疾病治疗主要使用拥有多种抗肿瘤效果的安罗替尼,其能够对肿瘤内血管生成起到阻碍作用,产生理想的抗肿瘤效果[2]。替雷丽珠单抗是临床所使用的新型人源化IgG4 抗程序性死亡受体1 单克隆抗体,能够发挥出抗肿瘤效应[3]。本次研究探讨内容为联合使用上述两种药物对NSCLC 患者所产生的成效。
1 对象与方法
1.1 研究对象 研究选择在2020 年6 月至2022 年7 月于福建医科大学附属漳州市医院接受治疗的84 例晚期非小细胞肺癌患者签订为本次研究的最终探究目标,参与本次研究的患者均曾经接受过吉西他滨、紫杉醇、多西他赛、培美曲塞联合铂类等药物治疗。所有患者均签署知情同意书,研究在伦理委员会监督下进行。
纳入标准:①与《外科学》之中对NSCLC 患者的临床判断标准相一致;②对治疗有基础了解,同意实施;③临床分期处于Ⅲb-Ⅳ期的患者,其中腺癌患者排除EGFR/ALK/ROS1 阳性;④患者确诊已经无法接受手术治疗;⑤能够耐受本次研究所使用相关药物;⑥精神状态无任何异常变化。排除标准:①患者在接受治疗前4 周时间接受外科手术治疗亦或者是存在外伤史的患者;②同时还表现出胸腔积液或恶性心包积液的患者。
1.2 方法 小组的划分按照标准执行,分为对照组和观察组。对照组:划分为对照组的患者,使用安罗替尼胶囊,每次服用剂量为12 mg,每天使用频次为1 次,患者接受该药物连续两周的治疗后再停药1 周,按照此方式完成为期3 个月的治疗。观察组:划分为观察组的患者,在前组治疗基础上联合使用替雷丽珠单抗完成治疗,每次药物使用的剂量为200 mg,通过静脉滴注的方式完成给药,使用频次为每3 周1 次,按照此方式完成为期3 个月的治疗。
1.3 观察指标 对以下指标进行观察研究:
(1)临床疗效:在对患者实施连续3 个月的临床疾病治疗之后,按照世界卫生组织肿瘤疗效评估标准的作用下对患者所表现出的临床成效结果进行相应的分析与比较[4],将其根据实际情况划分为以下几点:完全缓解(CR):患者所存在的靶病灶不再被临床观察到;部分缓解(PR):相较于接受治疗前,患者所存在的靶病灶组织所拥有的最长直径缩短了,其程度在20%~30%的范围内;疾病进展(PD):相较于接受临床干预工作前,患者的靶病灶组织所拥有的最长直径出现了增加,其程度处于20%~30%的范围内;疾病控制(SD):患者所表现出的成效处于CR与PD 状况之间。疾病控制率=CR +PR +SD。
(2)肿瘤标志物水平:根据患者所拥有的肿瘤标志物水平情况进行相应的分析与比较,其主要是通过对患者的外周静脉血液实施采集之后,该采集量应该达到5 ml,将其放置于离心半径为10 cm,转速保持于3500 r/min 的离心机之中,接受改状态下为其10 min 的离心治疗后,去最终标本的上清液。在使用放射免疫法的作用下对患者所拥有的各项血清肿瘤标志物的水平进行测量,其中主要涉及到对糖类抗原125(CA-125)、癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE)以及细胞酵素片段抗原211(CY-211)的水平情况测定,实施测定工作的时间点为接受治疗前以及接受治疗后3 个月。
(3)免疫功能指标:在使用细胞仪的作用下对患者所拥有的各项免疫功能指标进行相应的测定以及结果比较,其中主要包含的免疫指标有CD3+、CD4+、CD8+、CD4+/CD8+以及自然杀伤(NK)细胞的水平情况,实施测定工作的时间点为接受治疗前以及接受治疗后3 个月。
(4)血清相关细胞因子:按照肿瘤标志物相同的方式完成对血清标本的采集,之后在使用酶联免疫吸附法的作用下对血清相关细胞因子的水平情况进行测定,其中所测定的主要指标包括了表皮生长因子(epidermal growth factor,VEGF)、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)以及肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)的水平情况。
(5)不良反应:对患者治疗过程中出现不良反应的概率进行比较与分析,其中所涉及到的情况包括了胃肠道不适、肝肾功能异常、白细胞减少以及血小板减少等情况。
1.4 统计学方法 采用SPSS 21.0 分析,计量资料以表示,经t检验,计数资料经χ2检验,以n(%)表示,差异有统计学意义为P<0.05。
2 结果
2.1 对比两组一般资料 共纳入晚期非小细胞肺癌患者84例,两组各42例。对照组男性患者22例(52.38%),年龄范围为43~67 岁,均值(56.87±5.69)岁,其中表现为鳞癌、腺癌、腺鳞癌的患者数量分别为13 例、15 例以及14 例;观察组男性患者23 例(54.76%),年龄范围为43~68 岁,均值(56.58±5.64)岁,其中表现为鳞癌、腺癌、腺鳞癌的患者数量分别为14 例、15 例以及13 例。使参与者的基线资料进行相互之间的比较与分析,不具备差异性(P>0.05)。
2.2 对比两组疾病控制率 观察组疾病控制率高于对照组(P<0.05)。见表1。
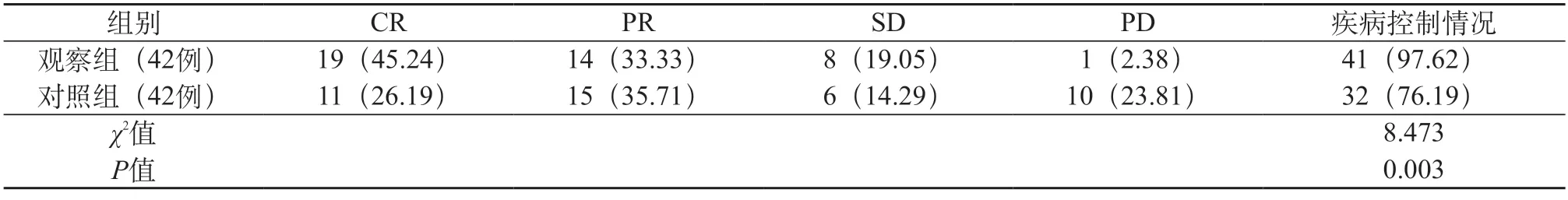
表1 对比两组疾病控制率 [例(%)]
2.3 对比两组肿瘤标志物水平 治疗前各肿瘤标志物水平未表现出差异(均P>0.05),治疗后各项指标水平均降低,且观察组低于对照组(均P<0.05)。见表2。
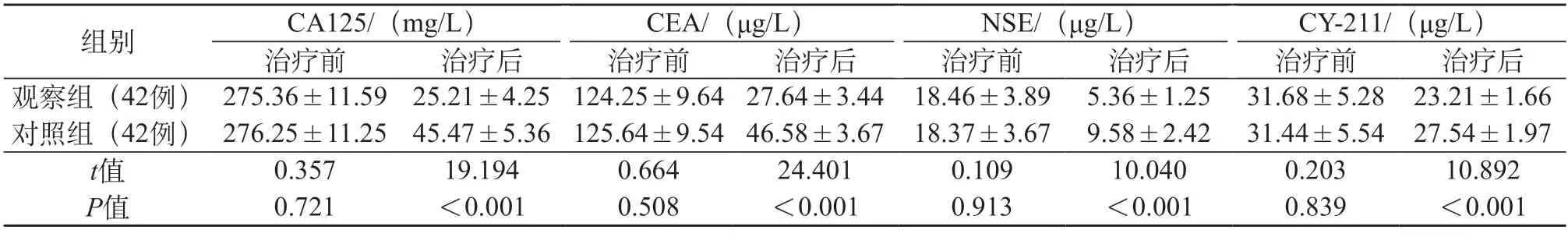
表2 对比两组肿瘤标志物水平
2.4 对比两组免疫功能指标水平 治疗前各免疫功能指标未表现出差异(均P>0.05),治疗后观察组CD3+、CD4+、CD4+/CD8+以及NK 水平均高于对照组,而CD8+水平低于对照组(均P<0.05)。见表3。

表3 对比两组免疫功能指标水平
2.5 对比两组血清相关细胞因子水平 治疗前两组无血清相关细胞因子水平差异(P>0.05),治疗后观察组各指标水平均低于对照组(均P<0.05)。见表4。
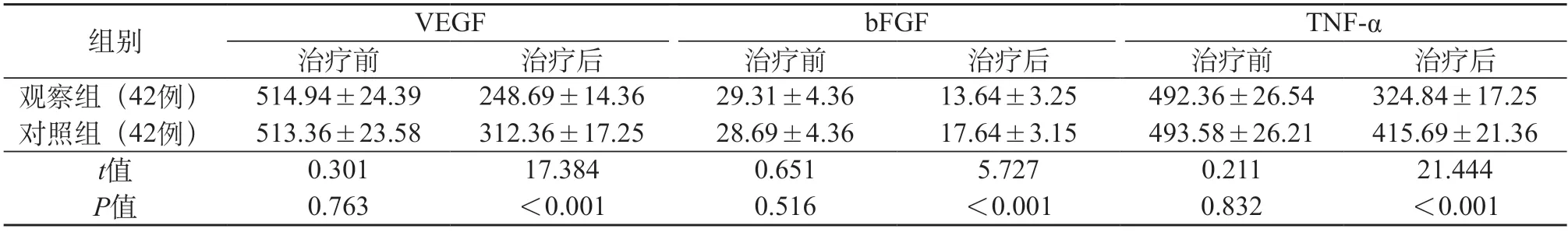
表4 对比两组血清相关细胞因子水平(ng/L)
2.6 对比两组不良反应发生率 两组出现不良反应的概率对比无差异(P>0.05)。见表5。

表5 对比两组不良反应发生率 [例(%)]
3 讨论
存在NSCLC 症状的患者在疾病早期阶段不表现出较为显著的临床症状,拥有非常强的隐匿性,当确诊时已错过最佳治疗时间,进入到中晚期,对临床开展的疾病治疗工作带来了较大的困难[5]。所以临床对于处于晚期阶段的NSCLC 患者,对其开展疾病治疗的原则就是让患者的生存时间得以延长,使其生活质量水平得到改善[6]。在本次研究使用的安替罗尼是一种新型的络氨酸激酶受体抑制剂,在治疗过程中,其对于成纤维生长因子受体以及血管内皮生长因子水平能够产生一定程度的阻碍作用[7]。在实际临床应用过程中,安罗替尼能够覆盖的肿瘤靶点相对较多,患者对于该药物所拥有的耐受程度也较高[8]。随着临床对于NSCLC 的相关研究不断深入开展,现阶段发现为患者开展免疫治疗能够对处于晚期的NSCLC 患者产生更为贴近理想的治疗成效,在临床实际使用过程中拥有重要的价值与意义[9]。研究发现临床使用的新型制剂PD-1 单抗能够对机体T 细胞表面所存在的PD-1 起到阻断的功效,从而使得机体内所含有的适应性免疫系统被激活,从而将肿瘤细胞杀灭[10]。本研究所使用的替雷丽珠单抗是属新型抗肿瘤免疫治疗药物中的一种,相关研究表明,该药物能够对机体出现的T 细胞是能或者衰竭状态起到改善亦或逆转功效,其能够产生更加积极的激活T 细胞杀伤能力的功能[11]。
在研究开展过程中,通过对患者使用替雷丽珠单抗联合安罗替尼的方式开展对晚期NSCLC 患者的治疗,观察组最终的疾病控制率高于对照组(P<0.05),表明了在使用安罗替尼的基础上,为患者使用替雷丽珠单抗开展疾病治疗,能够让患者获得更贴近理想的治疗成效[12]。这一结果的产生可能是因为两种药物的协同效应,安罗替尼的使用能够对肿瘤环境之中的免疫状态起到一定的调整作用,并且能够使得靶病灶的血供降低[13],在此基础上联合替雷丽珠单抗进行治疗,能够使靶病灶组织对于抗血管生成的药物敏感性有效增加,能够将肿瘤内部血管“正常”化的时间减慢,从而对抗血管生成的这一过程起到促进作用[14]。
综上所述,处于晚期阶段的非小细胞肺癌患者,在通过使用替雷丽珠单抗联合安罗替尼的作用下完成疾病治疗工作,能够使得患者获得更加理想的临床控制率,患者所最终得到的成效与理想状态更为相贴,对于肿瘤新生血管的产生起到了良好的阻碍作用,减少了血清肿瘤标志物的水平大小,让患者能够以更高质量的状态完成生活各项活动。

