学科交叉视域下高锰酸钾法测定水样中化学需氧量实验的 设计与实践
刘晓红,李姝,叶世海,楼兰兰
南开大学材料科学与工程学院,天津 300350
实验教学是高校本科教学的重要组成部分[1-3],是培养学生动手实践能力、观察记录实验现象能力、数据处理能力、创新思维和科学素养的重要途径[4-8],在人才培养过程中起着不可替代的基础作用[9]。实验训练对于培养学生的实践操作技能、安全意识和严谨的科学态度起着重要作用[10],是学生学习后续实验课程的关键环节,也是工作中解决实际技术难题的基础。南开大学津南校区化学国家级实验教学示范中心(以下简称“中心”),配合学校在本科教学中培养多学科交叉复合型人才的教育目标,在本科实验教学中积极探索与尝试先进的教学理念与方法[11-13]。
中心开设的无机及分析化学实验课程多年来是面向化学、环境工程、资源循环科学与工程、材料化学、材料物理和药学等专业学生的第一门专业必修实验课程,此课程与各专业课相互渗透,具有承上启下的重要作用。近年来学校实行大类招生培养,此课程是理科试验班类(物质科学与可持续发展)学生入学后的首门专业必修实验课程。学生通过学习此课程中的基础实验可获得感性认识,加深并巩固对化学基础理论和基本概念的理解。然而,此课程原有内容与潜在的环境类专业学生的专业发展存在不相匹配问题,所以中心在保证原有课程内容系统性和层次性基础上,新增加一个具有化学与环境知识交叉背景的5课时的“水样中化学需氧量的测定(KMnO4法)”分析化学实验。在此实验课堂教学中,在灵活地将化学与环境学科内容进行交叉融合教学时,可以从水质安全问题入手,以如何判断水质安全为切入点,借助氧化还原反应基本原理解释实验现象和实验原理,讲原理的同时融入环保意识,进而让学生树立“绿水青山就是金山银山”的可持续发展观,激发学生利用专业知识解决实际问题的兴趣,提升其专业学习认同感与自豪感。还能使其在实践中充分理解通过在不同学科领域中的深入研究和不断探索,构建完善的知识结构,掌握扎实的基础知识和基本技能,才能为将来更好地服务社会打下坚实的基础,进而为国家科学技术的卓越发展贡献自己的一份力量。在接下来的实验教学中,将基础理论知识与专业的实验操作技能培养紧密结合,在引导学生根据实验结果计算出水样的化学需氧量过程中,培养学生严谨求实的科学态度,通过比较日常生活废水与实验室自来水的化学需氧量值,使学生能够站在环境保护和可持续发展的角度思考环境工程领域的可持续问题,通过亲身体验,深刻理解节约水资源和不乱倾倒废液的重要性,并引入典型思政案例,进一步增强学生保护环境的意识。如上海交通大学的孔海南教授带领上海交通大学湖泊富营养化治理教师团队,以实际行动坚持“把科研论文写在祖国大地上”,通过把书本化学知识转化为解决实际问题的办法,让水质严重恶化的洱海又重现了昔日大理“母亲湖”的风采[14]。此高锰酸钾法测定水样的化学需氧量实验取得了良好的教学实践效果,提高了学生的实践能力、数据收集计算能力、创新能力、跨学科综合思维能力[15]以及运用化学专业知识解决环境领域实际问题的能力,有效促进了具有扎实理论基础、多学科背景知识和突出实践能力的复合型人才的培养。
1 中心开设的无机及分析化学实验课程教学现状
中心开设的无机及分析化学实验课程共计68学时一学期,每个教学班约有30名学生,原有实验项目包括5个无机化学实验和6个分析化学实验(表1)。为了提高本课程内容的多学科交叉融合性,激发具有不同学科背景学生的学习兴趣,培养学生的自主学习、探究实践以及创新能力,中心于2022-2023学年第一学期新增加一个“水样中化学需氧量的测定(KMnO4法)”分析化学实验。
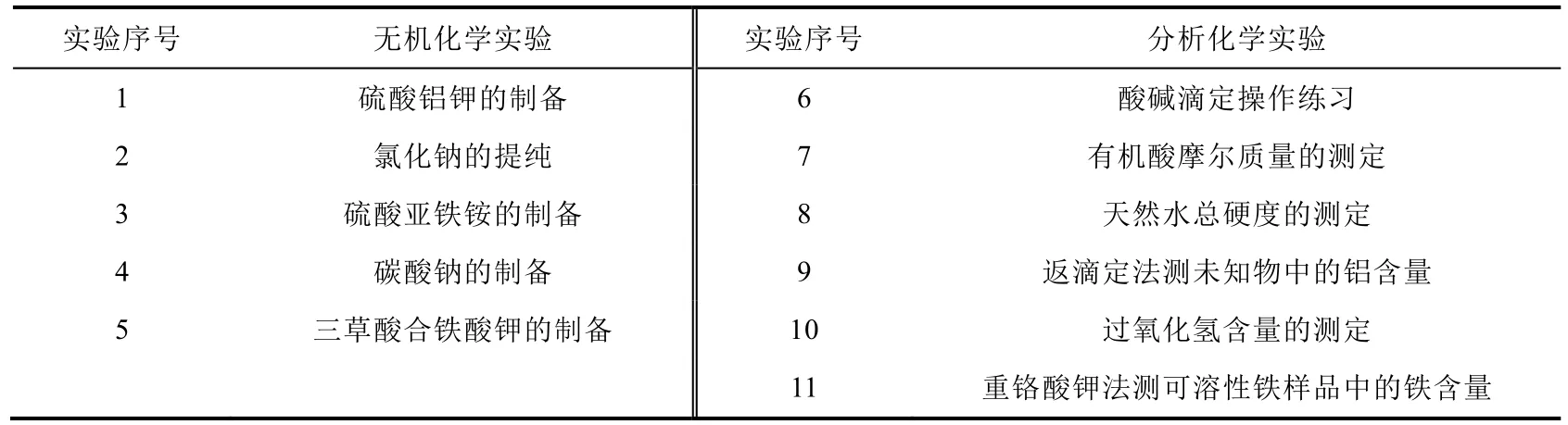
表1 中心开设的无机及分析化学实验课程原有实验内容汇总
2 水样中化学需氧量的测定(KMnO4法)实验教学设计与实践
2.1 实验项目设计背景
化学需氧量(Chemical oxygen demand,简称COD)的大小通常可作为反映水体中有机化合物及无机还原性物质污染程度的一项重要指标。COD值越高,说明水体污染越严重[16]。COD的测定有酸性高锰酸钾法[17,18](适于地表水、地下水、饮用水、生活用水等较为清洁的水体中COD的测定)、碱性高锰酸钾法[17,19](适于高Cl-水体,如海水)和重铬酸钾法[20](适于工业污水及生活污水中含有较多成分复杂的污染物质的水质)。本实验可在5课时内完成,通过让学生测定水样中的COD值,使学生在实践训练过程中夯实氧化还原滴定分析方法的基础理论,掌握一种评价水体污染程度的实验方法,具备一定评判水质污染程度的能力。
2.2 实验原理及教学目标
2.2.1 实验原理
COD是指在一定的条件下,采用一定的强氧化剂处理水样中的还原性物质(包括有机物、亚硝酸盐、硫化物和亚铁盐等)时,所消耗的氧化剂量折算成氧气的量[21],单位为mg·L-1。测定COD的方法中,酸性KMnO4法简便快速,是在酸性条件下用过量的高锰酸钾溶液(V1)将水样中多数有机化合物及无机还原性物质氧化,剩余的高锰酸钾溶液用定量且过量(VNa2C2O4)的草酸钠溶液还原,剩余的草酸钠溶液再用高锰酸钾溶液返滴定(V2)至溶液呈微红色。根据实验数据,可计算出水样的化学需氧量,从而可判断水样的污染程度。水样中的化学需氧量的计算公式[21]如下:
式中,V1、V2分别为KMnO4的加入体积和返滴定过量的Na2C2O4时消耗的体积,单位为mL;c-KMnO4为KMnO4溶液的平均浓度,cNa2C2O4表示Na2C2O4标准溶液的浓度,单位为mol·L-1;VNa2C2O4表示一次性加入的Na2C2O4标准溶液的体积,单位为mL;为氧的摩尔质量,8.00 g·L-1。根据有关实验数据,可计算出水样中的COD值。
2.2.2 实验教学目标
(1) 掌握高锰酸钾溶液的配制及用草酸钠作基准物质标定其准确浓度的方法,掌握草酸钠标准溶液的配制方法,培养学生减量法称量、移液、定容、滴定等基本操作技能。
(2) 掌握化学需氧量的定义和高锰酸钾法测定化学需氧量的基本原理和实验方法,能用滴定数据计算出水样的化学需氧量。
(3) 理解水样中化学需氧量测定的必要性,体会化学知识在解决环境实际问题中的应用,培养学生实事求是的科学态度,理论联系实际、分析解决问题和跨学科思维的能力,增强学生环境保护意识。
2.3 实验项目教学设计
2.3.1 主要实验设备
50 mL聚四氟酸式滴定管(A级);容量瓶(250 mL);烧杯(100 mL,250 mL);移液管(10 mL,25 mL);锥形瓶(250 mL);称量瓶;分析天平;加热磁力搅拌器。
2.3.2 实验试剂
高锰酸钾(分析纯);草酸钠(分析纯);硫酸溶液(1 : 3,约4.5 mol·L-1);水样。
2.3.3 实验操作步骤
(1) KMnO4溶液的配制与标定。
称取mKMnO4g的高锰酸钾固体于棕色试剂瓶中,加入500 mL蒸馏水,置于暗处静置一周后备用。准确称取m1,Na2C2O4g在0.1500-0.2000 g范围的Na2C2O4三份,分别置于250 mL锥形瓶中,各加入85 mL蒸馏水使其溶解,加热至溶液中有蒸气冒出,加入20 mL 1 : 3硫酸溶液,趁热用KMnO4溶液进行滴定。滴定初,当第一滴KMnO4溶液的紫红色完全褪去后,再滴入第二滴KMnO4溶液,滴定过程中溶液温度需保持在70-80 °C。接近终点时,KMnO4溶液紫红色褪去较慢,应减慢滴定速率,并充分摇匀,当滴入半滴或一滴KMnO4溶液,充分摇匀后溶液呈微红色且在30 s内不褪色即为滴定终点。记录消耗的KMnO4溶液体积,平行测定三次。计算KMnO4溶液的浓度平均值及相对平均偏差:
式中ci为第i次标定出的KMnO4溶液的浓度,单位为mol·L-1;KMnO4为KMnO4溶液的平均浓度,单位为mol·L-1。
(2) 草酸钠标准溶液的配制。
准确称取m2,Na2C2O4g的草酸钠固体于100 mL洁净的烧杯中,加100 mL蒸馏水溶解,再加入1 mL 1 : 3硫酸溶液,定量转移入250 mL容量瓶中,用蒸馏水稀释至刻度,摇匀,按实际称取质量计算其准确浓度。实验组中m2,Na2C2O4为1.800-2.000 g,对照组中m2,Na2C2O4分别为0.3000-0.4000 g和0.6000-0.8000 g。
(3) 酸性溶液中测定水样的化学需氧量。
移取25.00 mL水样分别置于三个锥形瓶中,向锥形瓶中各加入75 mL蒸馏水,然后一次性加入V1mL已标定的KMnO4溶液,10.00 mL 1 : 3 H2SO4溶液,加热板温度设置为90-100 °C,加热煮沸10 min(此时溶液的紫红色不褪去)。取下锥形瓶,趁热用移液管一次性加入Na2C2O4标准溶液VNa2C2O4mL,摇匀(此时溶液应呈无色透明),趁热立即用V2mL KMnO4溶液滴至溶液呈微红色,且在30 s内不褪色。记录KMnO4溶液的体积,平行测定三份。计算COD (mg·L-1)和相对平均偏差。
3 结果与讨论
3.1 KMnO4固体质量对溶液标定结果的影响
实验中固定基准物草酸钠的质量m1,Na2C2O4在0.1500-0.2000 g之间,改变配制500 mL高锰酸钾标准溶液时所称取的固体高锰酸钾的质量mKMnO4,并用滴定分析法标定高锰酸钾溶液的准确浓度,请见表2。结果发现:当称量的高锰酸钾质量为0.8-0.9 g时,滴定草酸钠时所消耗的高锰酸钾溶液体积在45.00 mL以上,当称量的高锰酸钾质量在1.6-1.7 g时,滴定时所消耗的高锰酸钾溶液的体积在20.00-30.00 mL之间,滴定误差相对较小,所以称取高锰酸钾固体进行溶液配制时,其质量范围为1.6-1.7 g,标定得到高锰酸钾溶液的平均浓度为0.02016 mol·L-1。
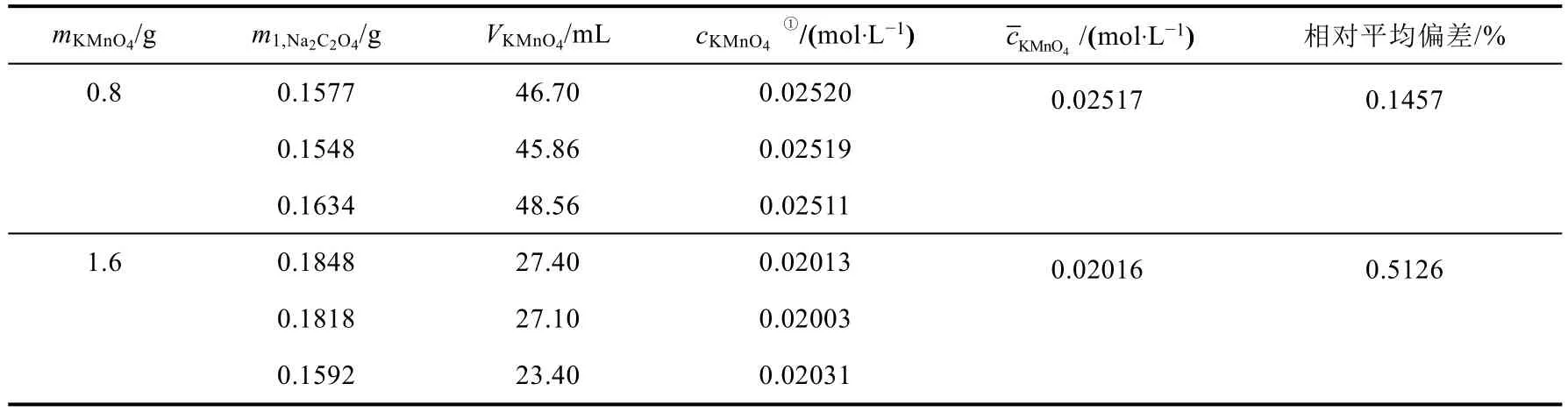
表2 KMnO4溶液的标定结果
3.2 Na2C2O4标准溶液的浓度对实验室自来水中COD测定的影响
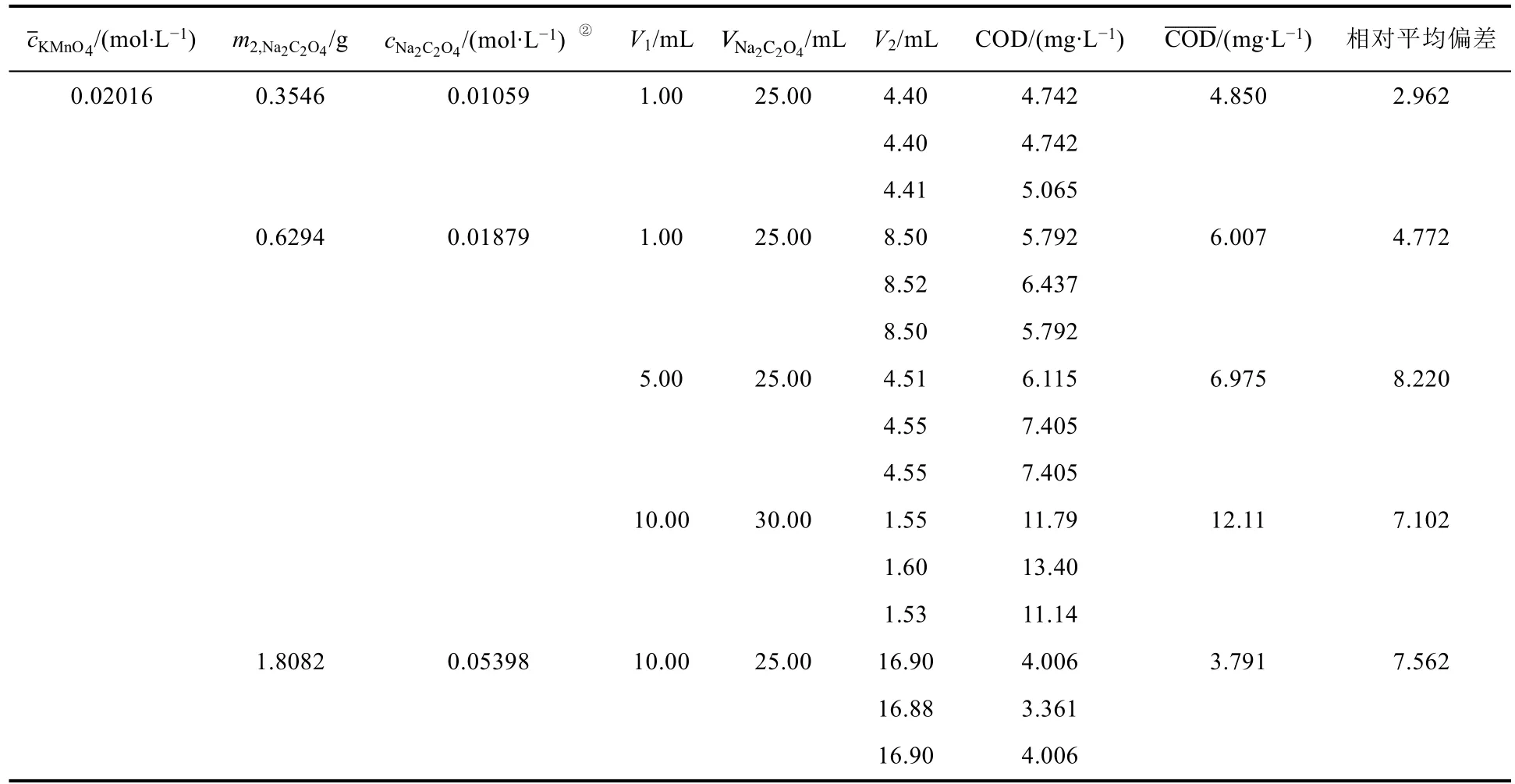
表3 草酸钠标准溶液浓度对实验室自来水中COD测定的影响
3.3 学生对不同水样中化学需氧量的测定结果对比
实验中学生分为实验组和对照组分别进行实验。实验条件为:称量1.6-1.7 g的高锰酸钾用于配制高锰酸钾溶液,准确称量1.800-2.000 g的草酸钠用于配制草酸钠标准溶液,且V1= 10.00 mL,VNa2C2O4= 25.00 mL。实验组中的25名学生采用津南校区实验室中自来水作为待测水样,对照组的58名学生则采用中水站消毒池中的生活污水作为测定对象,自主进行高锰酸钾溶液的配制及标定,再用配制的草酸钠标准溶液进行测定,根据滴定数据计算水样中的COD值。结果显示,实验组学生测得的实验室自来水的COD平均值为7.570 mg·L-1,对照组学生测得的中水站消毒池中的生活污水COD平均值为16.36 mg·L-1,表明中水站消毒池中的生活污水里含有的有机化合物及还原性物质含量明显高于实验室中自来水,实现了通过基础分析化学实验使学生获得对环境学科知识感性认识的目标。
4 实验考核
本实验考核评分由“预习报告(10%)+课堂实验操作(30%)+实验结果(40%,含实验报告规范撰写和实验数据精密度情况)+实验素养(20%)”四部分构成。实验课堂教学中,注重考查学生的化学基本操作技能、设备的基本操作、实验数据采集的严谨性与客观性、数据处理的科学性,要求学生必须到实验室进行实践操作,教师和研究生助教通过课堂巡回检查可基本了解学生对分析天平称量操作(15%)、溶解过程操作(10%)、转移与定容操作(25%)、溶液移取操作(10%)、滴定管的润洗、滴定、读数操作(30%)和数据记录(10%)的掌握情况和规范性。实验报告撰写的规范性及实验结果的精密度评价标准按实验中心要求进行评价。
5 教学效果评价
2022-2023学年第一学期的实验教学中,150名学生的实验完成度为100%,学生实验平均分为86分,其中4名学生在2022年天津市科学实验展演比赛中获得优秀奖。课程结束后及时对145名学生和5名教师进行问卷调查,问卷内容见表4。结果表明:学生和教师都对本实验的教学内容及教学过程予以高度评价(平均分为9.6和9.2分,见图1A和B),认为本实验在培养具有环境与化学学科知识的学生方面具有重要作用(评价的平均分为9.5和9.8分)。由图1A可知,学生认为本实验能有效帮助他们分析与解决问题能力(平均分为9.4和9.8分)、动手操作能力、实验现象观察能力以及数据收集、归纳处理能力的提高,教学育人效果明显。
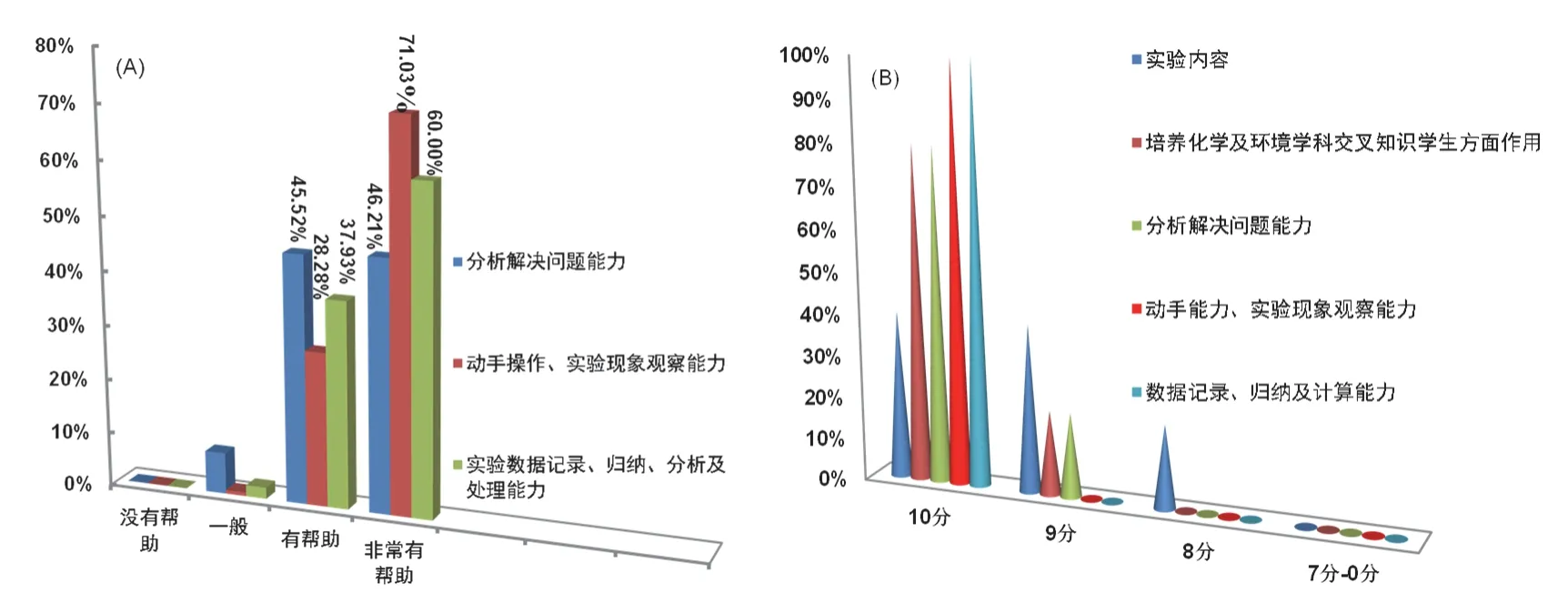
图1 (A) 学生对实验的评价;(B) 教师对实验内容及教学效果的评价
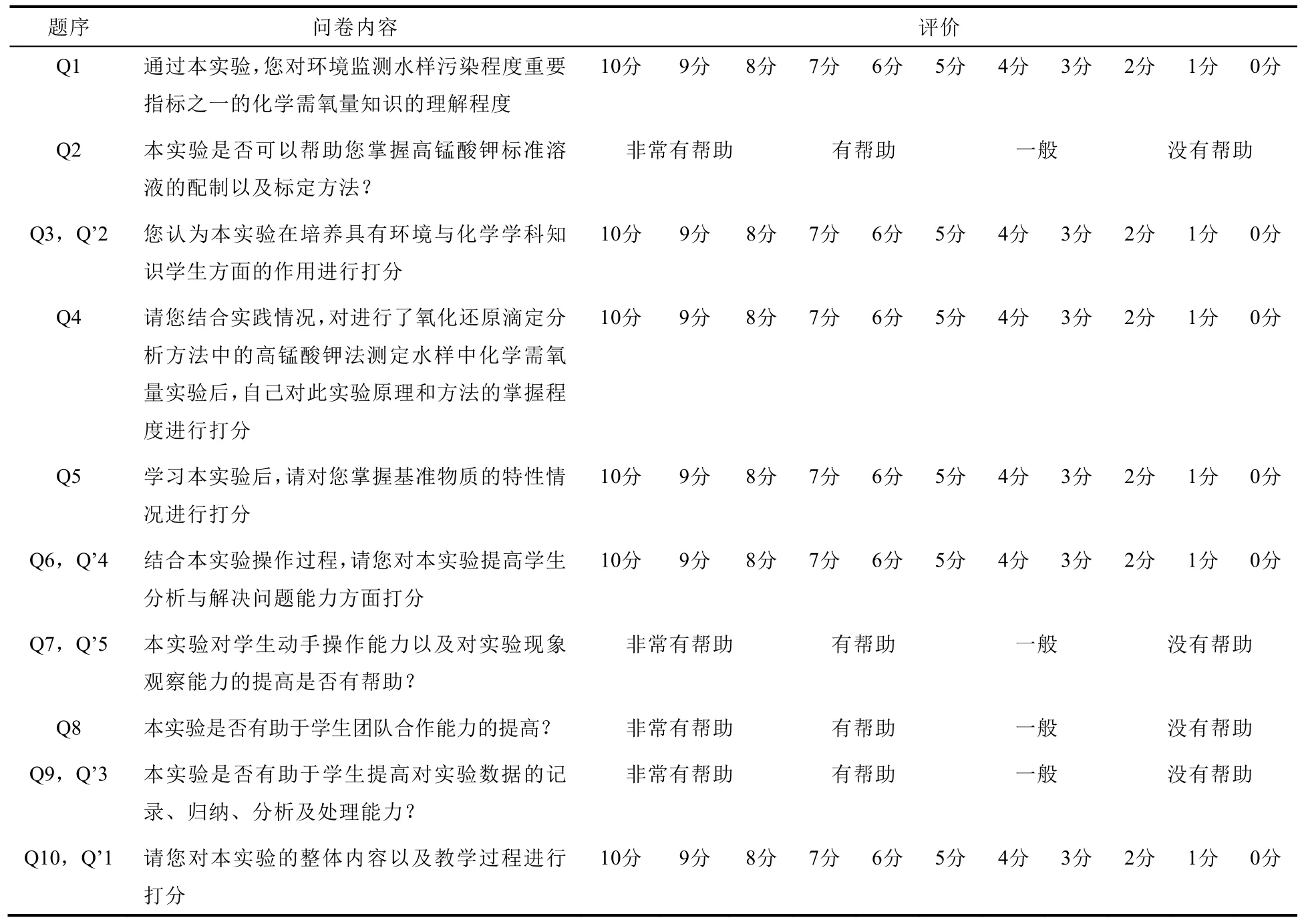
表4 学生(Q1-Q10)与教师(Q’1-Q’5)对本实验内容及教学效果的评价情况调查
6 拓展实验设计
学生可自行采集南开大学津南校区中水站清水池或曝气池或学校周边河流中的水样作为待测水样,采用高锰酸钾法进行水样中总耗氧量的测定。此外,本实验为酸性水样中COD的测定,学生可尝试在碱性介质中用KMnO4氧化有机化合物,待氧化反应完成后,用碘量法滴定或者采用重铬酸钾法测定水样的化学需氧量,从而提高学生的基础化学实验知识与实验操作基本技能。
7 结语
通过本实验的实践训练,学生可掌握一种测定水样中有机物和还原性物质的氧化还原滴定分析方法,并具备了一定评判水体污染程度的能力。问卷调查表明,本实验有助于培养学生运用化学专业知识融会贯通地解决环境领域实际问题的能力、跨学科综合思维能力以及数据归纳计算能力,有利于培养多学科知识背景复合型人才。教学实践表明,该实验内容全面,课时合理,育人效果明显,适合为化学、环境工程和资源循环科学与工程等专业学生开设。

