典型吸附剂在地下水污染防治中的应用研究
高优娜,赵 琼,杨志明,莫日根敖其尔
(1.内蒙古第三地质矿产勘查开发有限责任公司,内蒙古 呼和浩特 010011;2.内蒙古正华煤炭科工贸有限公司,内蒙古 呼和浩特 010000)
引言
地下水资源作为我国水资源体系中不可或缺的组成部分,支撑着农业灌溉、城市供水和工业生产,但随着工业化和城市化进程加速推进,地下水面临日益严重的污染威胁。例如,某城市是中国重要的工业中心之一,长期以来工业废水排放和农业污染物渗入地下水已导致地下水质量下降,引发了严重的地下水污染问题,不仅危及周边地区的生态环境,还威胁到了数百万人口的健康,对整个区域的可持续发展产生了负面影响。
1 研究背景与地区概况
某城市地下水污染问题与其地质特征密切相关,该地区的地质构造复杂且地下岩层多变,不同地层的渗透性差异巨大,导致了污染物在地下水中的迁移速度和路径存在着不均匀性。一些地层对污染物的传播具有较高的渗透性,而其它地层可能会限制污染物的传播,此区域水文特征还受到季节性降水和地下水补给带来的影响,再加上长期的过度开采和地下水污染,地下水位迅速下降造成水资源紧张的状况[1]。季节性降水波动使地下水位的恢复变得更加困难,加剧了地下水资源的压力。解决该地区地下水污染问题存在较多困难,并受制于地质和水文情况对其影响的复杂性,这突出了吸附剂在地下水污染防治中应用的迫切性。我们需要采取科学合理的措施保护地下水资源,以及更好地保障生态平衡和人类健康。
2 地下水污染及吸附剂的应用
2.1 地下水污染机制
在某城市地下水污染案例中,污染源多元化且传播途径复杂,这为地下水污染机制的深入研究提供了重要资料。作为一个重要的工业中心,各类工业生产活动导致大量有机物和重金属等污染物进入地下水,污染源主要包括化工厂、电子制造业、冶炼企业等;农业生产中的化肥、农药和兽药等化学品经雨水冲刷和渗透进入地下水,导致地下水中的氨氮、硝酸盐等含量升高;大量城市污水被排放到下水道系统中,其中一部分渗漏到地下水,这些污水中含有有机物、微生物和各种化学物质[2]。地下水受到地质特征的影响,不同地层中的地下水流速差异明显,导致污染物在地下水中的传播速度和路径不均匀,会在地下水中形成长期的渗透带。工农业生产过度开采地下水导致了地下水位下降,进一步加剧了污染物的迁移,地下水位降低使得地下水中的污染物更易到达浅层地下水,甚至影响地表水体。
2.2 吸附剂的定义与分类
吸附剂是一种具有特定化学或物理性质的材料,能够将溶液中的污染物吸附到其表面,吸附过程是通过吸附剂表面的活性位点吸附溶液中的离子、分子或颗粒物质实现的。吸附过程通常是一个可逆的物理或化学反应,具有较高的选择性和处理效率,使其成为地下水污染防治中的关键技术之一[3]。物理吸附是由于吸附剂表面的物理吸引力引起的,分子之间的范德华力和静电吸引力是吸附作用存在的主要原因。吸附通常在低温条件下进行,吸附与释放均可逆进行。化学吸附机制涉及化学键的形成,通常是通过共价键或离子键来完成吸附。化学吸附通常在高温条件下发生下,具有较高的选择性。
天然吸附剂在自然界中广泛存在,例如活性炭、黏土和硅胶等,可通过物理或化学处理提高其吸附性能,适用于地下水污染防治。疏水性吸附剂对疏水性污染物具有较高的亲和力,如石墨烯、活性炭等;亲水性吸附剂对亲水性污染物更具吸附性能,如改性氧化铁、聚合物树脂等;阳离子交换吸附剂通常用于去除带正电荷的污染物,如重金属离子;阴离子交换吸附剂主要用于去除带负电荷的污染物,如氨氮和硝酸盐等。在地下水污染防治过程中,选择合适的吸附剂非常重要,它们需要适应不同类型的污染物和水质特点,有助于高效去除地下水中的污染物,净化地下水资源,以减少地下水污染对环境和人类健康的威胁。
2.3 吸附剂在地下水污染防治中的作用机制
吸附剂在地下水污染防治中起到关键作用,其作用机制可以分为吸附原理和去除机制两个方面。吸附剂吸附原理是地下水污染治理的基础,在吸附过程中,吸附剂表面的活性位点与污染物之间相互作用,污染物从溶液中被吸附到吸附剂表面。吸附剂表面具有一定的亲和力,能够与污染物形成吸附作用,亲和力可以是物理亲和力,如范德华力、静电吸引力,也可以是化学亲和力,如氢键或共价键。根据地下水污染物的性质,吸附剂应具有较高的亲和性[4]。吸附过程达到平衡时,吸附剂表面的吸附位点为饱和状态,不再吸附更多的污染物。吸附平衡是吸附剂设计应用的关键,吸附平衡通常受到温度、溶液pH值、吸附剂的化学性质等因素的影响。
3 反排液中的离子成分和吸附模拟
3.1 反排液中的离子成分分析
反排液中的离子成分分析是地下水污染防治的关键环节,用于了解地下水污染程度并为后续的治理和处理提供关键数据[5]。取样点的反排液现场取样包括测量pH值、水温以及分析阳离子和阴离子种类及其浓度等。pH值是衡量反排液酸碱性的关键参数,相关人员可以使用pH电极在取样点现场测量pH值,酸性或碱性的pH值可能提示不同类型的污染源,例如低pH值可能暗示有酸性污染物的存在,如重金属酸性排放等。测量水温可以帮助理解地下水的温度变化,水温影响离子溶解度,因此在分析离子浓度时必须记录水温。反排液中离子成分统计见表1。

表1 反排液中离子成分统计表 单位:mg/L
反排液的pH值介于酸性和碱性之间(pH值=6.5),接近中性,表明反排液中没有明显的酸性或碱性污染物,中性pH值通常有利于大多数水体中的生态系统和生物多样性。水温通常受季节和地理位置的影响,25 ℃是相对较温暖的水温,但它可能是正常的季节性变化。Na+(17.4 mg/L)是地下水中的常见阳离子,其浓度在正常范围内;Fe3+(2.3 mg/L)浓度较低,高铁浓度可能来自于工业废水排放或地下水中铁的溶解;K+(71.5 mg/L)是地下水中的常见阳离子,其浓度在正常范围内;Ca2+(51.5 mg/L)是地下水中的常见阳离子,其浓度在正常范围内;Ba2+(30.5 mg/L)浓度较低,高钡浓度可能源自地质或工业污染;Mg2+(75.2 mg/L)是地下水中的常见阳离子,其浓度在正常范围内;Cl-(55.3 mg/L)浓度在正常范围内,可能来自自然水体或城市污水排放;CO32-(50.3 mg/L)浓度较低,高碳酸根浓度可能源自工业废水排放或地下水的碳酸盐岩层;SO42-(87.3 mg/L)浓度较高,可能来自工业活动或地下水中的硫酸盐。
3.2 吸附模拟方法介绍
吸附模拟方法是研究吸附剂如何与污染物相互作用以及如何去除它们的重要工具,相关人员在反排液成分分析的基础上,可以采用吸附模拟来进一步了解吸附剂的性能和效率。吸附等温线用于描述吸附剂上吸附物质的吸附和平衡,在分析反排液中的成分后,可以使用吸附等温线模型来预测吸附剂与溶液中各种阳离子和阴离子的相互作用。Langmuir模型假定吸附剂表面有固定数量的吸附位点,吸附物质在这些位点之间产生吸附和脱附的平衡,这个模型通常用于描述单层吸附。通过实验数据可以得到Langmuir等温线,其中的参数如最大吸附容量和吸附平衡常数可以用于评估吸附剂的性能,吸附等温线与Langmuir常数见图1所示。
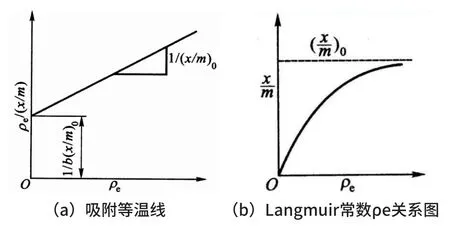
图1 吸附等温线与Langmuir常数关系图
吸附等温线横坐标为Langmuir常数ρe,ρe>1,纵坐标为ρe(x/m),见式(1):
Langmuir吸附等温模型中,吸附剂表面活性分布均匀,每个点均可吸附一个分子或离子,为单分子层吸附方式,吸附质所占面积保持一致。ρe很低时,1+bρe趋近于1;ρe很高时,1+bρe趋近于bρe。
吸附动力学模型用于描述吸附过程的速率和机制,在分析反排液成分后,可以使用吸附动力学模型来了解吸附剂与溶液中各种离子之间的吸附速率和平衡时间。Pseudo-First-Order模型假定吸附速率与吸附物质的浓度成比例关系,通过实验数据可以得到Pseudo-First-Order模型的参数,如吸附速率常数和平衡吸附量,以评估吸附剂的吸附速度。Pseudo-Second-Order模型假定吸附速率与吸附物质的浓度平方成比例关系,通过实验数据可以得到Pseudo-Second-Order模型的参数,如吸附速率常数和平衡吸附量,以评估吸附剂的吸附速度和吸附机制。综合以上模型,吸附等温线模型可用于了解吸附剂与溶液中离子的平衡,而吸附动力学模型则帮助我们了解吸附速率和机制。模型应用有助于优化吸附剂的设计和使用,以有效去除反排液中的污染物,提高地下水质量,保护环境和人类健康。
3.3 阳离子吸附剂对反排液的吸附模拟
在进行阳离子吸附剂对反排液的吸附模拟之前,相关人员首先需要选择适当的阳离子吸附剂,并确定吸附实验条件,然后进行吸附模拟和结果分析。根据反排液的离子成分分析情况,选择适合的阳离子吸附剂非常重要,考虑到反排液中的离子成分,如Na+、K+、Ca2+、Ba2+和 Mg2+,选择Amberlite IR-120强酸性离子交换树脂,具有高选择性,可以有效去除多种阳离子,具有优良的吸附性能。
在进行吸附实验时,相关人员需要确定以下吸附条件:吸附剂用量根据反排液的体积和阳离子浓度,确定适当的吸附剂用量,以确保有足够的吸附位点来去除阳离子;确定吸附平衡所需的时间,吸附实验将进行一定时间的搅拌或静置,以达到吸附平衡;进行吸附实验时,要控制温度以保持稳定条件,通常室温(约25 ℃)是一个合适的选择;根据反排液的pH值,可以调整吸附剂的pH值以最大程度地提高吸附效率;进行吸附实验后,可以选择Amberlite IR-120对吸附模拟进行分析,表2是吸附模拟结果的数据统计表。

表2 阳离子吸附模拟结果的数据统计表
吸附率可以通过式(2)计算:
分析结果应与实验数据相对比,以验证吸附模拟的准确性和吸附剂的性能,进一步的分析可以包括讨论吸附动力学模型(如Pseudo-First-Order或Pseudo-Second-Order模型)来了解吸附速率,以及通过吸附等温线模型(如Langmuir或Freundlich模型)来评估吸附平衡。这些分析有助于确定阳离子吸附剂的性能和适用性,为地下水污染治理提供重要信息。
3.4 阴离子吸附剂对反排液的吸附模拟
根据反排液中的阴离子成分分析,选择适当的阴离子吸附剂至关重要。考虑到反排液中的阴离子成分,如Cl-、CO32-和SO42-,相关人员可以选择一种离子交换树脂来进行吸附实验。一种常见的选择是强碱性离子交换树脂,其具有高选择性,可以有效去除多种阴离子。作为一个示例,可以选择规格型号为Purolite A520E的离子交换树脂,它适用于高效去除多种阴离子。相关人员应根据反排液的体积和阴离子浓度,确定适当的吸附剂用量,以确保有足够的吸附位点来去除阴离子;确定吸附平衡所需的时间,吸附实验将进行一定时间的搅拌或静置,以达到吸附平衡;要控制室温(约25 ℃)以保持稳定条件;根据反排液的pH值,调整吸附剂的pH值,以最大程度地提高吸附效率;进行吸附实验后,可以使用选择的阴离子吸附剂(例如Purolite A520E)对吸附模拟进行分析,表3是吸附模拟结果的数据统计表。

表3 阴离子吸附模拟结果的数据统计表
分析结果应与实验数据相对比,以验证吸附模拟的准确性和吸附剂的性能。进一步的分析可以包括讨论吸附动力学模型(如Pseudo-First-Order或Pseudo-Second-Order模型)来了解吸附速率,以及通过吸附等温线模型(如Langmuir或Freundlich模型)来评估吸附平衡。这有助于确定阴离子吸附剂的性能和适用性,为地下水污染治理提供重要信息。
4 结语
综上所述,地下水是人类生活和工业生产的重要水资源,地下水污染对环境和人类健康构成严重威胁。保护地下水资源对于可持续发展至关重要,研究区域的地质特征和水文情况对地下水污染的治理具有重要意义。将典型吸附剂应用于地下水污染防治,采用不同类型的吸附剂进行去除阳离子和阴离子污染物性能方面的实验,能够说明典型吸附剂在地下水污染防治中发挥着重要作用,可为地下水污染治理提供依据与方向。

