《原发性骨质疏松症诊疗指南(2022版)》解读
袁玲丹,宋利格
(1.同济大学附属同济医院内分泌代谢科,上海 200065; 2.同济大学医学院骨质疏松和代谢性骨病研究所,上海 200065; 3.同济大学医学院,上海 200092)
骨质疏松症(osteoporosis)是一种以骨量低下、骨组织微结构损坏,导致骨骼脆性增加,易发生骨折为特征的全身性骨病[1],按病因分类可分为原发性骨质疏松症和继发性骨质疏松症。该病最大的危害为骨质疏松性骨折,发生后导致残疾甚至死亡的风险明显增加,严重危害患者的生命健康和生活质量,给社会和家庭带来沉重的负担。目前,我国骨质疏松症及骨质疏松性骨折的发病率处于急速增长阶段,但我国居民对骨质疏松症的重视程度却远远不够,该状况将为我国防治骨质疏松带来严峻的挑战。基于我国骨质疏松症的防治现状,2022年12月,中华医学会骨质疏松和骨矿盐疾病分会制定并颁布了《原发性骨质疏松症诊疗指南(2022)》(以下简称新版指南)。新版指南在《原发性骨质疏松症诊疗指南(2017)》(以下简称2017版指南)的基础上,结合国内外研究新进展和最新国际指南共识,更新我国骨质疏松症的流行病学数据,完善骨质疏松症的发病机制,强调骨质疏松症及骨质疏松性骨折的筛查,增加抗骨质疏松症的新型药物,指导药物的序贯和联合使用,并提出根据骨折风险分层治疗策略,旨在为临床医生的诊疗工作提供切实可行的指导。本文就新指南的更新要点进行解读。
1 我国骨质疏松症的流行病学
新版指南更新了我国骨质疏松症及骨质疏松性骨折的流行病学数据。关于中国居民骨质疏松症的流行病学调查结果显示,我国50岁及以上人群中骨质疏松症患病率为19.2%,其中女性为32.1%,男性为6.9%;65岁及以上人群中骨质疏松症患病率为32%患有,其中女性高达51.6%,男性为10.7%[2]。据此,我国现有骨质疏松症患者已达9 000万人,该数据较2017版指南中估算的2006年骨质疏松症患病人数显著增加[2]。骨质疏松性骨折的发病率同样快速增长,尤其是髋部骨折,新版指南指出我国2016年髋部骨折总数较2012年增长3倍[3]。髋部骨折被称为“人生最后一次骨折”,髋部骨折1年后,致残率高达50%,致死率约为20%,因此髋部骨折是最严重的骨质疏松症骨折[4-5]。椎体骨折是最常见的骨质疏松性骨折,总体上椎体骨折患病率处于稳定趋势。而新版指南总结了全国及部分地区关于椎体骨折患病率的调查,还发现男性椎体骨折患病率与女性相当[4-5]。骨质疏松症的患病率具有显著性别差异,以女性居多,往往忽视了对男性骨质疏松症的防治,而事实证明骨质疏松症最终导致的椎体骨折并无显著性别差异,因此,新版指南强调椎体骨折的防治对男性和女性同样重要。骨质疏松性骨折不仅严重影响生命健康,还会造成巨大的医用支出,据预测,至2035年我国将花费1 320亿元用于主要脆性骨折的医疗,而至2050年相应的费用将增至1 630亿元,因此积极预防骨折的发生将极大地减轻个人、家庭及社会的负担。
目前我国骨质疏松症防治的形势严峻,面临“三高一低”的困境,即我国骨质疏松症患病率高,但我国居民对骨质疏松症的知晓率(7.4%)、诊断率(6.4%)均偏低,在脆性骨折发生后骨质疏松症的治疗率也很低(仅为30%)[2,6]。走出“三高一低”的困境,必须健全我国骨质疏松症防治管理体系,提高公众对骨质疏松症的认知程度和就医意识,通过早期筛查和识别高危人群并积极干预,以减少骨质疏松性骨折发生为目的,降低骨质疏松症及骨质疏松性骨折的流行。
2 骨质疏松症发病机制
2017版指南阐述了绝经后骨质疏松症和老年性骨质疏松症的发病机制,新版指南在此基础上新增了关于原发性骨质疏松症发病机制的研究新进展。越来越多的研究认为骨质疏松症与肠道菌群密切相关,肠道菌群紊乱造成骨免疫失衡,进一步影响骨代谢,促进骨质疏松症的发生[7-10]。细胞衰老也被认为是参与骨质疏松症的重要机制,衰老细胞分泌衰老相关表型,诱导衰老细胞形成,促进炎性衰老,破坏骨重建[11-18]。近年来,有学者在骨吸收-骨形成的二元调控理论的基础上,提出了骨血管生成-骨吸收-骨形成偶联的三元调控理论,补充和完善了骨质疏松症发病机制[19]。

3 骨质疏松症及骨质疏松性骨折筛查
多数骨质疏松症早期不易察觉,往往出现骨折等骨质疏松症并发症时才会被患者重视,对健康产生严重危害。因此新版指南更强调对骨质疏松症及骨质疏松性骨折高危人群的早期筛查,提倡早诊断,早治疗,减少骨质疏松症带来的不良后果。
新版指南与2017版指南均纳入了初步评估骨质疏松症风险工具:基于亚洲人骨质疏松症自我筛查工具(osteoporosis self-assessment tool for Asians,OSTA)和国际骨质疏松基金会(International Osteo-porosis Foundation,IOF)骨质疏松症风险一分钟测试题。需要注意的是,新版指南更新了IOF测试题。

4 骨质疏松症的辅助检查


表1 骨密度测量方法
除了基于骨密度测量的诊断方法外,临床上也可根据脆性骨折的情况进行骨质疏松症的诊断。脆性骨折是骨质疏松症的严重并发症,其中椎体骨折最为常见。X线检查仍是胸椎和腰椎脆性骨折的首选检测方法。只要发生髋部或椎体脆性骨折,即可诊断骨质疏松症,骨量减少患者(-2.5 原发性骨质疏松症的诊断不仅需要符合骨质疏松症的诊断标准,还需排除继发性骨质疏松症。影像学方面,新版指南强调了CT、MRI、核医学检查在鉴别诊断骨质疏松症与其他骨骼疾病上的价值。实验室检查方面,骨转换标志物(bone turnover markers,BTMs)也有助于原发性骨质疏松症和继发性骨质疏松症的鉴别,同时还有助于预测骨折风险、判断骨转换类型、评估药物疗效、监测治疗依从性等[29]。目前国际上没有统一的BTMs正常参考范围,经过我国学者不断研究,新版指南列出了主要骨转换生化标志参考范围,见表2[29-33]。 表2 主要骨转换生化指标参考值 抗骨质疏松药物包括骨吸收抑制剂、骨形成促进剂、双重作用药物、其他机制药物和中成药,可以有效增加骨密度,改善骨质量,降低骨折风险。骨吸收抑制剂包括双膦酸盐类药物(bisphosphonates)、RANKL单克隆抗体、降钙素(calcitonin)、雌激素(estrogens)、选择性雌激素受体调节剂。骨形成促进剂主要为甲状旁腺类似物,如特立帕肽。双重作用药物是指同时具有抑制骨吸收和促进骨形成双重作用的药物,如罗莫佐单抗(romosozumab)。新版指南纳入了更多国家药品监督管理局(NMPA)批准的新型抗骨质疏松药物,如米诺膦酸(minodronic acid)、地舒单抗(deno-sumab)、艾地骨化三醇(eldecalcitol)等。 新版指南中删除了第一代双膦酸盐类药物依替膦酸钠及氯膦酸二钠,增加了第三代双膦酸盐米诺膦酸,米诺膦酸已获得NMPA批准用于治疗绝经后骨质疏松症。与同为口服双膦酸盐类药物的阿仑膦酸钠相比,米诺膦酸的使用剂量低于阿仑膦酸钠(米诺膦酸的使用剂量为1 mg/d,阿仑膦酸钠的使用剂量为10 mg/d),因此显著减少了胃肠道不良反应的发生[40]。米诺膦酸可增加患者腰椎和髋部骨密度,降低椎体和非椎体骨折风险,但是对髋部骨折风险的影响尚不清楚。 地舒单抗是2020年6月获得NMPA批准,用于治疗高骨折风险的绝经后骨质疏松症的RNAKL抑制剂,推荐每半年皮下注射1次,60 mg/次。一项持续3年的多中心、随机、双盲、安慰剂对照临床试验显示,地舒单抗有效降低绝经后骨质疏松症患者椎体、非椎体和髋部骨折风险,继续用药并随访7年发现地舒单抗能增加腰椎和髋部骨密度[41-42]。值得注意的是,2023年2月,地舒单抗再次获得NMPA批准,用于治疗骨折高风险的男性骨质疏松症,成为中国首个用于男性骨质疏松症的抗RANKL单抗类药物。美国食品药品监督管理局(FDA)还批准地舒单抗用于糖皮质激素诱发的骨质疏松症(glucocorti-coid-induced osteoporosis,GIOP)。 艾迪骨化醇是新型活性维生素D类似物,更适用于肾功能减退、老年人及1α羟化酶缺乏或减少的患者。推荐每天口服0.5 μg或0.75 μg。艾迪骨化醇具有增加骨密度、降低椎体和非椎体骨折风险的功效,目前已批准用于绝经后骨质疏松症的治疗。相较于阿法骨化醇,研究发现即使在不额外补充维生素D或钙的情况下,艾地骨化醇更能增加腰椎、全髋和股骨颈骨密度[43]。 目前,罗莫佐单抗是唯一具有促进骨形成和抑制骨吸收双重作用的药物,具备独特的治疗优势,能有效增加骨密度,降低椎体及髋部骨折风险。2019年,FDA和欧洲药品监管局(European Medicines Agency,EMA)批准罗莫佐单抗上市,用于存在高骨折风险的绝经后女性。但目前罗莫佐单抗尚未在我国获得批准上市,仍处于Ⅲ期临床试验阶段。罗莫佐单抗总体安全性良好,但是可能会增加心肌梗死(心脏病发作)、卒中和心血管疾病死亡的风险,因此FDA对罗莫佐单抗发出了黑框警告[44]。 近年来,多个国际权威性的《原发性骨质疏松症诊疗指南》相继引入了“极高骨折风险”的概念。新版指南结合骨质疏松性骨折风险评估工具和重要危险因素,如脆性骨折史、跌倒史、低骨密度、长期使用糖皮质激素等,对“极高骨折风险”作出了定义[36]。同时,新版指南首次提出依据骨折风险分层选择治疗药物的策略,对于骨折高风险患者建议首选口服双膦酸盐,口服不耐受者可选择静脉注射唑来膦酸或皮下注射地舒单抗;对于极高骨折风险者,可选择特立帕肽、唑来膦酸、地舒单抗、罗莫佐单抗作为初始用药;而对于髋部骨折极高风险者,推荐唑来膦酸或地舒单抗。该分层治疗策略的目的是尽早识别“极高骨折风险”患者,采取积极有效的抗骨质疏松症治疗,减少骨折的发生,做到精准预防。 目前,多种抗骨质疏松症药物存在疗程限制,不能单药贯穿治疗始终,因此需要采取抗骨质疏松症药物的联合或序贯治疗,达到长期稳定骨密度的目的,同时增加药物经济学价值[55-56]。 与2017版指南相比,新版指南详细列举了序贯治疗的方案。对于地舒单抗的序贯治疗,新版指南推荐地舒单抗序贯唑来膦酸用于地舒单抗停药的患者,酌情推荐地舒单抗序贯特立帕肽用于地舒单抗使用时间过长或产生副反应的患者[57-58]。对于特立帕肽的序贯治疗,新版指南推荐特立帕肽序贯双膦酸盐类药物或地舒单抗治疗[59-60]。对于罗莫佐单抗的序贯治疗,新版指南推荐罗莫佐单抗序贯双膦酸盐类药物或地舒单抗,以达到稳定腰椎和髋部骨密度、降低骨折风险的目标[44]。尽管双膦酸盐类药物具有药物假期,但特殊情形下,仍需进行序贯治疗。对于口服双膦酸盐类药物效果不佳的高骨折风险或极高骨折风险患者、无法耐受者,新版指南推荐序贯唑来膦酸或地舒单抗治疗。与序贯唑来膦酸比较,序贯地舒单抗增加骨密度效果更显著[61-62]。同时,新版指南继续建议将维生素D与钙剂作为骨健康补充剂,在抗骨质疏松症疗程中联合应用。在抗骨质疏松症药物的联用时,不建议联合使用作用机制相同的药物,但酌情考虑特立帕肽可与唑来膦酸或地舒单抗作用机制不同的药物联用,用于骨折极高风险者[58,63]。 随着我国老龄化加剧,骨质疏松症患病率急剧增加,我国骨质疏松症防治形势逐渐严峻。新版指南结合国内外研究新进展和本国循证医学依据,制定了符合我国国情的诊疗策略。强调应重视骨质疏松性骨折,早期筛查高骨折风险和极高骨折风险患者,依据骨折风险分层予以治疗。抗骨质疏松症药物治疗,应遵循个体化和长期化原则,可采取序贯和联合治疗,避免疗程过长和不良反应发生。同时,期待完善并建立中国人群的骨折预测工具和骨密度参考数据库,验证新型抗骨质疏松药物的疗效、疗程和安全性,为未来骨质疏松症的诊疗提供可靠依据。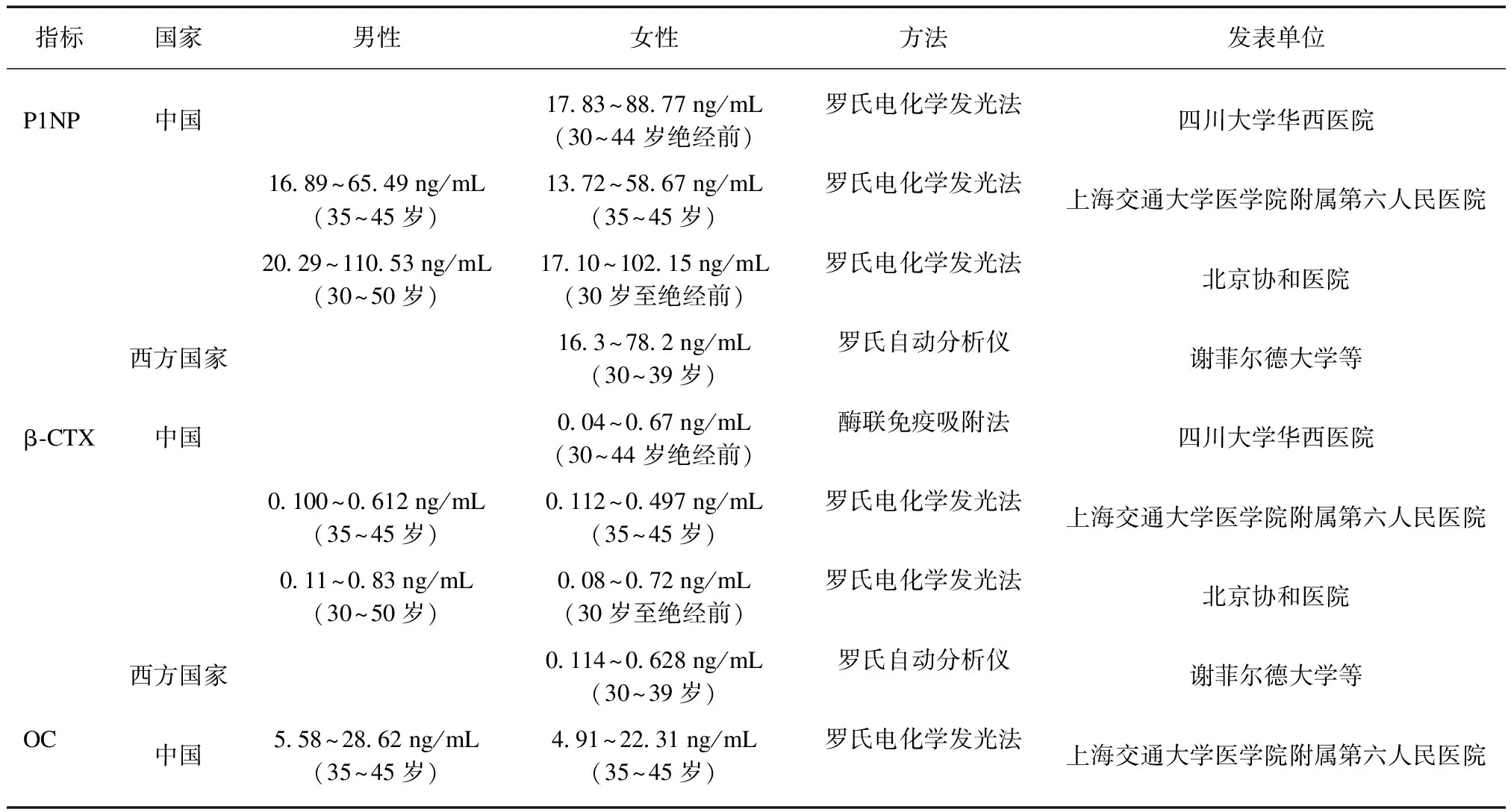
5 骨质疏松症治疗
5.1 骨健康基础补充剂

5.2 抗骨质疏松症药物
5.3 依据骨折风险分层选择药物
5.4 抗骨质疏松症药物的疗程


5.5 抗骨质疏松症药物的序贯和联合治疗
6 展 望

