氧化钙对磷石膏中可溶磷和可溶氟固化性能的影响
董万强,邓祥意*,张秋桐,史抒扬,吴 康,池汝安,2
1. 武汉工程大学资源与安全工程学院,湖北 武汉 430074;2. 湖北三峡实验室,湖北 宜昌 443007
我国磷矿资源较丰富,为磷化工产业链提供原料[1],其中大部分磷精矿用于湿法磷酸工艺,同时产生大量磷石膏工业固废[2],研究表明,每生产1 t 磷酸约产生5 t 磷石膏[3-4],磷石膏年均排放量约为8 000 万t[5]。由于我国磷石膏尚未形成大规模、高附加值的资源化利用途径,其综合利用率不足45%[6],大量磷石膏仍以露天堆存的方式处理,造成了严重的土地资源浪费及环境污染[7]。磷石膏的主要成分为CaSO4·2H2O,此外还含有少量的磷、氟、有机物等有害杂质[8-9],其中可溶磷和可溶氟易随雨水发生迁移,严重污染周边土壤和水体[10-12],因此,磷石膏中可溶磷和可溶氟的去除是解决磷石膏环境污染的有效手段,有利于实现磷石膏的综合利用[13]。
磷石膏中的磷主要来自湿法磷酸中洗涤工序未洗净的磷酸和未分解的磷灰石,根据磷元素的赋存状态可分为可溶磷、共晶磷和难溶磷,其中可溶磷主要以H3PO4、H2PO4-和HPO42-形式存在[14];磷石膏中的氟主要来自氟磷灰石的酸解,根据氟的赋存状态可分为可溶氟和难溶氟,其中可溶氟主要为NaF 和KF 的形式存在[15]。目前,磷石膏中可溶磷和可溶氟的脱除方法主要有水洗净化、石灰中和、酸浸和煅烧等工艺[16]。白有仙等[17]在固液比为1∶3 和室温条件下将磷石膏水洗3 次后,可溶磷去除率达到95%,洗涤后磷石膏中可溶磷质量分数低于0.1%;李展等[18]研究发现当磷石膏中石灰添加量为0.4%时,经过12 h 陈化后可溶磷和可溶氟的脱除率分别达到了93.27%和29.07%;彭家惠等[19]利用石灰对磷石膏陈化24 h 后,可溶磷和可溶氟脱除效果较好,但共晶磷含量未发生明显变化;付全军等[20]采用质量分数30%硫酸浸出磷石膏,在80 ℃条件下浸出45 min 后可溶磷和可溶 氟 的 脱 除 率 均 能 达 到90%;钟 雯[21]在300~500 ℃条件下煅烧磷石膏,磷石膏水溶性磷、氟的去除效率最高,去除率达60%以上,之后随着温度的继续升高去除率逐渐降低。
综上所述,磷石膏中可溶磷和可溶氟通过多次水洗和煅烧的方式去除工序较多,能耗高,成本相对较高;而酸浸虽较好地去除磷石膏中可溶磷、可溶氟和部分共晶磷,但处理后的磷石膏仍为强酸性,对周围环境造成二次污染;采用碱性物质对磷石膏进行处理,不仅可中和磷石膏的酸性,且可固化可溶磷、可溶氟和少量重金属离子,较好地避免了磷石膏中可溶态污染物的迁移,处置成本较低。本文以CaO 为固化剂,研究固化条件对磷石膏中可溶磷和可溶氟的影响,并采用响应曲面对固化工艺参数进行优化,通过溶液化学分析、沉淀产物扫描电子显微镜(scanning electron microscope,SEM)和X 射线衍射(X-ray diffractometer,XRD)分析可溶磷和可溶氟固化机理,以及沉淀产物的微观形貌和物相分析,以期为磷石膏中可溶磷和可溶氟的固化提供一定技术和理论支撑。
1 实验部分
1.1 材料与试剂
试验用磷石膏取自湖北宜昌湿法磷酸厂,X射线荧光光谱分析(X-ray fluorescence spectroscopy,XRF)结果如表1 所示,磷石膏中主要成分为硫酸钙和石英,难溶磷、共晶磷和可溶磷总质量分数为1.72%,难溶氟和可溶氟总质量分数为1.12%。磷石膏基本理化性质按照GB/T 5484—2012 石膏化学分析方法进行测定,结果见表2,其中可溶磷、可溶氟质量分数分别为0.82% 和1.02%,为磷石膏堆场的主要污染物质。磷石膏的SEM 图如图1(a)和(b)所示,磷石膏中硫酸钙晶体主要呈棒状和块状结构;磷石膏能谱如图1(c)所示,主要元素组成为Ca、S、Si、P、F,与磷石膏化学多元素分析一致;磷石膏XRD 图谱如图1(d)所示,磷石膏中主要物相为石膏和少量石英。试验用CaO 为分析纯,购于国药集团化学试剂有限公司,纯度大于96.0%,为非晶态粉末。
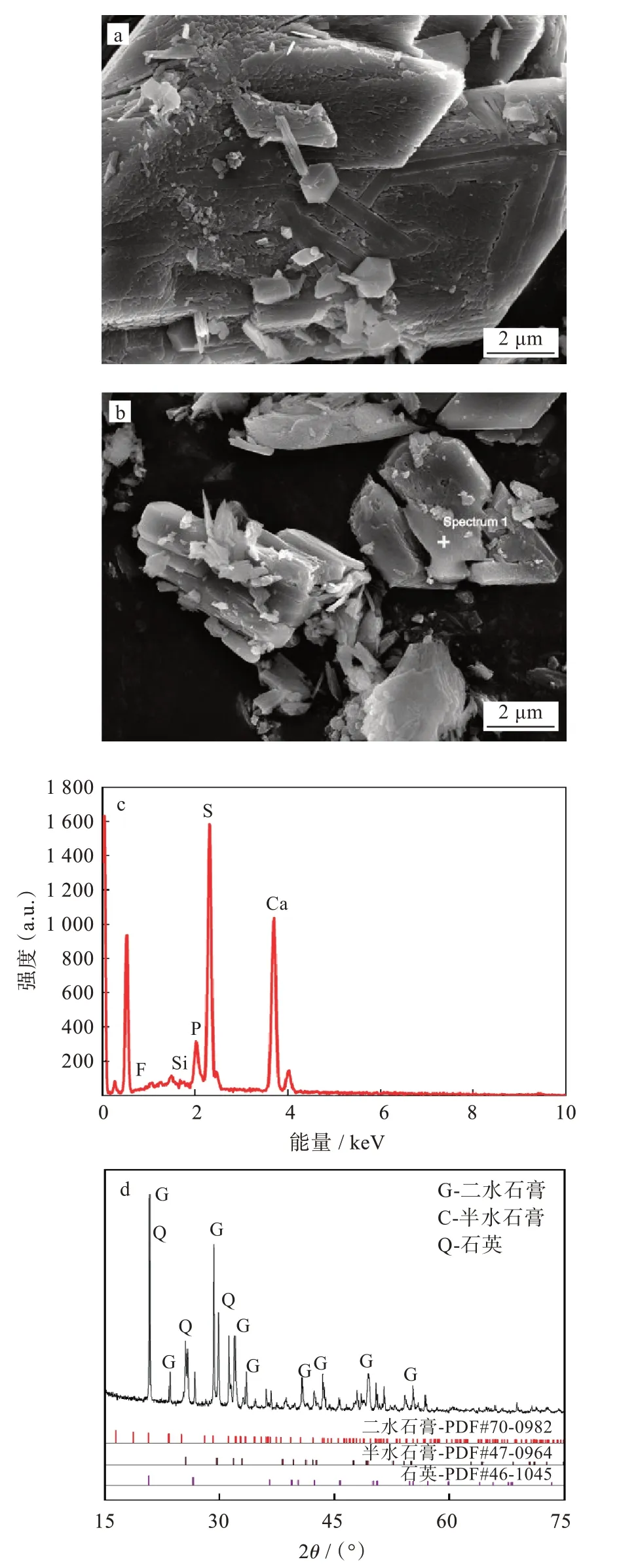
图1 磷石膏(a,b)SEM 图,(c)能谱图,(d)XRD 光谱Fig.1 SEM images(a,b),energy dispersive spectrum(c),XRD patterns(d)of phosphogypsum

表1 磷石膏化学多元素分析结果Tab.1 Results of chemical multielement analysis of phosphogypsum %

表2 磷石膏基本理化性质Tab.2 Basic physical and chemical properties of phosphogypsum
1.2 方 法
1.2.1 可溶磷和可溶氟的固化 准确称取50.00 g磷石膏于250 mL 碘量瓶中,加入一定量CaO 粉末,摇匀后加入适量蒸馏水,盖上玻璃塞,置于磁力搅拌器中于一定温度下搅拌,待反应结束后过滤,分析滤液中可溶磷和可溶氟的含量,计算可溶磷和可溶氟的固化率:
式(1)中,η为可溶磷、可溶氟的固化率,%;α为磷石膏原样中可溶磷、可溶氟的含量,mg/g;β为固化处理后滤液中可溶磷、可溶氟的含量,mg/mL;为固化试验中的液固比,mL/g。
1.2.2 检测方法 磷石膏固化后滤液中可溶磷和可溶氟的测定按照《水和废水检测分析方法(第四版)》的相关标准,可溶磷的测定采用磷钼蓝分光光度法,可溶氟的测定采用氟离子选择电极法[22]。利用酸度计测定溶液pH 值,并利用扫描电子显微镜(TESCAN MIRA LMS)对磷石膏以及磷石膏固化后的微观形貌和能谱进行分析。同时,采用X射线衍射仪(Rigaku SmartLab SE)测定磷石膏以及磷石膏固化后的物相组成变化。
2 结果与讨论
2.1 磷石膏固化影响因素
2.1.1 CaO 用量 CaO 对磷石膏可溶磷和可溶氟的固化效果影响显著,可中和磷石膏酸性,为体系提高Ca2+浓度,以便沉淀固化游离磷酸和氟离子,可溶磷和可溶氟固化反应方程式为[23]:
向磷石膏中加入适量CaO,液固比为2∶1,固化温度为30 ℃,反应时间为150 min。由图2(a)可知,随着CaO 用量(质量分数,下同)从1.0%增加到5.0%,可溶磷和可溶氟的固化率呈现先上升后趋于稳定的趋势。在相同的CaO 用量条件下,可溶氟的固化率高于可溶磷的固化率,当CaO 用量为3.0%时,可溶磷和可溶氟的固化率分别达到97.3%和98.5%。不同CaO 用量下体系pH 变化规律如图2(b)所示,随着反应的进行,CaO 逐渐溶解并中和磷石膏酸性,pH 呈逐渐增加的趋势,当CaO用量为1.0%时,体系pH 保持在3.36,可溶磷和可溶氟的固化率较低,表明CaO 用量偏低;当CaO 用量在2.0%~4.0%时,体系pH 在5.94~6.77 之间,可溶磷和可溶氟的固化率得到显著增强;当CaO 用量为5.0%时,体系pH 维持在较高水平,接近于CaO 饱和pH 值,可溶磷和可溶氟的固化率最高可达到98.1%和99.5%。根据上述分析综合考虑,选择CaO用量为3.0%。
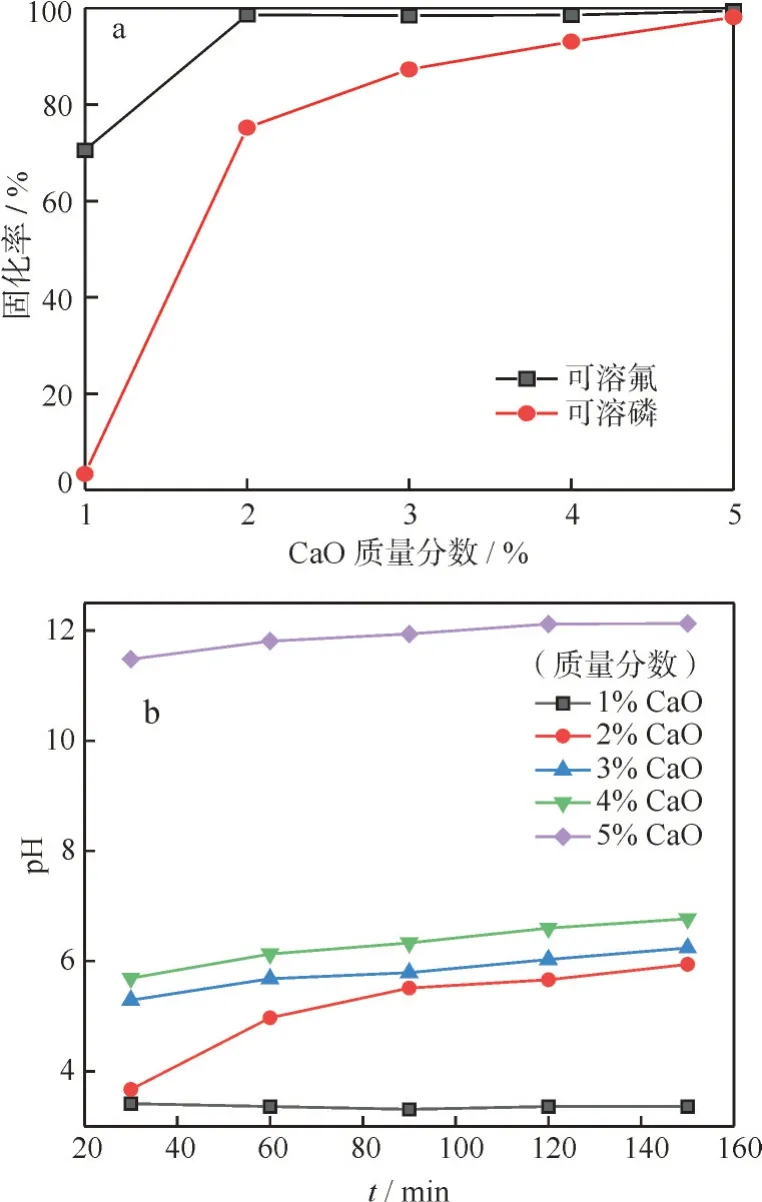
图2 (a)CaO 用量对可溶磷和可溶氟固化率的影响;(b)不同CaO 质量分数下体系pH 变化Fig.2 (a)Effects of CaO mass fraction on solidification efficiency of soluble phosphorus and fluorine;(b)Curves of pH changes with CaO mass fractions
2.1.2 液固比 在CaO 用量为3.0%,固化温度30 ℃,反应时间150 min 条件下,液固比对磷石膏中可溶磷和可溶氟的固化率的影响如图3(a)所示,随着液固比的增加,可溶磷和可溶氟的固化率逐渐下降。不同液固比下体系pH 的变化规律如图3(b)所示,相同CaO 用量和反应时间条件下,体系pH 随液固比的增加而降低。当体系液固比增加,磷 石 膏 中 可 溶 磷(PO43-、HPO42-、H2PO4-、H3PO4)、可溶氟(F-、HF 等)和H+的浓度随之降低,同时体系中CaO 的浓度亦随之降低,由式(1)和式(2)可知,当反应物浓度降低,不利于磷石膏中可溶磷和可溶氟的固化反应;但当液固比过高,磷石膏易沉积在底部,不利于机械搅拌分散,综合考虑,选取液固比为2∶1,此时磷石膏中可溶磷和可溶氟的固化率分别为97.2%和98.9%。
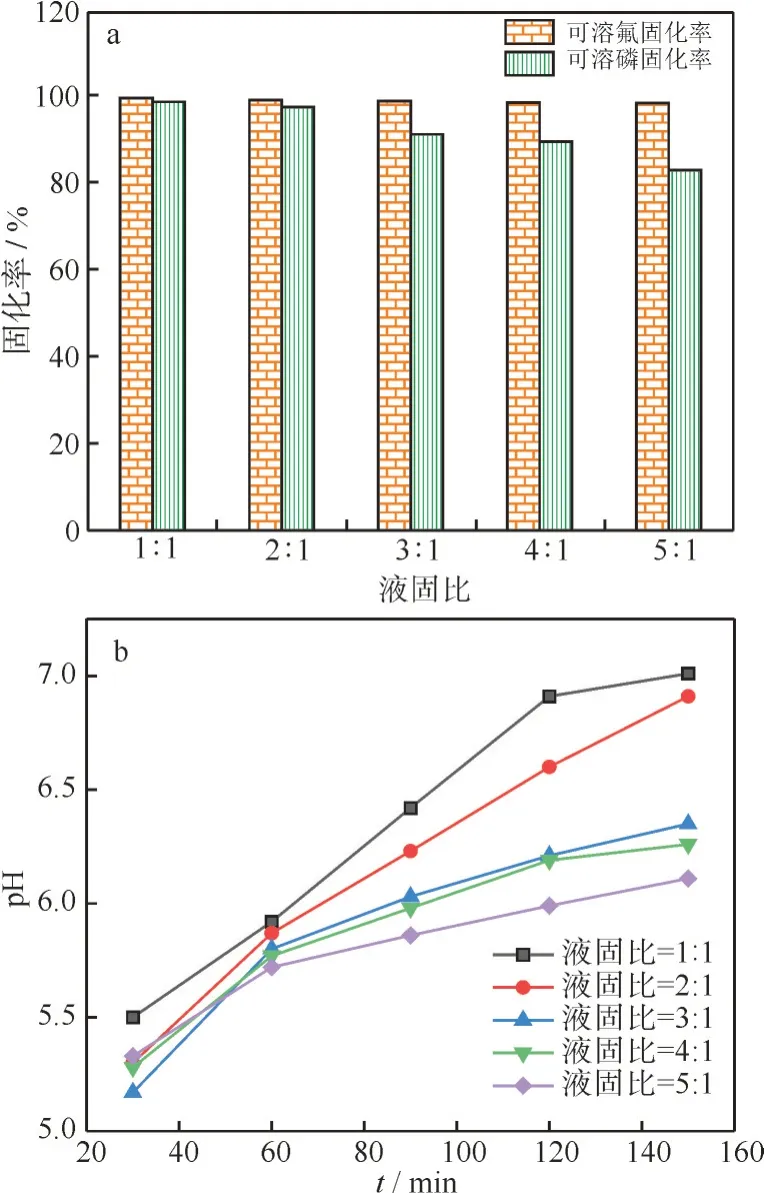
图3 (a)液固比对可溶磷和可溶氟固化率的影响;(b)不同液固比下pH 变化Fig.3 (a)Effects of liquid-solid ratio on solidification efficiency of soluble phosphorus and fluorine;(b)Curves of pH changes with liquid-solid ratios
2.1.3 温度和时间 在CaO 用量3.0%,液固比为2∶1,反应时间150 min 的条件下,温度对磷石膏中可溶磷和可溶氟的固化率的影响如图4(a)所示,随着反应温度的增加,可溶氟的固化率由99.1%增加到99.7%,可溶磷的固化率由97.2%缓慢增加至98.1%,不同温度下可溶磷和可溶氟的固化率保持在较高水平,固化率均大于97%,综合考虑成本,选择固化温度为30 ℃。反应时间对磷石膏中可溶磷和可溶氟的固化率的影响如图4(b)所示,随着反应时间增加,可溶磷的固化率逐渐增加,反应150 min 时达到最高值,为97.9%;可溶氟的固化反应较为迅速,反应30 min 内即可达到较高固化效果,随后保持相对稳定,可溶氟的固化率均在99%以上,反应150 min 可溶氟固化率为98.6%。
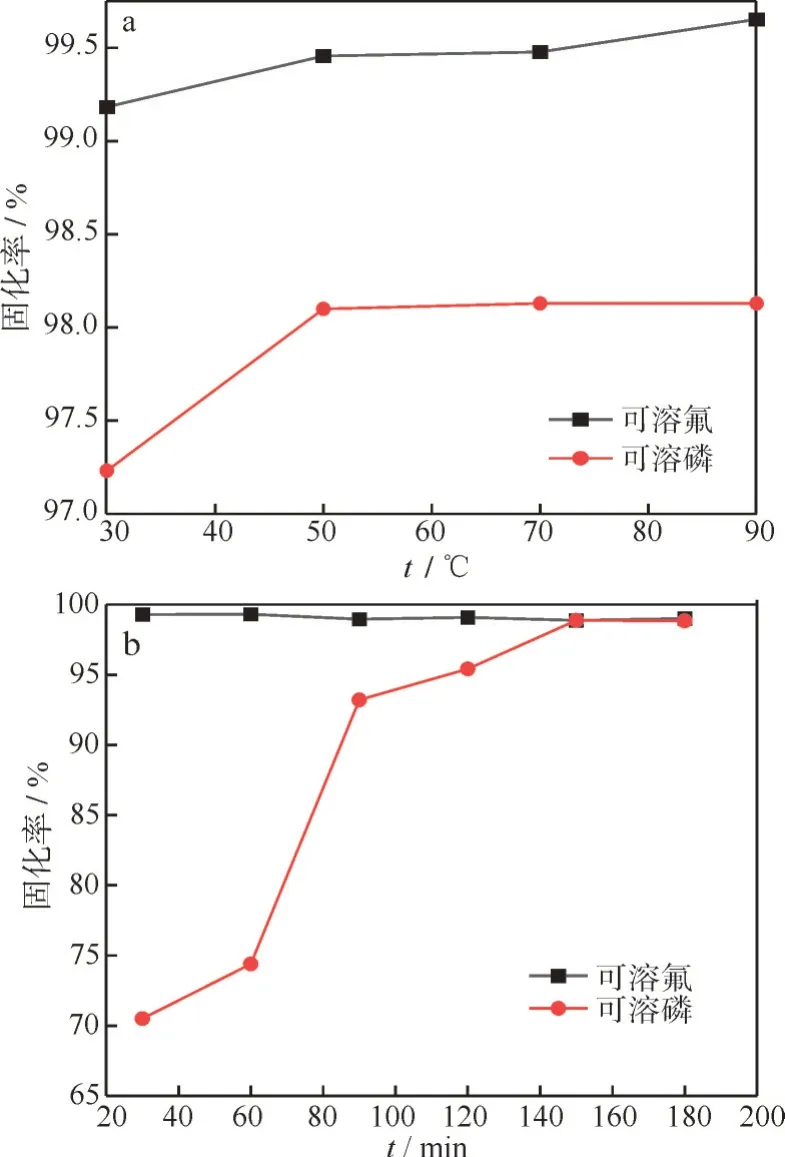
图4 温度(a)和时间(b)对磷石膏可溶磷、可溶氟固化率的影响Fig.4 Effects of temperature(a)and time(b)on solidification efficiency of soluble phosphorus and fluorine in phosphogypsum
2.2 可溶磷和可溶氟固化工艺参数优化
相同试验条件下,可溶氟的固化率均大于可溶磷的固化率,故将可溶磷固化率为响应值,运用Box-Behnken 设计原理进行响应曲面优化[24],以CaO 用量、液固比及反应时间为考察因素,3 因素3水平响应面试验设计表见表3。
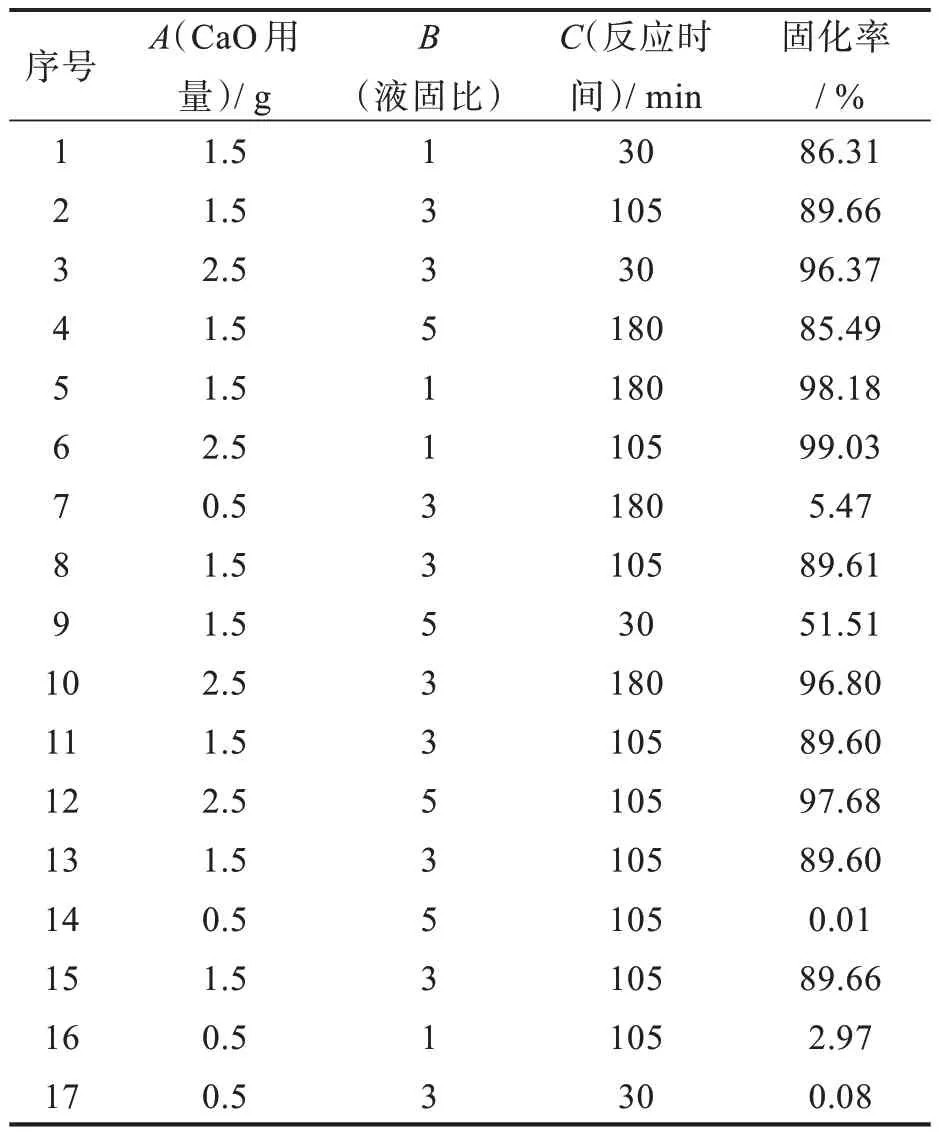
表3 响应面分析试验设计表Tab.3 Response surface analysis scheme
运用Design expert 软件对表3 中的数据进行拟合,拟合得到回归方程:
对上述回归方程进行方差分析,其结果如表4所示。

表4 响应面试验结果方差分析Tab.4 Variance analysis of response surface experiments results
由表4 可知,响应曲面模型F值为43.62,P<0.000 1,表明回归方程显著,拟合度较好;调整决定系数R2adj=0.960 0,表明可溶磷固化率的变化有96.00%来自CaO 用量、液固比和反应时间,对可溶磷的固化具有显著影响。方差分析结果表明,此3 因素对可溶磷的固化率影响的主次顺序为:CaO用量>液固比>反应时间,CaO 的用量对可溶磷的固化占主导作用。
等高线若呈椭圆形表示两因素之间交互作用显著,呈圆形则表示两因素交互作用不显著,3 因素彼此交互作用下的等高线和响应曲面如图5~图7所示,3因素两两交互作用均呈椭圆形,交互作用显著。由图5 可知,当反应时间不变,CaO 用量在3.0%~4.0%之间,液固比在(1∶1)~(4∶1)之间时可溶磷的固化率可取极大值;由图6 可知,当液固比不变,CaO 用量在3.0%~4.0%,反应时间在67.5~180 min 时可取极大值;由图7 可知,当CaO 用量不变,液固比在(1∶1)~(4∶1)之间,反应时间在67.5~180 min 时可取极大值。综上,可溶磷固化率最优时3 因素的取值范围为:CaO 用量为3.0%~4.0%,液固比为(1∶1)~(4∶1),反应时间为67.5~180.0 min。
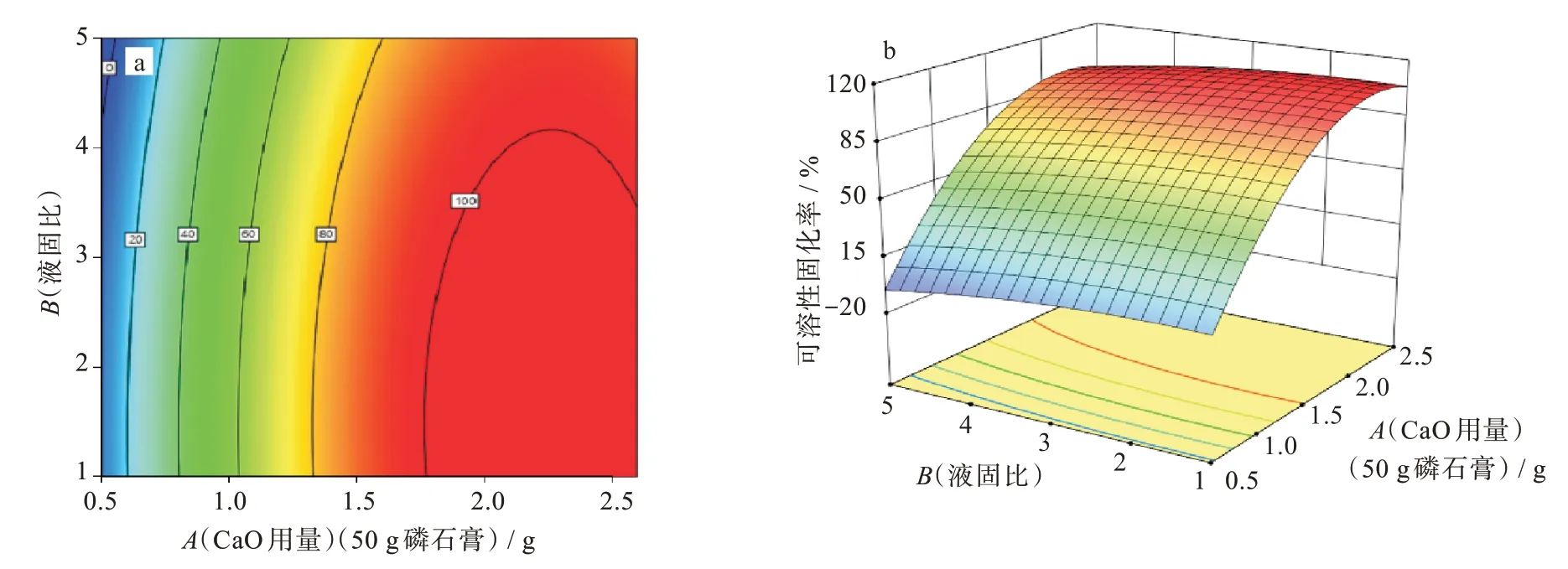
图5 CaO 用量和液固比的等高线及响应曲面Fig.5 Contour polt and response surface curves of CaO dosage and liquid-solid ratio
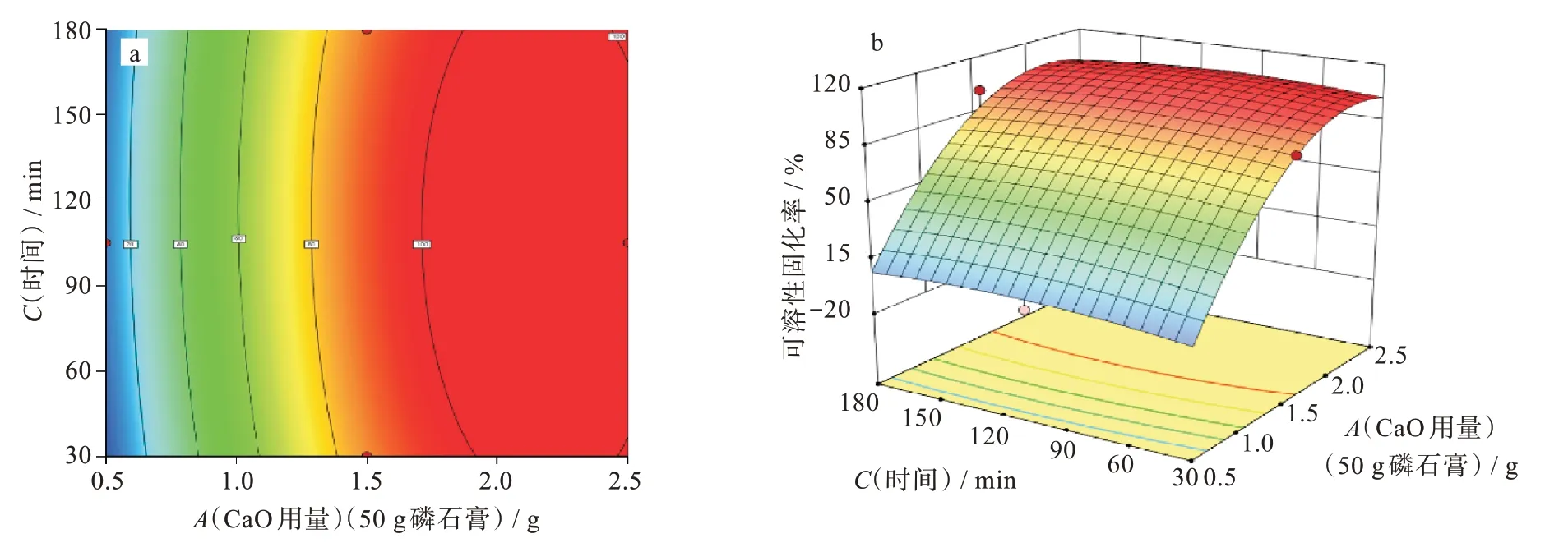
图6 CaO 用量和反应时间的等高线及响应曲面Fig.6 Contour plot and response surface curves of CaO dosage and reaction time
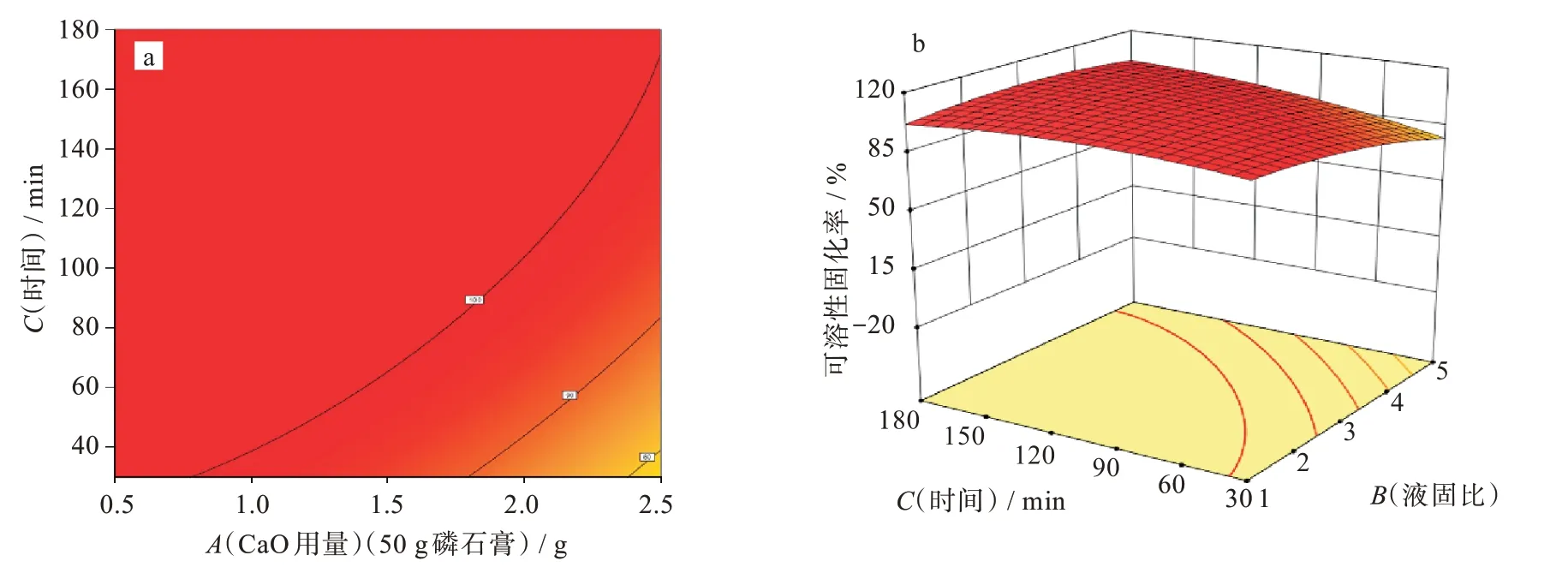
图7 液固比和反应时间的等高线及响应曲面Fig.7 Contour plot and response surface curves of liquid-solid ratio and reaction time
通过软件优化得到可溶磷固化的工艺参数为:CaO 用量3.30%,液固比1.90,反应时间为110 min,可溶磷固化率可达98.5%。在此条件下重复3 次进行可溶磷试验,可溶磷固化率分别为98.2%、99.2%和98.3%,取平均值为98.6%;可溶氟的固化率分别为99.5%、99.9%和99.6%,取平均值为99.7%,表明磷石膏中可溶磷和可溶氟均具有较好固化效果。
2.3 可溶磷和可溶氟固化机理
2.3.1 可溶磷和可溶氟的赋存状态 当CaO 加入磷石膏后,体系pH 升高并溶出部分Ca2+,磷石膏中可溶磷和可溶氟与Ca2+发生反应,溶液中可溶磷和可溶氟可能参与的反应如式(4)~式(10)所示:
当磷石膏固化反应液固比为1.90 时,磷石膏中的可溶磷(以PO43-计)和可溶氟(以F-计)的浓度约为0.06 mol/L 和0.28 mol/L,假设加入CaO 后体系中溶出的Ca2+足以使可溶磷和可溶氟沉淀,取Ca2+浓度为0.14 mol/L,根据式(4)~式(10)中化学反应及其平衡常数,绘制PO43-和F-在不同pH 下的赋存形式,如图8 所示。由图8(a)可知,在pH<3.5 的酸性环境中,可溶磷主要以CaH2PO4+、H2PO4-和H3PO4的形式存在,当3.5<pH<5.2 时,可溶磷主要以HPO4-形式与Ca2+结合形成CaHPO4·2H2O 沉淀,当pH>5.2 时,主要以Ca5(PO4)3OH 沉淀物的形式存在。由图8(b)可知,在pH<2.0 的酸性体系下,少量F-以HF 的形式存在,当pH>2.0,体系中的F-全部与Ca2+发生反应,生成CaF2沉淀。
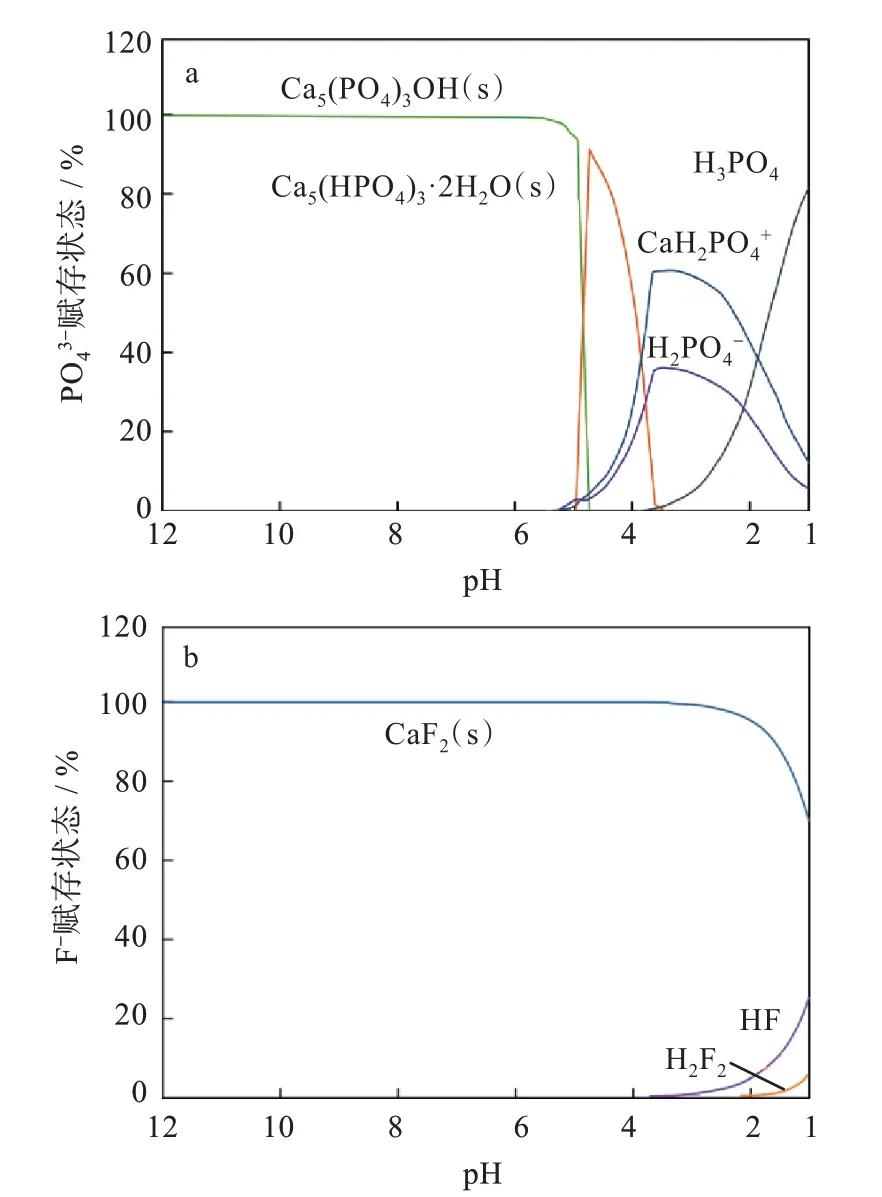
图8 可溶磷和可溶氟不同pH 下的赋存状态Fig.8 Occurrence state of soluble phosphorus and soluble fluorine at different pHs
当液固比为1.90 时,溶液pH>2.0,由溶液化学分析可知,添加CaO 所溶出的Ca2+优先与F-发生沉淀反应,随着pH 值继续升高至3.5,溶液中的Ca2+与可溶磷反应,开始析出CaHPO4·2H2O 沉淀。溶液化学分析结果表明,磷石膏中可溶氟发生固化时pH 更低,可溶氟与Ca2+固化反应优先发生,这与图2(a)和图4(b)中的研究结果相符。
2.3.2 固化产物微观结构及物相分析 磷石膏在液固比为1.90 条件下得到水洗液,固液分离后得到的液体中的可溶磷和可溶氟经CaO 沉淀得到的沉淀产物见图9。
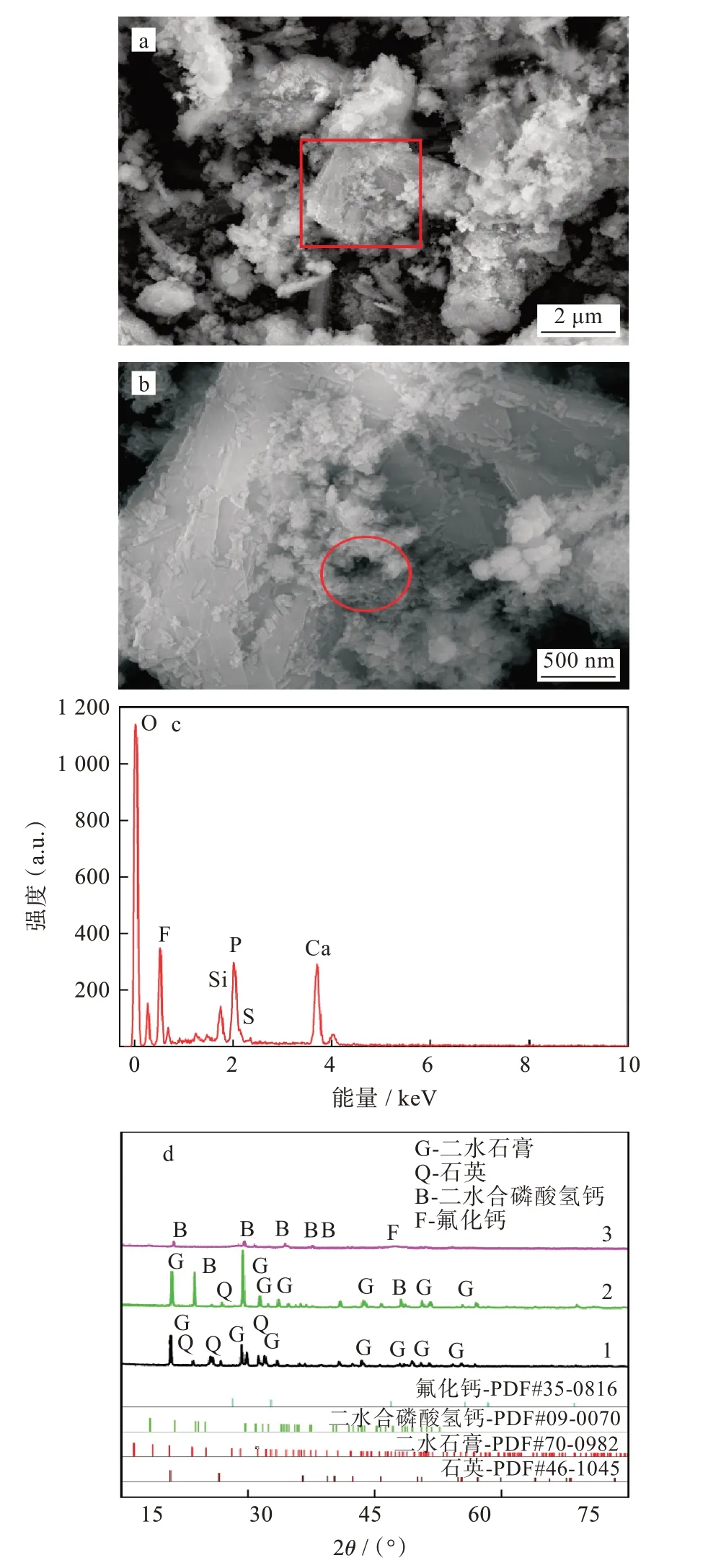
图9 磷石膏水洗-固化产物SEM 图(a,b),能谱(c),XRD 图谱(d)Fig.9 SEM images(a,b),energy dispersive spectrum(c),and XRD patterns(d)of solidification product in phosphogypsum washing solution
其微观结构如图9(a)和图9(b)所示,水洗液固化产物主要为大小不一的块状结构,表面附着结构松散的絮状结构,高倍镜下显示,絮状颗粒由细小的棒状结构组成,可能为可溶磷和可溶氟固化后形成的结晶体;固化产物EDS 能谱如图9(c)所示,固化产物主要为Ca、P、F、Si 和S 等元素组成,表明磷石膏中的可溶磷和可溶氟可与CaO 反应生成固相产物;磷石膏原样、磷石膏固化产物以及水洗-固化产物的XRD 图谱分别对应于图9(d)中1、2、3 曲线,对比图9(d)中1 和2 曲线可知,磷石膏中残余的SO42-和可溶磷经CaO 固化后主要形成透钙磷石(CaHPO4·2H2O)和二水石膏(CaSO4·2H2O),衍射峰明显增强;图9(d)中3 曲线表明,水洗-固化产物主要为透钙磷石(CaHPO4·2H2O)和二水石膏(CaSO4·2H2O),CaF2的XRD 衍射峰较弱,可溶氟主要以CaF2形式存在。
3 结 论
(1)磷石膏堆场中的可溶磷和可溶氟可随水体迁移,对周围生态环境造成一定危害。采用CaO 对磷石膏中可溶磷和可溶氟进行固化处理,在CaO 质量分数为3.0%,液固比为2.0,固化温度30 ℃,反应时间150 min 的条件下,可溶磷和可溶氟的固化率分别为97.2%和98.6%。
(2)利用响应曲面对可溶磷和可溶氟的固化进行工艺参数优化,3 因素对可溶磷的固化率影响的主次顺序为:CaO 用量>液固比>反应时间,其中CaO 的用量占主导作用,各因素存在一定交互作用,优化条件下可溶磷和可溶氟的固化率可达98.6%和99.7%。
(3)固化过程中可溶氟优先可溶磷生成沉淀,固化沉淀物主要呈块状结构,表面附着细小晶体颗粒,可溶磷主要以CaHPO4·2H2O 的形式析出,可溶氟则主要生成CaF2。

