六种嘧啶甲酸乙酯类化合物的合成及1H-NMR波谱分析
王新兵 董雯雯 顾承志 王航宇

摘要:目的 研究合成出的嘧啶甲酸乙酯类化合物的1H-NMR图谱,确证其结构并分析图谱规律;方法 经Biginelli缩合反应所得六种化合物,测定的1H -NMR图谱分别与计算机分析软件模拟结果及文献值相对照,比较各质子在图谱中的化学位移;结果 丰富了的波谱数据,找出并检定了相关化合物1H -NMR图谱出峰顺序和规律,并定性确证了化合物;结论 合成工艺可行且结构为预设化合物。
关键词:Biginelli缩合反应;氢核磁共振;合成;结构鉴定
中图分类号:中图分类号R914.5文献标志码:A文献标识码
Synthesis and1H-NMR spectral analysis of six pyrimidine ethyl formates
WANG Xinbing1,DONG Wenwen1,GU Chengzhi2,WANG Hangyu1*
(1 School of Pharmacy, Shihezi University,Shihezi, Xinjiang 832002, China;2 School of Chemical Engineering, Shihezi University,Shihezi, Xinjiang 832000,China)
Abstract: Objective 1H-NMR spectra of pyrimidine formic acid ethyl ester compounds were studied, and their structures were confirmed and analyzed. Methods Six compounds were obtained by Biginelli condensation reaction. The1H-NMR spectra measured were compared with the simulation results of computer analysis software and literature values respectively, and the chemical shifts of protons in the spectra were compared. Results With abundant spectral data, the1H-NMR peak sequence and regularity of related compounds were found and verified, and the compounds were qualitatively confirmed. Conclusion The synthetic process is feasible and the structure is the presupposition compound.
Key words: Biginelli condensation reaction;hydrogen nuclear magnetic resonance;synthesis;structural identification
1893年,Biginelli 首次报道了由芳香醛、乙酰乙酸乙酯和脲在催化剂浓盐酸的条件下经过缩合反应得到嘧啶甲酯类衍生物,其结构为嘧啶环4-苯取代的 3,4-二氢嘧啶-2-酮(英文简称:DHPM),其结构通式和编号(图1),此后这一合成方法被称为 Biginelli 反应[1]。在上世纪八十年代以后,由于发现此类化合物有广泛而实用的多种生物活性,如心血管方面、抗菌、抗病毒、消炎、抗肿瘤,抗滤过性病原体等[2-6]。因此,对Biginelli反应的研究引起了研究人员更多的关注,在合成条件和方法方面有很多文献报道,在缩短反应时间、提高产率、实现绿色化学、减少污染等方面有了很多可参考的工艺[7-18]。
本研究的主旨在于研讨该类化合物的氢核磁共振图谱的规律,参考了文献及早期研究的工艺条件,设计出6种具有典型取代特点的嘧啶甲酸乙酯类化合物,通过理论和文献研究,合成采用了后来证明可行的以硼酸为催化剂,甲苯为溶剂的合成条件,合成的化合物进行1H-NMR谱图研究和结构定性分析,通过对比实测数据与文献及计算机程序chemoffice2006模拟的结果,分析其规律,在丰富该类化合物结构种类的同时,得出适用的波谱定性数据的结论,并希望通过后续的碳核磁共振图谱、二维核磁共振及量子化学计算分析等研究,丰富结构研究相关数据,另外,预期后续还准备进行相关活性研究,为能优选出疗效较好、活性更佳的化合物做出努力。
1 材料与方法
1.1 材料
NMR使用Bruker 300 Uhrashield型核磁共振仪,测定溶剂为色谱纯的氘代二甲基亚砜,TMS为内标;试剂均为国产分析纯试剂,熔点测定使用WRS-2 型熔点测定仪(上海)。
1.2 方法
1.2.1 合成路线和方法
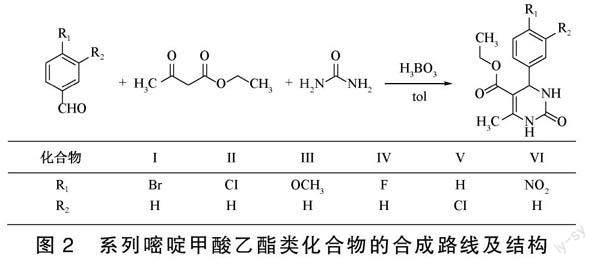
该类化合物的合成路线及各化合物结构见图2。
合成方法和处理以目标化合物I为例,在50 mL三颈烧瓶中加入20 mmol的对溴苯甲醛、20 mmol的乙酰乙酸乙酯、30 mmol的尿素和3 mmol的硼酸、25 mL甲苯,在115℃下油浴加熱,搅拌回流4 h。后将三颈烧瓶放在盛有冰水混合物的油浴锅中冷却10 min,产物析出,过滤得到的粗产品,用少量乙醇洗涤2~3次后滤干,并用95%乙醇重结晶,待干燥后进一步用硅胶进行柱层析(脱剂为乙酸乙酯-正己烷体积比为 10∶90 ),反应及柱层析过程监测,使用硅胶GF254薄层层析板结合层析后紫外灯254nm下显色观察,展开条件同柱层析,柱层析收集液蒸干得产物。
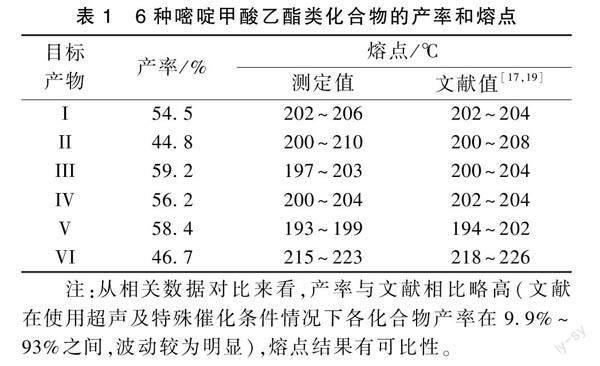
化合物II-VI的合成,均采用不同取代方式的相應芳醛,以相同的物料配比、反应条件和后处理方式,分别得到产物。各化合物产率和熔点见表1。
1.2.2 文献值
依据文献[19],得出了与合成化合物结构相同的部分氢谱数据(3组)。
1.2.3 电脑模拟计算
在电脑中安装wps office 2020 及chemoffice2006程序,使用chemoffice2006程序组中的chemdraw ultra 10.0程序,将相关化合物结构绘制后,模拟分析出各化合物氢核磁共振图谱和数据,并将模拟图和数据拷贝到wps office 2020中。
2 结果
2.1 嘧啶甲酸乙酯
根据设计的合成路线,得到了6个化合物,见图2。
2.2 所合成嘧啶甲酸乙酯氢核磁共振数据
将合成所得化合物实测氢谱汇总,见表2。
其中,由于化合物II和V的结构为同分异构体,且II和其他非V化合物均为苯环取代为对位的类似情况,故将所得波谱图罗列见图3,供后文讨论、分析。
另外,分析后确认化合物II图谱中低场端缺失了谱线,为补充图谱化学位移情况,以及分析结构中B环上有吸电基或供电基取代后谱图变化趋势,亦对比罗列出化合物III和VI的氢谱见图4。
2.3 计算机模拟嘧啶甲酸乙酯类化合物氢核磁共振数据
将合成各化合物结构用chemdraw ultra 10.0程序绘制,经程序模拟推算,得出图谱数据(图5)。
3 讨论
从实测图谱(表3、图3、图4)可以看出,合成出化合物的核磁共振氢谱的出峰位置、积分关系和偶合情况与设计的目标化合物结构可以一一对应,符合结构应有的化学环境特征,且图谱中基本没有杂质或干扰谱线,可以用图谱和数据确证化合物的结构。
将所测得数据分别与文献[19]中相同化合物(II、III和VI)图谱数据、计算机模拟所得数据汇总,得出了以下对照表(表3),可以分A环、B环和乙氧基三部分出峰情况进行讨论。
3.1 A环
总体来看,偏差较大的是模拟数据在1-NH、3-NH的结果,从计算机模拟图(图5)中以红色显示也表明其相对会有大的误差;3组数据在A环4-H和7-CH3的数据上误差都较小,总体文献值和实测值偏差较小,更具有可比性;实测值与文献结果对比说明,无论B环上如何取代,A环上1-NH、3-NH均在9.1-9.3 ppm和7.6~8.2 ppm之间,4-H均在5.1 ppm左右,7-甲基H在2.2 ppm左右。
3.2 B环
3组数据之间的误差都较小,该环数据在7.1~8.3 ppm之间,3组对应数据的差值为均小于0.33ppm,偶合关系亦合理;除了化合物V为间位取代有些特殊,其他化合物图谱符合对位双取代的谱型特点;实测值需要在细致分析具体多重峰裂峰情况后,依据规律选用多重峰几何中心位置,确定各氢的化学位移;从图3的分析表明,在各化合物呈现对位或间位取代变化后,峰形有所不同;从图4的分析表明,呈现对位取代时,9和13、10和12会分别出现化学环境相同情况,且取代基为吸电基,9和13化学位移小于10和12位,而若为推电基(如化合物III),则结果变为9和13化学位移大于10和12位。
3.3 乙氧基
A环上取代的乙氧基部分的三组对比数据之间的误差都较小,3组对应数据的差值均小于0.27 ppm;15-OCH2均在3.9~4.2 ppm之间、16-CH3均在1.0~1.3 ppm之间,实测数据与模拟值的差值较小,也都与计算机模拟结果相符,一一对应。
4 结论
本实验在文献合成路线的基础上进行了改良及优化,得到丰富结构中苯环取代变化类型的嘧啶甲酸乙酯类系列衍生物。通过参考计算机软件Chemdraw程序在氢谱的模拟结果和部分文献中可找到的参考值,进行合成目标化合物的实测图谱出峰规律和化学位移数值的探讨,明确了相应的谱线归属和规律,确定了化合物结构。
从整体分析过程及结果来分析,在进行氢核磁共振图谱研究时,当某种类型化合物结构和谱图特征对应情况不明确的前提下,研究者以计算机模拟为先导,预测出峰的大致排布顺序及组数等情况的研究思路,在进行特殊类型化合物的核磁共振氢谱解析工作中是可行的;同时,罗列的数据和图表也充分证明了此实验设计及操作方法步骤的合理性。相关的嘧啶甲酸乙酯类衍生物的图谱特征,如果能通过对照碳核磁共振、红外和质谱数据,以及使用其他光谱手段(如:二维核磁、x-晶体衍射技术)或量子化学的分析计算,来进一步测定和判断其更详细的结构信息,应能更好的解析结构和研究此类化合物,完善相应的结构定性信息。
嘧啶甲酸乙酯类制备方法和药效研究相关报道很多,这类化合物具有较高潜在应用价值,本文侧重于波谱数据的分析和讨论,相关化合物后续的结构设计合成、波谱图谱性质和活性分析,还需继续研究发现。
参考文献(References)
[1]BIGINELLI P.Synthesis of 3,4-dihydropyimidin-2(1H)-ones[J]. Chimica Italiana, 1893,23: 360-366.
[2]王喜存, 陈辉, 朱政, 等. 钯催化3,4-二氢嘧啶-2-硫酮C2位功能化衍生物的合成[J]. 西北师范大学学报 (自然科学版), 2020, 56 (4): 62-70.
WANG X C, CHEN H, ZHU Z, et al. Palladium catalyzed synthesis of C2 functional derivatives of 3,4-dihydropyrimidine-2-thione[J]. Journal of Northwest Normal University (Natural Science Edition), 2020,56 (4): 62-70.
[3]谢嘉霖, 彭化南, 叶红德. 6-甲基-4-(4-甲氧酰基苯基)-5-甲氧羰基-3,4-二氢嘧啶-2-酮的合成及与牛血清白蛋白的相互作用[J].应用化工, 2015, 44(7): 1285-1289.
XIE J L, PENG H N, YE H D. Synthesis of 6-methyl-4-(4-methoxyphenyl)-5-methoxycarbonyl-3,4-dihydropyrimidin-2-one and its interaction with bovine serum albumin[J]. Applied Chemistry,2015, 44 (7): 1285-1289.
[4]王浩貴,费莎,段晓晓, 等. 合成3,4-二氢嘧啶-2-酮衍生物的研究进展[J].合成技术及应用,2015,1(2): 24-28.
WANG H G, FEI S, DUAN X X, et al. Research progress in the synthesis of 3,4-dihydropyrimidin-2-one derivatives[J]. Synthesis Technology and Application, 2015, 1(2): 24-28.
[5]饶红红,权正军,白林, 等. 对映纯3,4-二氢嘧啶酮衍生物的合成研究进展[J]. 有机化学,2016, 36(2): 283-296.
RAO H H, QUAN Z J, BAI L, et al. Progress in the synthesis of enantiopure 3,4-dihydropyrimidinone derivatives[J]. Organic Chemistry, 2016,36(2): 283-296.
[6]向诗银,杨水金.3,4-二氢嘧啶-2-酮衍生物合成研究进展[J].精细石油化工进展,2014,15(1):53-55.
XIANG S Y, YANG S J. Research progress in the synthesis of 3,4-dihydropyrimidin- 2-one Derivatives[J]. Progress in Fine Petrochemical Industry, 2014,15(1): 53-55.
[7]权正军. 3,4-二氢嘧啶-2-酮及其衍生物的合成研究[D]. 兰州:西北师范大学, 2007.
QUAN Z J. Synthesis of 3,4-dihydropyrimidin- 2-one and its derivatives[D]. Northwest Normal University, 2007.
[8]宋志国, 赵润秋, 赵爽, 等. “一锅法”绿色合成N1-取代的3,4-二氢嘧啶酮衍生物[J]. 化学研究与应用, 2020, 32(9): 1731-1736.
SONG Z G, ZHAO R Q, ZHAO S, et al. “One pot”green synthesis of N1 substituted 3,4-dihydropyrimidinone derivatives[J]. Chemical Research and Application, 2020,32(9): 1731-1736.
[9]尹晓刚, 吴小云, 王野, 等. 超声法合成3,4-二氢嘧啶- 2(1H)-酮衍生物[J].合成化学,2016, 24(8): 684-688.
YIN X G,WU X Y,WANG Y, et al. Synthesis of 3, 4-dihydropyrimidine-2(1H)-one derivatives by ultrasonic method[J]. Synthetic Chemistry, 2016, 24(8): 684-688.
[10]腾召一,吴小云,尹晓刚.低共熔溶剂中 3,4-二氢嘧啶-2(1H)-酮衍生物的绿色合成[J].山东化工,2018, 47(22):21- 22.
TENG Z Y, WU X Y, YIN X G, Green synthesis of 3, 4- dihydropyrimidine- 2(1H)-one derivatives in low eutectic solvent[J]. Shandong Chemical Industry, 2018, 47(22): 21-22.
[11]赵雯辛,黄孟君,李胜男,等. SnCl2@MNPs催化Biginelli反应一锅法合成3,4-二氢嘧啶-2-酮衍生物[J].有机化学,2021,41(7):2743-2749.
ZHAO W X, HUANG M J, LI S N, et al. SnCl2@MNPs one pot synthesis of 3,4- dihydropyrimidin- 2-one derivatives by catalytic Biginelli reaction[J]. Organic Chemistry, 2021,41(7): 2743-2749.
[12]蒋卫华,滕巧巧,孟启,等. 树脂D001×7绿色催化Biginelli反应一锅合成3, 4-二氢嘧啶- 2-酮类化合物的研究[J]. 现代化工, 2020, 40(5): 90-94.
JIANG W H, TENG Q Q, MENG Q, et al. Study on one pot synthesis of Resin D001×7 3,4-dihydropyrimidine-2-one compounds by green catalytic Biginelli reaction[J]. Modern Chemical Industry, 2020, 40(5): 90-94.
[13]廖以人,陽志高,尹笃林. 新型椰壳炭固体磺酸催化3,4-二氢嘧啶-2(1H)-酮衍生物的合成[J]. 广东化工, 2015, 42(11): 96-97.
LIAO Y R,YANG Z G, YIN D L. Synthesis of 3, 4-dihydropyrimidine-2(1H)-one derivatives catalyzed by new coconut shell carbon solid sulfonic acid[J]. Guangdong Chemical Industry, 2015, 42(11): 96-97.
[14]刘烨. 3,4-二氢嘧啶-2(1H)-酮类化合物的设计、合成及活性评价[D]. 烟台:烟台大学, 2019.
LIU Y. Design, Synthesis and activity evaluation of 3,4-dihydropyrimidine- 2(1H)-ketone compounds[D]. Yantai University, 2019.
[15]徐玉林,龚文朋,杨水金.二氧化硅负载磷钨酸催化合成3,4-二氢嘧啶- 2(1H)-酮衍生物[J]. 应用化学, 2014, 31(10): 1203-1209.
XU Y L, GONG W M, YANG S J. Synthesis of 3,4-dihydropyrimidine-2(1H)-one derivatives catalyzed by phosphotungstic acid supported on silica[J]. Applied Chemistry, 2014, 31(10): 1203-1209.
[16]李丽, 刘庆俭, 隋雪燕. 微波促进下的Biginelli反应:5-(4-甲基苯甲酰基)-3,4-二氢嘧啶-2酮(硫酮)类衍生物的无溶剂合成[J]. 山东化工,2014,43(4): 6-7.
LI L, LIU Q J, SUI X Y. Microwave assisted Biginelli reaction: solvent-free synthesis of 5- (4-methylbenzoyl)-3, 4-dihydropyrimidine- 2- one(thione) derivatives[J]. Shandong Chemical Industry, 2014, 43(4): 6-7.
[17]杨志翔, 王金娟, 王文琛, 等. 微波辅助下联二萘酚酰胺催化剂在Biginelli反应中的应用[J]. 贵州师范大学学报(自然科学版), 2018, 36(5): 85-89.
YANG Z X, WANG J J, WANG W C, et al. Microwave assisted application of binaphthol amide catalyst in Biginelli reaction[J]. Journal of Guizhou Normal University(Natural Science Edition), 2018, 36(5): 85-89.
[18]李佰林,袁陈缘,蔡丽莎, 等. 离子液体催化微波促进下的3,4-二氢嘧啶-2-酮衍生物的无溶剂合成[J]. 化学工程师, 2016, 30(9): 10-13.
LI B L, YUAN C Y, CAI L S. et al. Microwave assisted solvent- free synthesis of 3,4-dihydropyrimidin-2-one derivatives catalyzed by ionic liquid[J]. Chemical Engineer, 2016, 30(9): 10-13.
[19]邓伟,刘晓玲,毛雪春, 等. 聚乙二醇负载苯磺酸催化Biginelli反应合成3,4-二氢嘧啶-2-酮衍生物的研究[J]. 江西师范大学学报(自然科学版), 2015, 39(1): 88-93.
DENG W, LIU X L, MAO X C,et al. Study on synthesis of 3, 4-dihydropyrimidin- 2-one derivatives by Biginelli reaction catalyzed by polyethylene glycol supported benzenesulfonic acid[J]. Journal of Jiangxi Normal University(Natural Science Edition), 2015, 39(1): 88-93.
(责任编辑:编辑唐慧)
收稿日期:中文收稿日期2022-10-12
基金项目:国家自然科学基金项目(81560566)
作者简介:王新兵(1975—),男,讲师,从事药物化学、药物分析及天然产物研究。
*通信作者:王航宇(1968—)男,教授,从事中药和天然药物研究,e-mail:49425601@qq.com。

