脑源定位技术的精度评估及其在实际中的应用*
朱千韵 张治国 梁 臻 张 力 李琳玲 张绍荣 黄 淦**
(1)深圳大学医学部生物医学工程学院,深圳 518037;2)广东省生物医学信息检测与超声成像重点实验室,深圳 518037;3)哈尔滨工业大学(深圳)计算机科学与技术学院,深圳 518055)
脑电图(electroencephalogram,EEG)和脑磁图(magnetoencephalography,MEG)是大脑生理信号的非侵入式脑功能性神经影像技术,在脑科学研究中具有重要科学意义和临床价值。脑源定位技术通过EEG/MEG信号分析大脑内部不同神经元活动的详细时空功能成像,是神经科学和心理学研究的有力工具,近年来逐步成为医学神经影像临床诊断和治疗的新途径[1]。脑源定位也被称作源定位或是脑电溯源,相比功能核磁共振成像,EEG/MEG 脑源定位的优势在于它是神经电活动的直接反映,且具有毫秒级极高的时间分辨率。脑源定位中的正问题[2]是通过等效电流偶极子模拟大脑神经元的电活动,建立头部容积传导模型,进一步求出不同神经元电活动传导到头皮表面各电极的EEG/MEG 信号。而脑源定位技术中的逆问题,则是通过头皮表面记录的EEG/MEG信号,反向推算出颅内神经元活动的位置、方向和强度信息。
近年来,随着EEG/MEG信号分析技术所取得的进展,脑源定位技术也越来越多地被应用于基础科学研究和临床的诊断治疗。在基础科研中,通过源定位技术可以分析大脑在源空间的连通性,因此能够较好地研究各种认知任务和静息状态期间大脑区域之间的相互作用[3]。在临床应用上,脑源定位技术已成为辅助医生进行癫痫和其他脑部疾病诊断治疗的有效手段。大脑源层面的连通性分析能够诊断癫痫和分析发作间期活动是如何影响大脑网络的,这可作为定位癫痫发作起始区和刺激区的工具[4],以及近年来也常作为患者脑网络功能的评估手段[5]。同时,由于脑源定位能够分析大脑活动的神经机制,因此常用于认知功能障碍的疾病诊断和治疗,例如注意缺陷与多动障碍(attention deficit and hyperactivity disorder,ADHD)[6]。
然而,实践操作和理论分析的不确定性使脑源定位技术准确性受到极大挑战。脑源定位过程主要由五个步骤组成(图1)。a.采集数据,包括个体电极定位、基准点采集以及个体解剖像的获取;b.构建头部容积传导模型[7];c.创建源空间及电极坐标配准;d.选择源成像方法计算皮层活动;e.统计报告源分析结果并可视化呈现。在实践操作中,不同的记录方式、头部建模误差、源建模误差、干扰噪声和测量电极数量等[8]因素对脑源定位的准确性都造成极大影响。在理论分析中,由于逆问题本质上是不适定的,即不同的EEG/MEG信号对应的神经元放电活动并不唯一,需要通过最小范数法(minimum norm estimates,MNE)和低分辨率电磁层析成像(low resolution electrical tomography,LORETA)等正则化技术去解决[9]。但不同逆问题算法的特性都会使源定位的结果产生差异。

Fig.1 Brain source localization technology for accuracy evaluation and application图1 脑源定位过程及精度评估方法和实际应用
据此,本文主要针对脑源定位的精度评估问题以及其在临床和科研中的应用进行分析。首先,本文回顾了近年来脑源定位的基本原理与主要发展过程。其次,从理论分析层面归纳了基于空间分辨率的精度指标,以及基于串扰和点扩散函数的评估方法,分析了不同的源定位方法中源的重叠程度和其他源对目标源的影响,以及从实践层面总结了记录方式、电极数量和密度、头部容积传导模型等因素对脑源定位精度的影响。此外,梳理了脑源定位技术在时频分析,连通性分析研究中的应用,以及其在癫痫、注意缺陷与多动障碍和其他脑部异常或疾病方面的临床应用。最后,在介绍了经典的最小范数法的算法基础上,梳理了非线性优化、波束成形、深度学习等技术在脑源定位中的发展现状和趋势。
1 脑源定位方法
1.1 基本原理和过程
脑源定位技术主要分正问题和逆问题两部分。正问题旨在模拟由大脑活动神经源产生的头部表面的电势,而逆问题旨在重建大脑中电流源的分布。通过头模型计算出的导联场矩阵作为正问题的解,输入到逆问题算法中计算出最终的逆解,以此来获取源的位置、强度和方向等信息,完成定位过程。
a.正问题。由于逆解的准确性很大程度上依赖于正问题的解,为了高精度求解脑电正演问题,容积传导模型应尽可能反映头部几何形状。目前该领域已提出了各种基于解析和头部数值的头模型方案,如三壳同心球[10]、椭球体[11]、偏心球体[12]或是双中心球体[13]来建立导联场矩阵以得到正问题的解。随着测量技术的进步,研究人员发现头部实际的几何形状以及个体颅骨的不同厚度和曲率对脑源定位产生了明显的影响,因此提出了边界元法(boundary element method,BEM)[10]、有限单位元法(finite element method,FEM)[14]和有限差分法(finite difference method,FDM)[15]这些常用的数值计算方法,结合几何形状更真实的头模型,以此更加精确地解决脑电正问题。BEM 通常与简化的三层头部模型结合使用,而FEM和FDM提供了对更复杂的几何形状和各向异性电导率进行建模的可能性。
b.逆问题。解决逆问题的主要方法分为非参数法和参数法。非参数方法采用分布式源模型,假设电流活动存在于整个脑活动范围,将整个连续的大脑皮层区域转化为一簇离散的子区域,每个区域是一个小三角形,叫做源。这种模型的源成像将问题转化为线性问题的求解,估计每个源的幅值,幅值越高的源越深。参数法也称为等效电流偶极子模型或时空偶极子拟合模型,将脑内局部的神经电活动等效为一个电流偶极子。由于偶极子的参数是未知的,记录得到的EEG 信号与源参数之间呈非线性关系,因此参数的调整过程有一定的困难。
1.2 最小范数方法
逆问题的不适定问题造成了解的不唯一,通过引入Tikhonov 正则化方法是解决这一问题最经典的手段[16],其中包括最小L1 范数和最小L2 范数法。最小L1 范数法包括最小电流估计(minimum current estimate,MCE)[17]、焦点欠定系统解决方案 (focal underdetermined system solution,FOCUSS)[18]、基 于 矢 量 的 时 空 最 小L1 范 数 解(vector-based spatial-temporal analysis using a L1-minimum-norm,VSETAL)[19]等。基于最小L2 范数的正则化方法主要包括最小范数估计(minimum norm estimates,MNE)[20]、低分辨率电磁层析成像(low resolution electrical tomography,LORETA)[21]、标准化的低分辨率脑电断层扫描(standardized low resolution brain electromagnetic tomography,sLORETA)[22]、精确的低分辨率脑电断 层 扫 描 (exact low resolution brain electromagnetic tomography,eLORETA)[23]等。
最小范数估计技术是解决逆问题的常用方法,其中MNE 适合于分布源模型,但存在深层皮质源定位不当的缺点。加权最小范数估计(weighted-MNE,WMNE)[24]补偿了MNE偏向弱源和表层源的趋势,通过对偶极子引入一组加权矩阵来校正这种趋势。进一步地,混合加权范数HWMN(hybrid WMNE)[25]克服了MNE 扩散模糊的源分布图像的缺点,增加了源定位精确度。此外,与MNE 相比,LORETA 虽然更适合处理深度源,但空间分辨率低,点源的局部图像模糊,图像分散。sLORETA 考虑实际信号中的生物学误差,假设生物学误差独立均匀地分布在整个大脑中,因此具有更好的精确定位和零错误定位。eLORETA 更加重视深层源,通过深度加权减少定位误差,在存在测量和结构化生物噪声的情况下提供零错误的精确定位。除此以外,研究者们还发展了基于此类最小范数技术的扩展算法,本文对这类逆问题算法的发展和优缺点进行了概括(表1)。
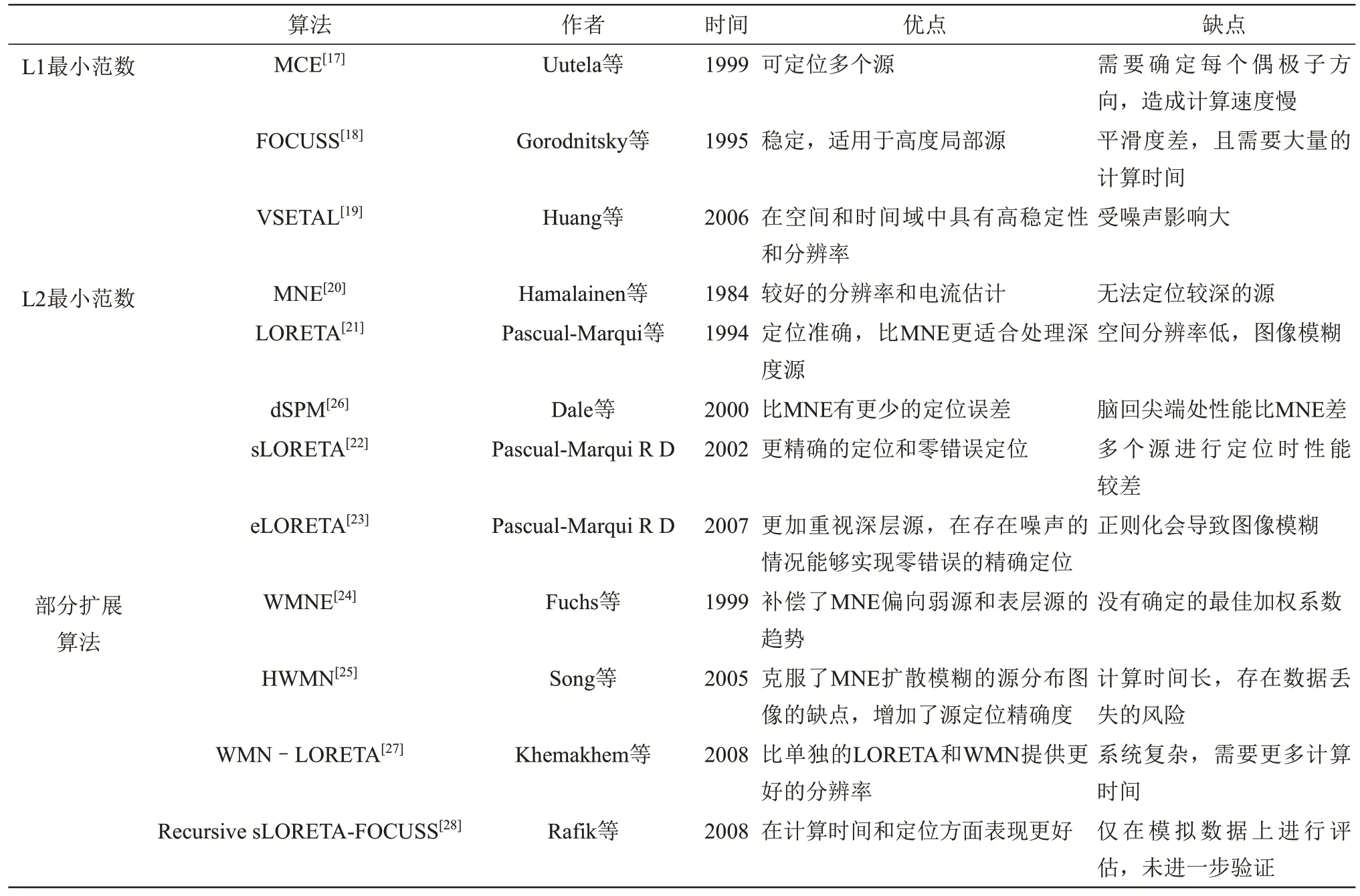
Table 1 Summary for technique based on minimum norm and extension algorithm表1 基于最小范数技术及扩展算法总结
1.3 工具软件的使用
在脑源定位的过程中,逆问题没有唯一的解,本章第1.2节已提出了几种经典的基于最小范数法的逆问题方法。目前已经有几个用于EEG 源成像的商业或学术软件包已经实施了类似或者替代的策略, 例 如 Brainstorm、 EEGLAB、 Fieldtrip、RECOR、MNE-Python和BrainVoyager等(表2)。

Table 2 Commonly used brain source localization kits or software表2 常用的脑源定位工具包或软件
2 定位精度的影响因素
脑源定位的精度是脑科学研究中的关键指标,定位精度受到多种因素的影响,主要包括记录方式、电极数量和密度以及头模型的构建。
2.1 记录方式对定位精度的影响
由于头部组织不同的电导率对EEG 导联场的影响,使用EEG和MEG两种不同的记录方式会导致定位精度的差异。Malmivuo等[29]使用半灵敏度体积作为源模型,假设整个大脑中的神经元在时间和方向上具有相同的激活概率,证明MEG 和EEG在半灵敏度体积的大小和灵敏度分布形式上的差异非常小,这代表着他们以非常相似的方式记录大脑的电活动。但在经验上往往认为MEG 的定位精度优于EEG,这是因为EEG的电极密度远低于MEG的电极密度。在2004 年,Malmivuo 等[30]进一步证明了在使用颅骨电导率的皮质源的球形模型中,当颅骨/大脑和头皮的电导率比为5/1、10/1、15/1时,EEG 的半灵敏度体积小于MEG 的半灵敏度体积,也就是说EEG 的空间分辨率优于MEG。Liu等[31]研究表明,对于相同数量的电极,在源位置和方向上平均而言,EEG 定位比MEG 定位更准确。Antonakakis 等[32]在2019 年的研究结果发现,使用不同模态对P20/N20分量的源重建有不可忽略的影响,虽然MEG 定位稳定,受头部建模及刺激方式的影响较小,但EEG 有助于确定源的方向和强度,因此可以在精细的个性化头模型的基础上利用EEG和MEG组合两种模式的互补信息。
2.2 电极数量对定位精度的影响
由于电极数量过少会导致对头皮电位采样不足,因此根据国际10-20系统,使用少电极记录脑电图的电极间距离最小为7 cm。现如今,高密度脑电图采样可支持数量多达256个的电极。对于高密度EEG,10-20 系统的空间分辨率主要受电极数量的限制,电极数量的增加可以提高EEG 的空间分辨率。具体来说,Sohrabpour 等[33]在2015 年对儿科癫痫患者脑电图通道数与脑源定位关系的研究中,证明了随着电极数量的增加,脑源定位的精确度越高。以用于识别癫痫发作区的ECoG记录作为金标准,当EEG的电极数从32依次变为64、96和128时,平均定位误差分别提高了4、1.3和1 mm。此外,Ryynanen 等[34]研究了在不同噪声水平下EEG 电极数量对空间分辨率的影响,发现对于高密度EEG,10-20 系统的空间分辨率主要受电极数量的限制,而噪声量对其的影响较低。但随着电极数量的增加,噪声对空间分辨率的影响也增加。根据文献中描述的规则,当颅骨/大脑和头皮的相对电导率为15/1时,如果相对噪声水平小于24%时,可使用64 个电极,当相对噪声水平小于9.2%,则可以使用128个电极获得更好的空间分辨率。
总之,在记录方式上,当电极数量相同时,EEG 的定位精度比MEG 更高。而未来将EEG 与MEG 或是其他模态相结合进行脑源定位分析有巨大潜力。对于电极数量来说,虽然数量越多越精确,但定位效果的改善随之减弱,因此根据需求选择合适的电极数量也能达到目标精度。同时,也需要根据现实环境的影响来选择电极数量的最佳方案。
2.3 头模型对定位精度的影响
正问题中的头模型也称为容积传导模型,在准确的脑源定位中起着核心作用。头模型的建立必须包含不同组织隔室的几何形状和电导率分布,由核磁共振成像(MRⅠ)扫描能够获得较为精确的几何形状。由于测量电导率的方法和被测样本的条件不同[35],颅骨致密物、颅骨海绵体、脑脊液、灰质和各向同性、各向异性的白质具有显著的差异。因此在2016 年Huang 等[7]开发了具有六层结构的New York Head 容积传导组织,在源成像和靶向经颅电刺激上都具有较高的准确性,相比普通BEM模型的10.8 mm定位误差,使用个性化头模型的定位精度高达6.9 mm。因此构建逼近真实的头部模型对于提高脑源定位的准确性是必不可少的。
目前进行溯源工作的相关研究中,大部分采用的头模型是由计算机仿真获得。为了减小计算机模拟建模的不确定性,有研究使用尸体大脑作为建模替代方法,测量了人体尸体头部中的电流分布[36],使用了36个定制的多点电极进行高密度的3D脑内测量,得出大约3/4的电流在头皮和颅骨上减弱的结论。这是由于死亡使脑组织的生物物理特性发生了巨大的变化,从而直接限制了离体与活体间的比较。
在脑研究中,体模实验可以系统地研究数据采集系统、重建算法和成像软件的性能,并随后为进一步的优化或实验提供合理的信息。因此近年来有许多研究通过医学成像和3D重建,使用3D打印技术创建更贴近真实人体的头部模型。在2020 年,有研究者成功使用3D 打印技术制作大鼠的头模型用于EEG 源定位[37],并且使用极细的同轴电缆实现的电偶极子来模拟大脑的神经活动。这表明使用物理手段进行头部模型的模拟进行脑源定位分析具有可行性。
3 定位精度的评估方法
逆问题算法的选择对计算定位区域至关重要,但由于不同算法之间难以直接比较定位效果,因此概括了不同的情况下的评估方法。同时,EEG 和MEG 作为非侵入式测量方法来定位神经元活动的精度依然存在争议,因此本章还介绍了临床植入电极的测量作为评估方法。
3.1 定位精度的理论评估
3.1.1 LORETA系列算法的空间分辨率比较
LORETA是高时间分辨率神经成像领域的一种创新方法,在该方法提出后的十几年间,研究者陆续提出了sLORETA和eLORETA,使得定位精度不断提升。LORETA系列采用空间分辨率来评估定位精度,使用Talairach 人脑图谱进行头部模型的模拟。每个源在网格点体素上都有一个固定位置,并由具有未知分量的电流密度向量定义,每个点的电活动强度和方向决定了在头皮上测量的电磁场。可以简单理解为脑容量被划分为3D 网格,网格由若干个体素构成,空间分辨率为每单元网格间的距离。LORETA的头部模型被划分为了2 394个体素,具有7 mm空间分辨率。同样条件下,sLORETA可产生5 mm 空间分辨率的6 430 个体素。eLORETA是重视更深层次源的方法,通过以更适当的方式选择权重矩阵,通过实现深度加权,将定位误差从12 mm减少到7 mm。
在三种逆问题算法中,sLORETA 的空间分辨率最高。LORETA产生的图像较模糊,空间分辨率相对较低,它能够确定大脑中活动最强烈的位置,但有一定的离散度。与在此之前的解决逆问题的其他方法相比,它的平均定位误差只有一个网格单元。在无噪声的仿真中,只有sLORETA 具有精确的零误差定位,有噪声的仿真中sLORETA 的定位误差最低,表明sLORETA是完美的一阶定位技术。与sLORETA 对比,发现eLORETA 在具有清晰和更少模糊质量的图像源的定位方面表现更好,同时能够更好地抑制不太重要的源[38]。
3.1.2 基于点扩散和串扰函数的评估方法
除了LORETA系列算法外,还有MNE、dSPM等经典算法也需要进行精度评估。由于每种算法属性不同,难以比较不同算法间的定位精度。因此,如何公平地评估和比较这些分布式逆解是一直以来关注的问题。
线性方法的空间分辨率可以使用分辨率矩阵进行评估,该矩阵分别包含点扩散函数(Point Spread Function,PSF) 和串扰函数(Cross-talk Function,CTF)。通过计算每个位置的PSF可以测试出大脑多个区域活动是否在正确位置周围产生峰值并且可以互相区分,评估它们的重叠程度。CTF则描述了具有单位强度的所有其他可能源将如何影响感兴趣源的源估计。本文归纳了多位研究者[39-40]在评估过程中描述PSF和CTF分布的不同方面的度量:a.峰值定位误差/偶极子定位误差(peak/dipole localization error,PLE/DLE),即估计的峰值与真实源位置之间的欧几里得距离;b.空间离散度(spatial dispersion,SD),评估两个分布源相互重叠的程度;c.分辨率指数(resolution Ⅰndices,RⅠ),反映特定位置的活动对该位置的幅度估计的贡献程度;d.总振幅(overall amplitude,OA),能够反映出不同源之间的相对差异。这些分辨率指标通过数学公式表述如表3所示。

Table 3 Summary for technique based on minimum norm and extension algorithm表3 评估指标的公式和描述
Hauk 等[39]对比了五种基于最小范数方法的PSF和CTF的的分辨率度量值——定位误差和空间离散度的分布,并且绘制了相应的直方图进行比较。得出MNE 对于浅层的源,PSF 的峰值出现在较为正确的位置,但误差随着源深度的增加进入脑沟而增加。外侧裂深部最大,误差超过5 cm。深度加权的MNE 方法的峰值定位误差较低,但在大脑深部区域仍有一些较高的值。dSPM在深部区域的PLE 较低,但浅层区域的表现不如MNE。sLORETA和eLORETA都显示了PSF的峰值具有零定位误差。对于CTF的分布都与PSF相似,可以得出无论使用何种方法,在大脑深处位置的源估计总是会从更接近电极的源中接收到明显更多的泄漏。通过比较PSF 的SD 表现,这些方法在外侧裂较深区域和颞下叶均显示出最高值,其中dSPM 和sLORETA尤其明显。
总而言之,不同的评估指标侧重点不同,应该根据关注的脑区和实验的需求来选择相应的评估指标。从峰值定位误差来看,sLORETA和eLORETA具有零定位误差。从空间离散度来看,MNE 和eLORETA 的表现较优。此外,在多个来源的情况下,估计幅度较大的来源可能会掩盖较弱的来源。
3.2 定位精度的实际评估
虽然EEG和MEG具有良好的时间和空间分辨率,但非侵入式方法来定位神经元活动的准确性和精确度始终存在争议。在临床上植入皮下或颅内电极进行记录是评价脑源定位全文精度的金标准之一。2019 年,Seeber 等[41]通过同时记录放置在皮下区域的电极和高密度的头皮电极来验证EEG 或MEG 测量的准确性。在进行深部脑刺激治疗的过程中,两名患有慢性多发性抽动的患者和两名患有强迫症的患者分别在丘脑和伏隔核植入电极来记录。最后将这些深层结构的局部场电位与大脑中从头皮脑电图重建的源估计进行比较,结果证明实际电极位置的颅内记录和源估计信号之间存在显著相关性。这说明了头皮脑电图能够重建皮下活动,因此使用EEG进行脑源定位是合理的。
Koessler 等[42]对10 名癫痫患者进行EEG 脑源定 位 , 并 通 过 立 体 脑 电 图(stereoelectroencephalography,sEEG)作为验证方法,来评估不同发作模式下的四种脑源定位方法的准确性。sEEG记录期间植入了7~10个电极,并使用64通道的脑电图进行头皮记录。对于不同患者,至少有一种定位方法产生了与sEEG定义的致癫痫区相同的定位,使用ECD 方法有9/10 获得了脑源定位方法和sEEG之间的最佳一致性。多信号分类(multiple signal classification, MUSⅠC) 和LORETA与sEEG的一致性为7/10,而sLORETA的一致性为5/10。其中,有四名患者在所有的脑源定位方法和sEEG 之间具有100%的一致性。进一步地,2020 年Sohrabpour 等[43]提出了FAST-ⅠRES 技术进行EEG 源定位,同时使用了颅内脑电图(intracranial electroencepholography,iEEG) 作 为金标准。研究结果证明了通过非侵入式手段测量的电生理信号能够对脑网络的位置和空间范围进行成像。
虽然通过在颅内植入电极进行记录能够直观地验证头皮脑电图的源定位方法,但通常是在特定的情况下,多数为临床上致病区域的测量,信号无法分布在全脑范围,难以执行复杂的任务。
3.3 其他精度评估方法
除了上述常用的评估方法,还有一些研究者提出了更为适用于其研究问题的方法。例如Tait等[44]评估了基于最小范数和波束成形估计方式的六种常用的源重建算法的性能,评估方法包括逆解的分辨率特性和传感器级数据的解释方差。结果表明,波束形成器的性能明显优于最小范数方法,sLORETA 是最小范数方法中性能最高的算法,接下来是MNE,最后是表现相似的wMNE 和eLORETA。
此外,Samuelsson 等[45]提出通过使用更通用的评估方法——受试者操作特征曲线(receiver operating characteristic curve,ROC)和精确召回特征曲线(precision recall curve,PRC)。ROC 分析量化了二元分类器系统的性能,PRC 被认为对不平衡数据集更好的衡量指标。另外,ROC 曲线下方面积(area under curve,AUC)可以用作源估计方法的空间精确度的衡量。根据此研究结果,dSPM在高信噪比下具有更高的定位误差,而MNE在AUC 分析中的性能稍差,主要原因是较深源的定位误差相对较高。
实际上,每种算法在不同的评估标准下表现不同,研究者需要根据其关心的研究问题选择合适的脑源定位算法,关注其特定属性,作为方法学指南进行更深入的研究。
4 脑源定位的应用
4.1 时-频分析与连通性分析的应用
脑源定位常与时频分析一起结合来研究大脑神经活动,对EEG 信号进行相位同步的方法用于检测相关电极信号之间的相位差,被识别为强相位同步的潜在源的信道可用于源定位[46]。此外,脑源定位和时频分析结合的方法还可以改进致癫痫区的定位[47]。时频分析即时频联合域分析,通过时间和频率的联合函数可以实现对目标信号在不同时间和频率的能量密度和强度的描述。非平稳信号具有随时间变化的统计特性,因此使用传统的傅里叶变换等方式获得的时间平均幅度谱不足以描述信号幅度、频率或相位的变化。在分析非平稳和多分量信号时,基于时频分析的技术优于基于单一的时域或频域的经典技术。对EEG 数据进行时频分析的方法主要包括短时傅里叶变换、连续小波变换、离散小波变换、希尔伯特变换等。
对于大脑内部活动的研究也常采用连通性分析的方式,大脑连接可分为结构连接、功能连接和有效连接其中,测量大脑功能连接的主要方法是脑电图,能够提供在认知过程中毫秒时间尺度上评估功能的连接动态。然而,这种方法具有局限性,例如脑电图缺乏脑源位置的信息以及由于体积电导和参考电极导致的信号混合,使得该方法对传感器空间同步测量的解释存在问题。
为了克服这些限制,目前EEG 源定位技术已被用于功能连接的分析中,主要可以分成两种不同的方法[48]。第一种方法是基于生物物理生成模型,它描述了神经源动力学和相互作用如何产生头皮脑电图,旨在直接估计来自传感器空间数据的源之间的功能连接,并需要先验假设网络结构。例如,神经质量模型有可能模拟神经集合的活动以及它们之间的联系,从而可以产生大脑节律或与事件相关的反应。另一种方法是无模型方式,即EEG 源成像结合多元连通性测量确定皮质活动的连通性模式,不需要对网络结构进行任何假设,共分为两个步骤。首先,使用逆问题算法确定源信号,可以基于分布式源模型或偶极源模型。接下来即可估计分布或偶极子源之间的功能连接。
功能性和有效性连通性分析通常用于深入了解癫痫或其他脑部疾病的网络性质。一方面,连通性分析用于确定癫痫或发作间期活动如何影响大脑网络,并且认知改善或下降可能与癫痫患者特定大脑网络的变化有关。另一方面,由于癫痫发作和尖峰在大脑中迅速传播,连通性分析被用作定位癫痫发作起始区和刺激区的工具[4]。根据Van Mierlo等[49]在2019 年的初步研究表明,即使在EEG/MEG 中没有明显的癫痫活动时,源连通性也有可能获得预后相关性,以帮助诊断癫痫类型,并预测治疗结果。除此以外,近年来功能连通性分析常用于评估患者脑网络功能。Ⅰandolo 等[5]对接受癫痫手术后儿童的EEG 进行研究,量化儿童功能性脑网络的变化。也有研究者对精神分裂症患者进行经颅电刺激来调节脑网络的功能链接。2022年,Yeh等[50]将基于源定位计算的功能连接结果作为参考,表明在前额叶皮层上使用经颅电刺激来调节伽马波段的功能网络连通性能够改善精神分裂症症状。
4.2 脑源定位的临床应用
目前,不同的脑源定位方法已应用在多种脑部异常和疾病的诊断和治疗中,其中关于诊断治疗癫痫和ADHD 的研究较多,除此以外,连通性分析在疾病中的应用也极为广泛。
癫痫治疗的最终目标是在不引起副作用的情况下使患者无癫痫发作,在耐药性局灶性癫痫中,切除病灶是疗效最高的治疗方法。多模式术前评估旨在通过描绘所谓的致癫痫区,但术前评估期间的神经影像学检查依赖于发作间期癫痫活动。因此,定位与发作间期癫痫活动互补的癫痫发作来源具有很高的临床价值。在术前评估过程中,通过非侵入脑电图长期记录可以识别癫痫发作症状,传统的EEG分析是基于对波形模式的视觉检测[51]。Lopes等[52]在2020年提出了一个框架来搜寻头皮脑电图并确定癫痫侧向化以帮助电极植入,使用eLORETA 来绘制从头皮EEG 记录的癫痫发作时期的源活动,然后使用锁相值构建功能网络并使用数学模型进行研究,通过从网络中移除不同的感兴趣区域(region of interest,ROⅠ)来模拟它们对网络在计算机中产生癫痫发作的能力的影响。
ADHD 是儿童和青春期普遍存在的神经精神障碍,它与许多认知功能障碍有关,包括认知控制缺陷。该疾病的特点是注意力不集中、多动和冲动适应症水平的改变,对ADHD 患者的脑源定位为疾病的诊断和治疗开辟了一条新途径[53]。2018年,Bluschke 等[6]在早期青少年ADHD 中研究了成功和缺陷多成分行为的神经机制,通过sLORETA 进行源定位分析,在单模态和双模态实验中,通过神经生理过程在下顶叶皮层中观察到反应选择机制。Mccracken 等[54]通过sLORETA 源定位分析来研究青年人对处理视听多感觉刺激的神经结构来源,发现ADHD 患者在神经水平上对多感官条件的反应与对照组不同。Mauriello等[55]则比较了ADHD患者和健康人对于面部注视的视觉处理功能,发现患者存在涉及视觉注视解码的脑损伤,表明了这种疾病相关的神经特征。
对于重度抑郁症患者,Kirsten等[56]使用基于网络的统计方法来比较对于治疗响应者和非响应者之间的连通性度量。通过使用LORETA 对重度抑郁症患者的静息态脑电图绘制源估计和连接测量,研究者发现alpha2波段内的预处理脑电图连接对电休克疗法治疗的疗效具有预测价值。除此以外,在2021 年,Xie 等[57]研究调查了头皮电极中神经信号的振荡特征,并绘制了大脑的功能连接。参与者在工作记忆任务中编码了复杂的视听对象,与单一模态对象编码相比,在视听对象编码期间,前额叶、顶叶、颞叶和枕叶这些皮层区域中theta 振荡频率的神经连通性显著。结果表明,theta 波段的局部振荡和区域间连通性在视听对象编码过程中发挥重要作用,并可能有助于形成多感官信息的工作记忆痕迹。
5 脑源定位的发展趋势
逆问题算法是脑源定位的核心技术,与定位精度以及临床应用息息相关。近年来,研究者在最小范数估计之外也提出了一些其他逆算法的发展思路。图2 回顾了不同方法下的逆问题算法发展历程。

Fig.2 The development and trend of inverse problem algorithm图2 逆问题算法的发展和趋势
a.最小范数方法。1984 年Hmlinen 提出MNE方法以来,在此基础上研究者又发展了LORETA系列、局部自回归平均值(local auto-regressive averages,LAURA)[58]和FOCUSS 的脑源定位方法,这些算法都是基于最小范数的技术所发展的,成为了目前最常用的经典技术。
b.非线性优化技术。当非线性优化程序用于解决脑电逆问题时,目标函数可能会产生多个局部解,因此研究者们提出元启发式算法来解决这类复杂的优化任务,对相关偶极子进行估计。主要包含的算法有模拟退火(simulated annealing algorithm,SA)[59]、遗传算法(genetic algorithm,GA)[60]、粒子群优化(particle swarm optimization,PSO)[61]和差分进化(differential evolution algorithm,DE)[62]等。
c.多信号分类技术。1998年,Mosher等[63]在MUSⅠC 的基础上提出了递归多信号分类(recursive MUSⅠC)的方法,通过递归使用子空间投影自动提取源的位置。此外,有研究者还在此基础上拓展了空间扩展的新皮质源多信号分类(ExSo-MUSⅠC)[64]和 投 影 多 信 号 分 类(RAPMUSⅠC)[65]的方法。
d.波束成形方法。波束成形器也称为空间滤波器,Van Veen 等[66]最早提出线性约束最小方差(linearly constrained minimum variance, LCMV)的方法,这种方法不需要对偶极子数量先验假设。在1999 年Van Hoey 等[67]提 出 使 用 波 束 成 形(beamforming,BF)技术进行EEG 源分析。用于空间滤波的波束形成技术,最初设计用于雷达信号处理的应用,它能够从测量的EEG 信号中提取大脑中预定义的感兴趣区域的源活动。Gross 等[68]在2001 年提出了相干源动态成像(dynamic imaging of coherent sources,DⅠCS),这是一种频域波束形成技术,可以研究大脑区域之间振荡活动和同步的皮层来源。2009年Antelis等[69]提出了使用卡尔曼滤波器和粒子滤波器(partical filter,PF)的解决方案应用在EEG 源定位上。同时,基于波束成形技术的扩展方法相继提出,包括波束成形粒子滤波(beamforming particle filter,BPF)[70]、多核BPF、序列蒙特卡罗(sequential Monte Carlo,SMC)[71]等方法。
e.稀疏理论方法。由于一般认为只有有限数量的大脑皮层区域在短时间内真正激活,因此近年来稀疏源定位越来越受到重视。2001 年提出的稀疏贝叶斯学习(sparse Bayesian learning,SBL)提供了一个统一的框架,通过此框架可对受生物学和数学约束的EEG 源进行估计。2018 年Ojeda 等[72]提出了新颖的SBL 算法,使用脑图谱对源的组稀疏分布进行了良好的初始化。另外,有学者先后提出了VB-SCCD 算法、时空统一断层扫描(spatiotemporal unifying tomography,STOUT)以及数据驱动的时空频率字典(STF dictionary)[73]等算法来计算源的稀疏解。
f.张量分析方法。基于张量的逆问题算法也逐渐用于优化脑电源定位问题当中,2004 年Miwakeichi 等[74]将典型多数分解应用于空间-时间-频率(space-time-frequency,STF)变换的EEG数据中。Becker等[75]在2010年提出了基于时空波矢量(space-time-wave-vector,STWV)数据的一种多路方法,它可以在嘈杂的环境中准确定位源,而且同时提取与每个源相关的时间行为。接下来的几年里,此研究团队又相继提出了用于扩展源定位的算法STWV-DA(STWV-Disk algorithm)和STFDA(STF-Disk algorithm)算法[76]。
g.贝叶斯方法。贝叶斯方法是通过设计不同的先验分布来解决逆问题不适定问题。根据先验约束不同,目前主要有基于空间约束先验和基于时空约束先验贝叶斯方法。基于空间约束的技术是利用皮层神经电活动在空间上的信息,约束源信号分布,1.2节提到的基于L2范数的方法即为使用的空间先验知识。基于时空先验约束的源定位技术则是进一步利用时域结构约束解空间,能够提高定位性能。在1997 年,Baillet 等[77]在考虑了空间先验之外,还提出了惩罚相邻时刻的幅度差的时间先验。在2004 年,Galka 等[78]提出了一种时空卡尔曼滤波的方法,利用状态空间表达式模型来表示时域信息。除此以外,使用时间基函数(temporal basis functions,TBFs)[79]能够降低算法计算复杂度,而且能有效减小噪声量的影响。
h.深度学习方法。随着人工智能的发展,使用深度学习进行脑源定位的研究也相继展开。基于人工神经网络的计算的逆解遵循数据驱动的方法,大量模拟EEG 数据样本用于训练人工神经网络以正确地将电极空间信号映射到源空间位置[80]。这可以改善实时脑源定位功能,提高医疗影像的成像质量。在2017 年,有研究者提出了一种解决非线性前向算子的逆问题[81],该方法基于经典正则化理论和深度学习中的卷积网络,在利用前向算子、噪声模型和正则化函数中编码的逆问题的先验信息的同时进行学习,实现了快速重建图像的目的。
Cui 等[82]在2019 年使用时空长短期记忆递归神经网络(long short term memory,LSTM)来识别单一来源的位置和时间进程。在此研究中,作者使用有限元法使用正向模型生成模拟数据,提出了一种脑源定位框架,以基于模拟训练数据估计源位置,模拟数据的结果对噪声信号表现出良好的鲁棒性。Hecker 等[83]则提出了ConvDip 的新颖卷积神经网络架构,用于解决分布式偶极子模型中的EEG 逆问题。ConvDip 能够从EEG 数据的单个时间点产生逆问题的解,并且定位准确,预测速度快,产生的伪影少,漏检率低。2021 年Wei 等[84]提出了一种使用空间基函数分解进行EEG 源定位的边缘稀疏基网络(edge sparse basis network,ESBN),结合了边缘稀疏先验和高斯源基。研究表明有监督的ESBN在合成数据中优于传统的数值方法,无监督微调在真实数据中提供了更多焦点和准确的定位。
在多种逆问题算法的发展历程中,最经典的算法还是基于最小范数的技术。但随着计算机计算能力的大幅增加使得深度学习在各个领域发展趋势不容小觑。此外,深度学习对算法的改进程度远远超过其他算法,定位精确性也大大提高,可预见基于深度学习的脑源定位技术将会成为未来的主要趋势。
6 总结与展望
本文主要回顾了脑源定位的基本原理与过程,并且根据脑源定位过程中产生的一系列对定位精度造成影响的因素进行梳理。从理论和实践的角度上总结了相应的精度评估指标,并且介绍了脑源定位技术在临床和科研上的应用和发展。
脑源定位从理论分析和实践操作层面中的精度评估是本文关注的问题,作者从理论的角度给出了五种不同的指标,分别为:LORETA系列的空间分辨率、所有算法适用的峰值定位误差/偶极子定位误差、空间离散度、分辨率指数和总振幅。在实际层面上,则介绍了记录方式、电极数量和密度、头部容积传导模型等因素对源定位精度的影响,以及在科学研究和疾病诊断方面的应用。脑源定位技术应用到大脑连通性分析能够帮助研究者更好地理解大脑认知活动上各个区域的联系与功能。同时,脑源定位也在多种脑部疾病或异常中得以应用,其中癫痫与ADHD 的诊断和治疗已到了临床阶段。最后本文总结了脑源定位的发展趋势,罗列了计算逆解的各类方法的发展历程。
脑源定位精度是一直以来的关注点,它受到多种因素的影响,主要包括记录方式、电极数量和密度、头模型以及逆问题算法。电极密度与精度成正相关,一般情况下128个电极就足够获得最佳分辨率。此外,本文概括了头部组织电导率以及头模型的仿真方法,使用计算机进行仿真模拟已是成熟的技术手段,使用物理方式建模进行源定位分析可能成为新的趋势。目前,脑源定位的精度在测量仪器的层面上已得到了极大的改善,但逆问题算法对定位的精确程度难以定量评估。因此本文总结了基于空间分辨率、基于点扩散以及串扰函数的评估方法对于不同脑源定位方法中源的重叠程度和其他源对目标源的影响,并给出相应的评价指标。但此类通过头皮表面测量的方法在准确度上始终存在争议,因此将临床上植入皮下或颅内电极进行记录作为评价脑源定位精度的金标准之一。虽然颅内电极记录能够直观地验证头皮脑电图源定位,但通常为临床上致病区域的测量,信号无法分布在全脑范围,也难以执行复杂的任务。因此,公平准确地评估脑源定位的精度在未来还需进一步的探究。最近Toi等[85]提 出 的fMRⅠ的 神 经 元 活 动 直 接 成 像(DⅠANA-fMRⅠ),在时间分辨率上达到了毫秒级的精度同时保留了MRⅠ的高空间分辨率,能够无创神经成像来检测神经元活动。由于其具有高时空分辨率,若能应用到人类大脑上,或许在未来可以应用在脑部疾病的病灶区的精准定位,以及其无创神经成像的优势更适合作为头皮脑电图源定位的精度评估手段。
此外,研究者们对于脑源定位中最重要的逆问题的解上保持着持续不断的探索和优化,从基于最小范数的技术发展以来,陆续提出了基于优化技术、多信号分类、波束成形、张量和稀疏理论等方法。近年来提出的卷积神经网络在脑源定位上的应用是基于数据驱动的方法,大量模拟EEG 数据样本用于训练网络,从而精确快速地将电极空间信号映射到源空间位置。随着计算机性能的增加以及人工智能技术的发展,目前深度学习在医疗领域上的应用越来越受欢迎,使用卷积神经网络进行脑源定位或许是新趋势。
- 生物化学与生物物理进展的其它文章
- 基于高密度单核苷酸多态性的共祖远亲缘关系预测算法准确性研究*
- Mechanism Study of Warm Transduction From Keratinocytes to Downstream TRPA1 in DRG Neurons*
- Study on Artificial Imaging at The Peripheral Retina Region*
- 全血分析在疾病筛查中的应用*
- Study on Apoptosis of Breast Cancer Cells Induced by Regulation of PI3K/Akt/mTOR Pathway by Syringin*
- Histone H3 Phosphorylation at Serine 10: Potential Biomarkers of Early Toxicity of Metal Nanoparticles*

