水液相下Eda酮式异构体与超氧化氢自由基反应的DFT理论计算










摘要:在M06-2X/SMD/6-311+G(d,p)理论水平下,研究水液相1个大气压、310.15K温度下依达拉奉(Eda)酮式异构体与超氧化氢自由基(·HO2)的反应机理.结果表明:Eda酮式异构体与·HO2的反应有抽H、加成和单电子转移3个过程;抽H反应主要通过·HO2抽取杂环H和甲基H实现,反应的自由能垒为77.1~78.7kJ/mol;加成反应可通过·HO2加成不饱和C的过程实现,加成自由能垒为48.2~95.0kJ/mol;加成到杂环上与甲基相连的C原子的放热反应最具优势,自由能垒为48.2kJ/mol;单电子转移的自由能垒为141.1kJ/mol,该过程不能实现.可见,水液相下Eda酮式异构体可通过抽H和加成反应消除·HO2.
关键词:依达拉奉酮式异构体;超氧化氢自由基;密度泛函理论;过渡态;Marcus理论;电子转移;自由能垒
中图分类号:O641.12文献标志码:A文章编号:1671-5489(2024)05-1254-13
DFT Theoretical Calculation of Reaction between Eda Keto Isomers and Superoxide Hydrogen Radical in Aqueous Liquid Phase
PAN Yu2,JIANGChunxu',WANG Haolin³,YANG Ying',DONGLeigang',WANG Zuocheng.4,LI Bing
(1.Theoretical Com putingCenter,Baicheng Normal University,Baicheng 137000,Jilin Province,China;2.College of Physics and Electronic Information,Baicheng Normal University,Baicheng 137000,Jilin Province,China;3.College of Forest,BeihuaUniversity,Jilin 132013,Jilin Province,China;4.College of Medicine,Hainan Vocational University of Science and Technology,Haikou 571126,China)
Abstract:At the theoretical level of M06-2X/SMD/6-311+G(d,p),we studied the reaction mechanism between Edaravone Eda)keto isomers and superoxide hydrogen radical HO2 in aqueous liquid phase at 1 atmospheric pressure and 310.15 K temperature.The results show that there are three processes in the reaction of Eda keto isomers with HO2:H extraction,addition and single electron transfer.The H extraction reaction is mainly achieved through HO extraction ofheterocyclic H and methyl H,and the free energy barrier of the reaction is 77.1-78.7 kJ/mol.The addition reaction can be realized by the process of HO2 addition to unsaturated C,and the free energy barrier of addition is 48.2-95.0 kJ/mol.The most advantageous exothermic reaction is the addition of C atoms connected to methyl groups on heterocycles,with a free energy barrier of 48.2 kJ/mol.The free energy barrier of single electron transfer is 141.1 kJ/mol,which is impossible.Therefore,the Eda keto isomer in aqueous liquid phase can eliminate·HOz by H extraction and addition reactions.
Keywords:Eda keto isomer;superoxide hydrogen radical;density functional theory;transitionstate;Marcustheory;electrontransfer;free energy barrier
超氧化氢自由基(·HO2)活性氧由生命体的自氧化作用产生,它是生命体内羟基自由基(·OH)的前体.·HO2、超氧阴离子自由基(O2-)和·OH等氧自由基的氧化能力强,它们在生命体内可通过氧化反应攻击蛋白质和DNA等有机分子,损伤生命体内正常细胞,并阻碍正常的新陈代谢,最终导致冠心病、痛风、脑卒中和癌症等慢性病以及机体衰老.·HO2的H原子还会被体内的其他有机基团取代,形成更大的氢超氧自由基(·LO2),攻击生命体内的DNA或RNA等生物大分子,·LO2与胸腺嘧啶和碱基的加成反应还会导致DNA遗传信息改变[2.不健康的生活方式、恶劣的情绪以及电磁波辐射会使生命体产生大量的·HO2等自由基,强紫外线照射会导致皮肤产生·HO2等自由基,及时消除各种自由基对健康有重要作用,因此药物分子通过与自由基发生反应从而消除自由基的研究具有重要意义.
文献[4-6]研究表明,依达拉奉(Eda,C10H10N2O)有较好的抗氧化和消炎作用,可清除大脑内部羟基基团;文献[7]研究表明,Eda分子能有效降低·HO2,O2和·OH等在生命体内的含量,从而抑制它们对生命体的副作用.为从理论上说明Eda分子的抗氧化活性,人们开展了Eda烯醇式异构体与·HO2,·OH和O2等自由基的反应机理研究.孙伟等]研究表明,·HO2抽烯醇式Eda的羟基H是无势垒反应,·HO2加成到烯醇式Eda中不饱和C的自由能垒多数在温和反应能垒83.6kJ/mol以下,说明烯醇式Eda具有清除·HO2的能力.王玲等[0]研究表明,Eda烯醇式异构体与·OH反应可通过抽H、加成和电子转移3个过程实现,反应能垒为2.8~77.9kJ/mol,低于温和反应能垒83.6kJ/mol[9],说明烯醇式Eda具有较好的消除·OH的能力.张雪娇等[研究表明,O:与Eda烯醇式异构体抽H原子反应的自由能垒为12.2~139.1kJ/mol,均低于极限反应能垒160.6kJ/mol[9],有些甚至低于反应自发进行的能垒40.2kJ/mol,说明烯醇式Eda具有清除O2的能力.
文献[12]研究表明,水液相下Eda烯醇式向酮式异构的自由能垒为73.4kJ/mol,低于酮式向烯醇式异构的能垒82.1kJ/mol,二者能垒均低于温和反应能垒83.6kJ/mol,Eda酮式与烯醇式可互变,且Eda酮式比烯醇式的分布高.但Eda酮式异构体消除·HO2反应的理论研究目前尚未见文献报道.为对Eda消除·HO2的机制有全面认识,并为研究Eda酮式异构体消除·OH和O2提供理论依据,本文在文献[8,10-11,13-17]的基础上,对水液相下Eda酮式异构体与·HO2反应进行研究.
1计算方法
采用处理主族元素以及氢键、范德华力等作用有较好表现的M06-2X[1820]泛函,在分裂弥散基组6-311+G(d,p)[21-22]水平及310.15K和1个标准大气压的水溶剂环境(即生命体内的一般环境)下,优化所有相关反应驻点物种结构,稳定驻点的红外振动无虚频,反应过程的过渡状态(鞍点)[2的红外振动有且只有一个虚频,过渡态与相关稳定驻点的关联性通过内禀反应坐标(IRC)计算24]确认,为获得精确的反应势能面以及相关复合物的结合与解离能,采用MN15[25]泛函,在高角动量基组6-311++G(2df,pd)[26]下计算相关体系的单点能.在结构优化和单点能计算时的水溶剂效应采用SMD模型[7]方法处理,物种的自由能是其自由能热校正与单点能之和,以反应物自由能为相对势能零点,绘制反应过程的势能面;反应的自由能垒(活化能)是鞍点(过渡态)能量与反应物能量之差;反应物复合物RC的结合能是相关反应物与RC的焓变,产物复合物PC的解离能为其与解离产物的焓变.
电子转移无过渡态,反应能垒△Gr用Marcus理论[28-29]计算:
其中λ为重组能,可表示为
其中△GSET为产物与反应物的自由能变,△EsET为产物与反应物的非绝热能变.
·HO2攻击7H形成的反应物复合物标记为RC-·HO2·7H,·HO2抽取7H的过渡态标记为TS_·HO2_7H,得到的产物复合物标记为PC_7H·H2O2;·HO2攻击1C形成的反应物复合物标记为RC-·HO2_1C,·HO2加成到1C的过渡态标记为TS_·HO2_1C,·HO2加成到1C得到的产物加合物标记为P_·HO2-1C;其他驻点标记法与此相似.
采用Gaussian16[30]程序计算,采用AIM2000程序[31]计算驻点关键点的pBcP(成键临界点BCP的电荷密度)与pRcP(成环临界点RCP的电荷密度)及其Laplace值V2p.
2结果与讨论
水溶剂环境下优化的Eda酮式异构体构型如图1所示.
计算表明,·HO2的H原子和2个O原子的电子自旋密度分别为-0.010,0.300,0.710,单电子在邻羟基O上分布最多,邻羟基O原子是·HO2与Eda酮式异构体发生反应的最佳位点(反应位原子).研究表明,相似于氨基酸分子与OH自由基的反应以及Eda烯醇式异构体与·HO2自由基的反应,Eda酮式异构体与·HO2自由基的反应同样有抽H、加成和电子转移3种情形.
2.1抽H过程
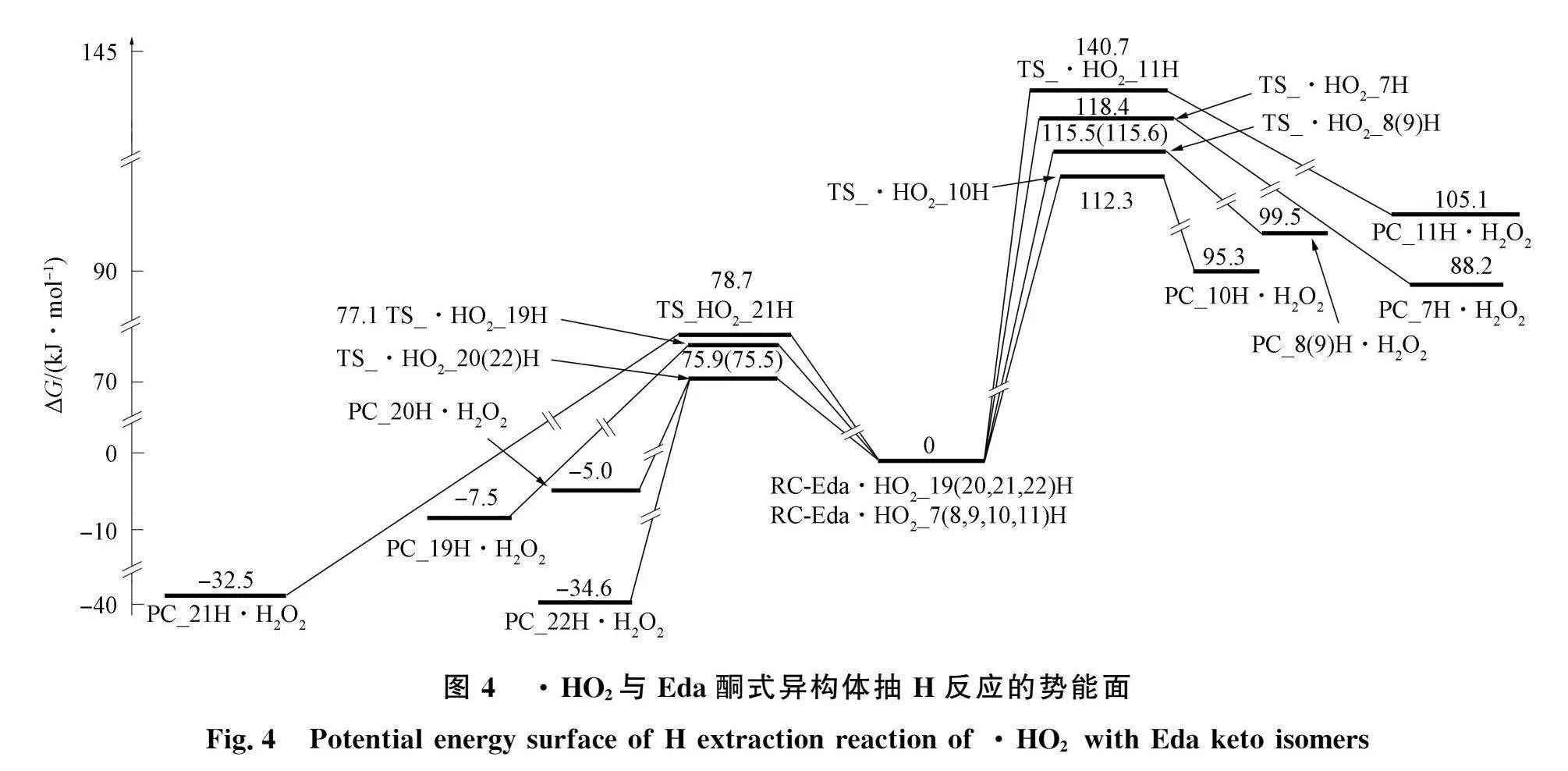
计算表明,·HO2抽Eda酮式异构体中甲基H和杂环H远低于抽苯环H的能垒,因此本文对抽甲基H和杂环H的过程进行较详细讨论.对抽甲基18H过程,研究发现无法形成反应物复合物,该反应是直接抽H过程,能垒相对较高,因此不进行讨论.7H是序号最小的H,该抽H过程能垒较高且产物复合物不稳定,对该抽H过程进行较详细讨论,以便与优势抽H过程进行比较.反应过程分别如图2和图3所示,反应过程的势能面如图4所示.
2.1.1·HO2抽7H
首先,·HO2从无穷远处(物理)攻击苯环的7H,当·HO2与7H的距离为0.25314nm时,·HO2与7H发生库仑作用,得到反应物复合物RC-·HO2·7H,放热0.1kJ/mol(即RC-·HO2·7H的结合能是0.1kJ/mol).该能量会被水溶剂迅速吸收,不能做后续反应的可资用能,后文相似处不再赘述.RC-·HO2·7H较Eda+·HO2体系稳定,·HO2抽取7H过程是先形成反应物复合物,再经过渡状态抽H的间接抽H过程,下文相似处不再赘述.
其次,RC-·HO2·7H的2C-7H键长从0.10811nm拉伸至0.13963 nm,其pBcp从0.28397减小至0.11976,V2p从-0.99075变为-0.11579,共价键2C-7H强度显著减弱,形成过渡态TS·HO27H,该过渡态产生的自由能垒为118.4kJ/mol.然后越过过渡态,7H继续向26O迁移,与·HO2结合成H2O2分子,得到产物复合物PC_7H·H2O2,其能垒为118.4kJ/mol,接近反应进行十分缓慢的能垒120.0kJ/mol,说明·HO2抽取Eda酮式异构体7H的过程十分缓慢,即Eda酮式异构体利用提供7H消除H2O2自由基的速率十分缓慢.
最后,PC_7H·H2O2解离成PC_7H自由基和H2O2,解离能为20.5kJ/mol,该过程可通过分子碰撞实现.NPA电荷计算表明,PC_7H·H2O2中H2O2的电荷量接近0,解离后得到H2O2的电荷量为0,说明该·HO2抽7H过程是H原子迁移.H2O2各原子电子自旋密度均为0,失去氧化能力,下文相似之处不再赘述.
2.1.2·HO2抽8H
首先,·HO2与8H发生库仑作用(26O与8H的距离为0.26709nm),得到RC-·HO2·8H反应物复合物,放热2.4 kJ/mol.其次,RC-·HO2·8H的3C-8H键长从0.10842nm拉伸至0.13930nm,3C-8H共价键强度显著减弱,形成过渡态TS·HO28H,该过渡态产生的能垒为115.5kJ/mol.然后越过过渡态,8H继续向26O迁移,得到PC_8H·H2O2产物复合物.该反应的能垒接近反应进行十分缓慢的能垒120.0kJ/mols,说明Eda酮式异构体通过提供8H消除H2O2自由基的速率十分缓慢.最后,PC_8H·H2O2解离成PC_8H自由基和H2O2,解离能为5.4kJ/mol,该过程容易实现.
2.1.3·HO2抽9H
首先,·HO2与9H发生库仑作用(26O与9H的距离为0.27338nm),得到RC-·HO2·9H反应物复合物,放热0.2kJ/mol.其次,RC-·HO2·9H的4C-9H键长从0.10836nm拉伸至0.14099nm,4C-9H共价键强度显著减弱,形成过渡态TS·HO2_9H,该过渡态产生的能垒为115.6kJ/mol.然后9H继续向26O迁移,得到PC_9H·H2O2产物复合物.Eda酮式异构体通过提供9H消除H2O2自由基的速率也十分缓慢.最后,PC_9H·H2O2解离成PC_9H自由基和H2O2,解离能为2.7kJ/mol.
2.1.4·HO2抽10H
首先,·HO2与10H发生库仑作用(26O与10H的距离为0.26984nm),得到RC-·HO2·10H反应物复合物,放热2.2kJ/mol.其次,RC-·HO2·10H的5C-10H键长从0.10843nm拉伸至0.300370.13957nm,5C-10H共价键强度显著减弱,形成过渡态TS·HO。10H,其产生的能垒为112.3kJ/mol.然后,10H继续向26O迁移,得到PC_10H·H2O2产物复合物.Eda酮式异构体通过提供10H消除H2O2自由基的速率也十分缓慢.最后,PC_10H·H2O2解离成PC_9H自由基和H2O2,解离能为5.7 kJ/mol.
2.1.5·HO2抽11H
首先,·HO2与11H发生库仑作用,同时与13N发生氢键作用(26O与11H的距离为0.26921nm,24H与13N的距离为0.16619nm),得到RC-·HO2·11H反应物复合物,放热28.3kJ/mol.其次,RC-·HO2·11H的6C-11H键长从0.10837nm拉伸至0.14047nm,6C-11H共价键强度显著减弱,形成过渡态TS·HO。11H,其产生的能垒为140.7kJ/mol.然后,11H继续向26O迁移,得到PC_11H·H2O2产物复合物.最后,PC_11H·H2O2解离成PC_11H自由基和H2O2,解离能为18.6 kJ/mol.过渡态TS·HO211H产生的能垒140.7kJ/mol接近反应很难进行的能垒145.0 kJ/mol,说明Eda酮式异构体不能通过提供11H消除·HO2.
2.1.6·HO2抽19H
首先,·HO2攻击甲基的19H,当26O与19H的距离为0.30037nm时,26O与19H发生库仑作用,24H与杂环π-氢键作用,得到反应物复合物RC-·HO2·19H(结合能为8.5kJ/mol).其次,RC-·HO2·19H的17C-19H键长从0.10837 nm拉伸至0.12757 nm,其pBcP从0.27196减小为0.16283,V2p从-0.90359变为-0.28891,17C-19H共价键强度减弱,形成过渡态TS·HO219H,过渡态产生的能垒为77.1kJ/mol.然后,越过过渡态,19H继续向26O迁移,得到PC_19H·H2O2产物复合物.过渡态TS·HO219H产生的能垒77.1kJ/mol低于温和反应能垒83.6 kJ/mol9,说明酮式Eda可通过提供19H消除·HO2.最后,PC_19H·H2O2解离成PC_19H自由基和H2O2,解离能为11.7 kJ/mol.
2.1.7·HO2抽20H
首先,·HO2从无穷远处攻击20H,当26O与20H的距离为0.32398nm时,26O与20H发生库仑作用,24H与杂环π-氢键作用,得到反应复合物RC-·HO2·20H(结合能为11.4kJ/mol).其次,17C-20H键长从0.10931nm拉伸至0.12754nm,共价键强度减弱,形成过渡态TS·HO。20H,产生的能垒为75.9kJ/mol.然后,20H继续向26O迁移,得到产物复合物PC_20H·H2O2.75.9kJ/mol低于温和反应能垒84.5kJ/mol,说明Eda酮式异构体可通过提供甲基氢20H消除·HO2.最后,PC_20H·H2O2解离成PC_20H自由基和H2O2,解离能为16.4 kJ/mol.
2.1.8·HO2抽21H
首先,·HO2从无穷远处攻击杂环的21H,当26O与21H的距离为0.26337nm时,26O与21H发生库仑作用,24H与杂环π-氢键作用,得到反应物复合物RC-·HO2·21H(结合能为8.4kJ/mol).其次,15C-21H键长从0.10925nm拉伸至0.13084nm,共价键强度减弱,形成过渡态TS·HO。21H,能垒为78.7kJ/mol.然后,21H继续向26O迁移,得到产物复合物PC_21H·H2O2.78.7kJ/mol低于温和反应能垒84.5kJ/mol,说明Eda酮式异构体可通过提供杂环氢21H消除·HO2.最后,PC_21H·H2O2解离成PC_21H自由基和H2O2,解离能为10.5 kJ/mol.
2.1.9·HO2抽22H
与上述情况相比,·HO2抽22H的抽H能垒最低,产物复合物最稳定.首先,·HO2从无穷远处攻击杂环氢22H,当26O与22H的距离为0.29523nm时,26O与22H发生库仑作用,24H与杂环及苯环π-氢键作用,得到反应复合物RC-·HO2·22H,结合能为10.8kJ/mol.其次,15C-22H键长从0.10936nm拉伸至0.12920nm,其pBce从0.27010减小至0.15390,V2p从-0.89682变为-0.24513,共价键强度减弱,形成过渡态TS·HO。22H,能垒为75.5kJ/mol.然后,22H继续向26O迁移,得到产物复合物PC_22H·H2O2.75.5kJ/mol低于温和反应能垒84.5kJ/mol[a],酮式Eda可通过提供22H消除·HO2.最后,PC_22H·H2O2解离成PC_22H自由基和H2O2,解离能为12.0kJ/mol.
由图4可见,·HO2抽H的自由能垒为0~140.7kJ/mol,均低于极限反应能垒160.6kJ/mol[9],Eda酮式异构体可通过提供H原子消除·HO2.·HO2抽杂环及甲基H的能垒均低于温和反应能垒83.6kJ/mol,远低于抽苯环H的能垒.原因是杂环及甲基的C-H键比苯环的C-H键红外振动频率小,C-H键活化程度好,·HO2抽杂环及甲基H比抽苯环H的C-H键长改变小.抽苯环H的产物复合物相对不稳定,表明·HO2抽H反应活性位点是杂环及甲基H.
2.2加成过程
研究表明,·HO2可加成到除杂环碳15C和甲基碳17C外所有不饱和的碳和氮上.对·HO2加成到1C(序号最小)和14C(能垒最小)的反应进行详细讨论,其他情况只做一般讨论.反应过程分别如图5和图6所示,反应的势能面如图7所示.
2.2.1·HO2加成到1C
首先,·HO2从物理无穷远处攻击1C,当26O-1C距离为0.32473nm时,pBcP和V2p分别为0.00663,0.02045,26O与1C发生库仑作用;同时,24H与苯环在π-氢键作用下形成RC-·HO21C反应物复合物,结合能为12.1kJ/mol.其次,·HO2继续向苯环运动,当26O-1C距离为0.18216nm时,二面角1C-2C-3C-4C从0.7°变为-5.3°,1C-2C-3C-5C从0.8°变为-6.2°,1C-2C-3C-6C从0.5°变为-6.3°,苯环的RCP和V2p分别从0.02260,0.16519降为0.02182,0.15849,苯环形变其大π键作用减弱;二面角12N-1C-2C-6C从-179.2°变为149.7°,形成过渡态TS_·HO2_1C,过渡态产生的内禀能垒为95.0kJ/mol.最后越过过渡态,·HO2继续向苯环运动,当26O-1C键长减小至0.14711nm时,其pCP和V2p分别为0.23579,-0.48364,26O-1C共价键作用,完成·HO2向1C的加成,得到加合产物P_·HO2-1C.
2.2.2·HO2加成到2C
首先,·HO2攻击2C,当26O-2C距离为0.32734nm时,26O与2C发生库仑作用,24H与苯环在π-氢键作用下形成RC-·HO2_2C反应物复合物,结合能为12.4kJ/mol.其次,·HO2继续向苯环运动,当26O-2C距离为0.18664nm时,苯环形变,共面性变差,其大π键作用减弱,过渡态TS_·HO22C形成,过渡态产生的能垒为73.6kJ/mol.最后,越过过渡态,·HO2继续向苯环运动,当26O-2C键长减小至0.14564nm时,形成26O-2C共价键,得到加合产物P_·HO2-2C.
2.2.3·HO2加成到3C
首先,·HO2攻击3C,当26O-3C距离为0.33441nm时,·HO2与Eda分子在π-氢键和范德华力作用下,形成RC-·HO2_3C反应复合物,结合能为9.1kJ/mol.其次,·HO2继续向苯环运动,当26O-3C距离为0.18340nm时,苯环共面性变差,大π键作用减弱,形成过渡态TS_·HO2_3C,过渡态产生的能垒为85.2kJ/mol.最后,越过过渡态,·HO2继续向苯环运动,当26O-3C键长减小至0.14527nm时,形成26O-3C共价键,得到加合产物P_·HO2-3C.
2.2.4·HO2加成到4C
首先,·HO2攻击4C,当26O-4C距离为0.33207nm时,·HO2与Eda分子(苯环部分)在π-氢键和范德华力作用下形成RC-·HO24C反应物复合物,结合能为9.6kJ/mol.其次,·HO2继续向苯环运动,当26O-4C距离为0.18726nm时,苯环共面性变差,大π键作用减弱,形成过渡态TS_·HO24C,过渡态产生的能垒为73.9kJ/mol.最后,越过过渡态,·HO2继续向苯环运动,当26O-4C键长减小至0.14588nm时,形成26O-4C共价键,得到加合产物P·HO2-4C.
2.2.5·HO2加成到5C
首先,·HO2攻击5C,当26O-5C距离为0.33046nm时,·HO2与Eda分子(苯环部分)在π-氢键和范德华力作用下,形成RC-·HO2_5C反应物复合物,结合能为10.6kJ/mol.其次,·HO2继续向苯环运动,当26O-5C距离为0.18356nm时,苯环共面性变差,大π键作用减弱,形成过渡态TS·HO25C,过渡态产生的能垒为83.9kJ/mol.最后,越过过渡态,·HO2继续向苯环运动,当26O-5C键长减小至0.14571nm时,26O-5C共价键作用,得到加合产物P·HO2-5C.
2.2.6·HO2加成到6C
首先,·HO2攻击6C,当26O-5C距离为0.33222nm时,·HO2与Eda分子(苯环部分)在π-氢键和范德华力作用下,形成RC-·HO2_6C反应物复合物,结合能为10.6kJ/mol.其次,·HO2继续向苯环运动,当26O-6C距离为0.18571nm时,苯环共面性变差,大π键作用减弱,形成过渡态TS_·HO26C,过渡态产生的能垒为69.7kJ/mol.最后,越过过渡态,·HO2继续向苯环运动,当26O-6C键长减小至0.14562nm时,26O-6C共价键作用,得到加合产物P_·HO2-6C.
2.2.7·HO2加成到14C
首先,·HO2攻击14C,当26O-14C距离为0.29838nm时,p和V2p分别为0.00891,0.03043,26O与14C发生库仑作用;同时,24H与杂环π-氢键作用,形成RC-·HO214C反应物复合物,结合能为9.6kJ/mol.其次,·HO2继续向杂环运动,当26O-14C距离为0.20020nm时,形成过渡态TS_·HO2_14C.从RC-·HO214C到TS_·HO2_14C过程,杂环的二面角12N-13N-14C-15C从-0.9°变为-14.2°,13N-14C-15C-16C从0.9°变为12.5°,杂环C与甲基C的二面角14C-15C-16C-17C从0.7°变为-6.6°,pRCP从0.04910降至0.04873,杂环与甲基的大π键作用减弱,TS_·HO2_14C产生的内禀能垒为48.2kJ/mol.最后,越过过渡态,·HO2继续向杂环运动,当26O-14C键长减小至0.14312nm时,其pBP和V2p分别为0.28219,-0.97880,26O-14C共价键作用,完成·HO2向14C的加成,得到加合产物P_·HO2-14C.
2.2.8·HO2加成到16C
首先,·HO2攻击16C,当26O-14C距离为0.28413nm时,26O与14C发生库仑作用,24H与杂环π-氢键作用,形成RC-·HO2_16C反应物复合物,结合能为10.6kJ/mol.其次,·HO2继续向杂环运动,当26O-16C距离为0.18465nm时,形成过渡态TS_·HO2_16C.从RC-·HO2_16C到TS·HO2_16C过程,杂环形变,大π键作用减弱,TS_·HO2_16C产生的内禀能垒为81.5kJ/mol.最后,越过过渡态,·HO2继续向杂环运动,当26O-16C键长减小至0.13710nm,同时12N-16C共价键断裂,·HO2加成到16C,形成加合产物P_·HO2-16C.
2.2.9·HO2加成到12N
该过程是直接加成.首先,·HO2从无穷远处攻击12N,不形成反应复合物.当26O-12N距离为0.15515nm时,形成过渡态TS_·HO2_12N.从Eda到TS_·HO2_12N过程,杂环严重形变,大π键作用显著减弱,TS·HO212N产生的内禀能垒为321.5kJ/mol.其次,越过过渡态,·HO2继续向杂环运动,当26O-12N键长减小至0.14214nm时,·HO2加成到12N,形成加合产物P_·HO-12N.
2.2.10·HO2加成到13N
该过程是间接加成.首先,·HO2攻击13N,当26O-13N距离为0.30876nm时,·HO2与Eda分子(杂环部分)在π-氢键和范德华力作用下,形成RC-·HO2_13N反应物复合物,结合能为9.7kJ/mol.其次,·HO2继续向杂环运动,当26O-13N距离为0.15543nm时,形成过渡态TS·HO213N.从RC-·HO213N到TS·HO213N过程,杂环严重形变,大π键作用减弱,TS_·HO213N产生的内禀能垒为139.5kJ/mol.最后,越过过渡态,·HO2继续向杂环运动,当26O-13N键长减小至0.14463nm,·HO2加成到13N,形成加合产物P·HO2-13N.
由图7可见,·HO2与Eda酮式异构体的相关C原子加成反应能垒为48.2~95.0kJ/mol,低于或接近温和反应能垒83.6kJ/mol[a],Eda酮式异构体可通过·HO2与其不饱和C的加成反应消除·HO2.·HO2与Eda酮式异构体的N原子加成反应能垒为139.5~321.5kJ/mol,接近或高于极限反应能垒160.6kJ/mola],Eda酮式异构体不能通过·HO2与其不饱和N的加成反应消除·HO2.·HO2与14C的加成反应最具优势,加成能垒为48.2kJ/mol,接近反应极易进行的能垒45.5kJ/mol,说明Eda酮式异构体与·HO2加成反应的活性位点是杂环的14C.·HO2与14C的加成反应产物最稳定,反应是放热过程.而其他加成过程的加成产物相对不稳定,反应是吸热过程,其中·HO2与N的加成反应产物不稳定,反应不能实现.
2.3单电子转移过程
单电子从Eda分子酮式异构体向。HO2转移,得到Edat和。HO2的反应过程以及相关物种的电荷分布(NPA电荷)如图8所示.
通过对基于反应物的产物Edat和HO2的高水平单点能计算,以及优化的反应物Eda酮式异构体和·HO2的高水平单点能计算,得到反应过程的非绝热能之差AEser=213.0 kJ/mol.通过对产物Edat和.HO,(优化的)与反应物Eda分子酮式异构体和.HO2(优化的)的高水平单点能及自由能校正计算,得到反应的自由能之差AGSET=132.6 kJ/mol.将数据代入式(2)得到反应的重组能A=80.4 kJ/mol.将数据代入式(1)得到Eda分子酮式异构体的单电子向.HO2转移的自由能垒AGtr=143.7 kJ/mol.该能垒低于反应不能进行的能垒160.5kJ/mol[9],但远高于温和反应能垒83.6 kJ/mol[9],说明水溶剂环境下电子从Eda酮式异构体向.HO2转移反应很慢,Eda酮式异构体通过电子转移消除·HO2的速率很小.
3结论
综上所述,本文在MN15/SMD/6-311++G(2df,pd)//M06-2X/SMD/6-311+G(d,p)双水平下研究了水溶剂环境1个大气压310.15 K温度下Eda酮式异构体与·HO2的反应机理,得到如下结论:
1)Eda酮式异构体与·HO2的反应有抽H、加成和单电子转移3种方式;
2)抽H反应主要在抽取杂环H和甲基H的反应通道实现,能垒为77.1~78.7kJ/mol;加成反应主要在.HO2加成到与甲基相连的杂环C的反应通道实现,能垒为48.2kJ/mol;单电子从Eda酮式异构体向.HO2转移的能垒为141.1 kJ/mol,该反应不能实现.
综上可见,水溶剂环境下Eda酮式异构体可以通过抽H和加成过程消除·HO2.
参考文献
[1]PÉREZ-GONZALEZ A,REBOLLAR-ZEPEDA Aм,LEÓN-CARMONA JR,etal.Reactivity Indexes and O-H Bond Dissociation Energiles of Alarge Series of Polyphenols:Implications for Their Freeradical Scavenging Activity[J].Journal of the Mexican Chemical Society,2012,56(3):241-249.
[2]王爱华.四种甘草黄酮化合物捕获体内自由基反应机理的理论研究[D].哈尔滨:哈尔滨理工大学,2018.(WANG A H.A Theoretical Study on the Reaction Mechanisms of Four Licorice Flavonoids Scavenging Free Radicals in Vivo[D].Harbin:Harbin University of Science and Technology,2018.)
[3]DE ZWART L L,MEERMANJн,COMMANDEUR J N,etal.Biomarkers of Free Radical Damage 202-22.
[4]金海峰,王月飞,郭林娜,等,依达拉奉通过抗炎、抗氧化对大鼠缺氧性肺动脉高压病理发展的抑制作用[J].中国老年学杂志,2022,42(21):5324-5328.(JIN HF,WANG Y F,GUO L N,etal.The Inhibitory Effect ofApplications in Experimental Animals and in Humans[J].Free Radical Biologyamp;.Medicine,1999,26(1/2):Edaravone on the Pathological Development of Hypoxic Pulmonary Hypertension in Rats through Anti-inflammatory and Antioxidant Effects[J].Chinese Journal of Gerontology,2022,42(21):5324-5328.)
[5]王娟,顾顺忠,陆洋,等.依达拉奉改善大鼠心肌缺血损伤和炎症反应[J].中南医学科学杂志,2022,50(4):495-498.(W ANG J,GU S Z.LU Y.et al.Edaravone Improves Myocardial Ischemic Injury and Inflammatory Response in Rats[J].Medical Science Journal of Central South China,2022,50(4):495-498.)
[6]KOBAYASHI T,KURODA S,TADA M,etal.Calcium-Induced Mitochondrial Swelling and Cytochrome c Release in the Brain:Its Biochemical Characteristics and Implication in Ischemic Neuronal Injury[J].Brain Research,2003,960(1/2):62-70.
[7]王蔚.依达拉奉对大鼠海马神经元损伤的影响效应及其作用机制的研究[D].南京:南京医科大学,2007.(WANG W.Study on Neuron Protection of Edaravone in Cultured Hippocampal Cells after Hypoxia-Reoxygenation Injury and in Hippocampal Region in Rats after Subaraclhnoid Hemorrhage[D].Nanjing:Nanjing Medical University,2007.)
[8]孙伟,姜春旭,梁晴晴,等.水液相下依达拉奉与过氧化氢自由基反应的DFT研究[J].南开大学学报(自然科学版),2023,56(6):94-104.(SUN W,JIANG C X,LIANG Q Q,etal.The DFT Study on the Reaction of Edaravone with Hydrogen Peroxide Radical in Aqueous Solution[J].Acta ScientiarumNaturalium Universitatis Nankaiensis,2023,56(6):94-104.)
[9] GORB L,LESZCZYNSKI J.Intramolecular Proton Transfer in Mono-and DihydratedTautomers of Guanine:An ab Initio Post Hartree-Fock Study[J].Journal of the American Chemical Society,1998,120:5024-5032.
[10]王玲,杨文富,杨应,等.水液相下依达拉奉消除羟自由基反应的密度泛函理论研究[J].江西师范大学学报(自然科学版),2023,47(6):582-593.(WANG L,YANG W F,YANG Y,etal.The Density Functional Theory Study on the Reaction of Edaravone Scavenging Hydroxyl Radical in Aqueous Solution[J].Journal of Jiangxi Normal University(Natural Science),2023,47(6):582-593.)
[11]张雪娇,杨应,杨文富,等.水液相下依达拉奉与超氧阴离子自由基反应的密度泛函理论[J].吉林大学学报(理学版),2023,61(6):1489-1500.(ZHANGX J,YANG Y,YANG W F,etal.Density Functional Theory of Reaction between Edaravone and Superoxide Anion Free Radical in Aqueous Liquid Phase[J].Journal of Jilin University(Science Edition),2023,61(6):1489-1500.)
[12]刘立新,陈静思,张雪娇,等.水溶剂环境下Eda酮式异构体消除超氧负离子自由基O:·的反应机理[J].江西师范大学学报,2024,48(3):221-232.(LIULX,CHENJS,ZHANG XJ,etal.Reaction Mechanism of Eda Ketone Isomer Eliminating Superoxide Anion Radical Oz·in Aqueous Solvent Environment[J].Journal of Jiangxi Normal University(Natural Science),2024,48(3):221-232.)
[13]罗香怡,高浩溟,姜丰,等.水液相下羟基自由基(水分子簇)诱导脯氨酸分子损伤的机理[J].复旦学报(自然科学版),2022,61(1):104-114.(LUOXY,GAO H M,JIANG F,etal.Mechanism of Proline Damage Induced by Hydroxyl Radicals(Water Molecules Clusters)in Water/Liquid Phase Environment[J].Journal of Fudan University(Natural Science),2022,61(1):104-114.)
[14]喻小继,潘宇,黄煜纯,等.水液相下羟基自由基诱导半胱氨酸分子损伤的机理[J].武汉大学学报(理学版),2023,69(3):373-383.(YU X J,PAN Y,HUANG Y C,etal.Mechanism of Cysteine Molecular Damage Induced by Hydroxyl Radical in Water-Liquid Phase Environment[J].Journal of Wuhan University(Natural Science Edition),2023,69(3):373-383.)
[15]李斌,黄筱珂,李双鹤,等.水液相下羟基自由基与两性Lys分子反应机理的量子化学研究[J].复旦学报(自然科学版),2023,62(2):263-272.(LI B,HUANG X K,LIS H,etal.Quantum Chemistry Study on the Reaction Mechanism of Hydroxyl Free Radical with Amphoteric Lys Molecule in Water-Liquid Phase Environmen[J].Journal of Fudan University(Natural Science),2023,62(2):263-272.)
[16]杨应,姜春旭,张雪娇,等.水液相下羟自由基诱导组氨酸分子损伤的密度泛函理论研究[J].南开大学学报(自然科学版),2023,56(4):92-100.(YANG Y,JIANG C X,ZHANG XJ,etal.Density Functional Theory Study of Hydroxyl Radical Induced Histidine Molecular Damage in Water-Liquid Phase[J].Acta ScientiarumNaturaliumUniversitatis Nankaiensis,2023,56(4):92-100.)
[17]马宏源,姜春旭,庄严,等.水环境下羟自由基致Asp分子损伤机理[J].,2019,57(5):1246-1254.(MA H Y,JIANG CX,ZHUANG Y,etal.Mechanism of Asp Molecular Damage Inducedby Hydroxyl Radicals in Water Environmen[J].Journal of Jilin University(Science Edition),2019,57(5):1246-1254.)
[18]牛鹤丽,杨应,徐岩,等.水液相下羟自由基与谷氨酸分子反应机理的量子化学研究[J].复旦学报(自然科学版),2024,63(1):143-154.(NIU H L,YANG Y,XU Y,etal.Quantum Chemistry Study on the Reaction Mechanism of Hydroxyl Radical with Glutamate Molecule in Water-Liquid Phase Environment[J].Journal of Fudan University(Natural Science),2024,63(1):143-154.)
[19]崔金玉,黄筱珂,张方坚,等,水液相下两性Lys→Mg()配合物对映异构的理论研究]南开大学学报(自然科学版),2023,56(5):99-112.(CUIJY,HUANG XK,ZHANG F J,etal.Theoretical Study on the Enantiomerism of Amphoteric LysMg(II Complex in Aqueous-Liquid Environment[J].Acta ScientiarumNaturalium Universitatis Nankaiensis,2023,56(5):99-112.)
[20]WANG Y,VERMA P,ZHANG L J,et al.M06-SX Screened-Exchange Density Functional for Chemistry and Solid-State Physics[J].Proceedings of the National Academy of Sciences of the United States of America,2020,117(5):2294-2301.
[21]徐春雪,杨应,张希花,等.水溶剂环境下两性苯丙氨酸分子对映异构的密度泛函理论研究[J].复旦学报(自然科学版),2023,62(4):486-495.(XU CX,YANGY,ZHANG X H,etal.Density Function Theoretical Study on the Enantiomerization of Amphoteric Phenylalanine Molecule in Water-Liquid Phase Environment[J].Journal of Fudan University(Natural Science),2023,62(4):486-495.)
[22]赵丽红,彭国强,郝成欣,等.水溶液环境下手性配合物Phe·Ca2+对映异构机理的DFT研究[J].中山大学学报(自然科学版)(中英文),2023,62(6):50-60.(ZHAO LI,PENG G.HAOC,etal.The DFT Study on the Isomerization Mechanism of Chiral Complexes Phe Ca2+in Aqueous Solution[J].Acta ScientiarumNaturalium Universitatis Sunyatseni,2023,62(6):50-60.)
[23]GARRETT B C,TRUHLAR D G.Criterion of Minimum State Density in the Transition State Theory of Bimolecular Reactions[J].The Journal of Chemical Physics,1979,70(4):1593-1598.
[24]HRATCHIAN H P.SCHLEGEL.H B.Using Hessian Updating to Increase the Efficiency of a Hessian Basec Predictor-Corrector Reaction Path Following Method[J].Journal of Chemical Theory and Computation,2005,1(1):61-69.
[25]YU H S,HE X,LI S H,et al.MN15:A Kohn-Sham Global-Hybrid Exchange-Correlation Density Functional with Broad Accuracy for Multi-reference and Single-Reference Systems and Noncovalent Interactions[J].Chemical Science,2016,7(8):5032-5051.
[26]喻小继,孟雪飞,黄煜纯,等.水液相下羟基负离子催化半胱氨酸旋光异构的机理.武汉大学学报(理学版)2023,69(3):384-392.(YU X J,MENG X F,HUANG Y C,etal.Optical Isomerism Mechanism of Cystenie Catalyzed by Hydroxyl Anion in Water-Liquid Phase Environment[J].Journal of Wuhan University(Natural Science Edition),2023,69(3):384-392.)
[27]MARENICH A V,CRAMER CJ,TRUHLAR D G.Universal Solvation Model Based on Solute Electron Density and on a Continuum Model of the Solvent Defined by the Bulk Dielectric Constant and Atomic Surface Tensions[J].The Journal of Physical Chemistry B,2009,113(18):6378-6396.
[28]MARCUS R A.Electron Transfer Reactions in Chemistry.Theory and Experiment[J].Pure and Applied Chemistry,1997,69(1):13-29.
[29]MARCUS R A.Electron Transfer Reactions in Chemistry.Theory and Experiment[J].Reviews of Modern Physics,1993,65(3):599-610.
[30]FRISCH M J,TRUCKS G W,SCHLEGEL H B,etal.Gaussian 16 Revision C.01[CP/CD].Pittsburgh:Gaussian Inc,2019.
[31]BIEGLER-KÖNBOHM F,SCHÖNOBOHM J,DERDAU R,etal.AIM 2000,Version 2.0[CP/CD].Ontario McMaster University,2002.
(责任编辑:单凝)

