含聚六亚甲基胍接触抗菌聚氨酯的制备与表征*
王润平,彭开美
(黔南民族师范学院 化学化工学院,贵州 都匀 558000)
细菌产生的危害是一个全球关注的问题。据1995-2007年疾病分类调查,中国细菌感染性疾病占全部疾病的18%~21%。在工业化国家,每年因住院病人感染导致的死亡人数高达17.5万[1]。因此,有效地抑制细菌的生长与繁殖,对提高人类生活质量、延长寿命等方面意义重大。接触杀菌聚合物是与细菌接触就能抑制细菌活性或灭杀细菌的一类聚合物。构建接触杀菌聚合物最常用的方式是通过共价键把具有抗菌活性的分子接枝于聚合物分子主链。
胍基具有很强的碱性,能在宽的pH范围内保持离子化状态。当其离子化后,胍基基团的正电荷离域到3个氮原子上,使其不但保持高温及碱稳定性,且电荷离域化的阳离子化合物的毒性要远小于非离域的季铵盐离子[2]。此外,相对于季铵盐离子与细菌细胞膜表面磷酸根离子的静电作用,胍基能与细菌细胞膜表面磷酸根离子形成双氢键[3],其抗菌活性要强于季铵盐离子。聚六亚甲基胍(PHMG)是一种已经商品化的含胍基抗菌剂,被广泛使用于化妆品与纺织品等行业[4]。
聚氨酯有优异的热稳定性及机械性能,在胶黏剂、合成纤维、泡沫塑料、涂料、生物医学移植及抗菌材料方面有广泛的应用[5-7]。点击化学,尤其是铜催化炔基-叠氮环加成(CuAAC)反应,具有强健、高效、正交的特性[8],是用于聚合物主链引入功能结构的好工具[9]。本文以点击化学为连接策略,在聚氨酯侧链引入聚六亚甲基胍(PHMG),制备了含胍聚合物(PU-PHMG),并测试其物理化学特性及抗菌活性。
1 实验部分
1.1 试剂与仪器
异佛尔酮二异氰酸酯(IPDI)、1,4-丁二醇(BDO)、溴化亚铜及五甲基二乙烯三胺(PMDETA),购自百灵威科技有限公司。聚丙二醇(PPG)、2,2-二(溴甲基)-1,3-丙二醇、二月桂酸二丁基锡、溴丙炔、叠氮化钠及三羟甲基丙烷(TMP),购自阿拉丁试剂有限公司。
热重分析曲线由德国Netzsch TG209测得,升温速率为 10 K/min。红外(FT-IR)光谱由美国Nicolet 6700红外光谱仪测得。
1.2 炔基修饰聚六亚甲基胍(PHMG-Al)的合成
在三口圆底烧瓶中,加入 5 g PHMG及 10 mL 二甲基亚砜(DMSO),加热至 60 ℃,待PHMG溶解后,降至室温,缓慢滴加溴丙炔DMSO溶液,室温搅拌过夜。反应停止,加入15×3 mL 丙酮清洗,于 50 ℃ 真空干燥箱中干燥 24 h,得到浅黄色稠状的炔基修饰聚六亚甲基胍(PHMG-Al)。
1.3 侧链含叠氮聚氨酯(PU-N3)的合成
2,2-双(叠氮甲基)丙烷-1,3-二醇(DAzD)合成过程参考Hu等[8]的文献,具体过程如下:烧瓶中依次加入 10.4 g 2,2-二(溴甲基)-1,3-丙二醇、6.5 g 叠氮化钠及 50 mL DMSO。在 110 ℃ 下反应 20 h。反应完成后,降至室温,加入 30 mL 去离子水,用乙酸乙酯萃取(90 mL×3),用食盐水(60 mL×3)清洗有机相,无水硫酸镁干燥,过滤,除去溶剂,得到最终产品为DAzD。
反应瓶中加入 30 g IPDI及 27.5 g PPG,搅拌均匀。反应物加热至 80 ℃,在此温度下反应 2 h,冷却至 40 ℃,加入 140 mL 无水DMF、4.68 g BDO、3 g TMP及 2.75 g DAzD。搅拌均匀,升温至 80 ℃,反应6~7 h。得到PU-N3固含量为34%的DMF溶液。
1.4 侧链接枝PHMG的聚氨酯(PU-PHMG)的合成
侧链接枝PHMG的聚氨酯(PU-PHMG)制备过程如下:反应瓶中加入 12 g 上述PU-N3溶液及 20 mL 含有PHMG-Al的DMF溶液,随后用氮气脱气 20 min。在一个史莱克瓶中加入 10 mL DMF,脱气 20 min,再加入 0.2 g 溴化亚铜及 360 μL 五甲基二乙烯三胺(PMDETA),脱气 10 min,得到催化剂溶液。将催化剂溶液用注射器转入上述三口瓶中,室温下反应 1 h。反应停止,加入去离子水析出,离心,得到固体。把固体在溶解于DMSO中,然后加入去离子水析出,如此重复3次,得到PHMG含量不同的样品:PU-PHMG 1(w=0.50%)、PU-PHMG 2(w=0.85%)、PU-PHMG 3(w=1.8%)。
取 1 g PU-PHMG溶于 8 mL DMSO中,倒入直径为 5 cm 的聚四氟乙烯培养皿中,在 75 ℃ 下干燥 24 h,冷却,脱膜,备用。
1.5 抗菌实验
不同膜对革兰氏阳性(金黄色葡萄球菌)及革兰氏阴性(大肠杆菌)的抗菌活性是通过抗菌drop-test分析方法[21]来确认的。具体过程是:细菌涂于琼脂板上并在 37 ℃ 下过夜培养。然后取单菌落于培养基中,在 37 ℃ 下保温 12 h,得到细菌悬液并把其稀释到 105CFU/mL,备用。长宽为 20 mm ×20 mm 的膜样品置于消毒的培养皿中,然后把 100 μL 细菌菌液滴于样品表面。纯聚氨酯PU膜作为对照。所有这些滴有细菌的样品膜在 37 ℃ 下保温 8 h,先用 5 mL 磷酸盐缓冲溶液简单冲洗,随后加入 15 mL 的磷酸盐缓冲溶液超声清洗,合并两次清洗液,摇匀。取 200 μL 的细菌悬液均匀的涂于琼脂板上,在 37 ℃ 下培养 24 h,对琼脂板上的菌落计数。注意,上述实验至少重复3次,且所有的聚合物样品膜都经乙醇清洗及在紫外光下辐照 30 min 消毒处理。
膜渗透测试的过程如下:10 mL 琼脂培养基注入到消毒的培养皿中并待其固化。培养基固化后把适量的细菌悬液均匀分散到琼脂表面,10 mm×10 mm×0.5 mm的聚合物膜贴合于琼脂表面上。培养皿在 37 ℃ 下保温 8 h。注意:上述实验至少重复3次,且所有的聚合物样品膜都经乙醇清洗及在紫外光下辐照 30 min 的消毒处理。
2 结果与分析
2.1 聚合物的合成与表征
通过逐步聚合,把功能单体2,2-双(叠氮甲基)丙烷-1,3-二醇(DAzD)引入到聚氨酯中,得到了可点击聚合物PU-N3(图1)。

图1 聚合物合成路线
由图2可知,2104 cm-1处为-N3的红外特征吸收峰峰,这说明成功的制备了PU-N3。随后,通过铜催化叠氮端炔环加成(CuAAC)反应,把炔基化修饰的聚六亚甲基胍(PHMG-Al)引入到聚氨酯的侧链。当加入PHMG-Al后(如图2所示),反应产物在 2104 cm-1处的红外吸收峰明显减弱,说明点击反应顺利的进行;而在 3308 cm-1及 3145 cm-1处出现了新的吸收峰,说明反应物中出现了PHMG的结构。这些结果充分证明了PHMG被成功接枝于聚氨酯的侧链。

图2 聚氨酯(PU)、可点击聚氨酯(PU-N3)及带聚六亚甲基胍侧链聚氨酯(PU-PHMG)的红外光谱
2.2 热稳定性
由于PHMG是一种热稳定性能较好的化合物,且点击反应生成的三唑环也具有很好的热稳定性能,因此,PU-PHMG的热稳定性要稍强于PU,如图3A所示。随着PHMG的引入,PU-PHMG的初始分解温度(Td)增大,其热稳定性有所提高(如图3B所示)。聚氨酯经历两个阶段的分解,其与相应的关于聚氨酯分解温度的研究相一致[10-11]。其中,第一个分解阶段发生在200~340 ℃ 的区间范围内;在此阶段,聚氨酯的氨基甲酸酯键开始降解,因此,聚氨酯分解成异氰酸酯、醇类、二级胺及二氧化碳[12]。此外,在第一分解阶段,随着PHMG的引入,最大分解速率的温度是出现一定的上升。对于第二个分解阶段,主要是C-O键的断裂,残余量的进一步减少。

图3 聚氨酯(PU)及带聚六亚甲基胍侧链聚氨酯(PU-PHMG 3)的TGA(A)与DTG(B)曲线
2.3 抗菌特性
通过对金黄色葡萄球菌(S.aureus)与大肠杆菌(E.coli)的抗菌活性测试,评估了PU-PHMG膜层的抗菌特性。聚氨酯PU作为对照,PU-PHMG膜层的接触杀菌率按公式(1)计算:
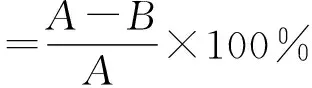
(1)
其中,A为与PU对照接触后的菌落数,B为PU-PHMG接触后的菌落数。
如图4所示,当PHMG在聚合物中的质量分数为0.50%时,对金黄色葡萄球菌的杀菌率为71%、对大肠杆菌的杀菌率为72%;而随着PHMG在聚合物中的质量分数达到0.85%时,基本上完全杀灭与其接触的细菌。由此可知,PU-PHMG对金黄色葡萄球菌及大肠杆菌都有着灭杀作用,且表现出优异的抗菌活性。
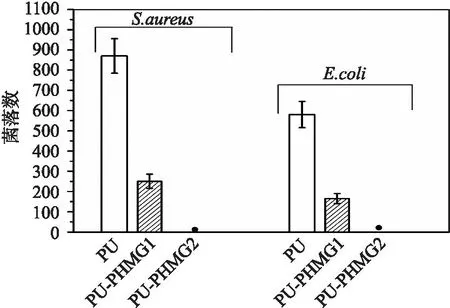
图4 与PU、PU-PHMG 1与PU-PHMG 2接触后,细菌在琼脂上的存活数
为了排除有微量的PHMG渗透而导致细菌被灭杀,把PU-PHMG 2浸泡于去离子水中3次,每次 5 h,干燥后测其抗菌活性,发现其与浸泡前没有明显的差异,依然表现出很强的抗菌活性,如图5所示。取PU-PHMG 2及物理混合(PU + PHMG-Al)膜层,对其进行抑菌圈测试,发现PU与PHMG-Al的物理混合膜层出现明显的抑菌圈,而PU-PHMG 2膜层没有出现抑菌圈。这些结果说明,PU-PHMG是通过接触杀菌的方式实现其抗菌功能的。

图5 PU-PHMG 2(A)及混合物膜(PU与PHMG-Al混合,B)对金黄色葡萄球菌的琼脂扩散测试
3 结论
以点击化学为连接策略,高效地制备了侧链含PHMG的聚氨酯(PU-PHMG)。抗菌测试表明,PU-PHMG对金黄色葡萄球菌及大肠杆菌表现出优异抗菌活性,并证明了点击化学是一种用于连接功能分子与聚合物的高效工具。抑菌圈等测试说明,PU-PHMG是通过接触杀菌的方式实现其抗菌功能。相对于PHMG的水溶特性,PU-PHMG接触性抗菌特性拓宽了PHMG的使用范围;而点击化学具有正交性的特点,通过可点击聚合物构建多功能聚合物是一种高效且便利的路径。

